총 26건
-
 방광암 면역치료 최초 IL-15 초작용제 '안크티바'안크티바(Anktiva®, 성분명: 노가펜데킨 알파 인바키셉트-pmln, nogapendekin alfa inbakicept-pmln, ImmunityBio)는 IL-15 초작용제(superagonist) 복합체로 개발된 최초의 방광 내 면역치료제다.2024년 4월 미국 FDA에서 유두종 유무와 관계없이 상피내암(CIS)을 동반한 BCG-불응성 비근육침윤성 방광암(non-muscle invasive bladder cancer, NMIBC) 성인 환자를 대상으로 BCG와 병용 사용하는 치료제로 승인됐다.방광암은 전 세계적으로 흔한 악성 종양 중 하나다. 국내에서도 발생 빈도가 높은 암종으로 알려져 있다. 이 중 약 75%는 비근육침윤성 방광암(NMIBC)으로 분류되며, 초기 치료는 대개 경요도 방광 종양 절제술(transurethral resection of bladder tumor, TURBT)로 시작된다.그러나 NMIBC는 60–70%의 재발률을 보이므로, TURBT 이후 방광 내 치료(intravesical therapy)가 질병의 재발을 억제하고 진행을 지연시키는 데 핵심적인 역할을 한다.현재 방광 내 치료는 크게 두 가지로 구분되며, 하나는 BCG 요법을 기반으로 하는 면역치료, 다른 하나는 미토마이신 C, 젬시타빈, 에피루비신, 독소루비신 등으로 구성되는 화학요법이다.BCG는 NMIBC의 표준 치료 중 하나이지만, 약 40%의 환자에서는 충분한 치료 효과를 보이지 못한다. 안크티바는 이러한 BCG-불응성 환자에서 방광 절제술을 피할 수 있는 새로운 치료 대안으로 개발됐다.IL-15는 NK 세포와 CD8⁺ T 세포의 활성, 증식, 기억 형성에 관여하는 중요한 사이토카인이다. 안크티바는 IL-15 변형체와 IL-15Rα의 sushi(반복 단백질 구조) domain이 결합한 IL-15 초작용제(superagonist) 복합체를 통해 NK 세포, CD4⁺ T 세포, CD8⁺ T 세포의 활성을 강력하게 유도하며, 특히 종양 특이적 기억 T 세포 반응을 증폭시켜 항종양 면역반응을 강화한다.임상시험에서 BCG 유지요법과 함께 안크티바를 투여받은 77명의 환자 중 62%(95% CI, 51–73)가 완전관해에 도달했다. 이 반응은 일부 환자에서 최대 47개월까지 지속됐다. 완전관해가 12개월 이상 유지된 비율은 58%, 24개월 이상 유지된 비율은 40%였다.치료 스케줄은 방광 내 카테터를 통한 유도요법(6주간 주 1회) 후, 4, 7, 10, 13, 19개월째의 유지요법(각 3주간 주 1회)으로 구성된다. 3개월 시점에 완전 반응이 확인되지 않으면 두 번째 유도요법을 시행할 수 있으며, 25개월 이후에도 완전 반응이 지속되는 경우에는 25, 31, 37개월째에 추가 BCG 유지투여를 실시할 수 있다. 투여 시 약물 혼합액은 방광 내에 2시간 동안 유지한 뒤 배출한다.안크티바 치료에는 몇 가지 중요한 주의사항이 있다. 방광절제술을 지연함으로써 전이성 방광암으로 진행할 위험이 존재하며, 배아–태아 독성 가능성이 보고되어 가임기 여성은 치료 중과 마지막 투여 후 최소 1주일 동안 피임이 필요하다.흔하게 보고되는 이상반응으로는 배뇨곤란, 혈뇨, 빈뇨, 절박뇨, 요로감염, 근골격계 통증, 발열 및 오한 등이 있으며, 실험실 검사에서는 크레아티닌 상승과 칼륨 상승이 비교적 흔하게 관찰된다.방광암(Bladder Cancer)이란 무엇인가?방광암은 요로계에서 가장 흔히 발생하는 악성 종양 중 하나로, 소변을 저장하는 장기인 방광의 점막 상피세포에서 주로 기원한다.전 세계적으로 방광암은 발생률과 사망률 측면에서 중요한 건강 문제를 야기하고 있으며, 특히 남성에서 높은 발생 빈도를 보인다. 방광암의 발생에는 흡연이 가장 강력한 위험 요인으로 작용하는 것으로 알려져 있다. 이 외에도 직업적 발암물질 노출, 만성 요로 감염 및 요로 결석 등이 발병과 연관돼 있다.조직학적으로 방광암의 대다수는 요로상피암(urothelial carcinoma)으로, 전체 방광암의 약 90%를 차지한다. 요로상피암은 방광뿐 아니라 요관, 신우, 요도 등 요로 전반에 걸쳐 발생할 수 있는 특성을 지니고 있다.이 외에도 만성 자극이나 염증과 관련된 편평세포암(squamous cell carcinoma), 드물게 선종 양상의 조직학적 특징을 보이는 선암(adenocarcinoma), 그리고 고도로 공격적인 생물학적 특성을 나타내는 소세포암(small cell carcinoma) 등 다양한 형태가 존재한다. 이러한 조직형의 차이는 임상적 경과, 치료 전략 및 예후와 밀접하게 연관되어 있어 진단 시 정확한 병리학적 분류가 필수적이다.방광암의 병기 결정은 치료 방침 수립과 예후 평가에 있어 핵심적인 요소이다. 국제적으로 널리 사용되는 TNM 병기 체계는 종양의 침윤 정도(T), 국소 림프절 전이 여부(N), 및 원격 전이 여부(M)에 기반하여 병기를 구분한다.특히 방광벽의 근육층 침윤 여부는 임상적 의사결정에서 매우 중요한 기준으로 작용한다. 종양이 점막층에 국한된 Ta 병기, 상피 내에서 편평하게 확산되는 상피내암(carcinoma in situ, CIS), 그리고 점막하층을 침범하나 근육층에는 도달하지 않은 T1 병기는 비근침윤성 방광암(non–muscle invasive bladder cancer, NMIBC)으로 분류된다.반면, 종양이 방광 근육층을 침범하는 T2 병기부터는 근침윤성 방광암(muscle invasive bladder cancer, MIBC)으로 정의되며, 이후 주변 지방조직(T3) 및 인접 장기(T4)로의 침윤 여부에 따라 병기가 상승한다. 림프절 전이(N1–N3)와 원격 전이(M1)의 존재는 질병의 진행을 시사하며 전신적 치료 전략이 요구된다.Non–Muscle Invasive Bladder Cancer(NMIBC) and Muscle Invasive Bladder Cancer(출처: https://cgoncology.com/science/).이와 같이 방광암은 조직학적 이질성과 침윤 정도에 따른 이분화된 임상 양상을 보이며, 병기 및 조직형은 환자의 치료 선택과 예후에 결정적인 영향을 미친다.비근침윤성 방광암(Non–muscle invasive bladder cancer, NMIBC)은 무엇인가?비근육 침습성 방광암(NMIBC)은 새로 진단되는 방광암의 약 75%를 차지하며, 병변이 주로 요로상피의 표층(Ta), 점막하층(T1) 또는 상피내암(CIS)에 국한되는 질환이다.NMIBC는 즉각적으로 생명을 위협하는 경우는 드물지만, 높은 재발률과 적지 않은 진행 위험으로 인해 임상적으로 중요한 도전 과제로 여겨진다. 실제로 환자의 약 50~70%가 초기 치료 이후 재발을 경험하며, 최대 30%는 근육 침습성 또는 전이성 방광암으로 진행한다.수십 년 동안 고위험군 NMIBC 환자에서 경요도 방광 종양 절제술(transurethral resection of bladder tumor, TURBT) 후 시행되는 BCG(Bacillus Calmette–Guérin) 치료는 재발과 진행을 효과적으로 억제하는 표준 치료로 자리매김해 왔다.그러나 BCG 치료의 임상적 이점에도 불구하고 약 40%의 환자에서 실패가 발생하며, 이 경우 추가적인 치료 전략이 필요하다. 이러한 환자군에서 전통적으로 가장 선호된 치료는 근치적 방광절제술(radical cystectomy)이었으나, 이 수술은 상당한 이환율과 삶의 질 저하를 초래하는 고난도 치료로, 실제 임상 적용에는 한계가 적지 않다.NMIBC의 위험도 분류—저위험군, 중간위험군, 고위험군—는 종양의 병기, 등급, 크기, 다초점성, 재발력 등의 임상·병리학적 지표를 종합해 이루어지며, 특히 고위험군 환자, 그중에서도 CIS 또는 T1 병변을 가진 환자는 진행 위험이 높아 보다 적극적인 치료가 요구된다.근치적 방광절제술은 BCG 불응 NMIBC에서 높은 질병 조절 효과를 보이지만, 그 침습성과 장기적인 기능 상실로 인해 방광을 보존하면서도 충분한 종양 조절을 달성할 수 있는 새로운 치료 전략의 필요성이 크게 대두되고 있다.이에 따라 면역관문억제제, 종양용해성 바이러스(oncolytic virus) 치료, 방광내 약물전달 플랫폼, 표적 치료제 등 다양한 신기술 기반 치료법이 개발되고 있으며, 이들 접근법은 방광 기능을 유지하면서도 지속적이고 임상적으로 의미 있는 치료 효과를 달성하는 것을 목표로 한다.최근 NMIBC 치료 환경은 과거와 달리 빠르게 확장되고 있으며, 새로운 약제의 등장, 기존 약물의 새로운 적응증 또는 약물 전달 방식의 진화, 그리고 완전히 새로운 치료 플랫폼의 출현 등 혁신적 변화가 지속되고 있다.초기에는 대부분의 신약 개발이 BCG 불응성 고위험군 NMIBC 환자를 대상으로 이루어졌으나, 점차 고위험군뿐 아니라 중간위험군 환자에서도 BCG와 직접 경쟁 가능한 후보 약제가 등장하면서 치료 선택지는 더욱 다양해지고 있다.비근침윤성 방광암(NMIBC)은 어떻게 치료하고, 치료 성적은 어떠한가?비근침윤성 방광암(NMIBC)은 대부분 경요도 방광 종양 절제술(TURBT) 후 시행되는 보조요법을 통해 관리된다. 이 질환의 임상적 특징은 높은 재발률과 상대적으로 낮은 진행률로 요약된다.실제로 5년 재발률은 50~70%에 이르며, 진행률은 10~20% 수준으로 보고된다. 이러한 자연경과는 단순 TURBT만으로는 장기적인 종양 조절이 어렵다는 점을 시사하며, 보조적 방광내 치료의 중요성을 부각시킨다.TURBT 직후 시행되는 단회 방광내 항암제 주입요법은 저위험군 및 일부 중위험군에서 재발률을 유의하게 낮추는 것으로 입증됐다. 특히 mitomycin C(MMC)는 절제 후 잔존 암세포를 제거하고 세포 재부착을 방지하는 작용을 통해 초기 재발 감소 전략의 표준요법으로 자리잡았다. 그러나 MMC를 포함한 기존 화학요법은 병변의 진행 억제 효과가 제한적이어서 고위험군에서는 단독 치료만으로는 충분하지 않다.고위험군 NMIBC, 특히 고등급 Ta/T1 병변 및 상피내암(CIS)의 경우 BCG 면역요법이 여전히 가장 강력하고 일관된 치료 효과를 제공한다. BCG의 초기 완전반응률은 유두종양에서 55~65%, CIS에서 70~75%로 보고되며, 재발 억제와 진행 위험 감소를 동시에 입증한 유일한 방광내 치료법이다.그럼에도 불구하고 전체 환자의 약 30~40%는 BCG에 초기 반응을 보이지 않는다. 초기 완전반응을 얻더라도 약 절반은 결국 재발한다. 여기에 장기화된 BCG 공급 부족 문제까지 겹치면서 고위험군 외의 환자에게 BCG 사용을 제한해야 하는 현실적인 어려움도 지속되고 있다.이러한 한계를 보완하기 위해 다양한 대체 전략이 개발되고 있다. Gemcitabine, Epirubicin, MMC 등 기존 항암제의 방광내 투여는 BCG 불응성 또는 BCG 금기 환자에서 활용되고 있으며, 특히 gemcitabine–docetaxel 병용요법은 BCG 불응 환자에서 1년 완전반응률 50~60%를 보이며 salvage therapy로 임상적 관심이 높아지고 있다.최근에는 방광보존 치료 옵션이 기존 면역요법을 넘어 유전자치료 영역으로까지 확장되고 있다. Nadofaragene firadenovec(AdstiladrinⓇ)은 IFN-α2b 유전자를 방광 점막에 전달하여 국소 면역반응을 활성화하는 비증식성 아데노바이러스 벡터 기반 치료제로, 고위험 BCG 불응성 NMIBC에서 2022년 미국 FDA 승인을 받았다. 주요 임상시험에서는 3개월 완전반응률 53%, 12개월 지속반응률 24~30%가 보고되며, BCG 불응성 환자에서 새로운 치료 기전의 확립이라는 의의를 가진다.종합하면 NMIBC 치료 전략은 위험군에 따라 크게 달라지며, 저위험군에서는 TURBT와 단회 항암제 주입만으로도 비교적 양호한 성적을 기대할 수 있다. 반면 고위험군에서는 BCG를 중심으로 한 적극적 면역치료가 필수적이며, BCG 불응성 증가와 공급 제한 문제로 인해 새로운 치료제 개발이 더욱 활발히 이루어지고 있다.Bacillus Calmette-Guérin(BCG)는 어떤 치료 방법인가?BCG는 1990년 미국 FDA에서 승인된 비특이적 면역요법으로, 비근육침윤성 방광암(NMIBC) 치료에 널리 사용돼 왔다.BCG의 항종양 효과는 Th1 중심의 면역 반응을 유도하는 기전에 기반한다. BCG가 요로상피세포에 부착되면 IL-1, IL-6, IL-8, TNF-α 등 다양한 사이토카인과 케모카인이 분비되며, 이로 인해 면역세포들이 방광 점막으로 집중된다. 이어서 대식세포, 호중구, 수지상세포 등 항원제시세포가 활성화되고, 변화된 사이토카인 환경 속에서 미성숙 CD4+ T 세포는 Th1 또는 Th2 세포로 분화한다.이 중 Th1 반응은 IFN-γ를 포함한 사이토카인 분비를 통해 BCG 치료 효과와 밀접히 연관되며, 반대로 IL-10을 중심으로 한 Th2 반응은 BCG 실패와 관련된다. 실제로 IL-10 억제 또는 IFN-γ 증가가 Th1 우세 상태를 유도하며, 이는 BCG 매개 종양 퇴행에 필수적인 요소로 알려져 있다.이처럼 BCG는 Th1 면역 반응을 활성화함으로써 방광암이 유발하는 면역 억제 환경을 극복하는 데 효과적이지만, 환자 예후를 더 향상시키기 위해서는 보다 강력한 면역조절 능력을 가진 새로운 치료제의 개발이 필요하다.특히 BCG에 반응하지 않는 NMIBC는 예후가 불량하고 전통적으로 치료 옵션이 제한적이었다. 고위험 BCG-불응성 질환의 경우 근치적 방광 절제술이 표준 치료로 권고되지만, 모든 환자가 수술을 감내할 수 있는 것은 아니다.임상시험 기준으로 BCG의 초기 완전반응률은 유두종양에서 약 55~65%, CIS에서 70~75% 수준이다. 그러나 전체 NMIBC 환자의 약 3분의 1은 BCG에 전혀 반응하지 않으며, 초기 반응을 보인 환자의 약 절반도 결국 재발하거나 진행을 경험한다.미국 FDA는 BCG-불응성 NMIBC를 다음과 같이 정의한다: ▲ 적절한 BCG 요법 후 12개월 이내 지속성 또는 재발성 CIS, 또는 재발성 Ta/T1 질환이 있는 경우(초기 유도 6회 중 ≥5회, 유지 3회 중 ≥2회 또는 2차 유도 6회 중 ≥2회 투여 완료를 ‘적절한 요법’으로 정의), ▲ 적절한 BCG 요법 후 6개월 이내 재발한 고등급 Ta/T1 질환, ▲ 유도요법 후 첫 평가에서 고등급 T1 질환이 확인된 경우이다.Bacillus Calmette-Guérin(BCG)-불응성은 왜 일어나는가?BCG-불응성은 단일 요인보다는 종양 미세환경, 면역반응의 왜곡, 종양세포의 생물학적 저항성이 복합적으로 작용하여 발생한다. 일부 NMIBC는 이미 강한 면역억제 환경을 형성하고 있어, BCG가 유도하는 Th1 중심 면역 반응이 충분히 활성화되지 못한다.이들 종양에서는 IL-10과 TGF-β 같은 면역억제성 사이토카인이 증가하고, Treg와 MDSC가 축적되며, 종양세포의 PD-L1 발현도 높아져 T 세포 기능이 억제된다. 이러한 환경에서는 BCG가 방출시키는 사이토카인이 존재하더라도 Th1 분화보다는 Th2 또는 억제성 면역반응이 우세해져 IFN-γ 중심의 항종양 면역이 제대로 형성되지 않는다.또한 종양세포 자체가 BCG에 대한 내성을 가지는 경우도 있다. 상피세포 표면의 BCG 부착·내재화에 필요한 integrin 등 분자의 발현이 낮거나, BCG가 유도하는 세포사멸 신호(TRAIL, Fas 등)에 저항성을 나타내는 경우가 이에 해당한다. 일부 NMIBC는 특정 유전자 변이나 생존 신호의 과활성화로 인해 BCG 면역 반응에 본질적으로 둔감하다.여기에 고령, 기저질환, 면역노화 등 환자 요인이 더해지면 APC 활성 및 T 세포 반응성이 감소해 BCG가 충분한 면역 강화 효과를 내지 못한다. 균주 간 면역원성 차이, BCG 부족으로 인한 불충분한 치료 역시 면역반응 축적을 방해해 불응 위험을 높인다.결국 BCG 불응성은 종양 미세환경의 면역억제성, Th1 면역 활성화의 실패, 종양세포의 내재적 저항성, 그리고 숙주 면역 기능 저하가 상호 작용하여 나타나는 복합적 면역치료 실패 현상으로 이해된다. 이러한 이유로 BCG 불응성 NMIBC에서는 보다 강력한 면역조절 능력을 갖춘 새로운 치료 전략이 필요하다.인터루킨-15(IL-15)는 어떤 역할을 하는가?IL-15는 공통 γ사슬(γc) 사이토카인 패밀리에 속하는 면역 조절 인자로, 선천 면역과 적응 면역의 경계를 연결하며 항종양 면역을 강화하는 데 핵심적인 역할을 수행한다. IL-2, IL-4, IL-7, IL-9, IL-21과 함께 γc 계열을 이루는 IL-15는 특히 CD8+ T 세포와 자연살해(NK) 세포의 발달, 생존, 증식, 그리고 기능적 활성화 전반을 조절하는 중심적 사이토카인이다.Pleiotropic Effects of IL-15(출처: Cells 2023, 12, 1611).이러한 생물학적 중요성은 다양한 전임상·임상 연구에서 반복적으로 입증되어 왔으며, IL-15가 항암 면역을 유지하는 데 필수적인 조절자로 작용함을 뚜렷하게 보여준다.생리학적으로 IL-15는 IL-15 수용체 α(IL-15Rα)와 함께 이종이량체 형태로 합성된다. IL-15Rα는 자체적으로 신호 전달 기능을 갖고 있지는 않지만 IL-15에 높은 친화도로 결합하여 내질망에서 안정적인 복합체를 형성하고 이를 세포 표면까지 운반함으로써 생물학적 기능 발현을 위한 핵심적인 플랫폼을 제공한다.이 복합체는 생산 세포 표면에 제시된 뒤 인접한 수용 세포의 IL-2/IL-15Rβ와 공통 γ사슬과 결합하여 신호를 전달하는데, 이러한 ‘트랜스제시(trans-presentation)’는 IL-15 생물학을 규정하는 대표적 기전이자 IL-2와 구별되는 가장 특징적인 작동 방식이다.따라서 IL-15와 IL-15Rα는 단핵구, 대식세포, 수지상세포, 혈관내피세포, 골수 및 림프절의 기질세포 등 다양한 세포 유형에서 발현되며, 특히 수지상세포와 대식세포가 주요 생산자인 것으로 보고되었다. 이들 세포는 항원 제시뿐 아니라 IL-15 제시 기능을 통해 CD8+ T 세포와 NK 세포의 생존 신호를 제공함으로써 면역계의 항상성을 유지하는 데 기여한다.IL-15 초작용제(superagonist) 복합체는 무엇인가?최근 면역조절 치료제 개발은 기존 사이토카인 신호 경로를 선택적으로 증폭하여 항종양 면역 반응을 극대화하는 방향으로 진화하고 있으며, 그 중심에는 IL-15 경로 기반의 차세대 초작용제(superagonist) 기술이 있다.IL-15는 본래 NK 세포와 CD8⁺ T 세포의 생존, 증식, 기억 형성에 핵심적인 사이토카인이지만, 생체 내 반감기가 짧고 수용체 결합 효율이 낮아 단독 활용에는 한계가 있었다.이러한 제약을 극복하기 위해 고안된 IL-15 초작용제 복합체는 IL-15의 생물학적 활성을 비약적으로 증폭하도록 설계된 구조적 혁신체로, 대표적인 예가 IL-15N72D 변형체와 IL-15Rα의 sushi 도메인을 융합한 노가펜데킨 알파 인바키셉트이다.IL-15N72D는 아스파라긴(N)에서 아스파트산(D)으로의 단일 아미노산 치환을 통해 수용체 친화성과 신호전달 강도를 향상시킨 기능적 변형체이며, IL-15Rα의 sushi 도메인 결합을 통해 자연적인 trans-presentation 기전을 모사하도록 설계되었다.이 두 구성요소는 IgG1 Fc 영역과 융합되어 약물의 안정성, 체내 반감기, 조직 내 지속 시간을 획기적으로 개선하며, 그 결과 NK 세포와 CD8⁺ T 세포의 활성화 및 항종양 세포독성 반응을 장기간 유도하는 강력한 IL-15 신호 증폭체를 형성한다.이러한 기전은 기존 BCG 치료로 유도되는 국소 면역 반응을 효과적으로 증폭시키며, BCG-불응성 비근육침윤성 방광암에서 관찰되는 높은 완전관해율과 반응 지속성을 설명하는 면역학적 기반을 제공한다.결과적으로 IL-15 변형체와 IL-15Rα가 융합된 초작용제 플랫폼은 단순한 사이토카인 보충을 넘어, 정밀하게 설계된 면역 신호 조절을 통해 종양 미세환경 내에서 효과적인 항암 면역을 재활성화하려는 현대 면역항암제 개발의 중요한 패러다임을 제시한다노가펜데킨 알파 인바키셉트의 약리 기전은?노가펜데킨 알파 인바키셉트는 IL-15 돌연변이체(IL-15N72D)와 IL-15Rα를 융합한 복합체로, 자연 면역세포가 제공하는 IL-15 제시 기전을 모방한다. 이를 통해 CD8+ T 세포, NK 세포, 기억 T 세포의 증식·활성화를 강하게 유도하면서도, 면역억제성 조절 T 세포의 확장은 최소화한다.전임상 모델에서 방광 내 투여된 노가펜데킨 알파 인바키셉트는 단독 또는 BCG와 병용 시 BCG 단독보다 우수한 항종양 효과를 보였다. 또한 비융합(native) IL-15에 비해 림프조직 내 지속시간이 길고, 약동학적 안정성이 크게 향상되어 보다 강력하고 지속적인 항종양 면역반응을 유발한다.결과적으로 노가펜데킨 알파 인바키셉트는 IL-15 신호를 증폭해 킬러 T 세포 중심의 면역반응을 재가동시키는 기전적 특성을 기반으로, BCG-불응성 NMIBC에서 의미 있는 치료적 이점을 제공하는 IL-15 기반 면역증강제이다.Immune Effects of nogapendekin alfa inbakicept(출처: Cells 2023, 12, 1611).위 사진자료에 대해 설명하면, A. 노가펜데킨 알파 인바키셉트는 인간 IgG1 Fc와 융합된 IL15Rα에 결합된 돌연변이(N72D) 인간 IL-15로 구성된다. B. 노가펜데킨 알파 인바키셉트는 IL-15 수용체를 통해 순환 면역 세포에 결합한다. C. 노가펜데킨 알파 인바키셉트가 림프구에 결합하면 자연 살해(NK) 세포와 CD8+ T 세포 집단이 활성화된다되고 확장되어 고효과 CD56 dim 및 CD56 bright NK 세포와 중앙 기억 T 세포(TCM)가 확장된다. D. 비장 CD8+ T 세포 표면의 CXCR3가 상향 조절되면 종양 미세 환경(TME)으로 이동할 가능성이 높아집니다. 활성화된 NK 세포도 종양으로 이동한다. E. 활성화된 종양 침윤 CD8+ T 림프구(TIL)는 MHC 클래스 I 복합체가 제시하는 종양 관련 항원 에피토프를 인식하여 암세포를 인식한다. 활성화된 CD8+ T 세포와 NK 세포는 세포독성이 증가하여 암세포 사멸을 유도한다.CD8+ T 세포는 IFNγ 및 TNF⍺와 같은 Th1 사이토카인을 분비하여 염증성 TME를 촉진하고 과립구 및 단핵구 골수유래 억제 세포(MDSC)의 PD-L1을 상향 조절합니다. 노가펜데킨 알파 인바키셉트는 NK TIL이 TGF-β의 영향에 저항성을 갖도록 하고 항체 의존성 세포독성(ADCC)을 증가시킬 수 있도록 한다.노가펜데킨 알파 인바키셉트의 치료적 위치는?비근육침윤성 방광암(NMIBC)은 초기 치료로 경요도 방광종양절제술(TURBT)이 시행되지만, 재발률이 높고 병변이 지속·활성화되는 경우가 많아 반복적 치료가 필요하다. 특히 CIS를 동반한 고위험군에서는 BCG 치료가 표준으로 자리잡아 있으나, 충분한 BCG 노출에도 불구하고 재발·지속·진행이 나타나는 BCG-불응성 환자군이 적지 않다.이러한 환자에서 근치적 방광적출술(radical cystectomy)은 표준 치료로 권고되지만, 고령, 동반질환, 삶의 질 저하에 대한 우려, 환자 선호 등의 이유로 수술 적용이 어려운 경우가 많다. 이에 따라 방광을 보존하면서도 충분한 항종양 효과를 제공할 수 있는 새로운 치료 전략의 필요성이 지속적으로 제기되어 왔다.노가펜데킨 알파 인바키셉트는 IL-15/IL-15Rα 복합체 기반의 IL-15 초작동제로, CD8+ T 세포와 NK 세포의 증식·활성화를 강력하게 유도하는 면역 증강형 생물학적 제제이다. NMIBC에서 BCG 치료는 국소 면역활성에 의존하지만, BCG-불응성 환자에서는 방광 내 면역 미세환경의 소진, T/NK 세포 감소, BCG 반응 저하 등이 주요 병태생리로 지적된다.이러한 맥락에서 노가펜데킨 알파 인바키셉트는 고갈된 면역계를 다시 활성화하여 기존 BCG 효과를 강화하고, 단독 BCG로는 확보하기 어려운 항종양 면역반응을 확대하는 기전적 장점을 가진다.전신 면역관문억제제인 pembrolizumab(키트루다)은 일부 환자에서 의미 있는 완전반응을 유도하지만, 전신 면역 관련 부작용과 장기 치료에 따른 독성·비용 부담이 중요한 제약으로 남아 있다. 반면 노가펜데킨 알파 인바키셉트는 방광 내 국소 투여를 기반으로 하여 전신 독성이 극히 낮으며, 고령 또는 동반질환이 많은 실제 진료 환경에서 사용하기 용이하다.또한 바이러스 벡터를 이용하는 AAV 기반 유전자치료제(nadofaragene firadenovec)와 달리 벡터 노출에 따른 안전성 우려가 없고, 기존 BCG 치료 패턴과 자연스럽게 연계되어 임상적 채택성이 높다는 점도 장점이다.노가펜데킨 알파 인바키셉트의 임상적 의미는 단순한 반응률 개선을 넘어, BCG-불응성 CIS 환자에서 방광적출술을 지연하거나 회피할 수 있는 실질적 치료 대안을 제공한다는 데에 있다.실제 임상에서 의미 있는 완전반응률과 지속기간이 확인되었으며, 이는 방광적출술을 바로 시행하기 어려운 환자에게 중요한 시간적 여유와 치료 선택권을 제공한다. 전신 독성의 부담이 거의 없고, BCG 기반 면역작동 기전을 확장하는 방식이라는 점 또한 치료적 위치를 공고히 한다.노가펜데킨 알파 인바키셉트(ANKTIVA)의 허가임상은 어떠한가?ANKTIVA의 효능은 QUILT-3.032(NCT03022825) 시험에서 평가되었다. 이 연구는 경요도 방광종양절제술(TURBT) 이후 BCG에 반응하지 않는 고위험 비근육침윤성 방광암(NMIBC) 중 상피내암(CIS)을 동반한 성인 환자 77명을 대상으로 한 단일군, 다기관 임상시험이었다. 여기에는 Ta/T1 유두상 병변의 동반 여부와 상관없이 CIS를 가진 환자들이 포함되었다.BCG 불응성 고위험군 NMIBC의 CIS는, 충분한 BCG 치료를 완료한 후 12개월 이내에 CIS가 단독으로 또는 Ta/T1 병변과 함께 지속되거나 재발한 경우로 정의되었다. 충분한 BCG 치료는 초기 유도요법 6회 중 최소 5회를 투여하고, 이어서 유지요법 3회 중 최소 2회 또는 두 번째 유도요법 6회 중 최소 2회를 투여한 경우로 정의되었다.치료 전 Ta 또는 T1 병변 환자들은 절제가 가능한 모든 병변을 제거하기 위해 TURBT를 시행받았다. 절제, 소작 또는 전기소작이 불가능한 잔여 CIS는 허용되었다. 한편 근침윤성 방광암(T2~T4), 국소 진행성, 전이성 또는 방광 외부(요도, 요관, 신우) 침범이 있거나 그 병력이 있는 환자는 시험에서 제외되었다.환자들은 유도요법 동안 ANKTIVA 400mcg와 BCG를 주 1회, 6주 연속 투여받았다. 이후 질병이 없거나 저등급 질환을 가진 경우 4, 7, 10, 13, 19개월째에 3주 간격으로 주 1회 추가 투여를 받았다. 치료 3개월 시점에 CIS가 지속되거나 고등급 Ta 병변이 남아 있는 경우에는 두 번째 유도요법을 받을 수 있었다. 치료 25개월 시점에 완전반응(CR)이 유지되는 환자는 25, 31, 37개월째에 동일한 방식으로 추가 투여가 가능했다.종양 상태 평가는 최대 2년 동안 3개월마다 시행되었다. 24개월 이후의 반응 평가는 각 기관의 진료 기준에 따라 시행되었다. 치료 시작 후 첫 6개월 동안은 무작위 또는 방광경 유도 조직검사가 필수적으로 시행되었다. 주요 효능 평가지표는 어느 시점에서든 완전반응을 달성했는지와(방광경 검사 및 필요 시 TURBT/조직검사 결과 음성, 요세포검사 음성 기준) 그 반응의 지속기간이었다.등록 환자의 중앙 연령은 73세(범위 50~91세)였고, 86%가 남성이었다. 인종 분포는 백인 90%, 흑인 6%, 아시아인 1%, 아메리칸 인디언/알래스카 원주민 1%, 미상 1%였다. ECOG 수행능력은 0점이 83%, 1점이 17%였다.연구 등록 시 종양 특성은 CIS 단독 69%, CIS + Ta 병변 21%, CIS + T1(±Ta) 병변 10%였다. 기저 질환 상태는 불응성 43%, 재발성 57%였다. 이전 BCG 투여 횟수의 중앙값은 12회(범위 8~45회)였고, 13%는 분할 용량 BCG를 받은 경험이 있었다. 방광경 영상 방식은 백색광 57%, 청색광 또는 협대역 영상 40%, 미상 3%였다.효능 결과는 표 3에 제시되어 있으며, 전체 환자의 31%(24명)는 두 번째 유도요법을 받았다.노가펜데킨 알파 인바키셉트의 쟁점을 무엇인가?노가펜데킨 알파 인바키셉트는 IL-15의 생물학적 활성을 기반으로 설계된 차세대 면역작용제로, 고위험 BCG 불응성 비근침윤성 방광암(NMIBC) 치료에서 새로운 치료적 가능성을 제시하고 있다.IL-15는 CD8⁺ T 세포와 NK 세포의 생존과 기능을 강화하는 핵심 사이토카인으로 알려져 있으나, 자연 상태의 IL-15는 짧은 반감기, 불안정한 구조, 수용체 결합의 가변성 등으로 인해 치료제로 활용하는 데 본질적인 제약이 존재해왔다.노가펜데킨 알파 인바키셉트는 IL-15와 IL-15Rα 수용체 도메인을 결합해 형성한 안정적 이종이량체 기반의 IL-15 초작용제로, 내재 IL-15에 비해 우수한 생체 내 안정성과 장기적 면역 활성 유도가 가능하다는 점에서 임상적 의미가 크다.특히 BCG 치료에 반응하지 않는 NMIBC 환자는 방광적출술이 표준 치료임에도 불구하고, 고령 및 동반질환 등으로 수술이 어려운 경우가 많아 실질적인 치료 공백이 존재해왔다. 이러한 점에서 BCG와 병용하여 국소 종양 미세환경을 재활성화할 수 있는 약제의 개발은 방광보존 전략을 확장할 수 있는 새로운 치료 패러다임이라 할 수 있다.노가펜데킨 알파 인바키셉트의 주요 장점은 BCG와 병용 시 강력한 상승효과를 보인다는 점이다. IL-15Rα와의 결합을 통해 강화된 생물학적 활성은 APC, NK 세포, CD8⁺ T 세포의 집적과 기능을 촉진하여 항종양 면역반응을 증폭시키며, 이는 허가 근거가 된 QUILT-3.032 연구에서 3개월 완전반응률 53%, 12개월 반응 지속률 24~30%로 나타났다.이러한 치료 성적은 기존 BCG 불응 환자에서 보고된 방광내 요법의 성적을 상회하는 결과이며, 이 약제가 임상적으로 의미 있는 반응을 유도하는 면역치료제로 기능함을 보여준다.그러나 노가펜데킨 알파 인바키셉트는의 개발과 허가 과정에는 여러 한계와 도전이 병존한다. 가장 큰 문제는 근거 임상이 무작위 대조군이 없는 단일군(single-arm) 연구로 수행되었다는 점으로, 이는 약제의 효과를 BCG 재투여 효과와 명확히 구분하기 어렵게 만들며, 역사적 대조(historical control)와의 비교에서 발생할 수 있는 해석의 변이를 피하기 어렵다.또한 환자군 내 BCG 노출량, CIS 단독 여부, 종양 특성 등에서 이질성이 존재하여 반응률과 반응 지속성의 정확한 비교가 제한된다. 반응의 지속성 역시 완전반응을 보인 환자의 일부에서만 장기적으로 유지되는 경향이 관찰되었고, 12개월 이후 장기 추적자료는 아직 충분히 축적되지 않아 방광보존 전략의 장기적 안전성과 유효성에 대한 확정적 결론을 내리기 어렵다.더불어 치료효과의 기저에 있는 종양면역미세환경의 상태가 환자별로 크게 달라, 이 약제가 NK/T 세포 결핍 또는 극도로 억제된 미세환경을 충분히 회복시키지 못하는 경우가 존재할 것으로 예상되며, 이러한 점은 향후 바이오마커 기반 환자선택 전략의 필요성을 시사한다.이처럼 노가펜데킨 알파 인바키셉트는 IL-15 생물학을 임상적으로 구현한 최초의 치료제로서 BCG 불응성 NMIBC라는 미충족 의료수요 영역에서 실질적인 치료 옵션을 제공하고 있다.초기 반응률과 독성 프로파일은 고무적이지만, 단일군 연구 설계, 병용요법의 기여도 분리 문제, 반응 지속성의 제한, 장기 추적자료 부족 등은 여전히 해결해야 할 과제로 남아 있다.그럼에도 불구하고 노가펜데킨 알파 인바키셉트는 기존 치료제와는 차별화된 기전을 바탕으로 난치성 NMIBC에서 방광보존 전력을 확장할 수 있는 중요한 면역치료제로 자리매김할 가능성이 높으며, 향후 병용 전략, 내성 기전 규명, 예측 바이오마커 개발 등을 통해 그 임상적 가치가 더욱 강화될 것으로 기대된다.참고문헌 1. Grace Lui et al. “Exploiting an Interleukin-15 Heterodimeric Agonist (N803) for Effective Immunotherapy of Solid Malignancies” Cells 2023, 12(12), 1611. 3. Richard S et al. “Non–muscle-invasive Bladder Cancer: Overview and Contemporary Treatment Landscape of Neoadjuvant Chemoablative Therapies” Reviews in Urology, Vol. 22 No. 2 2020. 3. Jong Ho Park et al. “The Emerging Treatment of BCG (Bacillus Calmette-Guérin)- Unresponsive Non–Muscle-Invasive Bladder Cancer“ Journal of Urologic Oncology 2024;22(3):246-255. 4. Aiman Waheed et al. “Nogapendekin alfa inbakicept-PMLN: first approval milestone for BCG-unresponsive noninvasive bladder cancer: editorial” Annals of Medicine & Surgery (2024) 86:6386–6388. 5. Brian L. Heiss et al. “FDA Approval Summary: Nogapendekin Alfa Inbakicept-pmln with BCG for BCG-unresponsive carcinoma in situ” Clin Cancer Res. 2025 October 15; 31(20): 4223–4229. 6. Vikram M et al. “Mechanism of action of nadofaragene firadenovec-vncg” Front. Oncol. 14:1359725. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-11-20 17:29:43최병철 박사
방광암 면역치료 최초 IL-15 초작용제 '안크티바'안크티바(Anktiva®, 성분명: 노가펜데킨 알파 인바키셉트-pmln, nogapendekin alfa inbakicept-pmln, ImmunityBio)는 IL-15 초작용제(superagonist) 복합체로 개발된 최초의 방광 내 면역치료제다.2024년 4월 미국 FDA에서 유두종 유무와 관계없이 상피내암(CIS)을 동반한 BCG-불응성 비근육침윤성 방광암(non-muscle invasive bladder cancer, NMIBC) 성인 환자를 대상으로 BCG와 병용 사용하는 치료제로 승인됐다.방광암은 전 세계적으로 흔한 악성 종양 중 하나다. 국내에서도 발생 빈도가 높은 암종으로 알려져 있다. 이 중 약 75%는 비근육침윤성 방광암(NMIBC)으로 분류되며, 초기 치료는 대개 경요도 방광 종양 절제술(transurethral resection of bladder tumor, TURBT)로 시작된다.그러나 NMIBC는 60–70%의 재발률을 보이므로, TURBT 이후 방광 내 치료(intravesical therapy)가 질병의 재발을 억제하고 진행을 지연시키는 데 핵심적인 역할을 한다.현재 방광 내 치료는 크게 두 가지로 구분되며, 하나는 BCG 요법을 기반으로 하는 면역치료, 다른 하나는 미토마이신 C, 젬시타빈, 에피루비신, 독소루비신 등으로 구성되는 화학요법이다.BCG는 NMIBC의 표준 치료 중 하나이지만, 약 40%의 환자에서는 충분한 치료 효과를 보이지 못한다. 안크티바는 이러한 BCG-불응성 환자에서 방광 절제술을 피할 수 있는 새로운 치료 대안으로 개발됐다.IL-15는 NK 세포와 CD8⁺ T 세포의 활성, 증식, 기억 형성에 관여하는 중요한 사이토카인이다. 안크티바는 IL-15 변형체와 IL-15Rα의 sushi(반복 단백질 구조) domain이 결합한 IL-15 초작용제(superagonist) 복합체를 통해 NK 세포, CD4⁺ T 세포, CD8⁺ T 세포의 활성을 강력하게 유도하며, 특히 종양 특이적 기억 T 세포 반응을 증폭시켜 항종양 면역반응을 강화한다.임상시험에서 BCG 유지요법과 함께 안크티바를 투여받은 77명의 환자 중 62%(95% CI, 51–73)가 완전관해에 도달했다. 이 반응은 일부 환자에서 최대 47개월까지 지속됐다. 완전관해가 12개월 이상 유지된 비율은 58%, 24개월 이상 유지된 비율은 40%였다.치료 스케줄은 방광 내 카테터를 통한 유도요법(6주간 주 1회) 후, 4, 7, 10, 13, 19개월째의 유지요법(각 3주간 주 1회)으로 구성된다. 3개월 시점에 완전 반응이 확인되지 않으면 두 번째 유도요법을 시행할 수 있으며, 25개월 이후에도 완전 반응이 지속되는 경우에는 25, 31, 37개월째에 추가 BCG 유지투여를 실시할 수 있다. 투여 시 약물 혼합액은 방광 내에 2시간 동안 유지한 뒤 배출한다.안크티바 치료에는 몇 가지 중요한 주의사항이 있다. 방광절제술을 지연함으로써 전이성 방광암으로 진행할 위험이 존재하며, 배아–태아 독성 가능성이 보고되어 가임기 여성은 치료 중과 마지막 투여 후 최소 1주일 동안 피임이 필요하다.흔하게 보고되는 이상반응으로는 배뇨곤란, 혈뇨, 빈뇨, 절박뇨, 요로감염, 근골격계 통증, 발열 및 오한 등이 있으며, 실험실 검사에서는 크레아티닌 상승과 칼륨 상승이 비교적 흔하게 관찰된다.방광암(Bladder Cancer)이란 무엇인가?방광암은 요로계에서 가장 흔히 발생하는 악성 종양 중 하나로, 소변을 저장하는 장기인 방광의 점막 상피세포에서 주로 기원한다.전 세계적으로 방광암은 발생률과 사망률 측면에서 중요한 건강 문제를 야기하고 있으며, 특히 남성에서 높은 발생 빈도를 보인다. 방광암의 발생에는 흡연이 가장 강력한 위험 요인으로 작용하는 것으로 알려져 있다. 이 외에도 직업적 발암물질 노출, 만성 요로 감염 및 요로 결석 등이 발병과 연관돼 있다.조직학적으로 방광암의 대다수는 요로상피암(urothelial carcinoma)으로, 전체 방광암의 약 90%를 차지한다. 요로상피암은 방광뿐 아니라 요관, 신우, 요도 등 요로 전반에 걸쳐 발생할 수 있는 특성을 지니고 있다.이 외에도 만성 자극이나 염증과 관련된 편평세포암(squamous cell carcinoma), 드물게 선종 양상의 조직학적 특징을 보이는 선암(adenocarcinoma), 그리고 고도로 공격적인 생물학적 특성을 나타내는 소세포암(small cell carcinoma) 등 다양한 형태가 존재한다. 이러한 조직형의 차이는 임상적 경과, 치료 전략 및 예후와 밀접하게 연관되어 있어 진단 시 정확한 병리학적 분류가 필수적이다.방광암의 병기 결정은 치료 방침 수립과 예후 평가에 있어 핵심적인 요소이다. 국제적으로 널리 사용되는 TNM 병기 체계는 종양의 침윤 정도(T), 국소 림프절 전이 여부(N), 및 원격 전이 여부(M)에 기반하여 병기를 구분한다.특히 방광벽의 근육층 침윤 여부는 임상적 의사결정에서 매우 중요한 기준으로 작용한다. 종양이 점막층에 국한된 Ta 병기, 상피 내에서 편평하게 확산되는 상피내암(carcinoma in situ, CIS), 그리고 점막하층을 침범하나 근육층에는 도달하지 않은 T1 병기는 비근침윤성 방광암(non–muscle invasive bladder cancer, NMIBC)으로 분류된다.반면, 종양이 방광 근육층을 침범하는 T2 병기부터는 근침윤성 방광암(muscle invasive bladder cancer, MIBC)으로 정의되며, 이후 주변 지방조직(T3) 및 인접 장기(T4)로의 침윤 여부에 따라 병기가 상승한다. 림프절 전이(N1–N3)와 원격 전이(M1)의 존재는 질병의 진행을 시사하며 전신적 치료 전략이 요구된다.Non–Muscle Invasive Bladder Cancer(NMIBC) and Muscle Invasive Bladder Cancer(출처: https://cgoncology.com/science/).이와 같이 방광암은 조직학적 이질성과 침윤 정도에 따른 이분화된 임상 양상을 보이며, 병기 및 조직형은 환자의 치료 선택과 예후에 결정적인 영향을 미친다.비근침윤성 방광암(Non–muscle invasive bladder cancer, NMIBC)은 무엇인가?비근육 침습성 방광암(NMIBC)은 새로 진단되는 방광암의 약 75%를 차지하며, 병변이 주로 요로상피의 표층(Ta), 점막하층(T1) 또는 상피내암(CIS)에 국한되는 질환이다.NMIBC는 즉각적으로 생명을 위협하는 경우는 드물지만, 높은 재발률과 적지 않은 진행 위험으로 인해 임상적으로 중요한 도전 과제로 여겨진다. 실제로 환자의 약 50~70%가 초기 치료 이후 재발을 경험하며, 최대 30%는 근육 침습성 또는 전이성 방광암으로 진행한다.수십 년 동안 고위험군 NMIBC 환자에서 경요도 방광 종양 절제술(transurethral resection of bladder tumor, TURBT) 후 시행되는 BCG(Bacillus Calmette–Guérin) 치료는 재발과 진행을 효과적으로 억제하는 표준 치료로 자리매김해 왔다.그러나 BCG 치료의 임상적 이점에도 불구하고 약 40%의 환자에서 실패가 발생하며, 이 경우 추가적인 치료 전략이 필요하다. 이러한 환자군에서 전통적으로 가장 선호된 치료는 근치적 방광절제술(radical cystectomy)이었으나, 이 수술은 상당한 이환율과 삶의 질 저하를 초래하는 고난도 치료로, 실제 임상 적용에는 한계가 적지 않다.NMIBC의 위험도 분류—저위험군, 중간위험군, 고위험군—는 종양의 병기, 등급, 크기, 다초점성, 재발력 등의 임상·병리학적 지표를 종합해 이루어지며, 특히 고위험군 환자, 그중에서도 CIS 또는 T1 병변을 가진 환자는 진행 위험이 높아 보다 적극적인 치료가 요구된다.근치적 방광절제술은 BCG 불응 NMIBC에서 높은 질병 조절 효과를 보이지만, 그 침습성과 장기적인 기능 상실로 인해 방광을 보존하면서도 충분한 종양 조절을 달성할 수 있는 새로운 치료 전략의 필요성이 크게 대두되고 있다.이에 따라 면역관문억제제, 종양용해성 바이러스(oncolytic virus) 치료, 방광내 약물전달 플랫폼, 표적 치료제 등 다양한 신기술 기반 치료법이 개발되고 있으며, 이들 접근법은 방광 기능을 유지하면서도 지속적이고 임상적으로 의미 있는 치료 효과를 달성하는 것을 목표로 한다.최근 NMIBC 치료 환경은 과거와 달리 빠르게 확장되고 있으며, 새로운 약제의 등장, 기존 약물의 새로운 적응증 또는 약물 전달 방식의 진화, 그리고 완전히 새로운 치료 플랫폼의 출현 등 혁신적 변화가 지속되고 있다.초기에는 대부분의 신약 개발이 BCG 불응성 고위험군 NMIBC 환자를 대상으로 이루어졌으나, 점차 고위험군뿐 아니라 중간위험군 환자에서도 BCG와 직접 경쟁 가능한 후보 약제가 등장하면서 치료 선택지는 더욱 다양해지고 있다.비근침윤성 방광암(NMIBC)은 어떻게 치료하고, 치료 성적은 어떠한가?비근침윤성 방광암(NMIBC)은 대부분 경요도 방광 종양 절제술(TURBT) 후 시행되는 보조요법을 통해 관리된다. 이 질환의 임상적 특징은 높은 재발률과 상대적으로 낮은 진행률로 요약된다.실제로 5년 재발률은 50~70%에 이르며, 진행률은 10~20% 수준으로 보고된다. 이러한 자연경과는 단순 TURBT만으로는 장기적인 종양 조절이 어렵다는 점을 시사하며, 보조적 방광내 치료의 중요성을 부각시킨다.TURBT 직후 시행되는 단회 방광내 항암제 주입요법은 저위험군 및 일부 중위험군에서 재발률을 유의하게 낮추는 것으로 입증됐다. 특히 mitomycin C(MMC)는 절제 후 잔존 암세포를 제거하고 세포 재부착을 방지하는 작용을 통해 초기 재발 감소 전략의 표준요법으로 자리잡았다. 그러나 MMC를 포함한 기존 화학요법은 병변의 진행 억제 효과가 제한적이어서 고위험군에서는 단독 치료만으로는 충분하지 않다.고위험군 NMIBC, 특히 고등급 Ta/T1 병변 및 상피내암(CIS)의 경우 BCG 면역요법이 여전히 가장 강력하고 일관된 치료 효과를 제공한다. BCG의 초기 완전반응률은 유두종양에서 55~65%, CIS에서 70~75%로 보고되며, 재발 억제와 진행 위험 감소를 동시에 입증한 유일한 방광내 치료법이다.그럼에도 불구하고 전체 환자의 약 30~40%는 BCG에 초기 반응을 보이지 않는다. 초기 완전반응을 얻더라도 약 절반은 결국 재발한다. 여기에 장기화된 BCG 공급 부족 문제까지 겹치면서 고위험군 외의 환자에게 BCG 사용을 제한해야 하는 현실적인 어려움도 지속되고 있다.이러한 한계를 보완하기 위해 다양한 대체 전략이 개발되고 있다. Gemcitabine, Epirubicin, MMC 등 기존 항암제의 방광내 투여는 BCG 불응성 또는 BCG 금기 환자에서 활용되고 있으며, 특히 gemcitabine–docetaxel 병용요법은 BCG 불응 환자에서 1년 완전반응률 50~60%를 보이며 salvage therapy로 임상적 관심이 높아지고 있다.최근에는 방광보존 치료 옵션이 기존 면역요법을 넘어 유전자치료 영역으로까지 확장되고 있다. Nadofaragene firadenovec(AdstiladrinⓇ)은 IFN-α2b 유전자를 방광 점막에 전달하여 국소 면역반응을 활성화하는 비증식성 아데노바이러스 벡터 기반 치료제로, 고위험 BCG 불응성 NMIBC에서 2022년 미국 FDA 승인을 받았다. 주요 임상시험에서는 3개월 완전반응률 53%, 12개월 지속반응률 24~30%가 보고되며, BCG 불응성 환자에서 새로운 치료 기전의 확립이라는 의의를 가진다.종합하면 NMIBC 치료 전략은 위험군에 따라 크게 달라지며, 저위험군에서는 TURBT와 단회 항암제 주입만으로도 비교적 양호한 성적을 기대할 수 있다. 반면 고위험군에서는 BCG를 중심으로 한 적극적 면역치료가 필수적이며, BCG 불응성 증가와 공급 제한 문제로 인해 새로운 치료제 개발이 더욱 활발히 이루어지고 있다.Bacillus Calmette-Guérin(BCG)는 어떤 치료 방법인가?BCG는 1990년 미국 FDA에서 승인된 비특이적 면역요법으로, 비근육침윤성 방광암(NMIBC) 치료에 널리 사용돼 왔다.BCG의 항종양 효과는 Th1 중심의 면역 반응을 유도하는 기전에 기반한다. BCG가 요로상피세포에 부착되면 IL-1, IL-6, IL-8, TNF-α 등 다양한 사이토카인과 케모카인이 분비되며, 이로 인해 면역세포들이 방광 점막으로 집중된다. 이어서 대식세포, 호중구, 수지상세포 등 항원제시세포가 활성화되고, 변화된 사이토카인 환경 속에서 미성숙 CD4+ T 세포는 Th1 또는 Th2 세포로 분화한다.이 중 Th1 반응은 IFN-γ를 포함한 사이토카인 분비를 통해 BCG 치료 효과와 밀접히 연관되며, 반대로 IL-10을 중심으로 한 Th2 반응은 BCG 실패와 관련된다. 실제로 IL-10 억제 또는 IFN-γ 증가가 Th1 우세 상태를 유도하며, 이는 BCG 매개 종양 퇴행에 필수적인 요소로 알려져 있다.이처럼 BCG는 Th1 면역 반응을 활성화함으로써 방광암이 유발하는 면역 억제 환경을 극복하는 데 효과적이지만, 환자 예후를 더 향상시키기 위해서는 보다 강력한 면역조절 능력을 가진 새로운 치료제의 개발이 필요하다.특히 BCG에 반응하지 않는 NMIBC는 예후가 불량하고 전통적으로 치료 옵션이 제한적이었다. 고위험 BCG-불응성 질환의 경우 근치적 방광 절제술이 표준 치료로 권고되지만, 모든 환자가 수술을 감내할 수 있는 것은 아니다.임상시험 기준으로 BCG의 초기 완전반응률은 유두종양에서 약 55~65%, CIS에서 70~75% 수준이다. 그러나 전체 NMIBC 환자의 약 3분의 1은 BCG에 전혀 반응하지 않으며, 초기 반응을 보인 환자의 약 절반도 결국 재발하거나 진행을 경험한다.미국 FDA는 BCG-불응성 NMIBC를 다음과 같이 정의한다: ▲ 적절한 BCG 요법 후 12개월 이내 지속성 또는 재발성 CIS, 또는 재발성 Ta/T1 질환이 있는 경우(초기 유도 6회 중 ≥5회, 유지 3회 중 ≥2회 또는 2차 유도 6회 중 ≥2회 투여 완료를 ‘적절한 요법’으로 정의), ▲ 적절한 BCG 요법 후 6개월 이내 재발한 고등급 Ta/T1 질환, ▲ 유도요법 후 첫 평가에서 고등급 T1 질환이 확인된 경우이다.Bacillus Calmette-Guérin(BCG)-불응성은 왜 일어나는가?BCG-불응성은 단일 요인보다는 종양 미세환경, 면역반응의 왜곡, 종양세포의 생물학적 저항성이 복합적으로 작용하여 발생한다. 일부 NMIBC는 이미 강한 면역억제 환경을 형성하고 있어, BCG가 유도하는 Th1 중심 면역 반응이 충분히 활성화되지 못한다.이들 종양에서는 IL-10과 TGF-β 같은 면역억제성 사이토카인이 증가하고, Treg와 MDSC가 축적되며, 종양세포의 PD-L1 발현도 높아져 T 세포 기능이 억제된다. 이러한 환경에서는 BCG가 방출시키는 사이토카인이 존재하더라도 Th1 분화보다는 Th2 또는 억제성 면역반응이 우세해져 IFN-γ 중심의 항종양 면역이 제대로 형성되지 않는다.또한 종양세포 자체가 BCG에 대한 내성을 가지는 경우도 있다. 상피세포 표면의 BCG 부착·내재화에 필요한 integrin 등 분자의 발현이 낮거나, BCG가 유도하는 세포사멸 신호(TRAIL, Fas 등)에 저항성을 나타내는 경우가 이에 해당한다. 일부 NMIBC는 특정 유전자 변이나 생존 신호의 과활성화로 인해 BCG 면역 반응에 본질적으로 둔감하다.여기에 고령, 기저질환, 면역노화 등 환자 요인이 더해지면 APC 활성 및 T 세포 반응성이 감소해 BCG가 충분한 면역 강화 효과를 내지 못한다. 균주 간 면역원성 차이, BCG 부족으로 인한 불충분한 치료 역시 면역반응 축적을 방해해 불응 위험을 높인다.결국 BCG 불응성은 종양 미세환경의 면역억제성, Th1 면역 활성화의 실패, 종양세포의 내재적 저항성, 그리고 숙주 면역 기능 저하가 상호 작용하여 나타나는 복합적 면역치료 실패 현상으로 이해된다. 이러한 이유로 BCG 불응성 NMIBC에서는 보다 강력한 면역조절 능력을 갖춘 새로운 치료 전략이 필요하다.인터루킨-15(IL-15)는 어떤 역할을 하는가?IL-15는 공통 γ사슬(γc) 사이토카인 패밀리에 속하는 면역 조절 인자로, 선천 면역과 적응 면역의 경계를 연결하며 항종양 면역을 강화하는 데 핵심적인 역할을 수행한다. IL-2, IL-4, IL-7, IL-9, IL-21과 함께 γc 계열을 이루는 IL-15는 특히 CD8+ T 세포와 자연살해(NK) 세포의 발달, 생존, 증식, 그리고 기능적 활성화 전반을 조절하는 중심적 사이토카인이다.Pleiotropic Effects of IL-15(출처: Cells 2023, 12, 1611).이러한 생물학적 중요성은 다양한 전임상·임상 연구에서 반복적으로 입증되어 왔으며, IL-15가 항암 면역을 유지하는 데 필수적인 조절자로 작용함을 뚜렷하게 보여준다.생리학적으로 IL-15는 IL-15 수용체 α(IL-15Rα)와 함께 이종이량체 형태로 합성된다. IL-15Rα는 자체적으로 신호 전달 기능을 갖고 있지는 않지만 IL-15에 높은 친화도로 결합하여 내질망에서 안정적인 복합체를 형성하고 이를 세포 표면까지 운반함으로써 생물학적 기능 발현을 위한 핵심적인 플랫폼을 제공한다.이 복합체는 생산 세포 표면에 제시된 뒤 인접한 수용 세포의 IL-2/IL-15Rβ와 공통 γ사슬과 결합하여 신호를 전달하는데, 이러한 ‘트랜스제시(trans-presentation)’는 IL-15 생물학을 규정하는 대표적 기전이자 IL-2와 구별되는 가장 특징적인 작동 방식이다.따라서 IL-15와 IL-15Rα는 단핵구, 대식세포, 수지상세포, 혈관내피세포, 골수 및 림프절의 기질세포 등 다양한 세포 유형에서 발현되며, 특히 수지상세포와 대식세포가 주요 생산자인 것으로 보고되었다. 이들 세포는 항원 제시뿐 아니라 IL-15 제시 기능을 통해 CD8+ T 세포와 NK 세포의 생존 신호를 제공함으로써 면역계의 항상성을 유지하는 데 기여한다.IL-15 초작용제(superagonist) 복합체는 무엇인가?최근 면역조절 치료제 개발은 기존 사이토카인 신호 경로를 선택적으로 증폭하여 항종양 면역 반응을 극대화하는 방향으로 진화하고 있으며, 그 중심에는 IL-15 경로 기반의 차세대 초작용제(superagonist) 기술이 있다.IL-15는 본래 NK 세포와 CD8⁺ T 세포의 생존, 증식, 기억 형성에 핵심적인 사이토카인이지만, 생체 내 반감기가 짧고 수용체 결합 효율이 낮아 단독 활용에는 한계가 있었다.이러한 제약을 극복하기 위해 고안된 IL-15 초작용제 복합체는 IL-15의 생물학적 활성을 비약적으로 증폭하도록 설계된 구조적 혁신체로, 대표적인 예가 IL-15N72D 변형체와 IL-15Rα의 sushi 도메인을 융합한 노가펜데킨 알파 인바키셉트이다.IL-15N72D는 아스파라긴(N)에서 아스파트산(D)으로의 단일 아미노산 치환을 통해 수용체 친화성과 신호전달 강도를 향상시킨 기능적 변형체이며, IL-15Rα의 sushi 도메인 결합을 통해 자연적인 trans-presentation 기전을 모사하도록 설계되었다.이 두 구성요소는 IgG1 Fc 영역과 융합되어 약물의 안정성, 체내 반감기, 조직 내 지속 시간을 획기적으로 개선하며, 그 결과 NK 세포와 CD8⁺ T 세포의 활성화 및 항종양 세포독성 반응을 장기간 유도하는 강력한 IL-15 신호 증폭체를 형성한다.이러한 기전은 기존 BCG 치료로 유도되는 국소 면역 반응을 효과적으로 증폭시키며, BCG-불응성 비근육침윤성 방광암에서 관찰되는 높은 완전관해율과 반응 지속성을 설명하는 면역학적 기반을 제공한다.결과적으로 IL-15 변형체와 IL-15Rα가 융합된 초작용제 플랫폼은 단순한 사이토카인 보충을 넘어, 정밀하게 설계된 면역 신호 조절을 통해 종양 미세환경 내에서 효과적인 항암 면역을 재활성화하려는 현대 면역항암제 개발의 중요한 패러다임을 제시한다노가펜데킨 알파 인바키셉트의 약리 기전은?노가펜데킨 알파 인바키셉트는 IL-15 돌연변이체(IL-15N72D)와 IL-15Rα를 융합한 복합체로, 자연 면역세포가 제공하는 IL-15 제시 기전을 모방한다. 이를 통해 CD8+ T 세포, NK 세포, 기억 T 세포의 증식·활성화를 강하게 유도하면서도, 면역억제성 조절 T 세포의 확장은 최소화한다.전임상 모델에서 방광 내 투여된 노가펜데킨 알파 인바키셉트는 단독 또는 BCG와 병용 시 BCG 단독보다 우수한 항종양 효과를 보였다. 또한 비융합(native) IL-15에 비해 림프조직 내 지속시간이 길고, 약동학적 안정성이 크게 향상되어 보다 강력하고 지속적인 항종양 면역반응을 유발한다.결과적으로 노가펜데킨 알파 인바키셉트는 IL-15 신호를 증폭해 킬러 T 세포 중심의 면역반응을 재가동시키는 기전적 특성을 기반으로, BCG-불응성 NMIBC에서 의미 있는 치료적 이점을 제공하는 IL-15 기반 면역증강제이다.Immune Effects of nogapendekin alfa inbakicept(출처: Cells 2023, 12, 1611).위 사진자료에 대해 설명하면, A. 노가펜데킨 알파 인바키셉트는 인간 IgG1 Fc와 융합된 IL15Rα에 결합된 돌연변이(N72D) 인간 IL-15로 구성된다. B. 노가펜데킨 알파 인바키셉트는 IL-15 수용체를 통해 순환 면역 세포에 결합한다. C. 노가펜데킨 알파 인바키셉트가 림프구에 결합하면 자연 살해(NK) 세포와 CD8+ T 세포 집단이 활성화된다되고 확장되어 고효과 CD56 dim 및 CD56 bright NK 세포와 중앙 기억 T 세포(TCM)가 확장된다. D. 비장 CD8+ T 세포 표면의 CXCR3가 상향 조절되면 종양 미세 환경(TME)으로 이동할 가능성이 높아집니다. 활성화된 NK 세포도 종양으로 이동한다. E. 활성화된 종양 침윤 CD8+ T 림프구(TIL)는 MHC 클래스 I 복합체가 제시하는 종양 관련 항원 에피토프를 인식하여 암세포를 인식한다. 활성화된 CD8+ T 세포와 NK 세포는 세포독성이 증가하여 암세포 사멸을 유도한다.CD8+ T 세포는 IFNγ 및 TNF⍺와 같은 Th1 사이토카인을 분비하여 염증성 TME를 촉진하고 과립구 및 단핵구 골수유래 억제 세포(MDSC)의 PD-L1을 상향 조절합니다. 노가펜데킨 알파 인바키셉트는 NK TIL이 TGF-β의 영향에 저항성을 갖도록 하고 항체 의존성 세포독성(ADCC)을 증가시킬 수 있도록 한다.노가펜데킨 알파 인바키셉트의 치료적 위치는?비근육침윤성 방광암(NMIBC)은 초기 치료로 경요도 방광종양절제술(TURBT)이 시행되지만, 재발률이 높고 병변이 지속·활성화되는 경우가 많아 반복적 치료가 필요하다. 특히 CIS를 동반한 고위험군에서는 BCG 치료가 표준으로 자리잡아 있으나, 충분한 BCG 노출에도 불구하고 재발·지속·진행이 나타나는 BCG-불응성 환자군이 적지 않다.이러한 환자에서 근치적 방광적출술(radical cystectomy)은 표준 치료로 권고되지만, 고령, 동반질환, 삶의 질 저하에 대한 우려, 환자 선호 등의 이유로 수술 적용이 어려운 경우가 많다. 이에 따라 방광을 보존하면서도 충분한 항종양 효과를 제공할 수 있는 새로운 치료 전략의 필요성이 지속적으로 제기되어 왔다.노가펜데킨 알파 인바키셉트는 IL-15/IL-15Rα 복합체 기반의 IL-15 초작동제로, CD8+ T 세포와 NK 세포의 증식·활성화를 강력하게 유도하는 면역 증강형 생물학적 제제이다. NMIBC에서 BCG 치료는 국소 면역활성에 의존하지만, BCG-불응성 환자에서는 방광 내 면역 미세환경의 소진, T/NK 세포 감소, BCG 반응 저하 등이 주요 병태생리로 지적된다.이러한 맥락에서 노가펜데킨 알파 인바키셉트는 고갈된 면역계를 다시 활성화하여 기존 BCG 효과를 강화하고, 단독 BCG로는 확보하기 어려운 항종양 면역반응을 확대하는 기전적 장점을 가진다.전신 면역관문억제제인 pembrolizumab(키트루다)은 일부 환자에서 의미 있는 완전반응을 유도하지만, 전신 면역 관련 부작용과 장기 치료에 따른 독성·비용 부담이 중요한 제약으로 남아 있다. 반면 노가펜데킨 알파 인바키셉트는 방광 내 국소 투여를 기반으로 하여 전신 독성이 극히 낮으며, 고령 또는 동반질환이 많은 실제 진료 환경에서 사용하기 용이하다.또한 바이러스 벡터를 이용하는 AAV 기반 유전자치료제(nadofaragene firadenovec)와 달리 벡터 노출에 따른 안전성 우려가 없고, 기존 BCG 치료 패턴과 자연스럽게 연계되어 임상적 채택성이 높다는 점도 장점이다.노가펜데킨 알파 인바키셉트의 임상적 의미는 단순한 반응률 개선을 넘어, BCG-불응성 CIS 환자에서 방광적출술을 지연하거나 회피할 수 있는 실질적 치료 대안을 제공한다는 데에 있다.실제 임상에서 의미 있는 완전반응률과 지속기간이 확인되었으며, 이는 방광적출술을 바로 시행하기 어려운 환자에게 중요한 시간적 여유와 치료 선택권을 제공한다. 전신 독성의 부담이 거의 없고, BCG 기반 면역작동 기전을 확장하는 방식이라는 점 또한 치료적 위치를 공고히 한다.노가펜데킨 알파 인바키셉트(ANKTIVA)의 허가임상은 어떠한가?ANKTIVA의 효능은 QUILT-3.032(NCT03022825) 시험에서 평가되었다. 이 연구는 경요도 방광종양절제술(TURBT) 이후 BCG에 반응하지 않는 고위험 비근육침윤성 방광암(NMIBC) 중 상피내암(CIS)을 동반한 성인 환자 77명을 대상으로 한 단일군, 다기관 임상시험이었다. 여기에는 Ta/T1 유두상 병변의 동반 여부와 상관없이 CIS를 가진 환자들이 포함되었다.BCG 불응성 고위험군 NMIBC의 CIS는, 충분한 BCG 치료를 완료한 후 12개월 이내에 CIS가 단독으로 또는 Ta/T1 병변과 함께 지속되거나 재발한 경우로 정의되었다. 충분한 BCG 치료는 초기 유도요법 6회 중 최소 5회를 투여하고, 이어서 유지요법 3회 중 최소 2회 또는 두 번째 유도요법 6회 중 최소 2회를 투여한 경우로 정의되었다.치료 전 Ta 또는 T1 병변 환자들은 절제가 가능한 모든 병변을 제거하기 위해 TURBT를 시행받았다. 절제, 소작 또는 전기소작이 불가능한 잔여 CIS는 허용되었다. 한편 근침윤성 방광암(T2~T4), 국소 진행성, 전이성 또는 방광 외부(요도, 요관, 신우) 침범이 있거나 그 병력이 있는 환자는 시험에서 제외되었다.환자들은 유도요법 동안 ANKTIVA 400mcg와 BCG를 주 1회, 6주 연속 투여받았다. 이후 질병이 없거나 저등급 질환을 가진 경우 4, 7, 10, 13, 19개월째에 3주 간격으로 주 1회 추가 투여를 받았다. 치료 3개월 시점에 CIS가 지속되거나 고등급 Ta 병변이 남아 있는 경우에는 두 번째 유도요법을 받을 수 있었다. 치료 25개월 시점에 완전반응(CR)이 유지되는 환자는 25, 31, 37개월째에 동일한 방식으로 추가 투여가 가능했다.종양 상태 평가는 최대 2년 동안 3개월마다 시행되었다. 24개월 이후의 반응 평가는 각 기관의 진료 기준에 따라 시행되었다. 치료 시작 후 첫 6개월 동안은 무작위 또는 방광경 유도 조직검사가 필수적으로 시행되었다. 주요 효능 평가지표는 어느 시점에서든 완전반응을 달성했는지와(방광경 검사 및 필요 시 TURBT/조직검사 결과 음성, 요세포검사 음성 기준) 그 반응의 지속기간이었다.등록 환자의 중앙 연령은 73세(범위 50~91세)였고, 86%가 남성이었다. 인종 분포는 백인 90%, 흑인 6%, 아시아인 1%, 아메리칸 인디언/알래스카 원주민 1%, 미상 1%였다. ECOG 수행능력은 0점이 83%, 1점이 17%였다.연구 등록 시 종양 특성은 CIS 단독 69%, CIS + Ta 병변 21%, CIS + T1(±Ta) 병변 10%였다. 기저 질환 상태는 불응성 43%, 재발성 57%였다. 이전 BCG 투여 횟수의 중앙값은 12회(범위 8~45회)였고, 13%는 분할 용량 BCG를 받은 경험이 있었다. 방광경 영상 방식은 백색광 57%, 청색광 또는 협대역 영상 40%, 미상 3%였다.효능 결과는 표 3에 제시되어 있으며, 전체 환자의 31%(24명)는 두 번째 유도요법을 받았다.노가펜데킨 알파 인바키셉트의 쟁점을 무엇인가?노가펜데킨 알파 인바키셉트는 IL-15의 생물학적 활성을 기반으로 설계된 차세대 면역작용제로, 고위험 BCG 불응성 비근침윤성 방광암(NMIBC) 치료에서 새로운 치료적 가능성을 제시하고 있다.IL-15는 CD8⁺ T 세포와 NK 세포의 생존과 기능을 강화하는 핵심 사이토카인으로 알려져 있으나, 자연 상태의 IL-15는 짧은 반감기, 불안정한 구조, 수용체 결합의 가변성 등으로 인해 치료제로 활용하는 데 본질적인 제약이 존재해왔다.노가펜데킨 알파 인바키셉트는 IL-15와 IL-15Rα 수용체 도메인을 결합해 형성한 안정적 이종이량체 기반의 IL-15 초작용제로, 내재 IL-15에 비해 우수한 생체 내 안정성과 장기적 면역 활성 유도가 가능하다는 점에서 임상적 의미가 크다.특히 BCG 치료에 반응하지 않는 NMIBC 환자는 방광적출술이 표준 치료임에도 불구하고, 고령 및 동반질환 등으로 수술이 어려운 경우가 많아 실질적인 치료 공백이 존재해왔다. 이러한 점에서 BCG와 병용하여 국소 종양 미세환경을 재활성화할 수 있는 약제의 개발은 방광보존 전략을 확장할 수 있는 새로운 치료 패러다임이라 할 수 있다.노가펜데킨 알파 인바키셉트의 주요 장점은 BCG와 병용 시 강력한 상승효과를 보인다는 점이다. IL-15Rα와의 결합을 통해 강화된 생물학적 활성은 APC, NK 세포, CD8⁺ T 세포의 집적과 기능을 촉진하여 항종양 면역반응을 증폭시키며, 이는 허가 근거가 된 QUILT-3.032 연구에서 3개월 완전반응률 53%, 12개월 반응 지속률 24~30%로 나타났다.이러한 치료 성적은 기존 BCG 불응 환자에서 보고된 방광내 요법의 성적을 상회하는 결과이며, 이 약제가 임상적으로 의미 있는 반응을 유도하는 면역치료제로 기능함을 보여준다.그러나 노가펜데킨 알파 인바키셉트는의 개발과 허가 과정에는 여러 한계와 도전이 병존한다. 가장 큰 문제는 근거 임상이 무작위 대조군이 없는 단일군(single-arm) 연구로 수행되었다는 점으로, 이는 약제의 효과를 BCG 재투여 효과와 명확히 구분하기 어렵게 만들며, 역사적 대조(historical control)와의 비교에서 발생할 수 있는 해석의 변이를 피하기 어렵다.또한 환자군 내 BCG 노출량, CIS 단독 여부, 종양 특성 등에서 이질성이 존재하여 반응률과 반응 지속성의 정확한 비교가 제한된다. 반응의 지속성 역시 완전반응을 보인 환자의 일부에서만 장기적으로 유지되는 경향이 관찰되었고, 12개월 이후 장기 추적자료는 아직 충분히 축적되지 않아 방광보존 전략의 장기적 안전성과 유효성에 대한 확정적 결론을 내리기 어렵다.더불어 치료효과의 기저에 있는 종양면역미세환경의 상태가 환자별로 크게 달라, 이 약제가 NK/T 세포 결핍 또는 극도로 억제된 미세환경을 충분히 회복시키지 못하는 경우가 존재할 것으로 예상되며, 이러한 점은 향후 바이오마커 기반 환자선택 전략의 필요성을 시사한다.이처럼 노가펜데킨 알파 인바키셉트는 IL-15 생물학을 임상적으로 구현한 최초의 치료제로서 BCG 불응성 NMIBC라는 미충족 의료수요 영역에서 실질적인 치료 옵션을 제공하고 있다.초기 반응률과 독성 프로파일은 고무적이지만, 단일군 연구 설계, 병용요법의 기여도 분리 문제, 반응 지속성의 제한, 장기 추적자료 부족 등은 여전히 해결해야 할 과제로 남아 있다.그럼에도 불구하고 노가펜데킨 알파 인바키셉트는 기존 치료제와는 차별화된 기전을 바탕으로 난치성 NMIBC에서 방광보존 전력을 확장할 수 있는 중요한 면역치료제로 자리매김할 가능성이 높으며, 향후 병용 전략, 내성 기전 규명, 예측 바이오마커 개발 등을 통해 그 임상적 가치가 더욱 강화될 것으로 기대된다.참고문헌 1. Grace Lui et al. “Exploiting an Interleukin-15 Heterodimeric Agonist (N803) for Effective Immunotherapy of Solid Malignancies” Cells 2023, 12(12), 1611. 3. Richard S et al. “Non–muscle-invasive Bladder Cancer: Overview and Contemporary Treatment Landscape of Neoadjuvant Chemoablative Therapies” Reviews in Urology, Vol. 22 No. 2 2020. 3. Jong Ho Park et al. “The Emerging Treatment of BCG (Bacillus Calmette-Guérin)- Unresponsive Non–Muscle-Invasive Bladder Cancer“ Journal of Urologic Oncology 2024;22(3):246-255. 4. Aiman Waheed et al. “Nogapendekin alfa inbakicept-PMLN: first approval milestone for BCG-unresponsive noninvasive bladder cancer: editorial” Annals of Medicine & Surgery (2024) 86:6386–6388. 5. Brian L. Heiss et al. “FDA Approval Summary: Nogapendekin Alfa Inbakicept-pmln with BCG for BCG-unresponsive carcinoma in situ” Clin Cancer Res. 2025 October 15; 31(20): 4223–4229. 6. Vikram M et al. “Mechanism of action of nadofaragene firadenovec-vncg” Front. Oncol. 14:1359725. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-11-20 17:29:43최병철 박사 -
종근당, 美 학회서 파이프라인 연구 성과 발표[데일리팜=최다은 기자] 종근당이 미국에서 열린 주요 국제 학회에서 항암제와 대사질환 치료제 등 핵심 파이프라인의 비임상 연구 성과를 잇달아 공개했다. 항체약물접합체(ADC), GLP-1 수용체 작용제, 면역항암제 등 혁신 신약 후보물질들의 연구 결과를 발표했다. 종근당은 지난 2일 미국 샌디에이고에서 열린 ‘World ADC 2025’에서 항체-약물 접합체(ADC) 기반 항암 신약 후보물질 ‘CKD-703’의 비임상 연구 결과를 발표했다.CKD-703은 종근당이 독자 개발한 간세포성장인자 수용체(c-Met) 타겟의 단일클론항체에 차세대 ADC 플랫폼 기술을 적용해 개발 중인 약물이다. 암세포만을 선택적으로 사멸시키는 기전을 가지고 있다. 지난 7월 미국 FDA로부터 임상 1·2a상 승인을 받아 비소세포폐암 및 고형암 환자를 대상으로 임상을 진행하고 있다.비임상 연구에서 CKD-703은 ▲c-Met에 대한 높은 결합 특이성과 암세포 내부로의 신속한 전달(internalization) 능력 ▲균일한 약물 결합 비율(DAR)과 향상된 혈중 안정성 ▲Fcγ 수용체 결합 최소화에 따른 내약성 개선 ▲다양한 c-Met 발현 모델에서 확인된 탁월한 종양 억제 효과를 보였다.지난 4일 미국 애틀란타에서 열린 ‘2025 미국비만학회(2025 Obesity Week)’에서는 경구용 GLP-1 수용체 작용제(GLP-1RA) 신약 후보물질 ‘CKD-514’의 비임상 연구 성과를 발표했다.종근당에 따르면 CKD-514는 용해도 개선을 통한 구조적 이점을 바탕으로 대동물 모델에서 우수한 경구 생체이용률(Dog BA)을 보였다. 경구용 비만치료제 오포글리프론(Orforglipron) 대비 적은 용량에서 체중 감소 효과와 동일 용량 대비 혈당 강하 효과를 나타냈다.CKD-514의 후속 화합물군 역시 오포글리프론과 세마글루타이드(Semaglutide)와의 비교 시험에서 두 약물과 동등하거나 우월한 대사 개선 효과가 있음을 확인했다는 것이 종근당 측 설명이다.지난 7일 미국 메릴랜드에서 열린 ‘2025 미국면역항암학회(SITC 2025)’에서 아데노신 A2A 수용체(A2AR) 길항제 신약 후보물질 ‘CKD-512’의 비임상 연구 결과를 발표했다.CKD-512는 종양미세환경에서 면역세포의 항종양 활성을 억제하는 아데노신 신호 전달 경로를 차단하는 면역항암 신약 후보물질이다. 현재 국내에서 임상 1상이 진행 중이며 대만에서도 임상 1상 승인을 받아 임상을 준비 중이다.CKD-512는 ▲A2A 수용체에 대한 높은 결합 친화력과 우수한 지속성을 통한 강력한 수용체 차단 과 ▲아데노신 농도가 높은 종양미세환경과 유사한 조건에서의 안정적인 면역세포 기능 회복 ▲T세포 활성 억제 신호 경로인 phospho-CREB 발현 억제 및 주변 면역세포 활성 증대를 통한 종양 내 전반적 면역 반응 강화 ▲면역관문억제제(ICI) 및 표준 항암치료와의 병용 시 강력한 항종양 시너지 효과 등 기존 임상 개발 중인 A2AR 길항제 대비 차별화된 약물학적 특성을 나타내고 있다.종근당 관계자는 "ADC 항암제부터 비만치료제, 면역항암제까지 종근당 혁신 파이프라인의 개발 경쟁력을 글로벌 무대에서 확인했다"며 "각 파이프라인의 차별화된 약물학적 특성과 비임상 성과를 바탕으로 혁신신약 개발을 앞당겨 나갈 것"이라고 말했다.2025-11-10 10:43:27최다은
-
 SITC2025 개막…국내 기업 면역항암 전략 '고도화'[데일리팜=황병우 기자] 미국 메릴랜드에서 열리는 미국면역항암학회(SITC 2025)에서 국내 제약·바이오 기업들이 면역반응의 조건과 병용요법 전략을 중심으로 한 연구 성과를 연이어 공개한다.올해로 40주년을 맞은 SITC는 면역반응의 작동 조건과 병용 효율을 중심으로 치료 전략이 논의되는 학회다.SITC2025는 11월 5일(현지시간) 사전 프로그램(Pre-Conference Program)을 시작으로 오는 7일부터 메인 발표가 시작될 예정이다. 최근 국내 면역항암제 파이프라인이 면역항암제의 반응 범위를 확장해 ‘다르게 듣는 방법’을 찾기 위한 전략을 추구하는 만큼 SITC의 문을 두드리는 기업도 늘어나는 추세다.이번 학회에서 국내 기업들은 환자 선별, 종양미세환경 조절, 신규 타깃 발굴, 병용 설계 최적화 등 서로 다른 접근을 통해 면역반응의 적용 범위를 넓히는 전략을 제시했다.루닛, AI 기반 면역환경 정량화로 환자 선택 기준 고도화먼저 지난해 여러 암종의 면역항암제 치료 반응 예측 연구를 발표했던 루닛은 올해도 AI 바이오마커 플랫폼 루닛 스코프를 활용한 연구초록 2편을 공개한다.연구는 AI 기반 종양미세환경 분석을 통한 비소세포폐암, 대장암 및 요로상피암의 면역표현형 식별 연구와 이 AI 기반 정량적 면역조직염색(IHC) 분석을 통한 종양관련항원과 림프구 간 공간적 상관관계 규명 연구가 포함된다.앞서 ESMO2025에서 루닛은 새로운 검사나 조직 채취 없이 기존 H&E(Hematoxylin & Eosin-stained slide) 슬라이드만으로 종양미세환경을 정량화해 치료 반응을 예측한 연구를 발표한 바 있다.AI 기반 TME 분석은 면역항암 효과가 나타날 가능성이 높은 환자를 사전에 구획하는 데 활용될 수 있어, 임상 설계 단계에서 선별·배제 기준과 병용 요법 시 투여 시점 결정 등에 직접적인 영향을 줄 수 있다는 점이 강조된다.서범석 루닛 대표는 "루닛 스코프는 글로벌 산학계에서 점차 인정받으며 치료반응 예측 AI 솔루션의 선도적 위치를 확보해가고 있다"며 "지속 성장하고 있는 면역항암제 시장에서 치료 효과 예측이라는 핵심 과제를 해결하는 기술로서 환자 맞춤형 정밀의료 실현에 기여하겠다"고 말했다.티움바이오, TU2218 기반 두경부암 병용 전략 공개티움바이오는 TGF-β/VEGF 경로를 동시에 억제하는 면역조절 신약 TU2218과 키트루다 병용요법의 재발·전이성 두경부암 임상 2상 중간 데이터를 최초로 발표할 예정이다.두경부암은 면역침투 저하와 미세환경 내 억제 신호에 의해 면역항암제 단독요법의 반응 유지가 어려운 대표적 암종으로 알려져 있다.TU2218은 면역세포 활성 억제 경로(TGF-β)와 종양 접근을 방해하는 혈관구조 조절(VEGF) 에 동시에 개입하는 구조를 갖고 있어, 면역반응이 작동할 수 있는 환경을 회복하는 접근으로 개발 중이다.현재 승인된 두경부암 1차 치료제로는 키트루다 단독요법, 키트루다와 화학요법 병용요법 그리고 세툭시맙과 화학요법 병용요법이 사용되고 있지만 치료반응 및 지속기간의 미충족수요가 있는 상황이다.김훈택 티움바이오 대표는 "이번 발표를 통해 TU2218의 항암제로서의 가능성과 가치를 전세계에 본격적으로 알리고, 치료제로서의 허가 및 글로벌 사업화를 목표로 개발을 가속화할 것"이라고 전했다.에스티큐브…BTN1A1 기반 면역반응 재가동 전략, PD-1 한계 보완 시도퍼스트인클래스(first-in-class) 신약을 노리는 에스티큐브는 SITC에서 BTN1A1 을 표적하는 항체 넬마스토바트의 전이성 대장암 대상 회사주도 1b/2상 초기 데이터를 발표한다.BTN1A1은 종양미세환경에서 CD8⁺ T세포 활성을 억제하는 면역조절 인자로 보고돼 있으며, PD-L1 발현과 독립적으로 암조직에서 높게 발현되는 특징이며, PD-L1 비발현·내성암 환자에서 새로운 면역반응 경로 확보 가능성이 연구되고 있다.이번 SITC에서는 총 4건의 초록이 채택됐으며, 이 중 2건은 LBA(Late-Breaking Abstract, 최신 임상연구 초록)로 선정됐다.구체적으로 발표는 항BTN1A1 항체 넬마스토바트와 TAS-102·베바시주맙 병용요법, 카페시타빈 병용요법을 중심으로 구성됐다.특히 PD-L1 발현 여부와 무관하게 암세포에서 발현되는 특성이 있으며, 이를 바탕으로 PD-L1 비발현·내성암 환자군에서 면역반응 회복 가능성을 확보하는 전략이 제시되고 있다.이번 발표의 의미는 표준치료제 기반 병용 전략에서 연속적인 초기 항암 활성과 내약성 신호가 확인됐다는 점이다.대상 환자군이 3차 치료 이상 전이성 대장암이라는 점을 고려하면, 치료 대안이 필요한 환자층에서 새로운 접근 가능성을 가늠하는 단계로 해석된다. 임상은 1b상을 마치고 현재 2상 환자 등록이 진행 중이다.에스티큐브 관계자는 "이번 대장암 임상 2건의 초기 및 중간 결과 발표는 향후 글로벌 제약사와의 협력 및 기술이전 논의에 있어 전략적 추진력을 확보하는 기반이 될 것으로 기대한다"고 밝혔다.셀트리온 , HER2 표적 다중항체 데이터 발표셀트리온은 HER2 표적 다중항체 면역항암제 CT-P72/ABP-102의 전임상 데이터를 발표한다.CT-P72/ABP-102는 셀트리온이 미국 에이비프로(Abpro)와 공동 개발 중인 다중항체 면역항암제로 HER2 발현 종양세포와 T세포를 연결해 세포 간 면역반응을 직접 유도하는 T세포 인게이저(TCE) 기반 구조를 갖는다.전임상에서는 HER2 고발현 종양에서 선택적 항암 활성이 관찰됐으며, 영장류 모델에서 고용량에서도 안전성 신호가 유지된 것으로 보고됐다.아직 전임상 단계인 만큼 추후 연구의 확장이 필요하지만 엔허투 내성이 있는 암세포의 치료 효과 비교한 동물 실험에서 CT-P72/ABP-102는 유의미한 종양성장억제능력을 나타낸 만큼 새로운 치료옵션에 대한 가능성을 보였다는 평가다.셀트리온은 이번 전임상 결과를 토대로 연내 국내외 주요 기관에 CT-P72/ABP-102의 1상 임상시험계획(IND)을 제출하고 본격적인 임상시험에 진입한다는 계획이다.셀트리온 관계자는 "다중항체 항암신약 CT-P72/ABP-102는 전임상을 통해 우수한 효능과 안전성을 확인하며 이번 SITC 2025에서 TOP 150 연구로 선정되는 등 높은 관심을 받고 있다"며 "향후에도 임상을 성공적으로 진행해 기존 약물보다 우수한 베스트 인 클래스 신약으로 개발할 수 있도록 최선을 다할 것"이라고 말했다.신라젠, BAL0891 면역관문억제제 시너지 가능성 발표 신라젠은 TTK/PLK1 이중 억제제 BAL0891과 면역관문억제제(ICI) 병용 전략 연구 2건을 포스터 발표할 예정이다.먼저 인체 조직을 모사한 종양미세환경 플랫폼 및 약리 모델링을 이용해 BAL0891의 면역 조절 최적화를 통한 ICI 병용 전략 가능성을 평가한 결과가 발표된다.또 BAL0891과 티슬렐리주맙을 병용하는 1상 연구에 대한 소개도 이뤄진다. 해당 연구는 미국·한국에서 약 30명 규모로 진행될 계획이다.신라젠 관계자는 "세계 최고 권위 학회 중 하나인 미국면역항암학회에서 BAL0891 연구 두 건이 채택된 배경에는 당사 및 관련 연구자들의 지속적인 노력이 수반되어 가능했다"며 "BAL0891과 면역관문억제제의 병용 조합에 대한 학계의 관심이 높은 만큼 티슬렐리주맙과의 병용 임상에서 좋은 결과를 도출해 혁신적인 암 치료 옵션을 제공할 수 있도록 최선을 다하겠다"라고 말했다.2025-11-06 12:00:28황병우
SITC2025 개막…국내 기업 면역항암 전략 '고도화'[데일리팜=황병우 기자] 미국 메릴랜드에서 열리는 미국면역항암학회(SITC 2025)에서 국내 제약·바이오 기업들이 면역반응의 조건과 병용요법 전략을 중심으로 한 연구 성과를 연이어 공개한다.올해로 40주년을 맞은 SITC는 면역반응의 작동 조건과 병용 효율을 중심으로 치료 전략이 논의되는 학회다.SITC2025는 11월 5일(현지시간) 사전 프로그램(Pre-Conference Program)을 시작으로 오는 7일부터 메인 발표가 시작될 예정이다. 최근 국내 면역항암제 파이프라인이 면역항암제의 반응 범위를 확장해 ‘다르게 듣는 방법’을 찾기 위한 전략을 추구하는 만큼 SITC의 문을 두드리는 기업도 늘어나는 추세다.이번 학회에서 국내 기업들은 환자 선별, 종양미세환경 조절, 신규 타깃 발굴, 병용 설계 최적화 등 서로 다른 접근을 통해 면역반응의 적용 범위를 넓히는 전략을 제시했다.루닛, AI 기반 면역환경 정량화로 환자 선택 기준 고도화먼저 지난해 여러 암종의 면역항암제 치료 반응 예측 연구를 발표했던 루닛은 올해도 AI 바이오마커 플랫폼 루닛 스코프를 활용한 연구초록 2편을 공개한다.연구는 AI 기반 종양미세환경 분석을 통한 비소세포폐암, 대장암 및 요로상피암의 면역표현형 식별 연구와 이 AI 기반 정량적 면역조직염색(IHC) 분석을 통한 종양관련항원과 림프구 간 공간적 상관관계 규명 연구가 포함된다.앞서 ESMO2025에서 루닛은 새로운 검사나 조직 채취 없이 기존 H&E(Hematoxylin & Eosin-stained slide) 슬라이드만으로 종양미세환경을 정량화해 치료 반응을 예측한 연구를 발표한 바 있다.AI 기반 TME 분석은 면역항암 효과가 나타날 가능성이 높은 환자를 사전에 구획하는 데 활용될 수 있어, 임상 설계 단계에서 선별·배제 기준과 병용 요법 시 투여 시점 결정 등에 직접적인 영향을 줄 수 있다는 점이 강조된다.서범석 루닛 대표는 "루닛 스코프는 글로벌 산학계에서 점차 인정받으며 치료반응 예측 AI 솔루션의 선도적 위치를 확보해가고 있다"며 "지속 성장하고 있는 면역항암제 시장에서 치료 효과 예측이라는 핵심 과제를 해결하는 기술로서 환자 맞춤형 정밀의료 실현에 기여하겠다"고 말했다.티움바이오, TU2218 기반 두경부암 병용 전략 공개티움바이오는 TGF-β/VEGF 경로를 동시에 억제하는 면역조절 신약 TU2218과 키트루다 병용요법의 재발·전이성 두경부암 임상 2상 중간 데이터를 최초로 발표할 예정이다.두경부암은 면역침투 저하와 미세환경 내 억제 신호에 의해 면역항암제 단독요법의 반응 유지가 어려운 대표적 암종으로 알려져 있다.TU2218은 면역세포 활성 억제 경로(TGF-β)와 종양 접근을 방해하는 혈관구조 조절(VEGF) 에 동시에 개입하는 구조를 갖고 있어, 면역반응이 작동할 수 있는 환경을 회복하는 접근으로 개발 중이다.현재 승인된 두경부암 1차 치료제로는 키트루다 단독요법, 키트루다와 화학요법 병용요법 그리고 세툭시맙과 화학요법 병용요법이 사용되고 있지만 치료반응 및 지속기간의 미충족수요가 있는 상황이다.김훈택 티움바이오 대표는 "이번 발표를 통해 TU2218의 항암제로서의 가능성과 가치를 전세계에 본격적으로 알리고, 치료제로서의 허가 및 글로벌 사업화를 목표로 개발을 가속화할 것"이라고 전했다.에스티큐브…BTN1A1 기반 면역반응 재가동 전략, PD-1 한계 보완 시도퍼스트인클래스(first-in-class) 신약을 노리는 에스티큐브는 SITC에서 BTN1A1 을 표적하는 항체 넬마스토바트의 전이성 대장암 대상 회사주도 1b/2상 초기 데이터를 발표한다.BTN1A1은 종양미세환경에서 CD8⁺ T세포 활성을 억제하는 면역조절 인자로 보고돼 있으며, PD-L1 발현과 독립적으로 암조직에서 높게 발현되는 특징이며, PD-L1 비발현·내성암 환자에서 새로운 면역반응 경로 확보 가능성이 연구되고 있다.이번 SITC에서는 총 4건의 초록이 채택됐으며, 이 중 2건은 LBA(Late-Breaking Abstract, 최신 임상연구 초록)로 선정됐다.구체적으로 발표는 항BTN1A1 항체 넬마스토바트와 TAS-102·베바시주맙 병용요법, 카페시타빈 병용요법을 중심으로 구성됐다.특히 PD-L1 발현 여부와 무관하게 암세포에서 발현되는 특성이 있으며, 이를 바탕으로 PD-L1 비발현·내성암 환자군에서 면역반응 회복 가능성을 확보하는 전략이 제시되고 있다.이번 발표의 의미는 표준치료제 기반 병용 전략에서 연속적인 초기 항암 활성과 내약성 신호가 확인됐다는 점이다.대상 환자군이 3차 치료 이상 전이성 대장암이라는 점을 고려하면, 치료 대안이 필요한 환자층에서 새로운 접근 가능성을 가늠하는 단계로 해석된다. 임상은 1b상을 마치고 현재 2상 환자 등록이 진행 중이다.에스티큐브 관계자는 "이번 대장암 임상 2건의 초기 및 중간 결과 발표는 향후 글로벌 제약사와의 협력 및 기술이전 논의에 있어 전략적 추진력을 확보하는 기반이 될 것으로 기대한다"고 밝혔다.셀트리온 , HER2 표적 다중항체 데이터 발표셀트리온은 HER2 표적 다중항체 면역항암제 CT-P72/ABP-102의 전임상 데이터를 발표한다.CT-P72/ABP-102는 셀트리온이 미국 에이비프로(Abpro)와 공동 개발 중인 다중항체 면역항암제로 HER2 발현 종양세포와 T세포를 연결해 세포 간 면역반응을 직접 유도하는 T세포 인게이저(TCE) 기반 구조를 갖는다.전임상에서는 HER2 고발현 종양에서 선택적 항암 활성이 관찰됐으며, 영장류 모델에서 고용량에서도 안전성 신호가 유지된 것으로 보고됐다.아직 전임상 단계인 만큼 추후 연구의 확장이 필요하지만 엔허투 내성이 있는 암세포의 치료 효과 비교한 동물 실험에서 CT-P72/ABP-102는 유의미한 종양성장억제능력을 나타낸 만큼 새로운 치료옵션에 대한 가능성을 보였다는 평가다.셀트리온은 이번 전임상 결과를 토대로 연내 국내외 주요 기관에 CT-P72/ABP-102의 1상 임상시험계획(IND)을 제출하고 본격적인 임상시험에 진입한다는 계획이다.셀트리온 관계자는 "다중항체 항암신약 CT-P72/ABP-102는 전임상을 통해 우수한 효능과 안전성을 확인하며 이번 SITC 2025에서 TOP 150 연구로 선정되는 등 높은 관심을 받고 있다"며 "향후에도 임상을 성공적으로 진행해 기존 약물보다 우수한 베스트 인 클래스 신약으로 개발할 수 있도록 최선을 다할 것"이라고 말했다.신라젠, BAL0891 면역관문억제제 시너지 가능성 발표 신라젠은 TTK/PLK1 이중 억제제 BAL0891과 면역관문억제제(ICI) 병용 전략 연구 2건을 포스터 발표할 예정이다.먼저 인체 조직을 모사한 종양미세환경 플랫폼 및 약리 모델링을 이용해 BAL0891의 면역 조절 최적화를 통한 ICI 병용 전략 가능성을 평가한 결과가 발표된다.또 BAL0891과 티슬렐리주맙을 병용하는 1상 연구에 대한 소개도 이뤄진다. 해당 연구는 미국·한국에서 약 30명 규모로 진행될 계획이다.신라젠 관계자는 "세계 최고 권위 학회 중 하나인 미국면역항암학회에서 BAL0891 연구 두 건이 채택된 배경에는 당사 및 관련 연구자들의 지속적인 노력이 수반되어 가능했다"며 "BAL0891과 면역관문억제제의 병용 조합에 대한 학계의 관심이 높은 만큼 티슬렐리주맙과의 병용 임상에서 좋은 결과를 도출해 혁신적인 암 치료 옵션을 제공할 수 있도록 최선을 다하겠다"라고 말했다.2025-11-06 12:00:28황병우 -
 에스티큐브, SITC서 대장암 자체 임상 첫 성과 발표[데일리팜=황병우 기자] 에스티큐브가 회사 주도의 전이성 대장암 첫 임상 데이터를 미국면역항암학회(SITC 2025)에서 발표한다.발표에는 넬마스토바트 병용요법의 전이성 대장암 대상 1b/2상 초기 데이터(1b상)와 연구자임상 중간 분석 결과가 포함된다.특히 넬마스토바트와 TAS-102(트리플루리딘-티피라실), 베바시주맙 병용요법에 대한 임상 데이터가 최초로 공개된다는 점에서 기대가 모아지고 있다.에스티큐브는 오는 7~9일 미국 메릴랜드주에서 열리는 SITC 2025에 참가해 항BTN1A1 면역관문억제제 넬마스토바트의 전이성 대장암 임상 결과와 신규 면역항암 타깃 BTN1A1 관련 최신 연구 성과를 발표한다고 3일 밝혔다.SITC는 면역항암 분야 최고 권위의 국제학술대회로, 글로벌 제약사 및 투자자들의 이목이 집중되는 행사다.BTN1A1은 에스티큐브가 독자 발굴한 면역관문단백질로, 종양미세환경 내 CD8⁺ T세포 활성을 억제하는 데 관여한다.에스티큐브는 BTN1A1 차단을 통해 항암면역반응을 강화할 수 있음을 다양한 종양 모델에서 확인했으며, 현재 대장암과 비소세포폐암을 대상으로 임상 2상을 진행 중이다.BTN1A1은 PD-1/PD-L1의 한계를 보완할 차세대 면역관문 타깃으로, 에스티큐브 면역항암 플랫폼의 핵심 자산으로 개발되고 있다.이번 SITC에서는 총 4건의 초록이 채택됐으며, 이 중 2건은 LBA(Late-Breaking Abstract, 최신 임상연구 초록)로 선정됐다.LBA에는 전이성 대장암을 대상으로 한 ▲넬마스토바트+TAS-102+베바시주맙 병용 임상 1b/2상 초기 결과(제목: Nelmastobart Combination Shows Excellent Tolerability and Early Antitumor Activity in Refractory mCRC) ▲넬마스토바트+카페시타빈 병용 연구자임상 1b/2상 중간 결과(제목: A Phase 1b/2 Study of Nelmastobart with Capecitabine in Patients with Refractory mCRC)가 포함됐다.두 연구는 모두 3차 치료 이상의 전이성 대장암 환자를 대상으로 진행됐으며, 넬마스토바트를 기반으로 한 표준치료제 병용요법에서 우수한 내약성과 항암 활성이 확인됐다.이번 결과는 넬마스토바트 병용 전략의 임상 확장성과 사업개발 논의를 뒷받침하는 핵심 자료로, 상세 데이터는 학회 발표를 통해 공개될 예정이다.이 중 넬마스토바트와 TAS-102, 베바시주맙 병용 임상 1b/2상은 1b상(6명) 완료 후 현재 2상 환자등록이 진행되고 있다.임상 2상은 BTN1A1 TPS(종양비율점수) 50% 이상 환자를 대상으로 한 바이오마커 기반 설계로, 개시 2개월 만에 목표 환자수 52명 중 18명(1b상 5명, 2상 13명)의 투약이 시작됐다. 환자 스크리닝 및 등록이 빠르게 이뤄지고 있어, 연내 환자등록 완료를 목표로 하고 있다.정규 초록에서는 BTN1A1의 면역억제 기전과 바이오마커 지표 관련 최신 연구성과가 소개된다.초록 제목은 ▲BTN1A1 Expression is Inversely Associated with CD8⁺ T Cell Infiltration in the Tumor Microenvironment of Lung and Colon Cancer(BTN1A1 발현은 폐암 및 대장암 종양미세환경 내 CD8⁺ T세포 침윤과 역상관 관계) ▲BTN1A1 Blockade Enhances Chemotherapy-Induced Anti-Tumor Immunity in Preclinical Lung Cancer Models(BTN1A1 억제는 폐암 전임상 모델에서 화학항암제로 유도된 항종양 면역반응을 강화)다.에스티큐브 관계자는 "BTN1A1 기반 면역항암 플랫폼은 기초 연구부터 임상 2상에 이르기까지 전주기에 걸쳐 과학적 타당성과 학술적 가치, 글로벌 경쟁력을 축적해 왔다"며 "이번 대장암 임상 2건의 초기 및 중간 결과 발표는 향후 글로벌 제약사와의 협력 및 기술이전 논의에 있어 전략적 추진력을 확보하는 기반이 될 것으로 기대한다"고 밝혔다.2025-11-03 17:28:17황병우
에스티큐브, SITC서 대장암 자체 임상 첫 성과 발표[데일리팜=황병우 기자] 에스티큐브가 회사 주도의 전이성 대장암 첫 임상 데이터를 미국면역항암학회(SITC 2025)에서 발표한다.발표에는 넬마스토바트 병용요법의 전이성 대장암 대상 1b/2상 초기 데이터(1b상)와 연구자임상 중간 분석 결과가 포함된다.특히 넬마스토바트와 TAS-102(트리플루리딘-티피라실), 베바시주맙 병용요법에 대한 임상 데이터가 최초로 공개된다는 점에서 기대가 모아지고 있다.에스티큐브는 오는 7~9일 미국 메릴랜드주에서 열리는 SITC 2025에 참가해 항BTN1A1 면역관문억제제 넬마스토바트의 전이성 대장암 임상 결과와 신규 면역항암 타깃 BTN1A1 관련 최신 연구 성과를 발표한다고 3일 밝혔다.SITC는 면역항암 분야 최고 권위의 국제학술대회로, 글로벌 제약사 및 투자자들의 이목이 집중되는 행사다.BTN1A1은 에스티큐브가 독자 발굴한 면역관문단백질로, 종양미세환경 내 CD8⁺ T세포 활성을 억제하는 데 관여한다.에스티큐브는 BTN1A1 차단을 통해 항암면역반응을 강화할 수 있음을 다양한 종양 모델에서 확인했으며, 현재 대장암과 비소세포폐암을 대상으로 임상 2상을 진행 중이다.BTN1A1은 PD-1/PD-L1의 한계를 보완할 차세대 면역관문 타깃으로, 에스티큐브 면역항암 플랫폼의 핵심 자산으로 개발되고 있다.이번 SITC에서는 총 4건의 초록이 채택됐으며, 이 중 2건은 LBA(Late-Breaking Abstract, 최신 임상연구 초록)로 선정됐다.LBA에는 전이성 대장암을 대상으로 한 ▲넬마스토바트+TAS-102+베바시주맙 병용 임상 1b/2상 초기 결과(제목: Nelmastobart Combination Shows Excellent Tolerability and Early Antitumor Activity in Refractory mCRC) ▲넬마스토바트+카페시타빈 병용 연구자임상 1b/2상 중간 결과(제목: A Phase 1b/2 Study of Nelmastobart with Capecitabine in Patients with Refractory mCRC)가 포함됐다.두 연구는 모두 3차 치료 이상의 전이성 대장암 환자를 대상으로 진행됐으며, 넬마스토바트를 기반으로 한 표준치료제 병용요법에서 우수한 내약성과 항암 활성이 확인됐다.이번 결과는 넬마스토바트 병용 전략의 임상 확장성과 사업개발 논의를 뒷받침하는 핵심 자료로, 상세 데이터는 학회 발표를 통해 공개될 예정이다.이 중 넬마스토바트와 TAS-102, 베바시주맙 병용 임상 1b/2상은 1b상(6명) 완료 후 현재 2상 환자등록이 진행되고 있다.임상 2상은 BTN1A1 TPS(종양비율점수) 50% 이상 환자를 대상으로 한 바이오마커 기반 설계로, 개시 2개월 만에 목표 환자수 52명 중 18명(1b상 5명, 2상 13명)의 투약이 시작됐다. 환자 스크리닝 및 등록이 빠르게 이뤄지고 있어, 연내 환자등록 완료를 목표로 하고 있다.정규 초록에서는 BTN1A1의 면역억제 기전과 바이오마커 지표 관련 최신 연구성과가 소개된다.초록 제목은 ▲BTN1A1 Expression is Inversely Associated with CD8⁺ T Cell Infiltration in the Tumor Microenvironment of Lung and Colon Cancer(BTN1A1 발현은 폐암 및 대장암 종양미세환경 내 CD8⁺ T세포 침윤과 역상관 관계) ▲BTN1A1 Blockade Enhances Chemotherapy-Induced Anti-Tumor Immunity in Preclinical Lung Cancer Models(BTN1A1 억제는 폐암 전임상 모델에서 화학항암제로 유도된 항종양 면역반응을 강화)다.에스티큐브 관계자는 "BTN1A1 기반 면역항암 플랫폼은 기초 연구부터 임상 2상에 이르기까지 전주기에 걸쳐 과학적 타당성과 학술적 가치, 글로벌 경쟁력을 축적해 왔다"며 "이번 대장암 임상 2건의 초기 및 중간 결과 발표는 향후 글로벌 제약사와의 협력 및 기술이전 논의에 있어 전략적 추진력을 확보하는 기반이 될 것으로 기대한다"고 밝혔다.2025-11-03 17:28:17황병우 -
 난소암 면역항암 새 전기…'키트루다' 첫 생존 근거 제시[베를린 2025 ESMO=황병우 기자] 난소암에서도 면역항암제가 생존기간을 유의하게 연장한 첫 근거가 나왔다.MSD의 키트루다(펨브롤리주맙) 병용요법이 플래티넘 내성 재발성 난소암 환자를 대상으로 한 3상 임상시험에서 무진행생존기간(PFS)과 전체생존기간(OS) 모두에서 유의한 개선을 보였다.이번 결과는 난소암에서 면역항암제가 생존이득을 입증한 첫 무작위 3상 임상으로 평가된다.KEYNOTE-B96 연구 발표 전경 지난 18일(현지시간) 유럽임상종양학회 연례학술회의(ESMO 2025)에서는 이전에 한 가지 이상의 백금기반 항암화학요법을 포함, 1~2차 전신 항암치료를 받은 난소암 환자 중 1차 치료에서 4주기 이상 백금기반 요법을 시행했으나 마지막 투약 후 6개월 이내에 질병이 진행된 백금 내성 환자를 대상으로 키트루다를 평가한 3상 임상, KEYNOTE-B96 연구 결과가 공개됐다.KEYNOTE-B96 연구는 유럽부인암임상연구그룹(ENGOT)과 MSD가 공동으로 수행한 다국가, 무작위, 이중맹검 3상 임상으로 1~2차 항암치료 후 6개월 이내 재발한 플래티넘 내성 상피성 난소암, 난관암, 복막암 환자 643명이 참여했다.환자들은 1:1로 키트루다(400mg, 6주 간격) 또는 플라시보를 투여받았으며, 각각 주간 파클리탁셀(80mg/m², 3주 주기 중 1·8·15일) 및 베바시주맙(10mg/kg, 2주 간격, 선택적 병용)과 병용했다.1차 중간분석(추적 15.6개월) 결과, 전체 모집단(ITT) 기준 PFS 중앙값은 키트루다 병용군 8.3개월, 대조군 6.4개월 그리고 위험비(HR)는 0.70(95% CI 0.58–0.84, P2025-10-19 20:06:13황병우
난소암 면역항암 새 전기…'키트루다' 첫 생존 근거 제시[베를린 2025 ESMO=황병우 기자] 난소암에서도 면역항암제가 생존기간을 유의하게 연장한 첫 근거가 나왔다.MSD의 키트루다(펨브롤리주맙) 병용요법이 플래티넘 내성 재발성 난소암 환자를 대상으로 한 3상 임상시험에서 무진행생존기간(PFS)과 전체생존기간(OS) 모두에서 유의한 개선을 보였다.이번 결과는 난소암에서 면역항암제가 생존이득을 입증한 첫 무작위 3상 임상으로 평가된다.KEYNOTE-B96 연구 발표 전경 지난 18일(현지시간) 유럽임상종양학회 연례학술회의(ESMO 2025)에서는 이전에 한 가지 이상의 백금기반 항암화학요법을 포함, 1~2차 전신 항암치료를 받은 난소암 환자 중 1차 치료에서 4주기 이상 백금기반 요법을 시행했으나 마지막 투약 후 6개월 이내에 질병이 진행된 백금 내성 환자를 대상으로 키트루다를 평가한 3상 임상, KEYNOTE-B96 연구 결과가 공개됐다.KEYNOTE-B96 연구는 유럽부인암임상연구그룹(ENGOT)과 MSD가 공동으로 수행한 다국가, 무작위, 이중맹검 3상 임상으로 1~2차 항암치료 후 6개월 이내 재발한 플래티넘 내성 상피성 난소암, 난관암, 복막암 환자 643명이 참여했다.환자들은 1:1로 키트루다(400mg, 6주 간격) 또는 플라시보를 투여받았으며, 각각 주간 파클리탁셀(80mg/m², 3주 주기 중 1·8·15일) 및 베바시주맙(10mg/kg, 2주 간격, 선택적 병용)과 병용했다.1차 중간분석(추적 15.6개월) 결과, 전체 모집단(ITT) 기준 PFS 중앙값은 키트루다 병용군 8.3개월, 대조군 6.4개월 그리고 위험비(HR)는 0.70(95% CI 0.58–0.84, P2025-10-19 20:06:13황병우 -
 티쎈트릭, 소세포폐암서 효과 두각…병용요법 시너지↑[데일리팜=손형민 기자] 로슈의 면역항암제 '티쎈트릭'이 소세포폐암 영역에서 가시적인 성과를 내고 있다. 기존 화학요법에 이어 표적치료제 병용요법이 미국에서 새롭게 승인받았으며, 유전자치료제 병용 임상도 순항중이다.소세포폐암 치료제 '젭젤카'16일 관련 업계에 따르면 미국 식품의약국(FDA)은 최근 티쎈트릭(아테졸리주맙)과 '젭젤카(러버넥티딘)' 병용요법을 광범위기 소세포폐암(ES-SCLC) 환자의 1차 유지치료에 승인했다.이번 허가로 티쎈트릭+젭젤카는 기존 티쎈트릭+카보플라틴+에토포사이드 이후 질병이 진행되지 않은 환자를 대상으로 하는 최초의 병용 유지요법으로 등극했다. 티센트릭+젭젤카는 미국 종합암네트워크(NCCN) 가이드라인에도 '선호 옵션(Category 2A)'으로 새롭게 포함됐다.젭젤카는 스페인 제약사 파마마가 개발한 소세포폐암 신약으로 국내에선 보령이 판매와 유통 독점권을 보유하고 있다. 북미 시장은 미국 제약바이오기업 재즈파마슈티컬스가 판매 중이다.젭젤카는 DNA 전사 과정을 방해해 암세포 증식을 억제하는 기전을 갖고 있다. 여기에 더해 젭젤카는 종양 관련 대식세포(TAM) 내 전사 활성도 억제한다. 이를 통해 암세포 주변 환경에서 발생하는 암세포 증식, 면역회피, 혈관 신생과 같은 종양 성장 기전을 동시에 억제하는 효과를 나타낸다.이번 승인의 근거가 된 임상3상 IMforte 연구에서 티쎈트릭+젭젤카 병용요법은 티쎈트릭 단독요법 대비 질병 진행 또는 사망 위험을 46% 감소시켰다.3.2개월 간의 유도요법 이후 측정된 전체생존기간(OS)은 병용군 13.2개월, 단독군 10.6개월이었다. 무진행생존기간(PFS)은 티쎈트릭+젭젤카군은 5.4개월 티쎈트릭 단독요법의 2.1개월 대비 유의하게 연장됐다.티쎈트릭은 이미 2019년 IMpower133 임상을 통해 화학요법 병용 1차 치료제로 승인된 바 있다. 이번 유지요법 확대 승인은 소세포폐암 치료 전주기에서 면역항암제의 역할을 한층 강화시켰다는 평가다.소세포폐암은 주로 폐 중심부 기도에서 처음 발병하며 진행 속도가 빠른 편에 속한다. 특히 전반적으로 악성도가 강해서 발견 당시에 이미 림프나 혈액의 순환을 통해 다른 장기나 반대편 폐, 혹은 종격동으로 전이돼 있는 경우가 대부분이다.다만 임상에서 대부분의 치료제들이 실패해 신약 필요도가 높은 상황이다. 티쎈트릭+젭젤카가 임상에서 좋은 효과를 보인 만큼 새로운 표준치료 옵션으로 자리할지 주목된다.유전자치료제와도 병용 가능성면역항암제 '티쎈트릭'현재 티쎈트릭은 유전자치료제와의 병용요법 가능성도 확인되고 있다.미국 제약바이오기업 젠프렉스는 유전자치료제 '레코르사(quaratusugene ozeplasmid)'와 티쎈트릭 병용요법을 소세포폐암 환자 유지치료용으로 개발 중이다.레코르사는 TUSC2(FUS1) 유전자를 기반으로 하는 비바이러스성 유전자치료제다. TUSC2는 정상 세포에서 암 발생을 억제하는 핵심 유전자로, 소세포폐암과 비소세포폐암 환자에서 흔히 소실되거나 불활성화돼 있다.젠프렉스는 암세포가 잃어버린 이 유전자를 플라스미드 DNA 형태로 재주입해 세포 내 신호전달 체계를 재설정하는 방식으로 접근했다. 즉, 암세포의 증식 신호를 차단하고 자멸 경로(apoptosis)를 복원해 세포를 스스로 파괴하게 만드는 것이다.특히 티쎈트릭과 같은 면역관문억제제 병용 시 PD-1 차단 후 활성화되는 TIM-3, LAG-3 등 보상적 면역회피 경로까지 동시에 억제할 수 있어, 면역항암제 내성 문제를 완화할 수 있다는 분석이다.현재 'Acclaim-3' 임상에서 티쎈트릭과 레코르사의 1상 용량 증량 단계가 완료됐으며, 2상 확장 단계 진입이 승인됐다.임상은 티쎈트릭+화학요법 치료 후 진행이 발생한 환자군을 대상으로 하며, 현재까지 용량 제한 독성이 확인되지 않았다. 1상 결과를 바탕으로 2상 권장용량은 0.12mg/kg으로 결정됐다.2상 확장 단계에서는 약 50명 환자가 미국 내 10~15개 기관에서 등록될 예정이며, 주요 평가지표는 치료 시작 후 18주 간의 무진행생존율이다.FDA는 지난 2023년 6월과 8월 해당 병용요법에 대해 각각 패스트트랙 지정)과 희귀의약품 지정을 부여했다.2025-10-16 06:08:44손형민
티쎈트릭, 소세포폐암서 효과 두각…병용요법 시너지↑[데일리팜=손형민 기자] 로슈의 면역항암제 '티쎈트릭'이 소세포폐암 영역에서 가시적인 성과를 내고 있다. 기존 화학요법에 이어 표적치료제 병용요법이 미국에서 새롭게 승인받았으며, 유전자치료제 병용 임상도 순항중이다.소세포폐암 치료제 '젭젤카'16일 관련 업계에 따르면 미국 식품의약국(FDA)은 최근 티쎈트릭(아테졸리주맙)과 '젭젤카(러버넥티딘)' 병용요법을 광범위기 소세포폐암(ES-SCLC) 환자의 1차 유지치료에 승인했다.이번 허가로 티쎈트릭+젭젤카는 기존 티쎈트릭+카보플라틴+에토포사이드 이후 질병이 진행되지 않은 환자를 대상으로 하는 최초의 병용 유지요법으로 등극했다. 티센트릭+젭젤카는 미국 종합암네트워크(NCCN) 가이드라인에도 '선호 옵션(Category 2A)'으로 새롭게 포함됐다.젭젤카는 스페인 제약사 파마마가 개발한 소세포폐암 신약으로 국내에선 보령이 판매와 유통 독점권을 보유하고 있다. 북미 시장은 미국 제약바이오기업 재즈파마슈티컬스가 판매 중이다.젭젤카는 DNA 전사 과정을 방해해 암세포 증식을 억제하는 기전을 갖고 있다. 여기에 더해 젭젤카는 종양 관련 대식세포(TAM) 내 전사 활성도 억제한다. 이를 통해 암세포 주변 환경에서 발생하는 암세포 증식, 면역회피, 혈관 신생과 같은 종양 성장 기전을 동시에 억제하는 효과를 나타낸다.이번 승인의 근거가 된 임상3상 IMforte 연구에서 티쎈트릭+젭젤카 병용요법은 티쎈트릭 단독요법 대비 질병 진행 또는 사망 위험을 46% 감소시켰다.3.2개월 간의 유도요법 이후 측정된 전체생존기간(OS)은 병용군 13.2개월, 단독군 10.6개월이었다. 무진행생존기간(PFS)은 티쎈트릭+젭젤카군은 5.4개월 티쎈트릭 단독요법의 2.1개월 대비 유의하게 연장됐다.티쎈트릭은 이미 2019년 IMpower133 임상을 통해 화학요법 병용 1차 치료제로 승인된 바 있다. 이번 유지요법 확대 승인은 소세포폐암 치료 전주기에서 면역항암제의 역할을 한층 강화시켰다는 평가다.소세포폐암은 주로 폐 중심부 기도에서 처음 발병하며 진행 속도가 빠른 편에 속한다. 특히 전반적으로 악성도가 강해서 발견 당시에 이미 림프나 혈액의 순환을 통해 다른 장기나 반대편 폐, 혹은 종격동으로 전이돼 있는 경우가 대부분이다.다만 임상에서 대부분의 치료제들이 실패해 신약 필요도가 높은 상황이다. 티쎈트릭+젭젤카가 임상에서 좋은 효과를 보인 만큼 새로운 표준치료 옵션으로 자리할지 주목된다.유전자치료제와도 병용 가능성면역항암제 '티쎈트릭'현재 티쎈트릭은 유전자치료제와의 병용요법 가능성도 확인되고 있다.미국 제약바이오기업 젠프렉스는 유전자치료제 '레코르사(quaratusugene ozeplasmid)'와 티쎈트릭 병용요법을 소세포폐암 환자 유지치료용으로 개발 중이다.레코르사는 TUSC2(FUS1) 유전자를 기반으로 하는 비바이러스성 유전자치료제다. TUSC2는 정상 세포에서 암 발생을 억제하는 핵심 유전자로, 소세포폐암과 비소세포폐암 환자에서 흔히 소실되거나 불활성화돼 있다.젠프렉스는 암세포가 잃어버린 이 유전자를 플라스미드 DNA 형태로 재주입해 세포 내 신호전달 체계를 재설정하는 방식으로 접근했다. 즉, 암세포의 증식 신호를 차단하고 자멸 경로(apoptosis)를 복원해 세포를 스스로 파괴하게 만드는 것이다.특히 티쎈트릭과 같은 면역관문억제제 병용 시 PD-1 차단 후 활성화되는 TIM-3, LAG-3 등 보상적 면역회피 경로까지 동시에 억제할 수 있어, 면역항암제 내성 문제를 완화할 수 있다는 분석이다.현재 'Acclaim-3' 임상에서 티쎈트릭과 레코르사의 1상 용량 증량 단계가 완료됐으며, 2상 확장 단계 진입이 승인됐다.임상은 티쎈트릭+화학요법 치료 후 진행이 발생한 환자군을 대상으로 하며, 현재까지 용량 제한 독성이 확인되지 않았다. 1상 결과를 바탕으로 2상 권장용량은 0.12mg/kg으로 결정됐다.2상 확장 단계에서는 약 50명 환자가 미국 내 10~15개 기관에서 등록될 예정이며, 주요 평가지표는 치료 시작 후 18주 간의 무진행생존율이다.FDA는 지난 2023년 6월과 8월 해당 병용요법에 대해 각각 패스트트랙 지정)과 희귀의약품 지정을 부여했다.2025-10-16 06:08:44손형민 -
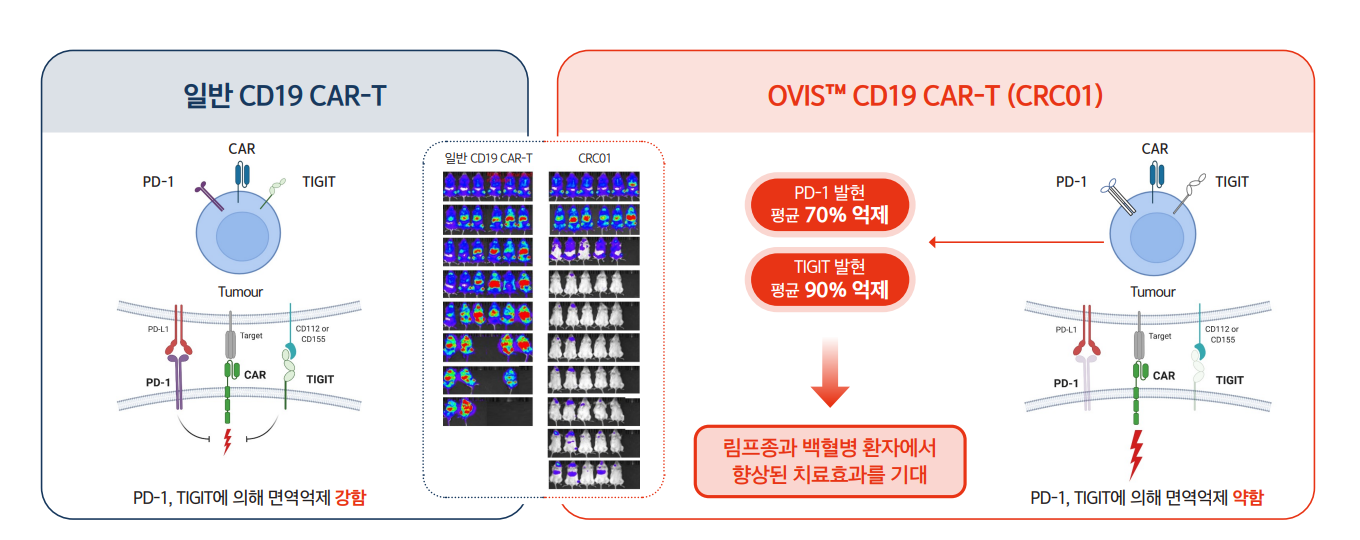 큐로셀, CAR-T 신약 개발 매진...올해 430억 조달[데일리팜=차지현 기자] 키메릭항원수용체 T세포(CAR-T) 치료제 개발 기업 큐로셀이 100억원 규모 전환사채(CB)를 발행한다. 올 초 330억원 규모 CB를 발행한 지 7개월 만에 또다시 자금 조달에 나섰다. 국산 CAR-T 치료제 상업화를 앞두고 대규모 지출이 발생하면서 재무 부담이 커진 데 따른 결정으로 풀이된다.19일 금융감독원에 따르면 큐로셀은 지난 17일 이사회를 열고 3회차 무기명식 이권부 무보증 사모 CB 발행을 의결했다. CB는 주식과 채권의 성격을 모두 지닌 주식연계채권이다. 채권자가 회사에 돈을 빌려주고 이자를 받다가 주가가 오르면 주식으로 전환할 수 있다.이번에 큐로셀이 발행하는 CB는 100억원 규모다. 하나벤처스가 운용하는 하나테크밸류업펀드2호가 물량을 인수하는 형태다. 해당 CB의 표면이자율은 0%, 만기이자율은 1%다. CB 전환가액은 4만1950원으로, CB 발행을 결정한 17일 큐로셀 종가 4만1900원보다 소폭 높다.큐로셀은 2016년 설립된 세포유전자치료제 개발 기업이다. CAR-T 기술과 면역관문억제제 기술을 융합한 OVIS 플랫폼을 기반으로 차세대 CAR-T 치료제를 개발 중이다. 대표 파이프라인 '안발셀'(제품명 림가토)은 국내 최초 식품의약품안전처 임상 승인을 획득한 제품으로 작년 말 식약처에 품목허가 신청 후 연내 출시를 목표로 하고 있다.큐로셀의 자금 조달은 올해 들어서만 두 번째다. 앞서 큐로셀은 지난 2월 330억원 규모 CB 발행을 결정했다. 이는 상장 당시 모집한 공모액 320억원을 웃도는 수준이다. 이번에 발행하는 CB까지 합하면 큐로셀은 코스닥 상장 이후 불과 2년도 채 되지 않아 430억원에 달하는 외부 투자를 추가 유치한 셈이다.큐로셀 CAR-T 치료제 '안발셀'(제품명 림가토) 개요 (자료: 큐로셀) 큐로셀이 CB 발행을 연이어 추진하는 배경에는 유동성 부족이 있다. 6월 말 기준 이 회사가 보유한 유동자산은 현금성자산 92억원을 포함해 325억원에 그친다. 반면 유동부채는 736억 원으로 집계됐다. 단기적으로 갚아야 할 빚이 당장 동원할 수 있는 자산보다 두 배 이상 많다는 얘기다.재무구조도 취약하다. 매출이 전무한 상황에서 림가토 상업화 준비로 인해 각종 제반 비용이 늘면서 적자 폭이 지속해서 증가한 탓이다. 큐로셀은 올 상반기 연결기준 영업손실 184억원, 당기순손실 175억원을 기록했다. 전년 동기 대비 영업손실은 약 20억원 늘었고 순손실은 12억원가량 증가했다.순손실이 이어지면서 결손금 규모도 불어났다. 큐로셀의 6월 말 기준 누적결손금은 2178억원에 달한다. 결손금이 자본을 갉아먹으면서 2023년 12월 말 591억원이었던 자본총계는 올 6월 말 294억원으로 반토막났다. 같은 시기 큐로셀 자본금은 72억원으로 현재 순손실 추세가 이어질 경우 1년 내 자본총계가 소진돼 자본잠식에 빠질 수 있는 상황이었다.큐로셀은 지난 7월 자산재평가를 통해 재무구조 개선 효과를 꾀했지만 순손실 누적 규모가 워낙 커 그 효과는 제한적이었다. 큐로셀은 대전 유성구 구룡동 817-2에 위치한 본사 토지와 건물에 대한 자산재평가를 실시, 재평가잉여금으로 172억원을 인식했다. 자산재평가란 기업이 보유한 유형자산의 장부가치를 시장가치에 맞춰 조정하는 절차로 현금흐름에는 변화가 없지만 자본잠식 우려를 덜어주는 효과가 있다.결과적으로 큐로셀은 이번 CB 발행으로 단기적으로 허가와 상업화 준비를 위한 현금을 확보하는 동시에 장기적으로 자본잠식 우려도 덜 수 있게 됐다. CB는 이자 지급과 원금 상환 의무가 있는 채권의 성격을 지니기 때문에 발행 시 회계상 부채로 분류된다. 하지만 향후 투자가가 CB를 주식으로 전환하면 해당 채권은 부채에서 소멸되고 그만큼 자본이 증가하게 된다.재무 안정성을 강화한 큐로셀은 림카토주 상업화와 함께 파이프라인 확장에도 속도를 낼 계획이다. 큐로셀은 3회차 CB 사용 목적에서 루푸스 신염 치료제 개발에 45억원, T세포 림프종 치료제에 40억원, 바이러스 벡터 내재화에 15억원을 배정했다. 앞서 발행한 2회차 CB의 경우 안발셀 적응증 확장에 140억원, 신규 CAR-T 치료제 개발에 120억원 등을 투입하겠다고 제시한 바 있다.2025-09-19 12:00:04차지현
큐로셀, CAR-T 신약 개발 매진...올해 430억 조달[데일리팜=차지현 기자] 키메릭항원수용체 T세포(CAR-T) 치료제 개발 기업 큐로셀이 100억원 규모 전환사채(CB)를 발행한다. 올 초 330억원 규모 CB를 발행한 지 7개월 만에 또다시 자금 조달에 나섰다. 국산 CAR-T 치료제 상업화를 앞두고 대규모 지출이 발생하면서 재무 부담이 커진 데 따른 결정으로 풀이된다.19일 금융감독원에 따르면 큐로셀은 지난 17일 이사회를 열고 3회차 무기명식 이권부 무보증 사모 CB 발행을 의결했다. CB는 주식과 채권의 성격을 모두 지닌 주식연계채권이다. 채권자가 회사에 돈을 빌려주고 이자를 받다가 주가가 오르면 주식으로 전환할 수 있다.이번에 큐로셀이 발행하는 CB는 100억원 규모다. 하나벤처스가 운용하는 하나테크밸류업펀드2호가 물량을 인수하는 형태다. 해당 CB의 표면이자율은 0%, 만기이자율은 1%다. CB 전환가액은 4만1950원으로, CB 발행을 결정한 17일 큐로셀 종가 4만1900원보다 소폭 높다.큐로셀은 2016년 설립된 세포유전자치료제 개발 기업이다. CAR-T 기술과 면역관문억제제 기술을 융합한 OVIS 플랫폼을 기반으로 차세대 CAR-T 치료제를 개발 중이다. 대표 파이프라인 '안발셀'(제품명 림가토)은 국내 최초 식품의약품안전처 임상 승인을 획득한 제품으로 작년 말 식약처에 품목허가 신청 후 연내 출시를 목표로 하고 있다.큐로셀의 자금 조달은 올해 들어서만 두 번째다. 앞서 큐로셀은 지난 2월 330억원 규모 CB 발행을 결정했다. 이는 상장 당시 모집한 공모액 320억원을 웃도는 수준이다. 이번에 발행하는 CB까지 합하면 큐로셀은 코스닥 상장 이후 불과 2년도 채 되지 않아 430억원에 달하는 외부 투자를 추가 유치한 셈이다.큐로셀 CAR-T 치료제 '안발셀'(제품명 림가토) 개요 (자료: 큐로셀) 큐로셀이 CB 발행을 연이어 추진하는 배경에는 유동성 부족이 있다. 6월 말 기준 이 회사가 보유한 유동자산은 현금성자산 92억원을 포함해 325억원에 그친다. 반면 유동부채는 736억 원으로 집계됐다. 단기적으로 갚아야 할 빚이 당장 동원할 수 있는 자산보다 두 배 이상 많다는 얘기다.재무구조도 취약하다. 매출이 전무한 상황에서 림가토 상업화 준비로 인해 각종 제반 비용이 늘면서 적자 폭이 지속해서 증가한 탓이다. 큐로셀은 올 상반기 연결기준 영업손실 184억원, 당기순손실 175억원을 기록했다. 전년 동기 대비 영업손실은 약 20억원 늘었고 순손실은 12억원가량 증가했다.순손실이 이어지면서 결손금 규모도 불어났다. 큐로셀의 6월 말 기준 누적결손금은 2178억원에 달한다. 결손금이 자본을 갉아먹으면서 2023년 12월 말 591억원이었던 자본총계는 올 6월 말 294억원으로 반토막났다. 같은 시기 큐로셀 자본금은 72억원으로 현재 순손실 추세가 이어질 경우 1년 내 자본총계가 소진돼 자본잠식에 빠질 수 있는 상황이었다.큐로셀은 지난 7월 자산재평가를 통해 재무구조 개선 효과를 꾀했지만 순손실 누적 규모가 워낙 커 그 효과는 제한적이었다. 큐로셀은 대전 유성구 구룡동 817-2에 위치한 본사 토지와 건물에 대한 자산재평가를 실시, 재평가잉여금으로 172억원을 인식했다. 자산재평가란 기업이 보유한 유형자산의 장부가치를 시장가치에 맞춰 조정하는 절차로 현금흐름에는 변화가 없지만 자본잠식 우려를 덜어주는 효과가 있다.결과적으로 큐로셀은 이번 CB 발행으로 단기적으로 허가와 상업화 준비를 위한 현금을 확보하는 동시에 장기적으로 자본잠식 우려도 덜 수 있게 됐다. CB는 이자 지급과 원금 상환 의무가 있는 채권의 성격을 지니기 때문에 발행 시 회계상 부채로 분류된다. 하지만 향후 투자가가 CB를 주식으로 전환하면 해당 채권은 부채에서 소멸되고 그만큼 자본이 증가하게 된다.재무 안정성을 강화한 큐로셀은 림카토주 상업화와 함께 파이프라인 확장에도 속도를 낼 계획이다. 큐로셀은 3회차 CB 사용 목적에서 루푸스 신염 치료제 개발에 45억원, T세포 림프종 치료제에 40억원, 바이러스 벡터 내재화에 15억원을 배정했다. 앞서 발행한 2회차 CB의 경우 안발셀 적응증 확장에 140억원, 신규 CAR-T 치료제 개발에 120억원 등을 투입하겠다고 제시한 바 있다.2025-09-19 12:00:04차지현 -
 K-바이오, 국제 폐암학회 출격...R&D 경쟁력 쇼케이스[데일리팜=손형민 기자] 항체약물접합체(ADC), 표적항암제, 면역항암제 등 다양한 국내사의 신약후보물질들이 글로벌 무대에서 가능성을 평가받는다. 주요 국내 제약바이오기업들은 오는 6일부터 4일 간 스페인 바르셀로나에서 열리는 세계폐암학회(WCLC 2025) 무대에 오른다. 리가켐바이오, 에스티큐브, 루닛 등이 각각 항체약물접합체(ADC), 신규 면역관문억제제, 인공지능(AI) 기반 정밀의료 전략에 대한 발표가 예고됐다.ADC·표적치료제 등 신규 타깃 개발 연구 공개리가켐바이오는 이번 학회에서 차세대 CEACAM5 항체 타깃 ADC 후보물질 ‘LCB58A’의 전임상 결과를 공개한다. LCB58A는 지난 2월 다안바이오테라퓨틱스에서 도입한 항체와 플랫폼 ‘콘쥬올(ConjuAll)’ 기술을 결합해 개발 중인 파이프라인이다.콘쥬올은 항체 특정 부위에 원하는 수량의 페이로드를 부착가능한 결합 방법, 혈중안정성과 암세포 특이적으로 약물 방출 능력이 뛰어난 링커 그리고 신규 기전의 페이로드로 구성돼 있다.LCB58A는 기존 CEACAM5-ADC의 한계였던 혈중 가용성 CEACAM5 결합 문제를 회피하고 암세포에만 특이적으로 작용하는 기전을 갖고 있다.공개된 초록에 따르면 전임상 결과, LCB58A는 비교 항체인 투사미타맙과 비교했을 때 더 우수한 세포 내재화를 보였다. 다양한 링커-페이로드 조합으로 제작한 ADC는 세포주 실험과 환자 유래 이종이식(PDX) 모델 모두에서 강력한 항종양 효과를 입증했다. 또 인간 CEACAM5 형질전환 마우스 모델에서 진행한 독성·약동학 연구에서도 효능 용량에서 양호한 안전성을 보였다.회사 측은 “혈중 가용성 CEACAM5 농도가 높은 종양 환경에서도 작용 가능성을 확인했다”며 “차세대 CEACAM5 타깃 치료 옵션으로 발전할 수 있다”고 설명했다.에스티큐브는 신규 면역관문 단백질 BTN1A1을 겨냥한 항체치료제 ‘넬마스토바트’의 연구성과를 발표한다. 이번 학회에서는 총 2건의 초록이 채택됐다.BTN1A1은 면역세포인 T세포의 활동을 억제함으로써 암세포에 대한 면역반응을 조절하는 단백질이다. 이 바이오마커는 정상세포에서 발현되지 않는 반면 암세포에서 강하게 발현되고 PD-L1과는 상호 배타적으로 발현한다. 에스티큐브는 BTN1A1을 타깃해 난치성 암에서 새로운 치료옵션이 될 수 있는 면역항암제를 개발하고 있다.에스티큐브는 비소세포폐암 환자 유래 오가노이드(PDO) 기반 연구 결과를 공개한다. 회사에 따르면 분석 결과 BTN1A1과 PD-L1은 상호배타적으로 발현했으며, 항 BTN1A1 항체는 도세탁셀과 병용 시 반응성이 크게 높아졌다. 특히 도세탁셀 투여 후 BTN1A1 발현이 특이적으로 증가하면서 PD-L1 음성 환자군에서 새로운 치료 전략이 될 가능성이 제시됐다.또 에스티큐브는 임상 1상 환자 샘플을 활용한 바이오마커 연구를 발표한다. 소세포폐암 3명, 비소세포폐암 1명의 조직을 분석한 결과, BTN1A1 양성·핵 YAP1 고발현 환자군에서 무진행생존기간(PFS)이 더 길게 나타났다. 안전성 측면에서도 저등급 피로·주입 관련 반응 외에는 양호한 내약성을 보였다.에스티큐브는 “BTN1A1은 기존 PD-1/PD-L1 억제제 불응 환자에서 의미 있는 표적이 될 수 있다”며 “올해부터 정밀의료 기반 바이오마커 선별 임상에 본격 착수했으며, 대장암과 폐암 후속 임상도 준비 중”이라고 밝혔다.WCLC 2024 전경(출처=WCLC). 루닛은 수술 전 항암화학·면역병용요법에서 환자 반응성을 예측할 수 있는 게놈·면역학적 지표 분석 결과를 공개한다.루닛은 EGFR/ALK 변이가 없는 비소세포폐암 환자 72명을 대상으로 AI 기반 병리 분석 솔루션 ‘Lunit-SCOPE IO’를 활용해 종양 침윤 림프구(TIL)와 유전체 변이를 통합 분석했다.그 결과, 9p24.1(포함 유전자 CD274) 소실은 비염증성 면역표현형과 연관되며 병리학적 완전관해율이 크게 낮았다. 또 선암(LUAD) 환자에서는 STK11 변이 및 19p13.3 소실이 치료 저항성을 높이는 주요 인자로 나타났다. 이러한 게놈 변화와 면역환경을 통합한 모델은 기존 임상 변수 대비 반응 예측 정확도를 크게 향상시켰다.연구진은 “치료 전 분자진단과 면역환경 분석을 통해 환자를 정밀 선별하는 것이 수술 전 보조요법 치료 성적 향상의 열쇠가 될 것”이라고 강조했다.2025-09-03 06:20:06손형민
K-바이오, 국제 폐암학회 출격...R&D 경쟁력 쇼케이스[데일리팜=손형민 기자] 항체약물접합체(ADC), 표적항암제, 면역항암제 등 다양한 국내사의 신약후보물질들이 글로벌 무대에서 가능성을 평가받는다. 주요 국내 제약바이오기업들은 오는 6일부터 4일 간 스페인 바르셀로나에서 열리는 세계폐암학회(WCLC 2025) 무대에 오른다. 리가켐바이오, 에스티큐브, 루닛 등이 각각 항체약물접합체(ADC), 신규 면역관문억제제, 인공지능(AI) 기반 정밀의료 전략에 대한 발표가 예고됐다.ADC·표적치료제 등 신규 타깃 개발 연구 공개리가켐바이오는 이번 학회에서 차세대 CEACAM5 항체 타깃 ADC 후보물질 ‘LCB58A’의 전임상 결과를 공개한다. LCB58A는 지난 2월 다안바이오테라퓨틱스에서 도입한 항체와 플랫폼 ‘콘쥬올(ConjuAll)’ 기술을 결합해 개발 중인 파이프라인이다.콘쥬올은 항체 특정 부위에 원하는 수량의 페이로드를 부착가능한 결합 방법, 혈중안정성과 암세포 특이적으로 약물 방출 능력이 뛰어난 링커 그리고 신규 기전의 페이로드로 구성돼 있다.LCB58A는 기존 CEACAM5-ADC의 한계였던 혈중 가용성 CEACAM5 결합 문제를 회피하고 암세포에만 특이적으로 작용하는 기전을 갖고 있다.공개된 초록에 따르면 전임상 결과, LCB58A는 비교 항체인 투사미타맙과 비교했을 때 더 우수한 세포 내재화를 보였다. 다양한 링커-페이로드 조합으로 제작한 ADC는 세포주 실험과 환자 유래 이종이식(PDX) 모델 모두에서 강력한 항종양 효과를 입증했다. 또 인간 CEACAM5 형질전환 마우스 모델에서 진행한 독성·약동학 연구에서도 효능 용량에서 양호한 안전성을 보였다.회사 측은 “혈중 가용성 CEACAM5 농도가 높은 종양 환경에서도 작용 가능성을 확인했다”며 “차세대 CEACAM5 타깃 치료 옵션으로 발전할 수 있다”고 설명했다.에스티큐브는 신규 면역관문 단백질 BTN1A1을 겨냥한 항체치료제 ‘넬마스토바트’의 연구성과를 발표한다. 이번 학회에서는 총 2건의 초록이 채택됐다.BTN1A1은 면역세포인 T세포의 활동을 억제함으로써 암세포에 대한 면역반응을 조절하는 단백질이다. 이 바이오마커는 정상세포에서 발현되지 않는 반면 암세포에서 강하게 발현되고 PD-L1과는 상호 배타적으로 발현한다. 에스티큐브는 BTN1A1을 타깃해 난치성 암에서 새로운 치료옵션이 될 수 있는 면역항암제를 개발하고 있다.에스티큐브는 비소세포폐암 환자 유래 오가노이드(PDO) 기반 연구 결과를 공개한다. 회사에 따르면 분석 결과 BTN1A1과 PD-L1은 상호배타적으로 발현했으며, 항 BTN1A1 항체는 도세탁셀과 병용 시 반응성이 크게 높아졌다. 특히 도세탁셀 투여 후 BTN1A1 발현이 특이적으로 증가하면서 PD-L1 음성 환자군에서 새로운 치료 전략이 될 가능성이 제시됐다.또 에스티큐브는 임상 1상 환자 샘플을 활용한 바이오마커 연구를 발표한다. 소세포폐암 3명, 비소세포폐암 1명의 조직을 분석한 결과, BTN1A1 양성·핵 YAP1 고발현 환자군에서 무진행생존기간(PFS)이 더 길게 나타났다. 안전성 측면에서도 저등급 피로·주입 관련 반응 외에는 양호한 내약성을 보였다.에스티큐브는 “BTN1A1은 기존 PD-1/PD-L1 억제제 불응 환자에서 의미 있는 표적이 될 수 있다”며 “올해부터 정밀의료 기반 바이오마커 선별 임상에 본격 착수했으며, 대장암과 폐암 후속 임상도 준비 중”이라고 밝혔다.WCLC 2024 전경(출처=WCLC). 루닛은 수술 전 항암화학·면역병용요법에서 환자 반응성을 예측할 수 있는 게놈·면역학적 지표 분석 결과를 공개한다.루닛은 EGFR/ALK 변이가 없는 비소세포폐암 환자 72명을 대상으로 AI 기반 병리 분석 솔루션 ‘Lunit-SCOPE IO’를 활용해 종양 침윤 림프구(TIL)와 유전체 변이를 통합 분석했다.그 결과, 9p24.1(포함 유전자 CD274) 소실은 비염증성 면역표현형과 연관되며 병리학적 완전관해율이 크게 낮았다. 또 선암(LUAD) 환자에서는 STK11 변이 및 19p13.3 소실이 치료 저항성을 높이는 주요 인자로 나타났다. 이러한 게놈 변화와 면역환경을 통합한 모델은 기존 임상 변수 대비 반응 예측 정확도를 크게 향상시켰다.연구진은 “치료 전 분자진단과 면역환경 분석을 통해 환자를 정밀 선별하는 것이 수술 전 보조요법 치료 성적 향상의 열쇠가 될 것”이라고 강조했다.2025-09-03 06:20:06손형민 -
 "퍼스트바이오 최고 전문가와 한국형 신약 전략 승부"[데일리팜=차지현 기자] "회사를 창업할 시기 마음속에 새긴 표어가 있다. 환자가 우선(Patient First)이라는 원칙이다. 수많은 갈림길 앞에 설 때마다 이 철학을 따라가고 있다."경기 용인시 본사에서 만난 김재은 퍼스트바이오테라퓨틱스 대표는 신약개발 방향성과 조직 운영 철학에 대해 이같이 말했다. 신약개발 갈림길에서든 경영 판단을 내릴 때든, 어려운 결정을 마주할 때 '어떤 선택이 환자에게 진짜 도움이 되는가'를 스스로에게 물어보면 복잡하던 상황도 의외로 명확해진다는 게 그의 설명이다.김재은 퍼스트바이오테라퓨틱스 대표 퍼스트바이오는 지난 2016년 김 대표가 설립한 신약개발 바이오텍이다. 환자가 우선이라는 철학이 사명에 고스란히 녹아 있다. 회사 이름에는 바이오 분야에서 최고(First)의 팀이 되겠다는 뜻도 포함됐다. 연구실의 발견이 아닌, 의료 현장에서 환자 삶을 바꾸는 신약을 만드는 게 이 회사의 포부다.김 대표는 글로벌 빅파마와와 국내 제약사 넘나들며 연구개발(R&D)부터 사업개발(BD), 전략 수립까지 전 주기를 두루 경험한 신약개발 전문가다. 그는 한국과학기술원(KAIST)에서 생명공학 학사와 생물과학 석사 학위 취득 후 미국 일리노이대 어바나-샴페인 캠퍼스에서 박사 학위를 취득했다. 김 대표는 미국 와이어스에서 신약개발의 시작점이라 할 수 있는 프로젝트 이니시에이션 업무를 맡아 과학적 타당성, 개발 경로, 사업성, 리스크 등을 종합적으로 분석했다.그는 와이어스에서 6년 넘게 근무한 뒤 프랑스 사노피에 합류했다. 김 대표는 사노피에서 신약 발굴·평가 부서(Search & Evaluation)에서 근무하며 수많은 국내 초기 신약 프로젝트를 검토하고 이를 사노피와 연결하는 작업을 주도했다. 김 대표는 사노피에서의 경험을 "신약개발의 시작점을 설계한다는 건 단순히 기술을 검토하는 수준을 넘어, 과학적 타당성, 규제 요건, 시장성, 경쟁 환경까지 종합적으로 고려해야 하는 '종합 예술'과도 같다는 사실을 실무를 통해 체감한 시기"라고 회상했다.이후 김 대표는 이후 GC녹십자, 한독 등 국내 제약사에 몸담았다. 당시는 국내 제약사 사이에서 '신약다운 신약'을 개발해보려는 움직임이 본격적으로 일기 시작한 때였다. 하지만 국내 제약사는 오랫동안 미투(Me-too)나 제네릭 중심 개발에 머물러 있었던 터라, 정작 신약개발의 출발점을 어떻게 설정해야 할지에 대한 개념이 부족한 상황이었다. 김 대표는 빅파마에서 체득한 노하우를 바탕으로, 국내 제약사의 R&D 체계 정립과 파이프라인 기획에 주도적인 역할을 했다.김 대표가 말하는 퍼스트바이오의 강점은 기초 체력이 탄탄한 회사라는 점이다. 초기 퍼스트바이오를 창업할 때 그가 구상한 모델은 기획형 바이오(Buy and Build)다. 이는 경험 많은 전문가와 풍부한 자본을 바탕으로 회사를 설립한 뒤 지속해서 밸류업을 시켜나가는 전략이다. 성장성이 높으면서 경쟁이 치열해 신속한 임상 개발이 요구되는 분야에 전력을 다해 시장을 선점하겠다는 아이디어다. 메신저리보핵산(mRNA) 기반 코로나19 백신 개발로 일약 스타덤에 오른 모더나가 대표적인 성공 사례로 꼽힌다.김 대표는 창업 초기부터 각 분야에서 실력을 인정받은 전문가들을 한 자리에 모았다. 김성곤 최고기술책임자(CTO)는 미국 머크와 종근당 효종연구소장을 거친 인물이다. 이진화 최고과학책임자(CSO)는 글락소스미스클라인(GSK), 한독 등을 거친 글로벌 R&D 전문가다. 이성규 최고운영책임자(COO)는 일리아스 바이오로직스 전략기획실장 등을 거친 인물로, 오름테라퓨틱에서 특허와 법무, 컴플라이언스 관련 업무를 맡았다.하지만 현실은 녹록지 않았다. 국내 바이오 시장은 기획형 바이오가 현실적으로 성공하기 어려운 구조였다. 자본과 제도적 기반이 충분하지 않았기 때문이다. 김 대표는 "신약 하나를 개발하는 데 수조원이 드는데, 우리나라가 투입하는 자금은 빅파마에 비해 턱없이 부족하다"면서 "이건 조기 축구회에 공 하나 쥐어주고 월드컵에서 우승하라고 하는 것과 다를 바 없다"고 했다.김 대표는 자금이 제한적인 국내 바이오 생태계에서 살아남기 위해 미국의 모델을 그대로 따라가기보다 한국형 전략으로 승부해야 한다고 판단했다. 한국 바이오텍은 미국 회사와는 달라야 한다는 것. 김 대표는 "차별화를 위해 퍼스트바이오의 기본 방침은 지적재산권(IP)을 100% 회사가 소유하도록 하고 있다"면서 "의약화학 역량을 전적으로 인하우스(in-house)로 보유해 히트물질 발굴부터 합성, 최적화 후보물질 선정(PCC)에 이르기까지 전 과정을 내부에서 완결할 수 있다는 것도 강점"이라고 했다.신약개발 효율성을 높이기 위해 인공지능(AI) 기술도 적극적으로 활용 중이다. 그는 "2021년도부터 AI 부서인 AID(Accelerated In-silico Discovery)팀을 신설했고 예측모델 등 독자적인 AI 플랫폼을 갖춰 고도화를 진행 중"이라며 "보유 AI 플랫폼을 이용하면 수십만개 이상 화합물 스크리닝과 후보물질군 확장을 통해 높은 신뢰도로 후보물질의 특성을 예측할 수 있다"고 했다.(자료: 퍼스트바이오테라퓨틱스) 이런 전략을 바탕으로 퍼스트바이오는 현재 ▲임상 1/2상 단계 면역항암제 후보물질 'FB849' ▲임상 1상 단계 퇴행성뇌질환 치료제 후보물질 'FB-101' 등 파이프라인을 운영 중이다. 전임상 단계의 뇌질환과 항암제 후보물질 4종(1ST-206, 1ST-104, FL-101, FL-102) 등도 보유했다. 이외 AI 신약 설계 엔진 플랫폼 '1ST-501', 표적단백질 분해(TPD) 발굴 플랫폼 '1ST-FINDER'도 확보한 상태다.FB849는 퍼스트바이오 파이프라인 중 개발 단계가 가장 앞서있다. FB849은 HPK1(hematopoietic progenitor kinase 1)을 타깃으로 하는 차세대 면역항암제다. 기존 면역관문억제제(ICI)에 불응하거나 내성을 보이는 환자군을 대상으로 단독 또는 병용요법으로 활용할 수 있는 가능성이 높은 물질이다. 현재 미국에서 임상 1상을 진행 중으로, 미국 모피트(Moffitt) 암센터 와 공동임상 계약을 체결, 협업 체계를 구축했다.FB-101은 퍼스트바이오의 첫 프로젝트다. c-Abl 저해제로, 퇴행성 뇌질환의 근원적인 병리 기전을 조절 가능한 신약으로 개발 중이다. 높은 뇌혈관장벽(BBB) 투과율과 낮은 오프타깃 독성, 우수한 선택성을 기반으로 경쟁 후보물질 대비 강점을 갖췄다는 게 김 대표의 설명이다.FB-101은 근위축성측삭경화증(ALS)과 파킨슨병을 적응증으로 해 임상을 진행하고 있다. 당초 미국에서 임상을 추진할 예정이었으나 자금 운용 효율성과 임상 진행 속도를 고려해 국내로 임상 거점을 전환했다. 국내에서 단일 용량 상승(SAD)과 반복 용량 상승(MAD) 시험을 마무리한 후 일본과 호주 환자를 대상으로 임상 1b과 2상으로 확장할 계획이다. 일본 시장을 선제적으로 공략해 조기 승인 가능성을 확보한 뒤, 자본과 밸류에이션을 끌어올린 상태에서 다시 미국과 글로벌 시장으로 확장한다는 구상이다.R&D 측면에서 가시화한 성과도 속속 나오고 있다. 퍼스트바이오는 지난 4월 리가켐바이오와 공동연구·기술이전 옵션 계약을 체결했다. 이번 계약은 단계별 기술이전 옵션이 포함된 광범위한 R&D 협력 구조로, 양사는 기존 항체약물복합체(ADC)의 한계를 극복할 수 있는 새로운 저분자 항암제와 차세대 페이로드(payload)를 공동 개발한다는 목표다. 해당 계약을 통해 퍼스트바이오는 리가켐바이오로부터 초기 연구자금을 확보했고 프로그램의 진척도에 따라 추가적인 연구비 지원도 받을 수 있게 됐다.올해 바이오USA에서 파이프라인 관련 미팅도 활발하게 진행했다. 김 대표는 "임상 단계 물질인 FB849와 FB-101 중심으로 활발한 논의가 이뤄졌다"면서 "ALS에 관심있는 일본 회사와도 미팅을 다수 진행했다"고 했다. 이어 그는 "이번 행사 참가는 퍼스트바이오의 파이프라인과 개발, 사업화 전략에 대한 시장의 관심을 재확인하고 동향을 파악할 수 있는 좋은 기회였다"면서 "후속 미팅과 비밀유지계약(CDA) 체결도 준비 중"이라고 덧붙였다.퍼스트바이오 지난달부터 상장 전 지분투자(Pre-IPO) 단계 신규 투자 유치를 본격화했다. 연내 클로징을 목표로 일본과 싱가포르, 홍콩 등 아시아 지역을 중심으로 해외 투자자를 물색 중이다. 앞서 퍼스트바이오는 2016년 시리즈A 80억원, 2018년 시리즈B 190억원, 2020년 브릿지펀딩 170억원, 2022년 시리즈C1 151억원, 2023년 시리즈C2 168억원 등 누적 760억원의 투자금을 유치한 바 있다.김 대표는 "지난달 기술보증기금 싱가포르지점 개소식에 초청돼 파이프라인과 사업을 소개하고 현지 벤처캐피탈(VC)과 미팅을 진행했다"면서 "FB849의 초기 임상 POC를 확인하고 2026년께 글로벌 기술이전에 성공한 뒤 2027년에 코스닥 상장하는 게 목표"라고 했다.2025-07-07 06:18:27차지현
"퍼스트바이오 최고 전문가와 한국형 신약 전략 승부"[데일리팜=차지현 기자] "회사를 창업할 시기 마음속에 새긴 표어가 있다. 환자가 우선(Patient First)이라는 원칙이다. 수많은 갈림길 앞에 설 때마다 이 철학을 따라가고 있다."경기 용인시 본사에서 만난 김재은 퍼스트바이오테라퓨틱스 대표는 신약개발 방향성과 조직 운영 철학에 대해 이같이 말했다. 신약개발 갈림길에서든 경영 판단을 내릴 때든, 어려운 결정을 마주할 때 '어떤 선택이 환자에게 진짜 도움이 되는가'를 스스로에게 물어보면 복잡하던 상황도 의외로 명확해진다는 게 그의 설명이다.김재은 퍼스트바이오테라퓨틱스 대표 퍼스트바이오는 지난 2016년 김 대표가 설립한 신약개발 바이오텍이다. 환자가 우선이라는 철학이 사명에 고스란히 녹아 있다. 회사 이름에는 바이오 분야에서 최고(First)의 팀이 되겠다는 뜻도 포함됐다. 연구실의 발견이 아닌, 의료 현장에서 환자 삶을 바꾸는 신약을 만드는 게 이 회사의 포부다.김 대표는 글로벌 빅파마와와 국내 제약사 넘나들며 연구개발(R&D)부터 사업개발(BD), 전략 수립까지 전 주기를 두루 경험한 신약개발 전문가다. 그는 한국과학기술원(KAIST)에서 생명공학 학사와 생물과학 석사 학위 취득 후 미국 일리노이대 어바나-샴페인 캠퍼스에서 박사 학위를 취득했다. 김 대표는 미국 와이어스에서 신약개발의 시작점이라 할 수 있는 프로젝트 이니시에이션 업무를 맡아 과학적 타당성, 개발 경로, 사업성, 리스크 등을 종합적으로 분석했다.그는 와이어스에서 6년 넘게 근무한 뒤 프랑스 사노피에 합류했다. 김 대표는 사노피에서 신약 발굴·평가 부서(Search & Evaluation)에서 근무하며 수많은 국내 초기 신약 프로젝트를 검토하고 이를 사노피와 연결하는 작업을 주도했다. 김 대표는 사노피에서의 경험을 "신약개발의 시작점을 설계한다는 건 단순히 기술을 검토하는 수준을 넘어, 과학적 타당성, 규제 요건, 시장성, 경쟁 환경까지 종합적으로 고려해야 하는 '종합 예술'과도 같다는 사실을 실무를 통해 체감한 시기"라고 회상했다.이후 김 대표는 이후 GC녹십자, 한독 등 국내 제약사에 몸담았다. 당시는 국내 제약사 사이에서 '신약다운 신약'을 개발해보려는 움직임이 본격적으로 일기 시작한 때였다. 하지만 국내 제약사는 오랫동안 미투(Me-too)나 제네릭 중심 개발에 머물러 있었던 터라, 정작 신약개발의 출발점을 어떻게 설정해야 할지에 대한 개념이 부족한 상황이었다. 김 대표는 빅파마에서 체득한 노하우를 바탕으로, 국내 제약사의 R&D 체계 정립과 파이프라인 기획에 주도적인 역할을 했다.김 대표가 말하는 퍼스트바이오의 강점은 기초 체력이 탄탄한 회사라는 점이다. 초기 퍼스트바이오를 창업할 때 그가 구상한 모델은 기획형 바이오(Buy and Build)다. 이는 경험 많은 전문가와 풍부한 자본을 바탕으로 회사를 설립한 뒤 지속해서 밸류업을 시켜나가는 전략이다. 성장성이 높으면서 경쟁이 치열해 신속한 임상 개발이 요구되는 분야에 전력을 다해 시장을 선점하겠다는 아이디어다. 메신저리보핵산(mRNA) 기반 코로나19 백신 개발로 일약 스타덤에 오른 모더나가 대표적인 성공 사례로 꼽힌다.김 대표는 창업 초기부터 각 분야에서 실력을 인정받은 전문가들을 한 자리에 모았다. 김성곤 최고기술책임자(CTO)는 미국 머크와 종근당 효종연구소장을 거친 인물이다. 이진화 최고과학책임자(CSO)는 글락소스미스클라인(GSK), 한독 등을 거친 글로벌 R&D 전문가다. 이성규 최고운영책임자(COO)는 일리아스 바이오로직스 전략기획실장 등을 거친 인물로, 오름테라퓨틱에서 특허와 법무, 컴플라이언스 관련 업무를 맡았다.하지만 현실은 녹록지 않았다. 국내 바이오 시장은 기획형 바이오가 현실적으로 성공하기 어려운 구조였다. 자본과 제도적 기반이 충분하지 않았기 때문이다. 김 대표는 "신약 하나를 개발하는 데 수조원이 드는데, 우리나라가 투입하는 자금은 빅파마에 비해 턱없이 부족하다"면서 "이건 조기 축구회에 공 하나 쥐어주고 월드컵에서 우승하라고 하는 것과 다를 바 없다"고 했다.김 대표는 자금이 제한적인 국내 바이오 생태계에서 살아남기 위해 미국의 모델을 그대로 따라가기보다 한국형 전략으로 승부해야 한다고 판단했다. 한국 바이오텍은 미국 회사와는 달라야 한다는 것. 김 대표는 "차별화를 위해 퍼스트바이오의 기본 방침은 지적재산권(IP)을 100% 회사가 소유하도록 하고 있다"면서 "의약화학 역량을 전적으로 인하우스(in-house)로 보유해 히트물질 발굴부터 합성, 최적화 후보물질 선정(PCC)에 이르기까지 전 과정을 내부에서 완결할 수 있다는 것도 강점"이라고 했다.신약개발 효율성을 높이기 위해 인공지능(AI) 기술도 적극적으로 활용 중이다. 그는 "2021년도부터 AI 부서인 AID(Accelerated In-silico Discovery)팀을 신설했고 예측모델 등 독자적인 AI 플랫폼을 갖춰 고도화를 진행 중"이라며 "보유 AI 플랫폼을 이용하면 수십만개 이상 화합물 스크리닝과 후보물질군 확장을 통해 높은 신뢰도로 후보물질의 특성을 예측할 수 있다"고 했다.(자료: 퍼스트바이오테라퓨틱스) 이런 전략을 바탕으로 퍼스트바이오는 현재 ▲임상 1/2상 단계 면역항암제 후보물질 'FB849' ▲임상 1상 단계 퇴행성뇌질환 치료제 후보물질 'FB-101' 등 파이프라인을 운영 중이다. 전임상 단계의 뇌질환과 항암제 후보물질 4종(1ST-206, 1ST-104, FL-101, FL-102) 등도 보유했다. 이외 AI 신약 설계 엔진 플랫폼 '1ST-501', 표적단백질 분해(TPD) 발굴 플랫폼 '1ST-FINDER'도 확보한 상태다.FB849는 퍼스트바이오 파이프라인 중 개발 단계가 가장 앞서있다. FB849은 HPK1(hematopoietic progenitor kinase 1)을 타깃으로 하는 차세대 면역항암제다. 기존 면역관문억제제(ICI)에 불응하거나 내성을 보이는 환자군을 대상으로 단독 또는 병용요법으로 활용할 수 있는 가능성이 높은 물질이다. 현재 미국에서 임상 1상을 진행 중으로, 미국 모피트(Moffitt) 암센터 와 공동임상 계약을 체결, 협업 체계를 구축했다.FB-101은 퍼스트바이오의 첫 프로젝트다. c-Abl 저해제로, 퇴행성 뇌질환의 근원적인 병리 기전을 조절 가능한 신약으로 개발 중이다. 높은 뇌혈관장벽(BBB) 투과율과 낮은 오프타깃 독성, 우수한 선택성을 기반으로 경쟁 후보물질 대비 강점을 갖췄다는 게 김 대표의 설명이다.FB-101은 근위축성측삭경화증(ALS)과 파킨슨병을 적응증으로 해 임상을 진행하고 있다. 당초 미국에서 임상을 추진할 예정이었으나 자금 운용 효율성과 임상 진행 속도를 고려해 국내로 임상 거점을 전환했다. 국내에서 단일 용량 상승(SAD)과 반복 용량 상승(MAD) 시험을 마무리한 후 일본과 호주 환자를 대상으로 임상 1b과 2상으로 확장할 계획이다. 일본 시장을 선제적으로 공략해 조기 승인 가능성을 확보한 뒤, 자본과 밸류에이션을 끌어올린 상태에서 다시 미국과 글로벌 시장으로 확장한다는 구상이다.R&D 측면에서 가시화한 성과도 속속 나오고 있다. 퍼스트바이오는 지난 4월 리가켐바이오와 공동연구·기술이전 옵션 계약을 체결했다. 이번 계약은 단계별 기술이전 옵션이 포함된 광범위한 R&D 협력 구조로, 양사는 기존 항체약물복합체(ADC)의 한계를 극복할 수 있는 새로운 저분자 항암제와 차세대 페이로드(payload)를 공동 개발한다는 목표다. 해당 계약을 통해 퍼스트바이오는 리가켐바이오로부터 초기 연구자금을 확보했고 프로그램의 진척도에 따라 추가적인 연구비 지원도 받을 수 있게 됐다.올해 바이오USA에서 파이프라인 관련 미팅도 활발하게 진행했다. 김 대표는 "임상 단계 물질인 FB849와 FB-101 중심으로 활발한 논의가 이뤄졌다"면서 "ALS에 관심있는 일본 회사와도 미팅을 다수 진행했다"고 했다. 이어 그는 "이번 행사 참가는 퍼스트바이오의 파이프라인과 개발, 사업화 전략에 대한 시장의 관심을 재확인하고 동향을 파악할 수 있는 좋은 기회였다"면서 "후속 미팅과 비밀유지계약(CDA) 체결도 준비 중"이라고 덧붙였다.퍼스트바이오 지난달부터 상장 전 지분투자(Pre-IPO) 단계 신규 투자 유치를 본격화했다. 연내 클로징을 목표로 일본과 싱가포르, 홍콩 등 아시아 지역을 중심으로 해외 투자자를 물색 중이다. 앞서 퍼스트바이오는 2016년 시리즈A 80억원, 2018년 시리즈B 190억원, 2020년 브릿지펀딩 170억원, 2022년 시리즈C1 151억원, 2023년 시리즈C2 168억원 등 누적 760억원의 투자금을 유치한 바 있다.김 대표는 "지난달 기술보증기금 싱가포르지점 개소식에 초청돼 파이프라인과 사업을 소개하고 현지 벤처캐피탈(VC)과 미팅을 진행했다"면서 "FB849의 초기 임상 POC를 확인하고 2026년께 글로벌 기술이전에 성공한 뒤 2027년에 코스닥 상장하는 게 목표"라고 했다.2025-07-07 06:18:27차지현 -
 세계 첫 텔로머레이스 억제제 '라이텔로'...국내 도입 예상5편: First-in-class 텔로머레이스 억제제, 골수이형성증후군 치료제 '라이텔로(Imetelstat)' 라이텔로(RyteloⓇ, 성분명: 이메텔스타트, Imetelstat, Geron)는 세계 최초의 올리고뉴클레오타이드 텔로머레이스 억제제(Oligonucleotide telomerase inhibitor)로 2024년 6월 미국 FDA와 2025년 3월 유럽 EMA에서 '적혈구 자극제(ESA)에 반응하지 않거나 효과가 소실되었거나 투여가 불가능한, 수혈 의존성 빈혈이 있으며 8주 동안 적어도 4단위 이상의 적혈구 수혈이 필요한 저위험에서 중간 1단계 위험군의 성인 골수이형성증후군(low-to intermediate-1 risk myelodysplastic syndromes, MDS) 환자 치료'에 승인되었다.대부분의 암세포 및 암 전구세포(cancer progenitor cells)는 높은 텔로머레이스 활성과 텔로미어 유지 능력을 통해 세포가 정상적인 복제 제한 없이 무한히 분열할 수 있는 능력(세포 불사성, cellular immortality)을 가지게 되므로, 텔로머레이스는 암 치료의 유망한 표적 중 하나가 된다이러한 기전에 기반하여 개발된 이메텔스타트는 텔로머레이스를 표적으로 하는 13개 염기 서열의 올리고뉴클레오타이드로, 인간 텔로머레이스 RNA(human telomerase RNA, hTR)의 주형(template) 영역에 선택적으로 결합하여 텔로머레이스 활성을 경쟁적으로 억제함으로써 암세포를 사멸한다.이메텔스타트의 약동학(PK), 약력학(PD), 용량-반응 관계(dose-response relationship), 유효성 및 안전성은 고형암 및 혈액암을 포함한 다양한 종양 모델에서 in vitro, in vivo, 그리고 임상시험을 통해 평가되었다. 특히, 저위험 골수형성이상증후군(LR-MDS) 및 골수증식성 종양을 포함한 혈액질환을 대상으로 한 연구가 집중적으로 수행되었다.핵심 3상 임상시험인 IMerge 연구에 따르면, 이메텔스타트 투여군은 위약군 대비 8주 및 24주 이상에서 적혈구 수혈 비의존성(red blood cell-transfusion independence, RBC-TI)에 도달한 환자의 비율이 통계적으로 유의하게 높았으며, 주요 이상반응으로는 일시적이며 조절 가능한 호중구감소증(neutropenia) 및 혈소판감소증(thrombocytopenia)이 관찰되어, 전반적으로 관리 가능한 안전성 프로파일을 보였다.저위험에서 중간 1단계 위험군의 성인 골수이형성증후군(Low-to intermediate-1 risk myelodysplastic syndromes, MDS)은 무엇인가?골수이형성증후군(MDS)은 혈액 생성 줄기세포의 클론성 이상으로 인해 발생하는 혈액 종양 질환군으로, 골수 내 이형성(dysplasia)과 비효율적인 조혈(hematopoiesis)을 특징으로 한다. 이 질환은 빈혈, 백혈구 감소증, 혈소판 감소증 등의 다양한 혈구감소증(cytopenia)이 나타날 수 있다.일부 MDS 환자는 급성 골수성 백혈병(AML)으로 진행되기도 하여, 임상 경과를 더욱 복잡하게 만든다. MDS 환자의 예후는 매우 다양하며, 염색체 이상 및 혈구감소증의 중증도와 같은 요인에 따라 영향을 받는다. 따라서, MDS 환자의 임상 경과와 치료 반응은 매우 다양하므로, 정확한 예후 분류는 치료 전략 수립 및 예후 예측에 있어 필수적이다.가장 널리 사용되는 예후 평가 시스템은 1997년 제시된 국제 예후 점수 시스템( International Prognostic Scoring System, IPSS)이며, 골수 내 아세포(blast) 비율, 세포유전학적 이상(cytogenetics), 혈구감소증의 수 등 세 가지 지표를 기반으로 환자를 위험(Low), 중간-1위험(Intermediate-1), 중간-2위험(Intermediate-2), 고위험(High)의 네 군으로 분류한다.이 중 저위험에서 중간-1위험군(low-to intermediate-1 risk)은 IPSS 점수 기준으로 0~1.0점에 해당하며, 비교적 안정된 임상 경과를 보이고, 적혈구 자극제(ESA)나 보존적 치료 등의 저강도 요법이 우선적으로 고려된다.2012년에는 기존 IPSS의 한계를 보완하기 위해 개정된 국제 예후 점수 시스템(IPSS-R)이 제안되었다. IPSS-R은 세포유전학적 이상을 5단계로 세분화하고, 골수 아세포 비율, 혈색소 농도, 혈소판 수, 절대 호중구 수 등 보다 정량적인 지표를 반영함으로써 환자를 매우 저위험(very low), 저위험(low), 중간위험(intermediate), 고위험(high), 매우 고위험(very high)의 5단계로 분류한다. 이 중 IPSS-R의 저위험 및 중간위험군은 대체로 기존 IPSS의 저위험 및 중간-1위험군과 대응된다.저위험~중간-1위험군 MDS 환자는 일반적으로 생존 기간이 길고, 급성 골수성 백혈병(AML)으로의 진행 위험이 낮은 편이나, 수혈 의존성 빈혈, 증상성 혈구감소증, 분자 유전학적 이상 유무에 따라 치료 방법의 세분화가 필요하다. 최근에는 유전자 변이 기반의 위험도 분류가 병용되며, 보다 정밀한 예후 예측과 치료 맞춤화에 기여하고 있다.이러한 MDS는 텔로미어(telomere) 단축과 관련된 조혈 줄기세포 기능 저하와 병적 클론의 형성을 특징으로 하며, 일부 클론은 텔로머레이스(telomerase)를 재활성화하여 불사성(immortality)을 획득하고 질환의 진행에 관여한다. 텔로머레이스는 이러한 병태생리적 역할로 인해 MDS에서 유망한 치료 표적이 된다.텔로미어(Telomere)는 어떤 물질인가? 2009년 노벨 생리의학상은 엘리자베스 블랙번(Elizabeth Blackburn), 캐럴 그라이더(Carol Greider), 잭 쇼스택(Jack Szostak)에게 수여되었다. 이들은 염색체 말단에 위치한 특수한 반복 서열 구조인 텔로미어(telomere)와 그 유지에 관여하는 효소인 텔로머레이스(telomerase)를 규명함으로써, 세포 분열 과정에서 유전 정보가 어떻게 안정적으로 보존되는지를 설명하는 데 기여하였다.노벨위원회는 "이들 세 명의 연구는 염색체가 세포 분열 과정 중 퇴화를 방지하고, 완전하게 복제될 수 있는지를 둘러싼 오랜 생물학적 의문에 대한 해답을 제공하였다"고 평가하였다.텔로미어에는 세포의 염색체 말단에 반복적인 DNA 서열이 존재하며, 이는 유전물질의 손상을 방지하고 염색체의 구조적 안정성을 유지하는 역할을 수행한다. 그러나 체세포는 분열을 반복할수록 텔로미어 길이(telomere length)가 '모래시계'처럼 점진적으로 짧아지며, 일정 임계점에 도달하면 세포는 증식을 멈추고 세포 노화(senescence)나 세포자멸사사(apoptosis)를 유도하게 된다(Figure 1).이때 텔로머레이스는 텔로미어의 말단을 연장할 수 있는 효소로 세포의 수명을 연장시키고, 이론적으로는 세포의 불사성(immortality)를 유도할 가능성을 지닌다. 이러한 텔로미어는 생물체의 노화 과정과 직접적으로 연관되어 있고, 또한 대부분의 암세포는 텔로머레이스의 활성을 통해 텔로미어 길이를 유지하거나 연장함으로써 무한 증식 능력을 가지게 된다. 즉, 텔로미어 단축은 세포 노화를 유도하는 반면, 텔로미어 보존은 암세포의 지속적 증식을 가능하게 한다. 따라서, 텔로미어 기능의 조절은 노화 억제 혹은 암 치료를 위한 잠재적 전략으로 제시되고 있다.텔로머레이스(Telomerase)란 무엇인가? 텔로머레이스(Telomerase)는 염색체 말단에 있는 3' 말단 돌출부(3' overhang)에 반복적인 염기서열을 추가하는 기능을 가진 리보핵단백질 복합체(ribonucleoprotein complex)로, 역전사효소(reverse transcriptase) 활성을 갖는다. 3' 말단 돌출부는 이중가닥 DNA 말단에서 한 가닥이 다른 가닥보다 더 길어 돌출된 형태로, 텔로미어 구조에서 텔로머레이스가 인식하고 작용하는 주요 부위이다.텔로머레이스는 자체의 RNA 구성요소인 TERC(telomerase RNA component)를 주형(template)으로 삼아, TERT(telomerase reverse transcriptase)의 역전사 효소 활성을 통해 반복적인 TTAGGG 염기서열을 합성함으로써 염색체 말단의 텔로미어를 연장한다(Figure 2). 인간의 경우, 텔로머레이스는 인간 텔로머레이스 역전사효소(human telomerase reverse transcriptase, hTERT) 유전자에 의해 암호화되는 촉매 소단위(catalytic subunit)와 인간 텔로머레이스 RNA(human telomerase RNA, hTR) 유전자 산물인 RNA 주형(template)을 중심으로 구성된 복합체이다. 여기에 dyskerin, NHP2, NOP10, GAR1 등 다양한 보조 단백질들이 결합하여, 효소 복합체의 구조적 안정성과 기능적 활성을 조절한다.텔로머레이스를 ‘자동차’ 전체에 비유한다면, TERT는 실제로 DNA를 합성하는 역할을 수행하는 ‘엔진’에 해당하며, hTR(또는 TERC)는 어떤 염기서열을 합성할지를 지시하는 ‘설계도’에 해당하는 RNA 주형으로 볼 수 있다.인체 내 약 120여 종의 세포 중 대부분은 텔로미어를 합성하는 효소인 텔로머레이스의 활성을 갖지 않으며, 이로 인해 세포는 분열이 반복될수록 텔로미어가 점진적으로 단축되고, 결국 복제에 따른 세포 노화(replicative senescence)에 도달하게 된다. 반면, 일부 높은 분열 능력을 가진 조직의 세포들은 예외적으로 텔로머레이스 활성을 유지한다.이러한 세포에는 모낭(hair follicle), 구강 편평상피(squamous epithelium), 피부 표피의 기저층(basal layer of epidermis), 제2형 폐포상피세포(type 2 alveolar epithelial cells), 간세포(hepatocytes), 장의 장선(intestinal crypts), 정원세포(spermatogonia) 등이 있다. 이들 세포에서 텔로머레이스 활성이 결여될 경우, 조직의 항상성 유지 및 생식 기능에 중대한 장애가 초래된다.특히, 정자 형성에 관여하는 정원세포(spermatogonia)에서 텔로머레이스 활성이 결여되면, 정자의 텔로미어 길이가 충분히 유지되지 못하고 단축된 상태로 전달된다. 이로 인해 형성된 배아는 텔로미어 단축에 기인한 세포 노화가 조기에 시작되며, 조기 노화(progeria)와 유사한 양상을 보일 수 있다. 실제로 이는 복제 양 돌리(Dolly) 사례에서 관찰된 바 있으며, 단축된 텔로미어가 수명 감소와 밀접하게 연관됨을 시사한다.이는 일반적인 체세포에서는 텔로머레이스 활성이 매우 낮은 수준으로 유지하지만, 생식세포와 줄기세포에서는 해당 효소가 구성효소(constitutive enzyme)로서 지속적으로 발현된다. 구성효소는 소화효소와 같이 항상 일정 수준으로 활성화되어 있는 효소이다.이에 반해 유도효소(inducible enzyme)는 특정 자극(예: 약물, 독성물질 등)에 의해 후천적으로 유도되는 효소이다. 이러한 분류 기준에 따라 텔로머레이스는 생식세포 및 줄기세포에서 구성효소로 기능하며, 암세포에서는 구성효소 및 유도효소적 특성을 보이는 이중적 성격을 가진다고 볼 수 있다.줄기세포 중에서도 배아줄기세포(embryonic stem cells) 및 유도만능줄기세포(induced pluripotent stem cells)는 고도로 안정된 텔로머레이스 활성을 보이며, 이로 인해 세포 분열에 따른 텔로미어의 단축이 거의 발생하지 않고, 복제에 따른 세포 노화에도 이르지 않는다.반면, 중간엽줄기세포(mesenchymal stem cells), 신경줄기세포(neural stem cells), 조혈모세포(hematopoietic stem cells) 등 성체 유래 줄기세포에서는 텔로머레이스 활성이 상대적으로 낮으며, 이로 인해 제한적인 텔로미어 단축이 관찰된다.TERT(Telomerase reverse transcriptase)란 무엇인가? 대부분의 체세포는 약 60~80회의 분열(population doublings) 이후 텔로미어가 임계 길이에 도달하게 되며, 이 시점에서 이중가닥 DNA 절단(double-strand break) 신호가 유도되어 복제에 따른 노화로 전환된다.이러한 현상은 체세포 내에서 텔로머레이스 활성이 거의 존재하지 않기 때문에 발생하는데, 이는 텔로머레이스의 RNA 구성 요소인 TERC(hTR)가 존재하더라도, 촉매 활성을 담당하는 TERT 유전자의 전사가 억제되어 있기 때문이다. 따라서, TERT 발현의 억제는 체세포에서 텔로머레이스 활성이 결핍되는 주요 원인이며, 텔로미어 단축의 분자적 기전으로 작용한다.뿐만 아니라, TERT는 단순한 텔로미어 연장 기능 외에도 텔로미어 말단의 캡핑(capping)과 전체 구조 유지에도 중요한 역할을 한다. 이는 다양한 암종의 약 80~90%에서는 TERT 발현이 재활성화되어 텔로머레이스 활성이 증가되어 있으며, 암세포의 불사화와 밀접하게 연관되어 있다.결과적으로, TERT 발현은 텔로미어 연장과 세포 노화 회피를 통해 암세포 특성이 획득되는 초기 단계에서 결정적인 분자 표지자로 작용한다. 이러한 TERT 발현 유도는 다양한 내•외부 요인 중 유전자 불안정성과 돌연변이가 가장 대표적인 기전으로 제시되고 있다.암의 발생 과정에서 텔로미어 길이의 보존이 빈번히 동반되며, 이는 주로 인간 텔로머레이스 역전사효소(hTERT)의 발현 증가에 따른 텔로머레이스 활성의 재개로 설명된다. 따라서 TERT의 발현 조절 기전은 텔로머레이스 기반 항암 치료법의 핵심 표적으로 주목받고 있으며, 암세포 특이적 바이오마커로서의 임상적 활용 가능성 또한 높다.텔로머레이스와 암과의 관계는 어떠한가? 텔로머레이스의 비정상적인 재활성화는 암세포에서 흔히 관찰되는데, 이는 텔로미어 단축으로 유도되는 세포자멸사를 회피하고 무한 증식 능력을 획득하는 데 핵심적인 기전으로 작용한다. 실제로, 전체 고형암 및 혈액암의 약 90% 이상에서 텔로머레이스 활성이 현저히 증가되어 있음이 관찰된다.여러 암 조직 생검에서 텔로머레이스 활성의 증가가 종양의 병기 및 악성도와 유의한 상관관계를 보이는 반면, 대부분의 정상 성인 조직에서는 텔로머레이스 활성이 거의 검출되지 않으며, 일부 조혈모세포나 면역세포에서만 일시적으로 나타나는 것으로 알려져 있다.이는 암세포 및 암전구세포에서 공통적으로 관찰되는 높은 수준의 텔로머레이스 발현과 텔로미어 유지 현상을 억제하여 암세포의 증식을 제한하는 치료 방법이 된다.특히, RNA 기반 치료법은 텔로머레이스의 RNA 구성요소인 hTR 또는 hTERT mRNA를 표적으로 하여 효소 활성을 간접적으로 억제하는 방식으로 주목받고 있다. 이 중 안티센스 올리고뉴클레오타이드(antisense oligonucleotides, ASO) 및 RNA 간섭(small interfering RNA, siRNA) 기술은 텔로머레이스 기능을 선택적으로 차단할 수 있는 새로운 접근법이다.대표적 예로는 이멜스타트(Imetelstat)가 있으며, 이는 인간 텔로머레이스 RNA(hTR)의 주형 영역에 상보적으로 결합하는 리간드 결합형 ASO로 설계되어, 텔로미어 연장 과정을 억제함으로써 암세포의 증식 억제를 유도한다. 이와 같은 RNA 기반 접근은 텔로머레이스 억제를 통한 항암 치료의 새로운 패러다임을 제시하며, 표적 치료제 개발에 있어 중요한 진전을 이끌고 있다.텔로머레이스 억제를 통한 항암 치료 전략은? 텔로머레이스를 표적으로 한 항암제 개발은 다양한 작용기전을 바탕으로 다방면에서 진행되고 있으며, 크게 RNA 기반 억제제, 전사 억제 화합물, G-사중나선 안정화제, 그리고 면역치료 백신 전략으로 구분할 수 있다.1. RNA 기반 억제제 가장 활발히 연구되고 있는 접근은 안티센스 올리고뉴클레오타이드(ASO) 또는 RNA 간섭(siRNA) 기술을 활용하여 텔로머레이스 RNA 구성요소(hTR 또는 TERC)를 표적으로 하는 전략이다. 이들 억제제는 텔로머레이스 복합체 내의 RNA 주형에 상보적으로 결합함으로써 효소 활성을 억제하거나, RNase H 의존적 분해를 유도하여 텔로머레이스 기능을 근본적으로 차단한다.대표적 약제인 이멜스타트(Imetelstat)는 티오포스포라마이드(thio-phosphoramidate) 변형을 적용한 ASO로, hTR의 템플릿 영역에 결합하여 텔로미어 연장을 저해한다.2. hTERT 전사 억제 저분자 화합물 이 저분자 화합물은 텔로머레이스의 촉매 소단위인 hTERT 유전자의 전사를 직접 억제하는 방식으로, 프로모터 영역 조절 또는 후성유전학적 메커니즘을 통해 유전자 발현 자체를 낮춘다. 일부 저분자 화합물은 hTERT 단백질에 직접 결합하여 효소 활성을 차단한다. 식물 유래 플라보노이드(예: genistein)가 TERT 전사를 억제하는 기능이 보고된 바 있으나 낮은 선택성과 잠재적인 세포독성으로 인해 임상 적용에는 제한이 있다.3. G-사중나선(G-quadruplex) 안정화제 이 안정화제는 텔로미어 말단에서 형성되는 G-사중나선 구조를 안정화시켜 텔로머레이스의 접근을 물리적으로 차단하는 방식이다. 해당 구조는 G-rich 반복 서열에서 자연적으로 형성되며, 일부 저분자 화합물은 이 구조에 특이적으로 결합하여 G-quadruplex 형태의 유지 및 안정화를 유도한다.이 방법은 효소가 아닌 기질을 표적으로 한다는 점에서 기존 억제제와 구별되며, 비교적 빠른 약효 발현이 가능하다. 그러나 G-rich 서열이 텔로미어 외에도 다양한 유전자의 조절부위에 존재하기 때문에, 표적 특이성 확보가 주요 과제로 남아 있다.4. 텔로머레이스를 항원으로 활용한 면역치료 텔로머레이스를 면역계의 표적으로 활용하는 전략도 개발되고 있다. 이는 hTERT 유래 펩타이드를 기반으로 하는 항암 백신을 통해, 텔로머레이스를 발현하는 종양세포를 면역세포가 인식하고 제거하도록 유도한다. 비소세포폐암(NSCLC), 췌장암 등 다양한 고형암에서 임상시험이 진행되고 있으며, 면역기억 반응을 통한 재발 억제 효과가 기대된다. 다만, 환자의 HLA 유형 및 종양미세환경(TME)에 따라 치료 반응의 편차가 존재하여, 정밀한 환자 선별 전략이 병행되어야 한다.이와 같이 텔로머레이스 억제 전략은 암세포 특이성이 높고 장기적인 종양 억제 효과를 유도할 수 있다는 점에서 유망한 접근이다. 그러나 기전상 텔로미어 길이의 점진적 단축을 필요로 하므로, 치료 효과 발현까지 수 주에서 수 개월이 소요되는 경향이 있다. 또한, 일부 암에서는 텔로머레이스 비의존적인 대체적 길이 조절(ALT, alternative lengthening of telomeres) 경로가 활성화되어 있어 단독요법으로는 제한적일 수 있다.이러한 한계를 극복하기 위해, 최근에는 DNA 손상 유도제, 면역관문억제제(PD-1/PD-L1 억제제), PARP 억제제 등과의 병용요법이 시도되고 있다. 또한 텔로머레이스 발현 수준, 텔로미어 길이 상태, ALT 경로 활성 여부 등을 고려한 환자 맞춤형 정밀의학적 접근이 병행됨으로써, 텔로머레이스 억제제의 임상적 유용성은 점차 확대되고 있다.뉴클레오타이드(Nucleotide)와 합성 올리고뉴클레오타이드의 차이는? 뉴클레오타이드는 모든 생명체에 보편적으로 존재하는 저분자 유기 화합물로, DNA와 RNA와 같은 핵산의 기본 단위이며 에너지 전달(ATP, GTP), 세포 신호전달(cAMP, cGMP), 효소 보조인자(NAD⁺, FAD) 등의 생리적 기능에 필수적인 역할을 수행한다. 이러한 분자는 세포 내에서 de novo 합성 경로 또는 재활용 경로(salvage pathway)를 통해 지속적으로 생성되며, 생명 유지에 핵심적인 역할을 한다.이에 반해, 올리고뉴클레오타이드는 일반적으로 몇 개에서 수십 개의 뉴클레오타이드가 공유결합으로 연결된 짧은 핵산 서열로, 인공적으로 합성된 생체분자이다. 자연적으로는 microRNA나 small nuclear RNA와 같은 일부 예외적인 경우를 제외하면 생체 내에서 잘 합성되지 않으며, 주로 화학적으로 합성되어 특정 유전 서열의 인식이나 분자 기능의 조절을 목적으로 활용된다.합성 올리고뉴클레오타이드는 분자생물학, 진단, 치료, 유전자 조작 등 다양한 분야에서 핵심 도구로 활용되고 있으며, 기능, 표적, 화학적 변형에 따라 , 다음과 같이 분류된다.첫째, 기능적 측면에서 ▲ mRNA 또는 pre-mRNA에 결합하여 유전자 발현을 억제하거나 RNA 스플라이싱을 조절하는 안티센스 올리고뉴클레오타이드(antisense oligonucleotide, ASO), ▲ RNA 간섭(RNAi)을 유도하여 표적 mRNA의 분해를 유도하는 소간섭 RNA(siRNA) 또는 마이크로 RNA(miRNA) 유사체, ▲ 고특이적으로 단백질에 결합하여 기능을 저해하거나 조절하는 압타머(aptamer), ▲ CRISPR 시스템에서 유전자 편집을 유도하는 가이드 RNA(guide RNA, gRNA), ▲ 전사인자와 결합하여 표적 유전자 조절을 간섭하는 디코이(decoy), ▲ PCR, qPCR, 유전자 탐지 등 핵산 분석 기술에 사용하는 프라이머(primer) / 프로브(probe) 등으로 분류된다.둘째, 표적 및 작용기전에 따라 ▲ DNA, ▲ mRNA, ▲ pre-mRNA, 또는 단백질 등 다양한 분자에 작용할 수 있으며, 그 기전은 전사 억제, 번역 차단, RNA 스플라이싱 조절, 단백질-핵산 상호작용 차단 등으로 확장된다.셋째, 화학 구조적 변형 측면에서 천연형(natural-type) 외에도 약물 안정성 및 효율성을 개선하기 위한 다양한 화학적 변형이 도입된다. 대표적으로 ▲ 인산기 산소를 황으로 치환하여 핵산분해효소 내성 증가를 위한 phosphorothioate(PS), ▲ 리보스의 2′ 위치에 화학기 추가로 결합력과 안정성 증가를 위한 2′-O-methyl RNA 및 2′-fluoro RNA, ▲ 리보스 고정을 통해 고결합 친화성 및 특이성 확보한 locked nucleic acid(LNA), ▲ 간세포 타깃팅 또는 세포 내 전달력 향상을 위한 GalNAc 또는 지질을 접합시킨 conjugated oligonucleotide 등이 있으며, 이는 체내 안정성, 표적 결합력, 약물 전달 효율성을 향상시키는 데 기여한다.요약하면, 뉴클레오타이드는 생명체 내에서 합성되는 주요 생리활성 분자인 반면, 올리고뉴클레오타이드는 외부에서 합성되어 생체 내 특정 유전자나 분자 기전을 정교하게 조절하기 위한 인공 핵산 서열이라는 점에서, 양자는 생성 방식과 생리적 존재 양상에서 본질적으로 다르다. 그럼에도 불구하고, 올리고뉴클레오타이드는 자연계 핵산의 기능을 모방하거나 확장함으로써 차세대 핵산 기반 치료제 및 진단 기술의 핵심 플랫폼으로 부상하고 있다.ASO(Antisense Oligonucleotide, 안티센스 올리고뉴클레오타이드)란? ASO는 mRNA를 표적으로 설계된 짧은 합성 단일가닥 DNA 분자로, 특정 mRNA 서열과 상보적으로 결합함으로써 유전자 발현을 억제하거나 조절하는 기능을 수행한다(Figure. 3).ASO는 비교적 간단한 화학 구조를 기반으로 하면서도, 전사체의 분해 유도, RNA 스플라이싱 (splicing) 조절, 번역 억제 등 다양한 작용기전을 통해 유전 정보의 흐름을 정교하게 제어할 수 있는 장점을 가진다.ASO의 작용기전은 화학적 변형 방식과 결합 표적에 따라 다양하게 구분된다. 대표적으로 RNase H 매개 분해는 ASO가 표적 mRNA와 이중가닥을 형성한 후, 세포 내 RNase H 효소에 의해 해당 mRNA가 분해되어 단백질 생성을 원천적으로 차단하는 기전이다.또한, 스플라이싱 조절용 ASO는 pre-mRNA의 엑손/인트론 경계부에 결합하여, 엑손 스키핑(skipping) 또는 보존을 유도함으로써 단백질의 구조와 기능을 변형시킬 수 있다. 이 외에도 번역 개시 억제, mRNA 안정성 저해 등 다양한 방식으로 작용이 가능하다.이러한 특성을 바탕으로, ASO는 기존 소분자 화합물이나 단백질 기반 치료제와 달리 기능 상실(loss-of-function) 혹은 기능 획득(gain-of-function) 유전자 돌연변이 모두를 정교하게 조절할 수 있다.그러나 ASO 치료제는 면역반응 유발, 비표적 결합(off-target effect), 체내 약물 전달 효율 등의 한계를 지니고 있으며, 이를 극복하기 위해 phosphorothioate 치환, 2′-O-methyl 및 LNA 변형, GalNAc 결합을 통한 간세포 표적화, 지질 나노입자 기반 전달체 등 다양한 기술적 발전이 이루어지고 있다.이러한 발전은 ASO의 치료적 효능을 향상시키는 데 핵심적인 기여를 하고 있으며, ASO 기반 핵산 치료제가 차세대 정밀의학 기반의 분자표적 치료제로 자리매김할 수 있는 가능성을 높이고 있다.텔로머레이스 표적 올리고뉴클레오타이드(Telomerase-targeted oligonucleotide, TTO)란? TTO는 표적 핵산 서열에 상보적으로 결합하는 구조를 가지면서도, 기존의 ASO와는 본질적으로 다른 작용기전을 가진다. 즉 일반적인 ASO는 mRNA의 분해(RNase H 의존적 경로) 또는 스플라이싱 조절을 통해 단백질 생성을 억제하지만, TTO는 hTR의 템플릿 서열에 직접 결합함으로써 텔로머레이스 효소 복합체의 활성 부위를 차단한다. 이는 효소의 기질 인식 및 촉매 반응 자체를 방해하는 비정형(non-canonical) ASO로 분류된다.이러한 TTO는 효소 작용 자체의 차단을 통해 효소 기능 차단(enzyme activity inhibition)이라는 새로운 패러다임을 제공한다. 특히 텔로머레이스 활성이 높은 암세포에서 선택적으로 작용함으로써, 정상세포에 대한 영향을 최소화하면서 암 특이적 억제 효과를 유도할 수 있다.대표적인 TTO로는 이메텔스타트(Imetelstat)가 있으며, 이는 hTR의 템플릿 영역에 상보적으로 결합하는 티오인산화(thio-phosphoramidate) 올리고뉴클레오타이드로 설계되었다.이메텔스타트는 어떤 약제인가? 이메텔스타트(Imetelstat, 제품명: 라이텔로 정맥주사, Rytelo®)는 텔로머레이스를 직접 표적으로 하는 최초의 올리고뉴클레오타이드 기반 치료제로, 2024년 미국 FDA로부터 승인받은 이후 골수이형성증후군(MDS) 치료 영역에서 새로운 치료 축으로 부상하고 있다. 이 약제의 승인 적응증은 "8주간 4단위 이상의 적혈구 수혈이 필요한 수혈 의존성 빈혈을 가진 저위험~중간-1 위험군 MDS 성인 환자 중, 적혈구생성자극제(ESA)에 반응하지 않거나 반응이 소실되었거나, 투여가 불가능한 경우"이다.이메텔스타트는 기존의 ASO와는 구별되는 비정형 ASO로 분류되며, 비정상적인 텔로머레이스 활성을 보이는 악성 조혈모세포(HSCs) 및 전구세포(HPCs)를 선택적으로 억제함으로써 병적 클론의 제거와 정상 조혈 기능의 회복을 유도하는 질환 수정형(disease-modifying) 치료 제이다.분자 구조적으로, 이메텔스타트는 13개의 뉴클레오타이드로 구성된 단일가닥 DNA 서열이며, 티오인산화(thio-phosphoramidate) 변형을 통해 핵산분해효소(nuclease) 저항성, 수용성, 대사적 안정성 등의 약물학적 특성이 향상되었다. 또한 5′ 말단에 팔미토일기(palmitoyl group)가 결합되어 소수성을 증가시켜 세포막 투과성 및 세포 내 유지성을 강화하며, 별도의 형질전환 과정 없이도 세포 내 작용이 가능하도록 설계되었다.전임상 연구에서는 이메텔스타트의 약물 노출과 텔로머레이스 억제 간의 명확한 약력학적 상관성이 확인되었고, 텔로머레이스 활성을 50% 이상 억제하는 수준의 약리 효과가 임상적으로 확보 가능한 범위 내에 있음이 입증되었다. 또한, 골수증식성 질환 모델(예: 본태성 혈소판증, 골수섬유증, 급성 골수성 백혈병 등)에서는 시험관 내(in vitro) 및 생체 내(in vivo) 실험 모두에서 강력한 항종양 활성을 나타냈다.특히 저위험 MDS 환자에서 이메텔스타트는 텔로미어 단축, hTERT 과발현, 분화 억제 등으로 특징지어지는 병적 조혈모세포 및 전구세포를 선택적으로 제거함으로써, 정상 조혈의 회복과 함께 적혈구 수혈 비의존 기간(RBC-TI)의 연장, 혈색소 수치의 향상, 염색체 이상 클론 및 돌연변이 부담의 감소를 유도하였다.아울러, 이메텔스타트는 면역회피 특성을 가진 악성 클론에서도 항암 활성을 유지함으로써, 기존 면역항암제 또는 세포독성 항암제에 비해 임상적 적용 가능성이 높다. 현재 진행 중인 다수의 임상시험 결과에 따라, MDS뿐 아니라 골수섬유증(myelofibrosis), 기타 혈액암 영역으로의 적응증 확장 가능성도 제시되고 있다.이메텔스타트의 약리 기전은? 이메텔스타트는 TERT-targeting telomerase complex inhibtor 또는 RNA-template targeting telomerase inhibitor로, 인간 텔로머라제의 RNA 구성 요소(hTR)의 주형 영역에 상보적으로 결합하여 텔로머레이스 복합체의 활성 부위에서 기질 결합 및 연장을 직접 차단한다. 즉 hTR의 주형 서열(3′-CAAUCCCAAUC-5′)에 상보적인 염기서열(5′-palmitate-TAGGGTTAGACAA-NH₂-3′)이 결합함으로써, 텔로머레이스 효소의 활성을 억제하여 텔로미어 말단에 반복 서열을 추가하는 기능을 경쟁적으로 차단한다. 이로 인해 암세포 내에서의 텔로미어 길이가 점진적으로 짧아지며, 결국 세포 노화 또는 세포자멸사를 유도하게 된다(Figure 4). 골수이형성증후군(MDS) 및 악성 줄기세포 및 전구세포에서 텔로머레이스 활성 및 인간 텔로머레이스 역전사효소(hTERT) RNA 발현이 증가한 것으로 보고되었다. 이에 여러 연구에서 이메텔스타트 치료가 텔로미어 길이 감소, 악성 줄기세포 및 전구세포의 증식 감소, 그리고 세포자멸사를 유도함으로써 세포 증식 억제 및 수명 단축 효과를 나타낸 것으로 보고되었다.또한, 이 약제는 텔로머레이스의 촉매 소단위인 hTERT의 발현을 억제함으로써 효소 활성을 이중적으로 저해하는데, 이 hTERT는 텔로머레이스 활성을 조절하는 주요 속도 제한 인자(rate-limiting component)로 알려져 있다.이러한 이멜스타트의 작용 기전은 항원-항체 반응이나 면역세포 활성화를 기반으로 하는 기존 면역항암제와는 달리, 종양 세포의 분열 및 생존을 유지하는 내재적 기전인 텔로머레이스 의존성을 직접 차단한다는 점에서 근본적인 차별성을 갖는다.이멜스타트(RYTELOⓇ) 3상 임상은 어떻게 진행되었나? 이메텔스타트의 임상적 유효성은 IMerge 3상 연구를 통해 입증되었다. 본 연구는 무작위배정, 이중눈가림, 위약대조, 다기관 임상시험으로 설계되었으며, 저위험 또는 중간-1위험군 골수이형성증후군(MDS) 환자 중 수혈 의존성을 보이는 성인 178명을 대상으로 시행되었다. 환자 등록 기준은 무작위배정 16주 전의 8주간 기간 동안 적어도 4단위 이상의 적혈구 수혈 필요 이력이 있는 경우로 정의되었다.등록 환자들은 모두 적혈구생성자극제(ESA)에 반응이 없었거나 반응이 소실되었거나, ESA 투여가 적절하지 않다고 판단된 경우였다. 주요 포함 기준에는 절대 호중구 수치 ≥ 1.5 × 10⁹/L, 혈소판 수 ≥ 75 × 10⁹/L이 포함되었으며, del(5q) 염색체 이상 보유자, 레날리도마이드(Lenalidomide) 또는 아자시티딘(Azacitidine)과 데시타빈(Decitabine) 같은 저메틸화제(hypomethylating agents, HMA) 치료 이력이 있는 환자는 제외되었다.무작위배정은 2:1 비율로 수행되어, RYTELO 7.1 mg/kg 정맥주사군(n=118) 또는 위약군(n=60)에 배정되었으며, 28일 주기(cycle)로 반복 투여되었다. 치료는 질병 진행, 용인할 수 없는 독성, 또는 환자의 자의적 중단 시점까지 지속되었다. 무작위배정은 기존 RBC 수혈 부담 및 IPSS 위험군 등급을 기준으로 계층화되었다. 모든 환자에게는 필요 시 적혈구 수혈을 포함한 지지요법(supportive care)이 병행 제공되었다.평가 기간은 RYTELO 투여군에서 중앙 추적기간 19.5개월(범위: 1.4–36.2개월), 위약군에서 17.5개월(범위: 0.7–34.3개월)이었으며, 주요 유효성 평가 변수는 적혈구 수혈 독립(RBC transfusion independence, RBC-TI) 달성 비율이었다. 이는 무작위배정 이후부터 차기 항암 치료 개시 전까지의 기간 중 연속된 8주(≥56일) 또는 연속된 24주(≥168일) 동안 적혈구 수혈이 전혀 이루어지지 않은 경우로 정의되었다.그 결과, 8주 이상 RBC-TI 도달률은 RYTELO 군에서 39.8%(95% CI: 30.9–49.3)로, 위약군의 15.0%(95% CI: 7.1–26.6) 대비 통계적으로 유의하게 높았다(p < 0.001). 또한 24주 이상 RBC-TI 도달률 역시 RYTELO 군에서 28.0% (95% CI: 20.1–37.0)로, 위약군 3.3% (95% CI: 0.4–11.5)와 비교하여 유의한 차이를 보였다(p < 0.001). 이러한 결과는 RYTELO가 ESA 불응 또는 부적합 환자군에서 수혈 의존성을 유의하게 줄이고, 적혈구계 조혈 회복을 유도할 수 있는 잠재력을 입증하는 것으로 해석된다.안전성 측면은 RYTELO 군에서 위약군 대비 ≥10% 이상, ≥5% 차이를 보인 주요 이상반응은 혈소판 감소, 백혈구 감소, 호중구 감소, AST/ALT/ALP 상승, 피로, 부분 트롬보플라스틴 시간 연장, 관절/근육통, COVID-19 감염, 두통 등이었다.따라서, RYTELO는 저위험 MDS 환자에서 임상적으로 의미 있는 수혈 독립 향상을 유도하였으며, 전반적으로 관리 가능한 안전성 프로파일을 보였다. 권장 투여 용량은 7.1 mg/kg이며, 4주마다 2시간에 걸쳐 정맥 투여한다. 이멜스타트의 앞으로의 예상은? 골수이형성증후군(MDS)은 조혈모세포의 분화 및 성숙에 결함이 생겨 비정상적 조혈과 말초 혈구감소증을 유발하는 이질적인 클론성 조혈장애이다. 특히 저위험군 MDS 환자에서는 만성적인 적혈구 수혈 의존성 빈혈이 주요 임상 양상으로 나타나며, 삶의 질 저하 및 철분 과부하에 의한 이차적 장기 손상이 주요 합병증으로 작용한다.현재까지 이들 환자에서 사용 가능한 치료제로는 적혈구생성자극제(ESA) 및 저메틸화제(HMA) 등이 있으나, 반응률의 한계와 장기 치료 효과에 대한 의문이 지속적으로 제기되고 있다.텔로머레이스는 텔로미어 길이를 유지하여 세포의 분열 한계를 극복하게 하는 핵심 효소로, 대부분의 암세포 및 악성 조혈모세포에서 비정상적으로 활성이 증가되어 있는 것이 특징이다. 이러한 활성을 선택적으로 억제함으로써 병적 조혈세포의 증식을 제한하고 정상 조혈을 회복시키는 접근은 질환의 근본 기전을 타겟으로 하는 질환 수정형(disease-modifying) 치료전략으로 주목받고 있다.이메텔스타트(Imetelstat)는 인간 텔로머레이스 복합체(hTERT/hTR)에 직접 결합하여 활성을 경쟁적으로 억제하는 first-in-class 올리고뉴클레오타이드 기반 치료제로, 텔로미어 유지 능력을 상실하게 하여 세포 자멸사 및 증식 억제를 유도한다. 특히 병적 조혈모세포(HSCs/HPCs)와 백혈병 줄기세포(LSCs)에 선택적으로 작용하며, 정상 조혈세포에 대한 영향은 제한적으로 보고되고 있다.IMerge 3상 임상시험에서 이메텔스타트는 ESA에 반응하지 않거나 부적합한 저위험~중간-1 위험군 MDS 환자를 대상으로 통계적으로 유의한 적혈구 수혈 독립 효과를 입증하였다. 8주 이상 수혈 독립률(RBC-TI)은 이메텔스타트군에서 39.8%, 위약군에서 15.0%로 나타났으며, 24주 이상 수혈 독립률도 각각 17.8%와 1.6%로 유의한 차이를 보였다. 이는 기존 치료옵션에 반응하지 않는 환자 집단에 있어 새로운 치료 패러다임을 제시한 근거로 평가된다.다만, 현재 이메텔스타트는 저위험 MDS + ESA 실패 + 수혈 의존성 빈혈이라는 제한된 적응증으로 승인되어 있으며, TP53 돌연변이나 고위험군 MDS는 제외 대상에 해당된다. 또한 치료 효과 발현까지 수 주에서 수개월이 소요되며, 호중구감소증(72%) 및 혈소판감소증(65%) 등 고빈도의 혈액학적 이상반응이 동반될 수 있다는 점은 임상적 고려가 필요하다.그럼에도 불구하고, 텔로머레이스라는 근원적 분자 표적을 겨냥한 이메텔스타트는 기존 화학요법 및 면역조절제와는 차별화된 기전을 통해 조혈계 악성질환에 있어 정밀의학적 치료 전략으로서의 가능성을 보여주고 있다. 이미 미국 및 유럽에서 승인된 약제로서, 향후 국내 도입과 더불어 적응증 확대, 병용요법, 고위험 환자군에서의 임상적 검토가 필요할 것으로 예상한다.참고문헌 1. Alexander Vaiserman, Dmytro Krasnienkov “Telomere Length as a Marker of Biological Age: State-of-the-Art, Open Issues, and Future Perspectives” Front. Genet. 11:630186(2021). 2. Virginia Boccardi “Aging, Cancer, and Inflammation: The Telomerase Connection” J. Mol. Sci. 2024, 25(15), 8542. 3. Virginia Boccardi, and Luigi Marano “Aging, Cancer, and Inflammation: The Telomerase Connection” Int. J. Mol. Sci. 2024, 25, 8542. 4. Zachary Schrank, Nabiha Khan, Chike Osude, Sanjana Singh et al. “Oligonucleotides Targeting Telomeres and Telomerase in Cancer” Molecules 2018, 23, 2267. 5. Ashley L. Lennoxm, Fei Huang, Melissa Kelly Behrs, Mario González-Sales et al. “Imetelstat, a novel, first-in-class telomerase inhibitor:Mechanism of action” Clin Transl Sci. 2024;17:e70076 6. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-06-13 06:24:02최병철 박사
세계 첫 텔로머레이스 억제제 '라이텔로'...국내 도입 예상5편: First-in-class 텔로머레이스 억제제, 골수이형성증후군 치료제 '라이텔로(Imetelstat)' 라이텔로(RyteloⓇ, 성분명: 이메텔스타트, Imetelstat, Geron)는 세계 최초의 올리고뉴클레오타이드 텔로머레이스 억제제(Oligonucleotide telomerase inhibitor)로 2024년 6월 미국 FDA와 2025년 3월 유럽 EMA에서 '적혈구 자극제(ESA)에 반응하지 않거나 효과가 소실되었거나 투여가 불가능한, 수혈 의존성 빈혈이 있으며 8주 동안 적어도 4단위 이상의 적혈구 수혈이 필요한 저위험에서 중간 1단계 위험군의 성인 골수이형성증후군(low-to intermediate-1 risk myelodysplastic syndromes, MDS) 환자 치료'에 승인되었다.대부분의 암세포 및 암 전구세포(cancer progenitor cells)는 높은 텔로머레이스 활성과 텔로미어 유지 능력을 통해 세포가 정상적인 복제 제한 없이 무한히 분열할 수 있는 능력(세포 불사성, cellular immortality)을 가지게 되므로, 텔로머레이스는 암 치료의 유망한 표적 중 하나가 된다이러한 기전에 기반하여 개발된 이메텔스타트는 텔로머레이스를 표적으로 하는 13개 염기 서열의 올리고뉴클레오타이드로, 인간 텔로머레이스 RNA(human telomerase RNA, hTR)의 주형(template) 영역에 선택적으로 결합하여 텔로머레이스 활성을 경쟁적으로 억제함으로써 암세포를 사멸한다.이메텔스타트의 약동학(PK), 약력학(PD), 용량-반응 관계(dose-response relationship), 유효성 및 안전성은 고형암 및 혈액암을 포함한 다양한 종양 모델에서 in vitro, in vivo, 그리고 임상시험을 통해 평가되었다. 특히, 저위험 골수형성이상증후군(LR-MDS) 및 골수증식성 종양을 포함한 혈액질환을 대상으로 한 연구가 집중적으로 수행되었다.핵심 3상 임상시험인 IMerge 연구에 따르면, 이메텔스타트 투여군은 위약군 대비 8주 및 24주 이상에서 적혈구 수혈 비의존성(red blood cell-transfusion independence, RBC-TI)에 도달한 환자의 비율이 통계적으로 유의하게 높았으며, 주요 이상반응으로는 일시적이며 조절 가능한 호중구감소증(neutropenia) 및 혈소판감소증(thrombocytopenia)이 관찰되어, 전반적으로 관리 가능한 안전성 프로파일을 보였다.저위험에서 중간 1단계 위험군의 성인 골수이형성증후군(Low-to intermediate-1 risk myelodysplastic syndromes, MDS)은 무엇인가?골수이형성증후군(MDS)은 혈액 생성 줄기세포의 클론성 이상으로 인해 발생하는 혈액 종양 질환군으로, 골수 내 이형성(dysplasia)과 비효율적인 조혈(hematopoiesis)을 특징으로 한다. 이 질환은 빈혈, 백혈구 감소증, 혈소판 감소증 등의 다양한 혈구감소증(cytopenia)이 나타날 수 있다.일부 MDS 환자는 급성 골수성 백혈병(AML)으로 진행되기도 하여, 임상 경과를 더욱 복잡하게 만든다. MDS 환자의 예후는 매우 다양하며, 염색체 이상 및 혈구감소증의 중증도와 같은 요인에 따라 영향을 받는다. 따라서, MDS 환자의 임상 경과와 치료 반응은 매우 다양하므로, 정확한 예후 분류는 치료 전략 수립 및 예후 예측에 있어 필수적이다.가장 널리 사용되는 예후 평가 시스템은 1997년 제시된 국제 예후 점수 시스템( International Prognostic Scoring System, IPSS)이며, 골수 내 아세포(blast) 비율, 세포유전학적 이상(cytogenetics), 혈구감소증의 수 등 세 가지 지표를 기반으로 환자를 위험(Low), 중간-1위험(Intermediate-1), 중간-2위험(Intermediate-2), 고위험(High)의 네 군으로 분류한다.이 중 저위험에서 중간-1위험군(low-to intermediate-1 risk)은 IPSS 점수 기준으로 0~1.0점에 해당하며, 비교적 안정된 임상 경과를 보이고, 적혈구 자극제(ESA)나 보존적 치료 등의 저강도 요법이 우선적으로 고려된다.2012년에는 기존 IPSS의 한계를 보완하기 위해 개정된 국제 예후 점수 시스템(IPSS-R)이 제안되었다. IPSS-R은 세포유전학적 이상을 5단계로 세분화하고, 골수 아세포 비율, 혈색소 농도, 혈소판 수, 절대 호중구 수 등 보다 정량적인 지표를 반영함으로써 환자를 매우 저위험(very low), 저위험(low), 중간위험(intermediate), 고위험(high), 매우 고위험(very high)의 5단계로 분류한다. 이 중 IPSS-R의 저위험 및 중간위험군은 대체로 기존 IPSS의 저위험 및 중간-1위험군과 대응된다.저위험~중간-1위험군 MDS 환자는 일반적으로 생존 기간이 길고, 급성 골수성 백혈병(AML)으로의 진행 위험이 낮은 편이나, 수혈 의존성 빈혈, 증상성 혈구감소증, 분자 유전학적 이상 유무에 따라 치료 방법의 세분화가 필요하다. 최근에는 유전자 변이 기반의 위험도 분류가 병용되며, 보다 정밀한 예후 예측과 치료 맞춤화에 기여하고 있다.이러한 MDS는 텔로미어(telomere) 단축과 관련된 조혈 줄기세포 기능 저하와 병적 클론의 형성을 특징으로 하며, 일부 클론은 텔로머레이스(telomerase)를 재활성화하여 불사성(immortality)을 획득하고 질환의 진행에 관여한다. 텔로머레이스는 이러한 병태생리적 역할로 인해 MDS에서 유망한 치료 표적이 된다.텔로미어(Telomere)는 어떤 물질인가? 2009년 노벨 생리의학상은 엘리자베스 블랙번(Elizabeth Blackburn), 캐럴 그라이더(Carol Greider), 잭 쇼스택(Jack Szostak)에게 수여되었다. 이들은 염색체 말단에 위치한 특수한 반복 서열 구조인 텔로미어(telomere)와 그 유지에 관여하는 효소인 텔로머레이스(telomerase)를 규명함으로써, 세포 분열 과정에서 유전 정보가 어떻게 안정적으로 보존되는지를 설명하는 데 기여하였다.노벨위원회는 "이들 세 명의 연구는 염색체가 세포 분열 과정 중 퇴화를 방지하고, 완전하게 복제될 수 있는지를 둘러싼 오랜 생물학적 의문에 대한 해답을 제공하였다"고 평가하였다.텔로미어에는 세포의 염색체 말단에 반복적인 DNA 서열이 존재하며, 이는 유전물질의 손상을 방지하고 염색체의 구조적 안정성을 유지하는 역할을 수행한다. 그러나 체세포는 분열을 반복할수록 텔로미어 길이(telomere length)가 '모래시계'처럼 점진적으로 짧아지며, 일정 임계점에 도달하면 세포는 증식을 멈추고 세포 노화(senescence)나 세포자멸사사(apoptosis)를 유도하게 된다(Figure 1).이때 텔로머레이스는 텔로미어의 말단을 연장할 수 있는 효소로 세포의 수명을 연장시키고, 이론적으로는 세포의 불사성(immortality)를 유도할 가능성을 지닌다. 이러한 텔로미어는 생물체의 노화 과정과 직접적으로 연관되어 있고, 또한 대부분의 암세포는 텔로머레이스의 활성을 통해 텔로미어 길이를 유지하거나 연장함으로써 무한 증식 능력을 가지게 된다. 즉, 텔로미어 단축은 세포 노화를 유도하는 반면, 텔로미어 보존은 암세포의 지속적 증식을 가능하게 한다. 따라서, 텔로미어 기능의 조절은 노화 억제 혹은 암 치료를 위한 잠재적 전략으로 제시되고 있다.텔로머레이스(Telomerase)란 무엇인가? 텔로머레이스(Telomerase)는 염색체 말단에 있는 3' 말단 돌출부(3' overhang)에 반복적인 염기서열을 추가하는 기능을 가진 리보핵단백질 복합체(ribonucleoprotein complex)로, 역전사효소(reverse transcriptase) 활성을 갖는다. 3' 말단 돌출부는 이중가닥 DNA 말단에서 한 가닥이 다른 가닥보다 더 길어 돌출된 형태로, 텔로미어 구조에서 텔로머레이스가 인식하고 작용하는 주요 부위이다.텔로머레이스는 자체의 RNA 구성요소인 TERC(telomerase RNA component)를 주형(template)으로 삼아, TERT(telomerase reverse transcriptase)의 역전사 효소 활성을 통해 반복적인 TTAGGG 염기서열을 합성함으로써 염색체 말단의 텔로미어를 연장한다(Figure 2). 인간의 경우, 텔로머레이스는 인간 텔로머레이스 역전사효소(human telomerase reverse transcriptase, hTERT) 유전자에 의해 암호화되는 촉매 소단위(catalytic subunit)와 인간 텔로머레이스 RNA(human telomerase RNA, hTR) 유전자 산물인 RNA 주형(template)을 중심으로 구성된 복합체이다. 여기에 dyskerin, NHP2, NOP10, GAR1 등 다양한 보조 단백질들이 결합하여, 효소 복합체의 구조적 안정성과 기능적 활성을 조절한다.텔로머레이스를 ‘자동차’ 전체에 비유한다면, TERT는 실제로 DNA를 합성하는 역할을 수행하는 ‘엔진’에 해당하며, hTR(또는 TERC)는 어떤 염기서열을 합성할지를 지시하는 ‘설계도’에 해당하는 RNA 주형으로 볼 수 있다.인체 내 약 120여 종의 세포 중 대부분은 텔로미어를 합성하는 효소인 텔로머레이스의 활성을 갖지 않으며, 이로 인해 세포는 분열이 반복될수록 텔로미어가 점진적으로 단축되고, 결국 복제에 따른 세포 노화(replicative senescence)에 도달하게 된다. 반면, 일부 높은 분열 능력을 가진 조직의 세포들은 예외적으로 텔로머레이스 활성을 유지한다.이러한 세포에는 모낭(hair follicle), 구강 편평상피(squamous epithelium), 피부 표피의 기저층(basal layer of epidermis), 제2형 폐포상피세포(type 2 alveolar epithelial cells), 간세포(hepatocytes), 장의 장선(intestinal crypts), 정원세포(spermatogonia) 등이 있다. 이들 세포에서 텔로머레이스 활성이 결여될 경우, 조직의 항상성 유지 및 생식 기능에 중대한 장애가 초래된다.특히, 정자 형성에 관여하는 정원세포(spermatogonia)에서 텔로머레이스 활성이 결여되면, 정자의 텔로미어 길이가 충분히 유지되지 못하고 단축된 상태로 전달된다. 이로 인해 형성된 배아는 텔로미어 단축에 기인한 세포 노화가 조기에 시작되며, 조기 노화(progeria)와 유사한 양상을 보일 수 있다. 실제로 이는 복제 양 돌리(Dolly) 사례에서 관찰된 바 있으며, 단축된 텔로미어가 수명 감소와 밀접하게 연관됨을 시사한다.이는 일반적인 체세포에서는 텔로머레이스 활성이 매우 낮은 수준으로 유지하지만, 생식세포와 줄기세포에서는 해당 효소가 구성효소(constitutive enzyme)로서 지속적으로 발현된다. 구성효소는 소화효소와 같이 항상 일정 수준으로 활성화되어 있는 효소이다.이에 반해 유도효소(inducible enzyme)는 특정 자극(예: 약물, 독성물질 등)에 의해 후천적으로 유도되는 효소이다. 이러한 분류 기준에 따라 텔로머레이스는 생식세포 및 줄기세포에서 구성효소로 기능하며, 암세포에서는 구성효소 및 유도효소적 특성을 보이는 이중적 성격을 가진다고 볼 수 있다.줄기세포 중에서도 배아줄기세포(embryonic stem cells) 및 유도만능줄기세포(induced pluripotent stem cells)는 고도로 안정된 텔로머레이스 활성을 보이며, 이로 인해 세포 분열에 따른 텔로미어의 단축이 거의 발생하지 않고, 복제에 따른 세포 노화에도 이르지 않는다.반면, 중간엽줄기세포(mesenchymal stem cells), 신경줄기세포(neural stem cells), 조혈모세포(hematopoietic stem cells) 등 성체 유래 줄기세포에서는 텔로머레이스 활성이 상대적으로 낮으며, 이로 인해 제한적인 텔로미어 단축이 관찰된다.TERT(Telomerase reverse transcriptase)란 무엇인가? 대부분의 체세포는 약 60~80회의 분열(population doublings) 이후 텔로미어가 임계 길이에 도달하게 되며, 이 시점에서 이중가닥 DNA 절단(double-strand break) 신호가 유도되어 복제에 따른 노화로 전환된다.이러한 현상은 체세포 내에서 텔로머레이스 활성이 거의 존재하지 않기 때문에 발생하는데, 이는 텔로머레이스의 RNA 구성 요소인 TERC(hTR)가 존재하더라도, 촉매 활성을 담당하는 TERT 유전자의 전사가 억제되어 있기 때문이다. 따라서, TERT 발현의 억제는 체세포에서 텔로머레이스 활성이 결핍되는 주요 원인이며, 텔로미어 단축의 분자적 기전으로 작용한다.뿐만 아니라, TERT는 단순한 텔로미어 연장 기능 외에도 텔로미어 말단의 캡핑(capping)과 전체 구조 유지에도 중요한 역할을 한다. 이는 다양한 암종의 약 80~90%에서는 TERT 발현이 재활성화되어 텔로머레이스 활성이 증가되어 있으며, 암세포의 불사화와 밀접하게 연관되어 있다.결과적으로, TERT 발현은 텔로미어 연장과 세포 노화 회피를 통해 암세포 특성이 획득되는 초기 단계에서 결정적인 분자 표지자로 작용한다. 이러한 TERT 발현 유도는 다양한 내•외부 요인 중 유전자 불안정성과 돌연변이가 가장 대표적인 기전으로 제시되고 있다.암의 발생 과정에서 텔로미어 길이의 보존이 빈번히 동반되며, 이는 주로 인간 텔로머레이스 역전사효소(hTERT)의 발현 증가에 따른 텔로머레이스 활성의 재개로 설명된다. 따라서 TERT의 발현 조절 기전은 텔로머레이스 기반 항암 치료법의 핵심 표적으로 주목받고 있으며, 암세포 특이적 바이오마커로서의 임상적 활용 가능성 또한 높다.텔로머레이스와 암과의 관계는 어떠한가? 텔로머레이스의 비정상적인 재활성화는 암세포에서 흔히 관찰되는데, 이는 텔로미어 단축으로 유도되는 세포자멸사를 회피하고 무한 증식 능력을 획득하는 데 핵심적인 기전으로 작용한다. 실제로, 전체 고형암 및 혈액암의 약 90% 이상에서 텔로머레이스 활성이 현저히 증가되어 있음이 관찰된다.여러 암 조직 생검에서 텔로머레이스 활성의 증가가 종양의 병기 및 악성도와 유의한 상관관계를 보이는 반면, 대부분의 정상 성인 조직에서는 텔로머레이스 활성이 거의 검출되지 않으며, 일부 조혈모세포나 면역세포에서만 일시적으로 나타나는 것으로 알려져 있다.이는 암세포 및 암전구세포에서 공통적으로 관찰되는 높은 수준의 텔로머레이스 발현과 텔로미어 유지 현상을 억제하여 암세포의 증식을 제한하는 치료 방법이 된다.특히, RNA 기반 치료법은 텔로머레이스의 RNA 구성요소인 hTR 또는 hTERT mRNA를 표적으로 하여 효소 활성을 간접적으로 억제하는 방식으로 주목받고 있다. 이 중 안티센스 올리고뉴클레오타이드(antisense oligonucleotides, ASO) 및 RNA 간섭(small interfering RNA, siRNA) 기술은 텔로머레이스 기능을 선택적으로 차단할 수 있는 새로운 접근법이다.대표적 예로는 이멜스타트(Imetelstat)가 있으며, 이는 인간 텔로머레이스 RNA(hTR)의 주형 영역에 상보적으로 결합하는 리간드 결합형 ASO로 설계되어, 텔로미어 연장 과정을 억제함으로써 암세포의 증식 억제를 유도한다. 이와 같은 RNA 기반 접근은 텔로머레이스 억제를 통한 항암 치료의 새로운 패러다임을 제시하며, 표적 치료제 개발에 있어 중요한 진전을 이끌고 있다.텔로머레이스 억제를 통한 항암 치료 전략은? 텔로머레이스를 표적으로 한 항암제 개발은 다양한 작용기전을 바탕으로 다방면에서 진행되고 있으며, 크게 RNA 기반 억제제, 전사 억제 화합물, G-사중나선 안정화제, 그리고 면역치료 백신 전략으로 구분할 수 있다.1. RNA 기반 억제제 가장 활발히 연구되고 있는 접근은 안티센스 올리고뉴클레오타이드(ASO) 또는 RNA 간섭(siRNA) 기술을 활용하여 텔로머레이스 RNA 구성요소(hTR 또는 TERC)를 표적으로 하는 전략이다. 이들 억제제는 텔로머레이스 복합체 내의 RNA 주형에 상보적으로 결합함으로써 효소 활성을 억제하거나, RNase H 의존적 분해를 유도하여 텔로머레이스 기능을 근본적으로 차단한다.대표적 약제인 이멜스타트(Imetelstat)는 티오포스포라마이드(thio-phosphoramidate) 변형을 적용한 ASO로, hTR의 템플릿 영역에 결합하여 텔로미어 연장을 저해한다.2. hTERT 전사 억제 저분자 화합물 이 저분자 화합물은 텔로머레이스의 촉매 소단위인 hTERT 유전자의 전사를 직접 억제하는 방식으로, 프로모터 영역 조절 또는 후성유전학적 메커니즘을 통해 유전자 발현 자체를 낮춘다. 일부 저분자 화합물은 hTERT 단백질에 직접 결합하여 효소 활성을 차단한다. 식물 유래 플라보노이드(예: genistein)가 TERT 전사를 억제하는 기능이 보고된 바 있으나 낮은 선택성과 잠재적인 세포독성으로 인해 임상 적용에는 제한이 있다.3. G-사중나선(G-quadruplex) 안정화제 이 안정화제는 텔로미어 말단에서 형성되는 G-사중나선 구조를 안정화시켜 텔로머레이스의 접근을 물리적으로 차단하는 방식이다. 해당 구조는 G-rich 반복 서열에서 자연적으로 형성되며, 일부 저분자 화합물은 이 구조에 특이적으로 결합하여 G-quadruplex 형태의 유지 및 안정화를 유도한다.이 방법은 효소가 아닌 기질을 표적으로 한다는 점에서 기존 억제제와 구별되며, 비교적 빠른 약효 발현이 가능하다. 그러나 G-rich 서열이 텔로미어 외에도 다양한 유전자의 조절부위에 존재하기 때문에, 표적 특이성 확보가 주요 과제로 남아 있다.4. 텔로머레이스를 항원으로 활용한 면역치료 텔로머레이스를 면역계의 표적으로 활용하는 전략도 개발되고 있다. 이는 hTERT 유래 펩타이드를 기반으로 하는 항암 백신을 통해, 텔로머레이스를 발현하는 종양세포를 면역세포가 인식하고 제거하도록 유도한다. 비소세포폐암(NSCLC), 췌장암 등 다양한 고형암에서 임상시험이 진행되고 있으며, 면역기억 반응을 통한 재발 억제 효과가 기대된다. 다만, 환자의 HLA 유형 및 종양미세환경(TME)에 따라 치료 반응의 편차가 존재하여, 정밀한 환자 선별 전략이 병행되어야 한다.이와 같이 텔로머레이스 억제 전략은 암세포 특이성이 높고 장기적인 종양 억제 효과를 유도할 수 있다는 점에서 유망한 접근이다. 그러나 기전상 텔로미어 길이의 점진적 단축을 필요로 하므로, 치료 효과 발현까지 수 주에서 수 개월이 소요되는 경향이 있다. 또한, 일부 암에서는 텔로머레이스 비의존적인 대체적 길이 조절(ALT, alternative lengthening of telomeres) 경로가 활성화되어 있어 단독요법으로는 제한적일 수 있다.이러한 한계를 극복하기 위해, 최근에는 DNA 손상 유도제, 면역관문억제제(PD-1/PD-L1 억제제), PARP 억제제 등과의 병용요법이 시도되고 있다. 또한 텔로머레이스 발현 수준, 텔로미어 길이 상태, ALT 경로 활성 여부 등을 고려한 환자 맞춤형 정밀의학적 접근이 병행됨으로써, 텔로머레이스 억제제의 임상적 유용성은 점차 확대되고 있다.뉴클레오타이드(Nucleotide)와 합성 올리고뉴클레오타이드의 차이는? 뉴클레오타이드는 모든 생명체에 보편적으로 존재하는 저분자 유기 화합물로, DNA와 RNA와 같은 핵산의 기본 단위이며 에너지 전달(ATP, GTP), 세포 신호전달(cAMP, cGMP), 효소 보조인자(NAD⁺, FAD) 등의 생리적 기능에 필수적인 역할을 수행한다. 이러한 분자는 세포 내에서 de novo 합성 경로 또는 재활용 경로(salvage pathway)를 통해 지속적으로 생성되며, 생명 유지에 핵심적인 역할을 한다.이에 반해, 올리고뉴클레오타이드는 일반적으로 몇 개에서 수십 개의 뉴클레오타이드가 공유결합으로 연결된 짧은 핵산 서열로, 인공적으로 합성된 생체분자이다. 자연적으로는 microRNA나 small nuclear RNA와 같은 일부 예외적인 경우를 제외하면 생체 내에서 잘 합성되지 않으며, 주로 화학적으로 합성되어 특정 유전 서열의 인식이나 분자 기능의 조절을 목적으로 활용된다.합성 올리고뉴클레오타이드는 분자생물학, 진단, 치료, 유전자 조작 등 다양한 분야에서 핵심 도구로 활용되고 있으며, 기능, 표적, 화학적 변형에 따라 , 다음과 같이 분류된다.첫째, 기능적 측면에서 ▲ mRNA 또는 pre-mRNA에 결합하여 유전자 발현을 억제하거나 RNA 스플라이싱을 조절하는 안티센스 올리고뉴클레오타이드(antisense oligonucleotide, ASO), ▲ RNA 간섭(RNAi)을 유도하여 표적 mRNA의 분해를 유도하는 소간섭 RNA(siRNA) 또는 마이크로 RNA(miRNA) 유사체, ▲ 고특이적으로 단백질에 결합하여 기능을 저해하거나 조절하는 압타머(aptamer), ▲ CRISPR 시스템에서 유전자 편집을 유도하는 가이드 RNA(guide RNA, gRNA), ▲ 전사인자와 결합하여 표적 유전자 조절을 간섭하는 디코이(decoy), ▲ PCR, qPCR, 유전자 탐지 등 핵산 분석 기술에 사용하는 프라이머(primer) / 프로브(probe) 등으로 분류된다.둘째, 표적 및 작용기전에 따라 ▲ DNA, ▲ mRNA, ▲ pre-mRNA, 또는 단백질 등 다양한 분자에 작용할 수 있으며, 그 기전은 전사 억제, 번역 차단, RNA 스플라이싱 조절, 단백질-핵산 상호작용 차단 등으로 확장된다.셋째, 화학 구조적 변형 측면에서 천연형(natural-type) 외에도 약물 안정성 및 효율성을 개선하기 위한 다양한 화학적 변형이 도입된다. 대표적으로 ▲ 인산기 산소를 황으로 치환하여 핵산분해효소 내성 증가를 위한 phosphorothioate(PS), ▲ 리보스의 2′ 위치에 화학기 추가로 결합력과 안정성 증가를 위한 2′-O-methyl RNA 및 2′-fluoro RNA, ▲ 리보스 고정을 통해 고결합 친화성 및 특이성 확보한 locked nucleic acid(LNA), ▲ 간세포 타깃팅 또는 세포 내 전달력 향상을 위한 GalNAc 또는 지질을 접합시킨 conjugated oligonucleotide 등이 있으며, 이는 체내 안정성, 표적 결합력, 약물 전달 효율성을 향상시키는 데 기여한다.요약하면, 뉴클레오타이드는 생명체 내에서 합성되는 주요 생리활성 분자인 반면, 올리고뉴클레오타이드는 외부에서 합성되어 생체 내 특정 유전자나 분자 기전을 정교하게 조절하기 위한 인공 핵산 서열이라는 점에서, 양자는 생성 방식과 생리적 존재 양상에서 본질적으로 다르다. 그럼에도 불구하고, 올리고뉴클레오타이드는 자연계 핵산의 기능을 모방하거나 확장함으로써 차세대 핵산 기반 치료제 및 진단 기술의 핵심 플랫폼으로 부상하고 있다.ASO(Antisense Oligonucleotide, 안티센스 올리고뉴클레오타이드)란? ASO는 mRNA를 표적으로 설계된 짧은 합성 단일가닥 DNA 분자로, 특정 mRNA 서열과 상보적으로 결합함으로써 유전자 발현을 억제하거나 조절하는 기능을 수행한다(Figure. 3).ASO는 비교적 간단한 화학 구조를 기반으로 하면서도, 전사체의 분해 유도, RNA 스플라이싱 (splicing) 조절, 번역 억제 등 다양한 작용기전을 통해 유전 정보의 흐름을 정교하게 제어할 수 있는 장점을 가진다.ASO의 작용기전은 화학적 변형 방식과 결합 표적에 따라 다양하게 구분된다. 대표적으로 RNase H 매개 분해는 ASO가 표적 mRNA와 이중가닥을 형성한 후, 세포 내 RNase H 효소에 의해 해당 mRNA가 분해되어 단백질 생성을 원천적으로 차단하는 기전이다.또한, 스플라이싱 조절용 ASO는 pre-mRNA의 엑손/인트론 경계부에 결합하여, 엑손 스키핑(skipping) 또는 보존을 유도함으로써 단백질의 구조와 기능을 변형시킬 수 있다. 이 외에도 번역 개시 억제, mRNA 안정성 저해 등 다양한 방식으로 작용이 가능하다.이러한 특성을 바탕으로, ASO는 기존 소분자 화합물이나 단백질 기반 치료제와 달리 기능 상실(loss-of-function) 혹은 기능 획득(gain-of-function) 유전자 돌연변이 모두를 정교하게 조절할 수 있다.그러나 ASO 치료제는 면역반응 유발, 비표적 결합(off-target effect), 체내 약물 전달 효율 등의 한계를 지니고 있으며, 이를 극복하기 위해 phosphorothioate 치환, 2′-O-methyl 및 LNA 변형, GalNAc 결합을 통한 간세포 표적화, 지질 나노입자 기반 전달체 등 다양한 기술적 발전이 이루어지고 있다.이러한 발전은 ASO의 치료적 효능을 향상시키는 데 핵심적인 기여를 하고 있으며, ASO 기반 핵산 치료제가 차세대 정밀의학 기반의 분자표적 치료제로 자리매김할 수 있는 가능성을 높이고 있다.텔로머레이스 표적 올리고뉴클레오타이드(Telomerase-targeted oligonucleotide, TTO)란? TTO는 표적 핵산 서열에 상보적으로 결합하는 구조를 가지면서도, 기존의 ASO와는 본질적으로 다른 작용기전을 가진다. 즉 일반적인 ASO는 mRNA의 분해(RNase H 의존적 경로) 또는 스플라이싱 조절을 통해 단백질 생성을 억제하지만, TTO는 hTR의 템플릿 서열에 직접 결합함으로써 텔로머레이스 효소 복합체의 활성 부위를 차단한다. 이는 효소의 기질 인식 및 촉매 반응 자체를 방해하는 비정형(non-canonical) ASO로 분류된다.이러한 TTO는 효소 작용 자체의 차단을 통해 효소 기능 차단(enzyme activity inhibition)이라는 새로운 패러다임을 제공한다. 특히 텔로머레이스 활성이 높은 암세포에서 선택적으로 작용함으로써, 정상세포에 대한 영향을 최소화하면서 암 특이적 억제 효과를 유도할 수 있다.대표적인 TTO로는 이메텔스타트(Imetelstat)가 있으며, 이는 hTR의 템플릿 영역에 상보적으로 결합하는 티오인산화(thio-phosphoramidate) 올리고뉴클레오타이드로 설계되었다.이메텔스타트는 어떤 약제인가? 이메텔스타트(Imetelstat, 제품명: 라이텔로 정맥주사, Rytelo®)는 텔로머레이스를 직접 표적으로 하는 최초의 올리고뉴클레오타이드 기반 치료제로, 2024년 미국 FDA로부터 승인받은 이후 골수이형성증후군(MDS) 치료 영역에서 새로운 치료 축으로 부상하고 있다. 이 약제의 승인 적응증은 "8주간 4단위 이상의 적혈구 수혈이 필요한 수혈 의존성 빈혈을 가진 저위험~중간-1 위험군 MDS 성인 환자 중, 적혈구생성자극제(ESA)에 반응하지 않거나 반응이 소실되었거나, 투여가 불가능한 경우"이다.이메텔스타트는 기존의 ASO와는 구별되는 비정형 ASO로 분류되며, 비정상적인 텔로머레이스 활성을 보이는 악성 조혈모세포(HSCs) 및 전구세포(HPCs)를 선택적으로 억제함으로써 병적 클론의 제거와 정상 조혈 기능의 회복을 유도하는 질환 수정형(disease-modifying) 치료 제이다.분자 구조적으로, 이메텔스타트는 13개의 뉴클레오타이드로 구성된 단일가닥 DNA 서열이며, 티오인산화(thio-phosphoramidate) 변형을 통해 핵산분해효소(nuclease) 저항성, 수용성, 대사적 안정성 등의 약물학적 특성이 향상되었다. 또한 5′ 말단에 팔미토일기(palmitoyl group)가 결합되어 소수성을 증가시켜 세포막 투과성 및 세포 내 유지성을 강화하며, 별도의 형질전환 과정 없이도 세포 내 작용이 가능하도록 설계되었다.전임상 연구에서는 이메텔스타트의 약물 노출과 텔로머레이스 억제 간의 명확한 약력학적 상관성이 확인되었고, 텔로머레이스 활성을 50% 이상 억제하는 수준의 약리 효과가 임상적으로 확보 가능한 범위 내에 있음이 입증되었다. 또한, 골수증식성 질환 모델(예: 본태성 혈소판증, 골수섬유증, 급성 골수성 백혈병 등)에서는 시험관 내(in vitro) 및 생체 내(in vivo) 실험 모두에서 강력한 항종양 활성을 나타냈다.특히 저위험 MDS 환자에서 이메텔스타트는 텔로미어 단축, hTERT 과발현, 분화 억제 등으로 특징지어지는 병적 조혈모세포 및 전구세포를 선택적으로 제거함으로써, 정상 조혈의 회복과 함께 적혈구 수혈 비의존 기간(RBC-TI)의 연장, 혈색소 수치의 향상, 염색체 이상 클론 및 돌연변이 부담의 감소를 유도하였다.아울러, 이메텔스타트는 면역회피 특성을 가진 악성 클론에서도 항암 활성을 유지함으로써, 기존 면역항암제 또는 세포독성 항암제에 비해 임상적 적용 가능성이 높다. 현재 진행 중인 다수의 임상시험 결과에 따라, MDS뿐 아니라 골수섬유증(myelofibrosis), 기타 혈액암 영역으로의 적응증 확장 가능성도 제시되고 있다.이메텔스타트의 약리 기전은? 이메텔스타트는 TERT-targeting telomerase complex inhibtor 또는 RNA-template targeting telomerase inhibitor로, 인간 텔로머라제의 RNA 구성 요소(hTR)의 주형 영역에 상보적으로 결합하여 텔로머레이스 복합체의 활성 부위에서 기질 결합 및 연장을 직접 차단한다. 즉 hTR의 주형 서열(3′-CAAUCCCAAUC-5′)에 상보적인 염기서열(5′-palmitate-TAGGGTTAGACAA-NH₂-3′)이 결합함으로써, 텔로머레이스 효소의 활성을 억제하여 텔로미어 말단에 반복 서열을 추가하는 기능을 경쟁적으로 차단한다. 이로 인해 암세포 내에서의 텔로미어 길이가 점진적으로 짧아지며, 결국 세포 노화 또는 세포자멸사를 유도하게 된다(Figure 4). 골수이형성증후군(MDS) 및 악성 줄기세포 및 전구세포에서 텔로머레이스 활성 및 인간 텔로머레이스 역전사효소(hTERT) RNA 발현이 증가한 것으로 보고되었다. 이에 여러 연구에서 이메텔스타트 치료가 텔로미어 길이 감소, 악성 줄기세포 및 전구세포의 증식 감소, 그리고 세포자멸사를 유도함으로써 세포 증식 억제 및 수명 단축 효과를 나타낸 것으로 보고되었다.또한, 이 약제는 텔로머레이스의 촉매 소단위인 hTERT의 발현을 억제함으로써 효소 활성을 이중적으로 저해하는데, 이 hTERT는 텔로머레이스 활성을 조절하는 주요 속도 제한 인자(rate-limiting component)로 알려져 있다.이러한 이멜스타트의 작용 기전은 항원-항체 반응이나 면역세포 활성화를 기반으로 하는 기존 면역항암제와는 달리, 종양 세포의 분열 및 생존을 유지하는 내재적 기전인 텔로머레이스 의존성을 직접 차단한다는 점에서 근본적인 차별성을 갖는다.이멜스타트(RYTELOⓇ) 3상 임상은 어떻게 진행되었나? 이메텔스타트의 임상적 유효성은 IMerge 3상 연구를 통해 입증되었다. 본 연구는 무작위배정, 이중눈가림, 위약대조, 다기관 임상시험으로 설계되었으며, 저위험 또는 중간-1위험군 골수이형성증후군(MDS) 환자 중 수혈 의존성을 보이는 성인 178명을 대상으로 시행되었다. 환자 등록 기준은 무작위배정 16주 전의 8주간 기간 동안 적어도 4단위 이상의 적혈구 수혈 필요 이력이 있는 경우로 정의되었다.등록 환자들은 모두 적혈구생성자극제(ESA)에 반응이 없었거나 반응이 소실되었거나, ESA 투여가 적절하지 않다고 판단된 경우였다. 주요 포함 기준에는 절대 호중구 수치 ≥ 1.5 × 10⁹/L, 혈소판 수 ≥ 75 × 10⁹/L이 포함되었으며, del(5q) 염색체 이상 보유자, 레날리도마이드(Lenalidomide) 또는 아자시티딘(Azacitidine)과 데시타빈(Decitabine) 같은 저메틸화제(hypomethylating agents, HMA) 치료 이력이 있는 환자는 제외되었다.무작위배정은 2:1 비율로 수행되어, RYTELO 7.1 mg/kg 정맥주사군(n=118) 또는 위약군(n=60)에 배정되었으며, 28일 주기(cycle)로 반복 투여되었다. 치료는 질병 진행, 용인할 수 없는 독성, 또는 환자의 자의적 중단 시점까지 지속되었다. 무작위배정은 기존 RBC 수혈 부담 및 IPSS 위험군 등급을 기준으로 계층화되었다. 모든 환자에게는 필요 시 적혈구 수혈을 포함한 지지요법(supportive care)이 병행 제공되었다.평가 기간은 RYTELO 투여군에서 중앙 추적기간 19.5개월(범위: 1.4–36.2개월), 위약군에서 17.5개월(범위: 0.7–34.3개월)이었으며, 주요 유효성 평가 변수는 적혈구 수혈 독립(RBC transfusion independence, RBC-TI) 달성 비율이었다. 이는 무작위배정 이후부터 차기 항암 치료 개시 전까지의 기간 중 연속된 8주(≥56일) 또는 연속된 24주(≥168일) 동안 적혈구 수혈이 전혀 이루어지지 않은 경우로 정의되었다.그 결과, 8주 이상 RBC-TI 도달률은 RYTELO 군에서 39.8%(95% CI: 30.9–49.3)로, 위약군의 15.0%(95% CI: 7.1–26.6) 대비 통계적으로 유의하게 높았다(p < 0.001). 또한 24주 이상 RBC-TI 도달률 역시 RYTELO 군에서 28.0% (95% CI: 20.1–37.0)로, 위약군 3.3% (95% CI: 0.4–11.5)와 비교하여 유의한 차이를 보였다(p < 0.001). 이러한 결과는 RYTELO가 ESA 불응 또는 부적합 환자군에서 수혈 의존성을 유의하게 줄이고, 적혈구계 조혈 회복을 유도할 수 있는 잠재력을 입증하는 것으로 해석된다.안전성 측면은 RYTELO 군에서 위약군 대비 ≥10% 이상, ≥5% 차이를 보인 주요 이상반응은 혈소판 감소, 백혈구 감소, 호중구 감소, AST/ALT/ALP 상승, 피로, 부분 트롬보플라스틴 시간 연장, 관절/근육통, COVID-19 감염, 두통 등이었다.따라서, RYTELO는 저위험 MDS 환자에서 임상적으로 의미 있는 수혈 독립 향상을 유도하였으며, 전반적으로 관리 가능한 안전성 프로파일을 보였다. 권장 투여 용량은 7.1 mg/kg이며, 4주마다 2시간에 걸쳐 정맥 투여한다. 이멜스타트의 앞으로의 예상은? 골수이형성증후군(MDS)은 조혈모세포의 분화 및 성숙에 결함이 생겨 비정상적 조혈과 말초 혈구감소증을 유발하는 이질적인 클론성 조혈장애이다. 특히 저위험군 MDS 환자에서는 만성적인 적혈구 수혈 의존성 빈혈이 주요 임상 양상으로 나타나며, 삶의 질 저하 및 철분 과부하에 의한 이차적 장기 손상이 주요 합병증으로 작용한다.현재까지 이들 환자에서 사용 가능한 치료제로는 적혈구생성자극제(ESA) 및 저메틸화제(HMA) 등이 있으나, 반응률의 한계와 장기 치료 효과에 대한 의문이 지속적으로 제기되고 있다.텔로머레이스는 텔로미어 길이를 유지하여 세포의 분열 한계를 극복하게 하는 핵심 효소로, 대부분의 암세포 및 악성 조혈모세포에서 비정상적으로 활성이 증가되어 있는 것이 특징이다. 이러한 활성을 선택적으로 억제함으로써 병적 조혈세포의 증식을 제한하고 정상 조혈을 회복시키는 접근은 질환의 근본 기전을 타겟으로 하는 질환 수정형(disease-modifying) 치료전략으로 주목받고 있다.이메텔스타트(Imetelstat)는 인간 텔로머레이스 복합체(hTERT/hTR)에 직접 결합하여 활성을 경쟁적으로 억제하는 first-in-class 올리고뉴클레오타이드 기반 치료제로, 텔로미어 유지 능력을 상실하게 하여 세포 자멸사 및 증식 억제를 유도한다. 특히 병적 조혈모세포(HSCs/HPCs)와 백혈병 줄기세포(LSCs)에 선택적으로 작용하며, 정상 조혈세포에 대한 영향은 제한적으로 보고되고 있다.IMerge 3상 임상시험에서 이메텔스타트는 ESA에 반응하지 않거나 부적합한 저위험~중간-1 위험군 MDS 환자를 대상으로 통계적으로 유의한 적혈구 수혈 독립 효과를 입증하였다. 8주 이상 수혈 독립률(RBC-TI)은 이메텔스타트군에서 39.8%, 위약군에서 15.0%로 나타났으며, 24주 이상 수혈 독립률도 각각 17.8%와 1.6%로 유의한 차이를 보였다. 이는 기존 치료옵션에 반응하지 않는 환자 집단에 있어 새로운 치료 패러다임을 제시한 근거로 평가된다.다만, 현재 이메텔스타트는 저위험 MDS + ESA 실패 + 수혈 의존성 빈혈이라는 제한된 적응증으로 승인되어 있으며, TP53 돌연변이나 고위험군 MDS는 제외 대상에 해당된다. 또한 치료 효과 발현까지 수 주에서 수개월이 소요되며, 호중구감소증(72%) 및 혈소판감소증(65%) 등 고빈도의 혈액학적 이상반응이 동반될 수 있다는 점은 임상적 고려가 필요하다.그럼에도 불구하고, 텔로머레이스라는 근원적 분자 표적을 겨냥한 이메텔스타트는 기존 화학요법 및 면역조절제와는 차별화된 기전을 통해 조혈계 악성질환에 있어 정밀의학적 치료 전략으로서의 가능성을 보여주고 있다. 이미 미국 및 유럽에서 승인된 약제로서, 향후 국내 도입과 더불어 적응증 확대, 병용요법, 고위험 환자군에서의 임상적 검토가 필요할 것으로 예상한다.참고문헌 1. Alexander Vaiserman, Dmytro Krasnienkov “Telomere Length as a Marker of Biological Age: State-of-the-Art, Open Issues, and Future Perspectives” Front. Genet. 11:630186(2021). 2. Virginia Boccardi “Aging, Cancer, and Inflammation: The Telomerase Connection” J. Mol. Sci. 2024, 25(15), 8542. 3. Virginia Boccardi, and Luigi Marano “Aging, Cancer, and Inflammation: The Telomerase Connection” Int. J. Mol. Sci. 2024, 25, 8542. 4. Zachary Schrank, Nabiha Khan, Chike Osude, Sanjana Singh et al. “Oligonucleotides Targeting Telomeres and Telomerase in Cancer” Molecules 2018, 23, 2267. 5. Ashley L. Lennoxm, Fei Huang, Melissa Kelly Behrs, Mario González-Sales et al. “Imetelstat, a novel, first-in-class telomerase inhibitor:Mechanism of action” Clin Transl Sci. 2024;17:e70076 6. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-06-13 06:24:02최병철 박사 -
 티움바이오, 후보물질 임상 순항...글로벌 파트너링 성과[데일리팜=황병우 기자] 바이오벤처 티움바이오가 여성질환·면역항암·희귀질환 분야 혁신 신약 개발로 주목받고 있다.최근 경구용(GnRH 길항제) 신약후보 ‘메리골릭스’의 자궁근종 2상 성공 소식을 알리며 기술력을 입증, 차세대 면역항암제와 혈우병 치료제 파이프라인도 속도를 내는 중이다.김훈택 티움바이오 대표는 글로벌 파트너십 전략과 기업 비전을 공유하며, 메리골릭스의 성과에 대해 "국내 바이오벤처가 쉽지 않은 여성질환 치료제 개발에서 의미있는 결과를 냈다"며 자신감을 나타냈다.여성질환 치료 혁신의 선봉, 메리골릭스의 가치최근 티움바이오가 주목받은 이유는 메리골릭스(Merigolix, TU2670/DW-4902)의 자궁근종 국내 임상 2상 성공을 발표했기 때문이다.김훈택 티움바이오 대표대원제약과의 공동 개발을 통해 진행된 자궁근종 임상 2상에서 주 평가지표와 부 평가지표 모두 유의미한 개선 효과를 확보하면서 사업화 가능성이 한층 커졌다.티움바이오의 메리골릭스는 경구용 성선자극호르몬 방출호르몬 길항제(GnRH antagonist)로, 기존 주사제 위주의 GnRH 작용제 대비 복용 편의성이 높고 투약 초기 호르몬 급상승 부작용이 없는 것이 강점이다.인터뷰에 동석한 김선미 티움바이오 응용약물합성실장은 "메리골릭스 한 제품으로 자궁내막증, 자궁근종, 보조생식술(ART) 등 최소 3가지 질환을 표적 할 수 있다"며 "메리골릭스는 유럽 임상 2a상에서 자궁내막증 치료 효과와 안전성을 입증한 바 있다"고 설명했다.메리골릭스 자궁근종 임상 2상은 월경과다 증상 개선을 1차 평가지표로 진행됐으며, 총 71명의 환자를 고용량·중간 용량·저용량·위약군에 무작위 배정해 12주간 하루 한 번 경구 투여하고 12주 관찰한 결과, 모든 용량군에서 위약 대비 월경과다 증상이 유의하게 개선됐다.김 실장은 "위약군에서는 월경량이 전혀 줄지 않았지만, 메리골릭스 투여군에서는 대부분 환자의 출혈이 정상 수준으로 감소, 통계적 유의성을 확실히 달성하는 등 경쟁 약물과의 비교에서도 우월한 효능이 확인됐다"고 밝혔다.메리골릭스의 이번 연구 성과는 자궁내막증에 이어 자궁근종에서도 기대 이상의 우수한 약효를 보였다는 점에서 긍정적으로 평가 받고 있다. 하나의 작용기전으로 여러 질환을 치료할 수 있는 약물을 개발하는 티움바이오의 플랫폼 전략이 효과를 보이고 있기 때문이다.김 대표는 "자궁내막증 적응증으로 약효를 확인한 뒤 자궁근종으로 확장하는 식으로 리스크를 분산시키면서도 파급력을 극대화한 것"이라며 "예상대로 자궁근종에서도 뛰어난 결과를 얻어 플랫폼 전략의 유효성을 확인했다"고 밝혔다.차세대 면역항암제와 희귀질환 치료제 개발 드라이브티움바이오는 여성질환 외에도 면역항암제와 희귀질환 치료제 파이프라인을 두 축으로 성장동력을 마련하고 있다.면역항암제 후보물질인 'TU2218'은 TGF-β 신호억제와 VEGF 혈관형성 억제라는 이중 저해 기전을 내세운 경구용 면역항암제로, 면역관문억제제(ICIs)의 효과를 방해하는 TGF-β 및 VEGF 경로를 동시에 막아 항암면역 반응을 극대화하는 것을 목표로 개발 중이다.티움바이오는 향후 TU2218을 키트루다 병용 요법의 시너지 강화제로 개발해 기존 면역치료에 반응하지 않거나 효과가 미미한 환자들에게 새로운 옵션을 제공한다는 계획이다. 현재 담도암과 두경부암을 핵심 타깃 암종으로 선정해 연구를 진행 중이다.이에 대해 김 대표는 "TGF-β 경로 활성과 면역억제 성향이 높은 암이 어디인지 과학적으로 많은 연구를 거쳤고, 약효를 확실히 보일 수 있는 암종으로 담도암과 두경부암을 선택했다"며 "기존 면역항암제 단독 반응률이 30~40%에 불과한데, TU2218과의 병용으로 반응률을 끌어올리고 내약성을 개선해 전체 생존기간(OS)을 증가시킬 수 있을 것으로 기대한다"고 설명했다.아울러 다가오는 미국임상종양학회(ASCO 2025)에서 포스터 발표를 통해 지금까지 투여한 대상자들에 대한 임상 2a상 중간결과를 발표할 계획으로, 이후 추가 투약을 확대해 진행한 후 최종 임상 결과 발표는 내년에 가능할 것으로 전망 중이다.(왼쪽부터) 김훈택 티움바이오 대표, 김선미 티움바이오 응용약물합성실장 희귀질환 분야에서는 혈우병 치료제 'TU7710'이 티움바이오의 주력 파이프라인이다.TU7710은 중화항체 보유 혈우병 환자를 대상으로 한 후보물질로 기존 약물 대비 반감기를 획기적으로 늘린 장기지속성 치료제를 목표로 개발 중이다.회사에 따르면 대부분 시장을 점유하고 있는 노보노디스크의 '노보세븐'의 경우 반감기가 2~3시간으로 매우 짧아 효과 유지를 위해 자주 투여해야 하고 비용도 막대한 부담이 있다.반면 티움바이오의 TU7710은 노보세븐 대비 6~7배 긴 반감기를 보여 투여 빈도와 치료비용 부담을 크게 줄일 수 있을 것으로 기대된다. 현재 TU7710은 1a상을 마무리하고 본격적인 환자 대상 임상 진입을 앞두고 있다.김 대표는 "TU7710은 노보세븐보다 월등히 긴 반감기를 통해 출혈 에피소드에 신속히 대응하고 수술 시 출혈 예방까지 가능한 효과적 약물이 될 것"이라며 "혈우병 치료제는 임상 성공률이 굉장히 높다. 효과에 대해 1%의 의심만 있을 뿐 99%는 확신한다"고 강조했다.그는 이어 "혈우병은 임상 성공확률(26%)이 다른 질환 대비 훨씬 높고, 임상 소요 기간도 길지 않아 4~5년의 개발기간을 거쳐 2028년~2029년쯤 상용화를 목표로 하고 있다"며 "세계 시장 규모 약 2조원으로 추산되는 중화항체 보유 혈우병 치료제 분야에서 TU7710이 50% 이상 시장을 점유할 수 있을 것"이라고 기대했다."글로벌 진출 전략, 파이프라인 특성 맞춤 파트너 모색"여러 혁신 신약 파이프라인을 보유한 티움바이오이지만, 후속 임상 및 글로벌 상용화 단계에서는 외부 파트너십 전략이 필수적이다.이에 대해 김 대표는 "국내 바이오벤처가 모든 것을 자체 수행하긴 어렵다. 파트너링을 어떻게 설정하고 확장하는지가 매우 중요하다. 각 파이프라인 특성에 따라 적합한 글로벌 파트너를 모색 중이다"고 밝혔다.실제 회사는 메리골릭스의 경우 국내는 대원제약, 중국은 한소제약과 이미 라이선스 계약을 맺었고 유럽과 미국도 지역별로 파트너십을 추진하는 전략을 택했다.면역항암제나 희귀질환 신약들 역시 해당 분야 전문기업과 협력해 개발 속도를 높이고 상업화 성공률을 극대화한다는 계획이다.한편 티움바이오는 재무 건전성 확보와 주가 안정화를 통해 장기적 도약 기반을 다지고 있다.최근 증권가에서 거론된 이른바 오버행 이슈에 대해, 김 대표는 "회사 재무 상태는 전혀 나빠진 적이 없다"고 일축했다.풍부한 현금 보유액과 탄탄한 운영 자금으로 사업을 영위해왔지만, 주가 하락으로 투자자들이 막연한 불안을 느끼게 되자 과감한 자금 조달 및 최대주주의 자사주 추가 매입 등을 통해 시장 신뢰를 회복했다는 설명이다.김 대표는 "주가가 많이 내려가면 '회사에 무슨 문제가 있나'라고 의심하게 마련"이라며 "이를 해소하고자 주요 오버행 물량을 정리했고, 앞으로도 신약 개발 성과로 신뢰를 쌓아가는 것이 최우선"이라고 강조했다.이와 관련해 지난 3월 티움바이오는 최대주주인 김훈택 대표가 특수관계인이가 재무적투자자와 함께 2대주주였던 한국투자파트너스의 잔여지분을 전량 매입해 오버행 우려를 해소했고, 이에 힘입어 주가도 안정세를 찾은 바 있다.그는 "신약이 허가되고 매출로 로열티 수입이 들어오기까지 3~4년이 걸릴 것으로 보고 그 기간을 안정적으로 유지하는 게 중요하고 현재 자금조달 계획은 없다"고 언급했다.글로벌 혁신 신약을 향한 도전을 이어가는 티움바이오의 최종 목표는 무엇일까? 이에 대해 김 대표는 '감동을 주는 회사'를 만들고 싶다고 전했다.그는 "최근 스마트 바이오로직스(Smart Biologics)라는 키워드로 스마트한 신약 개발을 추구하는 방향으로 전환 했다"며 "그동안 축적된 생물학 및 화학적 역량에 독창적인 아이디어를 접목해 과거와는 완전히 다른 똑똑한 신약 개발을 해야 글로벌 경쟁에서 살아남을 수 있다"고 전했다.중국 등 거대 자본을 앞세운 경쟁자들을 이기기 위해서라도 묵묵히 열심히 하는 것만으로는 부족하고, 한발 앞선 스마트 혁신이 필요하다는 의미다.끝으로 김 대표는 "티움바이오는 이러한 전략 아래 메리골릭스를 비롯한 주력 파이프라인의 가치를 극대화하고, 협력과 소통을 통해 궁극적으로 환자와 투자자 모두에게 감동을 줄 수 있는 회사를 지향하고 있다"고 덧붙였다.2025-05-30 06:00:19황병우
티움바이오, 후보물질 임상 순항...글로벌 파트너링 성과[데일리팜=황병우 기자] 바이오벤처 티움바이오가 여성질환·면역항암·희귀질환 분야 혁신 신약 개발로 주목받고 있다.최근 경구용(GnRH 길항제) 신약후보 ‘메리골릭스’의 자궁근종 2상 성공 소식을 알리며 기술력을 입증, 차세대 면역항암제와 혈우병 치료제 파이프라인도 속도를 내는 중이다.김훈택 티움바이오 대표는 글로벌 파트너십 전략과 기업 비전을 공유하며, 메리골릭스의 성과에 대해 "국내 바이오벤처가 쉽지 않은 여성질환 치료제 개발에서 의미있는 결과를 냈다"며 자신감을 나타냈다.여성질환 치료 혁신의 선봉, 메리골릭스의 가치최근 티움바이오가 주목받은 이유는 메리골릭스(Merigolix, TU2670/DW-4902)의 자궁근종 국내 임상 2상 성공을 발표했기 때문이다.김훈택 티움바이오 대표대원제약과의 공동 개발을 통해 진행된 자궁근종 임상 2상에서 주 평가지표와 부 평가지표 모두 유의미한 개선 효과를 확보하면서 사업화 가능성이 한층 커졌다.티움바이오의 메리골릭스는 경구용 성선자극호르몬 방출호르몬 길항제(GnRH antagonist)로, 기존 주사제 위주의 GnRH 작용제 대비 복용 편의성이 높고 투약 초기 호르몬 급상승 부작용이 없는 것이 강점이다.인터뷰에 동석한 김선미 티움바이오 응용약물합성실장은 "메리골릭스 한 제품으로 자궁내막증, 자궁근종, 보조생식술(ART) 등 최소 3가지 질환을 표적 할 수 있다"며 "메리골릭스는 유럽 임상 2a상에서 자궁내막증 치료 효과와 안전성을 입증한 바 있다"고 설명했다.메리골릭스 자궁근종 임상 2상은 월경과다 증상 개선을 1차 평가지표로 진행됐으며, 총 71명의 환자를 고용량·중간 용량·저용량·위약군에 무작위 배정해 12주간 하루 한 번 경구 투여하고 12주 관찰한 결과, 모든 용량군에서 위약 대비 월경과다 증상이 유의하게 개선됐다.김 실장은 "위약군에서는 월경량이 전혀 줄지 않았지만, 메리골릭스 투여군에서는 대부분 환자의 출혈이 정상 수준으로 감소, 통계적 유의성을 확실히 달성하는 등 경쟁 약물과의 비교에서도 우월한 효능이 확인됐다"고 밝혔다.메리골릭스의 이번 연구 성과는 자궁내막증에 이어 자궁근종에서도 기대 이상의 우수한 약효를 보였다는 점에서 긍정적으로 평가 받고 있다. 하나의 작용기전으로 여러 질환을 치료할 수 있는 약물을 개발하는 티움바이오의 플랫폼 전략이 효과를 보이고 있기 때문이다.김 대표는 "자궁내막증 적응증으로 약효를 확인한 뒤 자궁근종으로 확장하는 식으로 리스크를 분산시키면서도 파급력을 극대화한 것"이라며 "예상대로 자궁근종에서도 뛰어난 결과를 얻어 플랫폼 전략의 유효성을 확인했다"고 밝혔다.차세대 면역항암제와 희귀질환 치료제 개발 드라이브티움바이오는 여성질환 외에도 면역항암제와 희귀질환 치료제 파이프라인을 두 축으로 성장동력을 마련하고 있다.면역항암제 후보물질인 'TU2218'은 TGF-β 신호억제와 VEGF 혈관형성 억제라는 이중 저해 기전을 내세운 경구용 면역항암제로, 면역관문억제제(ICIs)의 효과를 방해하는 TGF-β 및 VEGF 경로를 동시에 막아 항암면역 반응을 극대화하는 것을 목표로 개발 중이다.티움바이오는 향후 TU2218을 키트루다 병용 요법의 시너지 강화제로 개발해 기존 면역치료에 반응하지 않거나 효과가 미미한 환자들에게 새로운 옵션을 제공한다는 계획이다. 현재 담도암과 두경부암을 핵심 타깃 암종으로 선정해 연구를 진행 중이다.이에 대해 김 대표는 "TGF-β 경로 활성과 면역억제 성향이 높은 암이 어디인지 과학적으로 많은 연구를 거쳤고, 약효를 확실히 보일 수 있는 암종으로 담도암과 두경부암을 선택했다"며 "기존 면역항암제 단독 반응률이 30~40%에 불과한데, TU2218과의 병용으로 반응률을 끌어올리고 내약성을 개선해 전체 생존기간(OS)을 증가시킬 수 있을 것으로 기대한다"고 설명했다.아울러 다가오는 미국임상종양학회(ASCO 2025)에서 포스터 발표를 통해 지금까지 투여한 대상자들에 대한 임상 2a상 중간결과를 발표할 계획으로, 이후 추가 투약을 확대해 진행한 후 최종 임상 결과 발표는 내년에 가능할 것으로 전망 중이다.(왼쪽부터) 김훈택 티움바이오 대표, 김선미 티움바이오 응용약물합성실장 희귀질환 분야에서는 혈우병 치료제 'TU7710'이 티움바이오의 주력 파이프라인이다.TU7710은 중화항체 보유 혈우병 환자를 대상으로 한 후보물질로 기존 약물 대비 반감기를 획기적으로 늘린 장기지속성 치료제를 목표로 개발 중이다.회사에 따르면 대부분 시장을 점유하고 있는 노보노디스크의 '노보세븐'의 경우 반감기가 2~3시간으로 매우 짧아 효과 유지를 위해 자주 투여해야 하고 비용도 막대한 부담이 있다.반면 티움바이오의 TU7710은 노보세븐 대비 6~7배 긴 반감기를 보여 투여 빈도와 치료비용 부담을 크게 줄일 수 있을 것으로 기대된다. 현재 TU7710은 1a상을 마무리하고 본격적인 환자 대상 임상 진입을 앞두고 있다.김 대표는 "TU7710은 노보세븐보다 월등히 긴 반감기를 통해 출혈 에피소드에 신속히 대응하고 수술 시 출혈 예방까지 가능한 효과적 약물이 될 것"이라며 "혈우병 치료제는 임상 성공률이 굉장히 높다. 효과에 대해 1%의 의심만 있을 뿐 99%는 확신한다"고 강조했다.그는 이어 "혈우병은 임상 성공확률(26%)이 다른 질환 대비 훨씬 높고, 임상 소요 기간도 길지 않아 4~5년의 개발기간을 거쳐 2028년~2029년쯤 상용화를 목표로 하고 있다"며 "세계 시장 규모 약 2조원으로 추산되는 중화항체 보유 혈우병 치료제 분야에서 TU7710이 50% 이상 시장을 점유할 수 있을 것"이라고 기대했다."글로벌 진출 전략, 파이프라인 특성 맞춤 파트너 모색"여러 혁신 신약 파이프라인을 보유한 티움바이오이지만, 후속 임상 및 글로벌 상용화 단계에서는 외부 파트너십 전략이 필수적이다.이에 대해 김 대표는 "국내 바이오벤처가 모든 것을 자체 수행하긴 어렵다. 파트너링을 어떻게 설정하고 확장하는지가 매우 중요하다. 각 파이프라인 특성에 따라 적합한 글로벌 파트너를 모색 중이다"고 밝혔다.실제 회사는 메리골릭스의 경우 국내는 대원제약, 중국은 한소제약과 이미 라이선스 계약을 맺었고 유럽과 미국도 지역별로 파트너십을 추진하는 전략을 택했다.면역항암제나 희귀질환 신약들 역시 해당 분야 전문기업과 협력해 개발 속도를 높이고 상업화 성공률을 극대화한다는 계획이다.한편 티움바이오는 재무 건전성 확보와 주가 안정화를 통해 장기적 도약 기반을 다지고 있다.최근 증권가에서 거론된 이른바 오버행 이슈에 대해, 김 대표는 "회사 재무 상태는 전혀 나빠진 적이 없다"고 일축했다.풍부한 현금 보유액과 탄탄한 운영 자금으로 사업을 영위해왔지만, 주가 하락으로 투자자들이 막연한 불안을 느끼게 되자 과감한 자금 조달 및 최대주주의 자사주 추가 매입 등을 통해 시장 신뢰를 회복했다는 설명이다.김 대표는 "주가가 많이 내려가면 '회사에 무슨 문제가 있나'라고 의심하게 마련"이라며 "이를 해소하고자 주요 오버행 물량을 정리했고, 앞으로도 신약 개발 성과로 신뢰를 쌓아가는 것이 최우선"이라고 강조했다.이와 관련해 지난 3월 티움바이오는 최대주주인 김훈택 대표가 특수관계인이가 재무적투자자와 함께 2대주주였던 한국투자파트너스의 잔여지분을 전량 매입해 오버행 우려를 해소했고, 이에 힘입어 주가도 안정세를 찾은 바 있다.그는 "신약이 허가되고 매출로 로열티 수입이 들어오기까지 3~4년이 걸릴 것으로 보고 그 기간을 안정적으로 유지하는 게 중요하고 현재 자금조달 계획은 없다"고 언급했다.글로벌 혁신 신약을 향한 도전을 이어가는 티움바이오의 최종 목표는 무엇일까? 이에 대해 김 대표는 '감동을 주는 회사'를 만들고 싶다고 전했다.그는 "최근 스마트 바이오로직스(Smart Biologics)라는 키워드로 스마트한 신약 개발을 추구하는 방향으로 전환 했다"며 "그동안 축적된 생물학 및 화학적 역량에 독창적인 아이디어를 접목해 과거와는 완전히 다른 똑똑한 신약 개발을 해야 글로벌 경쟁에서 살아남을 수 있다"고 전했다.중국 등 거대 자본을 앞세운 경쟁자들을 이기기 위해서라도 묵묵히 열심히 하는 것만으로는 부족하고, 한발 앞선 스마트 혁신이 필요하다는 의미다.끝으로 김 대표는 "티움바이오는 이러한 전략 아래 메리골릭스를 비롯한 주력 파이프라인의 가치를 극대화하고, 협력과 소통을 통해 궁극적으로 환자와 투자자 모두에게 감동을 줄 수 있는 회사를 지향하고 있다"고 덧붙였다.2025-05-30 06:00:19황병우 -
 항암신약부터 AI 예측까지…K-바이오, ASCO 출격[데일리팜=김진구 기자] 닷새 앞으로 다가온 미국임상종양?회 연례학술대회(ASCO 2025)에 한국 제약바이오기업들이 출격한다.이번 ASCO 2025에선 LG화학의 미국 자회사 아베오를 비롯해 티움바이오, 온코닉테라퓨틱스, 이뮨온시아가 각각 항암신약의 임상 성과를 선보인다. 루닛은 AI를 활용한 항암제의 치료 반응성 예측 결과를 대거 소개할 예정이다.ASCO 2025는 오는 30일부터 내달 3일까지 미국 시카고에서 개최된다. ASCO는 ASCO는 미국암연구학회(AACR), 유럽종양학회(ESMO)와 함께 세계 3대 암 학술대회로 꼽힌다. 매년 전 세계 120개국 400여개 이상 기업이 참여해 최신 항암 데이터를 소개한다.LG화학 자회사 아베오, 신장암 치료제 ‘포티브다’ 임상 3상 결과 공개26일 업계에 따르면 국내 제약바이오기업 가운데선 LG화학, 티움바이오, 온코닉테라퓨틱스, 이뮨온시아, 루닛 등이 올해 행사에서 임상 결과를 발표한다.LG화학은 미국 자회사인 아베오(AVEO)를 통해 자체개발 신장암 치료제 ‘포티브다(티보자닙)’의 최신 데이터를 발표한다. 아베오는 2017년 유럽 의약품청(EMA), 2021년 미 식품의약국(FDA)으로부터 포티브다의 허가를 획득했다. LG화학은 2022년 아베오를 5억7100만 달러(약 7000억원)에 인수한 바 있다.이번에 발표되는 포티브다 연구는 ‘TiNivo-2’라는 이름의 글로벌 임상3상이다. 이전에 옵디보(니볼루맙)+여보이(이필리무맙) 또는 VEGF TKI+면역항암제 조합으로 치료받은 전이성 신세포암 환자를 대상으로 포티브다+옵디보 병용요법 또는 포티브다 단독요법의 2차 치료 효과를 살피는 내용이다.앞서 동일한 포티브다+옵디보 병용 임상 3상에선 1차 지표 충족에 실패한 만큼, 임상 전략 변경을 통한 재도전이 성공했을지 여부로 주목을 받는다. 아베오 측은 해당 임상에서 대조군으로 쓰인 포티브다 단독투여 환자 결과를 통해 2차 치료제로서 가능성을 확인했다는 입장이다. 회사는 포티브다 단독투여 시 무진행생존기간(PFS) 지표에서 임상적 유의성이 입증됐다고 설명했다.아베오는 이외에 두경부암 치료 후보물질 ‘파이클라투주맙(ficlatuzumab)’의 임상 3상 결과를 발표한다. 파이클라투주맙은 종양을 키우는 간세포 성장인자(HGF)의 작용을 억제하는 기전의 단일항체 기반 표적항암제다. LG화학은 두경부암 치료에 쓰이는 표적항암제 ‘얼비툭스(세툭시맙)’ 단일 요법을 대조군으로 파이클라투주맙과 얼비툭스 병용요법의 3상 결과를 소개할 예정이다.이밖에 암성 악액질 치료를 위한 항-GDF15 항체 ‘AV-380’의 1상b 용량증가 시험도 포스터로 발표한다.티움바이오·온코닉테라퓨틱스·이뮨온시아, 임상 중간결과 소개티움바이오는 담도암·두경부암을 타깃으로 한 후보물질 ‘TU2218’과 면역항암제 ‘키트루다(펨브롤리주맙)’의 병용요법 임상 2상 중간결과를 이번 행사에서 최초 공개한다.TU2218은 키트루다와 같은 면역항암제의 반응률을 극대화하기 위하여 암세포의 성장과 전이에 관여하는 ‘형질전환성장인자(TGF-ß)’와 ‘혈관내피생성인자(VEGF)’의 시그널을 동시에 차단하는 경구형 이중 저해제다. TGF-β와 VEGF 이중 타깃 기전이 종양미세환경(TME) 개선을 통해 면역항암제의 감수성 향상을 이끌어낸다는 게 회사의 설명이다.티움바이오는 두경부암과 담도암의 1차·2차 치료제 진입을 목표로 TU2218의 임상 2상을 진행 중이다. 두경부암·담도암의 경우 기존 치료제의 생존기간(OS)이 6개월~1년으로 짧은 편이다. 회사는 “미충족 의료 수요가 높은 분야에서 TU2218이 의미 있는 생존기간 연장 데이터를 확보했다”고 설명했다. 온코닉테라퓨틱스는 차세대 이중표적항암제 신약 후보물질 ‘네수파립(Nesuparib)’ 관련 2건의 임상 데이터를 발표한다.첫 번째 발표는 전이성 췌장암을 대상으로 진행 중인 1b/2상과 1b상의 ‘진행 중 임상(Trial in progress)’에 대한 내용이다. 췌장암은 치료제 선택지가 제한적인 대표적 난치암으로, 이번 발표는 네수파립이 해당 질환에서의 치료 옵션으로서 가능성을 타진하고 있다는 점에서 의미가 있다고 회사는 설명했다.두 번째 발표는 자궁내막암 환자를 대상으로 연구자 주도 임상 2상 진행 중인 ‘PENELOPE 스터디’에 대한 진행중 임상(Trial in progress) 발표다. 이 임상은 네수파립과 면역관문억제항암제 ‘키트루다’와의 병용을 통한 자궁내막암에서의 새로운 치료 옵션을 탐색하는 내용이다.온코닉테라퓨틱스 관계자는 “이번 발표 선정은 치료 옵션이 부족한 췌장암과 자궁내막암 분야에서 네수파립이 새로운 대안으로 주목을 받고 있는 것”이라며, “높은 관심을 받고 있는 만큼 고통받는 환자들을 위해 개발 속도를 높이고, 네수파립의 가치를 글로벌 항암 커뮤니티를 통해 입증해 나갈 것”이라고 말했다.이뮨온시아도 ASCO 2025에 임상 데이터 발표를 예고했다. 발표 내용으로는 면역관문 단백질 CD47을 타깃하는 단클론항체 ‘IMC-002’의 임상 1b상 결과가 유력하게 전망된다. 이 약물은 CD47과 SIRPα 신호를 차단해 대식세포가 암세포를 제거할 수 있도록 유도하는 기전이다.루닛, AI 기반 ‘항암제 치료반응성 예측 기술’ 성과 발표 예고루닛은 AI를 기반으로 항암제의 치료 반응성을 예측하는 기술을 대거 선보인다.루닛은 AI 바이오마커 플랫폼 ‘루닛 스코프’를 활용한 연구 성과 12건을 이번 ASCO 2025에서 발표한다고 밝혔다. 가장 관심을 모으는 데이터는 HER2 양성 담도암 환자 대상 엔허투(트라스투주맙 데룩스테칸) 치료 효과 예측 연구 결과다.일본 국립암센터(NCCE)와 공동으로 진행한 이번 연구에선 HER2 양성 담도암 환자 288명의 면역조직화학(IHC) 슬라이드 이미지를 분석하는 과정에 루닛 스코프의 ‘uIHC’를 적용, 암세포의 HER2 발현 강도와 세포 내 위치(세포막·세포질 등)에 따른 발현 분포를 정량적으로 평가했다.그 결과 루닛 AI는 HER2 발현의 강도뿐 아니라, HER2 발현의 세포막 특이도가 환자의 치료 반응을 더 잘 예측할 수 있음을 입증했다. 엔허투 투약 환자 29명 중 HER2 세포막 특이도가 높은 환자들의 무진행 생존기간 중앙값(mPFS)은 11.0개월로, 세포막 특이도가 낮은 환자군의 4.2개월에 비해 개선된 치료 결과를 나타냈다.AI가 식별한 환자 중에는 기존의 HER2 발현 강도 측정 방식으로는 발견되지 않았던 환자가 추가로 포함됐는데, 이는 AI를 활용한 세포막 특이도 분석 방식이 기존 방식보다 더 많은 엔허투 치료 반응 환자를 식별해낼 수 있음을 시사한다고 회사 측은 설명했다.이와 함께 루닛은 위암 환자의 '클라우딘18.2(CLDN18.2)' 단백질 발현과 면역 표현형 예측에 관한 연구 결과를 발표한다. 루닛에 따르면 클라우딘18.2를 타깃으로 하는 치료는 위암 치료의 새로운 대안으로 떠올랐지만, 검체 부족과 추가 비용·시간 등에 대한 부담으로 현실적인 제약이 따랐다.루닛은 이를 해결하기 위해 기본적인 H&E 슬라이드만으로 클라우딘18.2 발현을 예측하는 AI 모델을 개발했다. 이 모델은 위암 환자군에서 클라우딘18.2 양성 환자를 예측하는 성능 지표인 AUROC값이 0.751로 높게 나타났다. 클라우딘18.2 발현 여부는 면역관문억제제 치료에 대한 반응과도 연관이 있어, 단독 화학요법 대비 무진행 생존기간(PFS)과 전체 생존기간(OS)이 유의하게 연장되는 것을 확인했다.대체로 AACR에선 초기 임상이나 전임상 결과가, ASCO에선 후기 임상 결과가 발표된다는 점에서 기술이전이나 파트너십 논의도 활발한 편이다. 제약업계에선 후기 임상 데이터의 상업적 가치가 부각되는 만큼, 국내 제약바이오기업의 성과 발표는 향후 글로벌 시장 진출의 교두보가 될 것이란 기대가 제기왼다.미국임상종양?회 30일 개막2025-05-26 12:00:29김진구
항암신약부터 AI 예측까지…K-바이오, ASCO 출격[데일리팜=김진구 기자] 닷새 앞으로 다가온 미국임상종양?회 연례학술대회(ASCO 2025)에 한국 제약바이오기업들이 출격한다.이번 ASCO 2025에선 LG화학의 미국 자회사 아베오를 비롯해 티움바이오, 온코닉테라퓨틱스, 이뮨온시아가 각각 항암신약의 임상 성과를 선보인다. 루닛은 AI를 활용한 항암제의 치료 반응성 예측 결과를 대거 소개할 예정이다.ASCO 2025는 오는 30일부터 내달 3일까지 미국 시카고에서 개최된다. ASCO는 ASCO는 미국암연구학회(AACR), 유럽종양학회(ESMO)와 함께 세계 3대 암 학술대회로 꼽힌다. 매년 전 세계 120개국 400여개 이상 기업이 참여해 최신 항암 데이터를 소개한다.LG화학 자회사 아베오, 신장암 치료제 ‘포티브다’ 임상 3상 결과 공개26일 업계에 따르면 국내 제약바이오기업 가운데선 LG화학, 티움바이오, 온코닉테라퓨틱스, 이뮨온시아, 루닛 등이 올해 행사에서 임상 결과를 발표한다.LG화학은 미국 자회사인 아베오(AVEO)를 통해 자체개발 신장암 치료제 ‘포티브다(티보자닙)’의 최신 데이터를 발표한다. 아베오는 2017년 유럽 의약품청(EMA), 2021년 미 식품의약국(FDA)으로부터 포티브다의 허가를 획득했다. LG화학은 2022년 아베오를 5억7100만 달러(약 7000억원)에 인수한 바 있다.이번에 발표되는 포티브다 연구는 ‘TiNivo-2’라는 이름의 글로벌 임상3상이다. 이전에 옵디보(니볼루맙)+여보이(이필리무맙) 또는 VEGF TKI+면역항암제 조합으로 치료받은 전이성 신세포암 환자를 대상으로 포티브다+옵디보 병용요법 또는 포티브다 단독요법의 2차 치료 효과를 살피는 내용이다.앞서 동일한 포티브다+옵디보 병용 임상 3상에선 1차 지표 충족에 실패한 만큼, 임상 전략 변경을 통한 재도전이 성공했을지 여부로 주목을 받는다. 아베오 측은 해당 임상에서 대조군으로 쓰인 포티브다 단독투여 환자 결과를 통해 2차 치료제로서 가능성을 확인했다는 입장이다. 회사는 포티브다 단독투여 시 무진행생존기간(PFS) 지표에서 임상적 유의성이 입증됐다고 설명했다.아베오는 이외에 두경부암 치료 후보물질 ‘파이클라투주맙(ficlatuzumab)’의 임상 3상 결과를 발표한다. 파이클라투주맙은 종양을 키우는 간세포 성장인자(HGF)의 작용을 억제하는 기전의 단일항체 기반 표적항암제다. LG화학은 두경부암 치료에 쓰이는 표적항암제 ‘얼비툭스(세툭시맙)’ 단일 요법을 대조군으로 파이클라투주맙과 얼비툭스 병용요법의 3상 결과를 소개할 예정이다.이밖에 암성 악액질 치료를 위한 항-GDF15 항체 ‘AV-380’의 1상b 용량증가 시험도 포스터로 발표한다.티움바이오·온코닉테라퓨틱스·이뮨온시아, 임상 중간결과 소개티움바이오는 담도암·두경부암을 타깃으로 한 후보물질 ‘TU2218’과 면역항암제 ‘키트루다(펨브롤리주맙)’의 병용요법 임상 2상 중간결과를 이번 행사에서 최초 공개한다.TU2218은 키트루다와 같은 면역항암제의 반응률을 극대화하기 위하여 암세포의 성장과 전이에 관여하는 ‘형질전환성장인자(TGF-ß)’와 ‘혈관내피생성인자(VEGF)’의 시그널을 동시에 차단하는 경구형 이중 저해제다. TGF-β와 VEGF 이중 타깃 기전이 종양미세환경(TME) 개선을 통해 면역항암제의 감수성 향상을 이끌어낸다는 게 회사의 설명이다.티움바이오는 두경부암과 담도암의 1차·2차 치료제 진입을 목표로 TU2218의 임상 2상을 진행 중이다. 두경부암·담도암의 경우 기존 치료제의 생존기간(OS)이 6개월~1년으로 짧은 편이다. 회사는 “미충족 의료 수요가 높은 분야에서 TU2218이 의미 있는 생존기간 연장 데이터를 확보했다”고 설명했다. 온코닉테라퓨틱스는 차세대 이중표적항암제 신약 후보물질 ‘네수파립(Nesuparib)’ 관련 2건의 임상 데이터를 발표한다.첫 번째 발표는 전이성 췌장암을 대상으로 진행 중인 1b/2상과 1b상의 ‘진행 중 임상(Trial in progress)’에 대한 내용이다. 췌장암은 치료제 선택지가 제한적인 대표적 난치암으로, 이번 발표는 네수파립이 해당 질환에서의 치료 옵션으로서 가능성을 타진하고 있다는 점에서 의미가 있다고 회사는 설명했다.두 번째 발표는 자궁내막암 환자를 대상으로 연구자 주도 임상 2상 진행 중인 ‘PENELOPE 스터디’에 대한 진행중 임상(Trial in progress) 발표다. 이 임상은 네수파립과 면역관문억제항암제 ‘키트루다’와의 병용을 통한 자궁내막암에서의 새로운 치료 옵션을 탐색하는 내용이다.온코닉테라퓨틱스 관계자는 “이번 발표 선정은 치료 옵션이 부족한 췌장암과 자궁내막암 분야에서 네수파립이 새로운 대안으로 주목을 받고 있는 것”이라며, “높은 관심을 받고 있는 만큼 고통받는 환자들을 위해 개발 속도를 높이고, 네수파립의 가치를 글로벌 항암 커뮤니티를 통해 입증해 나갈 것”이라고 말했다.이뮨온시아도 ASCO 2025에 임상 데이터 발표를 예고했다. 발표 내용으로는 면역관문 단백질 CD47을 타깃하는 단클론항체 ‘IMC-002’의 임상 1b상 결과가 유력하게 전망된다. 이 약물은 CD47과 SIRPα 신호를 차단해 대식세포가 암세포를 제거할 수 있도록 유도하는 기전이다.루닛, AI 기반 ‘항암제 치료반응성 예측 기술’ 성과 발표 예고루닛은 AI를 기반으로 항암제의 치료 반응성을 예측하는 기술을 대거 선보인다.루닛은 AI 바이오마커 플랫폼 ‘루닛 스코프’를 활용한 연구 성과 12건을 이번 ASCO 2025에서 발표한다고 밝혔다. 가장 관심을 모으는 데이터는 HER2 양성 담도암 환자 대상 엔허투(트라스투주맙 데룩스테칸) 치료 효과 예측 연구 결과다.일본 국립암센터(NCCE)와 공동으로 진행한 이번 연구에선 HER2 양성 담도암 환자 288명의 면역조직화학(IHC) 슬라이드 이미지를 분석하는 과정에 루닛 스코프의 ‘uIHC’를 적용, 암세포의 HER2 발현 강도와 세포 내 위치(세포막·세포질 등)에 따른 발현 분포를 정량적으로 평가했다.그 결과 루닛 AI는 HER2 발현의 강도뿐 아니라, HER2 발현의 세포막 특이도가 환자의 치료 반응을 더 잘 예측할 수 있음을 입증했다. 엔허투 투약 환자 29명 중 HER2 세포막 특이도가 높은 환자들의 무진행 생존기간 중앙값(mPFS)은 11.0개월로, 세포막 특이도가 낮은 환자군의 4.2개월에 비해 개선된 치료 결과를 나타냈다.AI가 식별한 환자 중에는 기존의 HER2 발현 강도 측정 방식으로는 발견되지 않았던 환자가 추가로 포함됐는데, 이는 AI를 활용한 세포막 특이도 분석 방식이 기존 방식보다 더 많은 엔허투 치료 반응 환자를 식별해낼 수 있음을 시사한다고 회사 측은 설명했다.이와 함께 루닛은 위암 환자의 '클라우딘18.2(CLDN18.2)' 단백질 발현과 면역 표현형 예측에 관한 연구 결과를 발표한다. 루닛에 따르면 클라우딘18.2를 타깃으로 하는 치료는 위암 치료의 새로운 대안으로 떠올랐지만, 검체 부족과 추가 비용·시간 등에 대한 부담으로 현실적인 제약이 따랐다.루닛은 이를 해결하기 위해 기본적인 H&E 슬라이드만으로 클라우딘18.2 발현을 예측하는 AI 모델을 개발했다. 이 모델은 위암 환자군에서 클라우딘18.2 양성 환자를 예측하는 성능 지표인 AUROC값이 0.751로 높게 나타났다. 클라우딘18.2 발현 여부는 면역관문억제제 치료에 대한 반응과도 연관이 있어, 단독 화학요법 대비 무진행 생존기간(PFS)과 전체 생존기간(OS)이 유의하게 연장되는 것을 확인했다.대체로 AACR에선 초기 임상이나 전임상 결과가, ASCO에선 후기 임상 결과가 발표된다는 점에서 기술이전이나 파트너십 논의도 활발한 편이다. 제약업계에선 후기 임상 데이터의 상업적 가치가 부각되는 만큼, 국내 제약바이오기업의 성과 발표는 향후 글로벌 시장 진출의 교두보가 될 것이란 기대가 제기왼다.미국임상종양?회 30일 개막2025-05-26 12:00:29김진구 -
 흑색종 환자에 '암타그비' 투여…중위험 연구 정부 승인[데일리팜=이정환 기자] 정부가 T세포 치료제 암타그비를 활용해 불응성 흑색종 환자를 치료하는 중위험 임상연구를 승인했다.동종 조혈모세포 이식 소아청소년 가운데 표준치료에 저항성·불응성을 보이는 다중 바이러스 감염증 환자에게 다중 바이러스 항원 특이적 면역세포인 T세포를 투여하는 고위험 임상연구도 허용했다.23일 보건복지부는 제5차 첨단재생의료 및 첨단바이오의약품 심의위원회 의결 결과를 통해 이같이 밝혔다.심의위는 가톨릭서울성모병원, 삼성서울병원 등 임상연구계획 총 4건(고위험 2건, 중위험 2건)을 심의했다. 이 중 2건은 적합, 2건은 부적합 의결했다.흑색종 환자 '암타그비' 투약 임상연구 승인적합 의결된 과제는 면역관문억제제 치료에 실패한 불응성(난치성) 흑색종 환자를 대상으로 환자 본인으로부터 유래한 종양침윤림프구(CT-SP)의 안전성·유효성 평가를 위한 중위험 임상연구이다.흑색종은 피부에 있는 멜라닌 세포에서 발생하는 악성종양이다. 피부암의 1~4%이지만 사망률은 가장 높다.종양침윤림프구는 종양 미세환경에 존재하는 림프구로 종양세포를 인지하고 파괴한다. 종양이질성과 종양세포의 면역기피를 극복하고 종양세포를 사멸시킬 가능성이 높다.종양침윤림프구 치료제는 고형암을 대상으로 세계 최초 허가된 T 세포치료제 '암타그비'다.국내외에서 다양한 고형암을 대상으로 종양침윤림프구 치료제의 임상시험이 진행 중이다.해당 연구는 국내에서 개발한 제조 방법으로 만든 종양침윤림프구를 투여하고 이상반응 확인 등 안전성 평가와 객관적 반응률·무진행 생존기간 등을 확인하는 유효성 평가를 목표로 한다.대부분의 기존 치료에 실패한 국내 흑색종 환자에게 종양침윤림프구를 이용한 새로운 치료 방법을 제공하기 위해서다.다중바이러스 감염 환자 T세포 투여도 허용동종 조혈모세포를 이식한 소아청소년 중 표준치료에 저항성·불응성을 보이는 다중 바이러스 감염 또는 관련 감염증 환자를 대상으로 다중 바이러스 항원 특이적 면역세포인 T 세포(VST)를 투여하는 고위험 임상연구다.동종조혈모세포이식 과정에서 주로 발생하는 이식편대숙주병은 기증자의 면역세포가 환자의 조직을 공격하는 주요 중증 합병증이다.이를 관리하기 위해 강력한 면역억제제가 사용되며 그 부작용으로 환자 전반적인 면역력이 약화되어 감염에 취약해진다.이로 인해 환자 체내 잠복감염 바이러스들이 재활성화되어 감염을 일으키는데, 기존 치료제인 항바이러스제는 여러 바이러스를 동시에 억제하기 어렵고 장기 사용 시 내성이 생길 수 있으며 신장·간독성이 높다.해당 연구는 다중 바이러스 항원에 특이적인 T 세포를 이용하여 동시에 다중 바이러스를 억제하고 면역 기억을 통해 장기적으로 재발도 방지하는 것을 목표로 한다.식품의약품안전처장은 고위험 임상연구 신속·병합 검토를 통해 연구자의 제출 자료가 타당함을 심의위원회에 통보했다.절차에 따라 재생의료기관은 식약처장 승인 통보를 받은 후 임상연구를 실시하게 된다.김우기 첨단재생의료 및 첨단바이오의약품 심의위원회 사무국장은 "심의위원회는 임상연구 활성화를 위해 보완이 필요한 임상연구계획에 대해 재심의 결정을 통해 연구자가 보완할 수 있도록 기회를 부여하여 최종 적합 의결했다"고 설명했다.2025-05-23 11:31:53이정환
흑색종 환자에 '암타그비' 투여…중위험 연구 정부 승인[데일리팜=이정환 기자] 정부가 T세포 치료제 암타그비를 활용해 불응성 흑색종 환자를 치료하는 중위험 임상연구를 승인했다.동종 조혈모세포 이식 소아청소년 가운데 표준치료에 저항성·불응성을 보이는 다중 바이러스 감염증 환자에게 다중 바이러스 항원 특이적 면역세포인 T세포를 투여하는 고위험 임상연구도 허용했다.23일 보건복지부는 제5차 첨단재생의료 및 첨단바이오의약품 심의위원회 의결 결과를 통해 이같이 밝혔다.심의위는 가톨릭서울성모병원, 삼성서울병원 등 임상연구계획 총 4건(고위험 2건, 중위험 2건)을 심의했다. 이 중 2건은 적합, 2건은 부적합 의결했다.흑색종 환자 '암타그비' 투약 임상연구 승인적합 의결된 과제는 면역관문억제제 치료에 실패한 불응성(난치성) 흑색종 환자를 대상으로 환자 본인으로부터 유래한 종양침윤림프구(CT-SP)의 안전성·유효성 평가를 위한 중위험 임상연구이다.흑색종은 피부에 있는 멜라닌 세포에서 발생하는 악성종양이다. 피부암의 1~4%이지만 사망률은 가장 높다.종양침윤림프구는 종양 미세환경에 존재하는 림프구로 종양세포를 인지하고 파괴한다. 종양이질성과 종양세포의 면역기피를 극복하고 종양세포를 사멸시킬 가능성이 높다.종양침윤림프구 치료제는 고형암을 대상으로 세계 최초 허가된 T 세포치료제 '암타그비'다.국내외에서 다양한 고형암을 대상으로 종양침윤림프구 치료제의 임상시험이 진행 중이다.해당 연구는 국내에서 개발한 제조 방법으로 만든 종양침윤림프구를 투여하고 이상반응 확인 등 안전성 평가와 객관적 반응률·무진행 생존기간 등을 확인하는 유효성 평가를 목표로 한다.대부분의 기존 치료에 실패한 국내 흑색종 환자에게 종양침윤림프구를 이용한 새로운 치료 방법을 제공하기 위해서다.다중바이러스 감염 환자 T세포 투여도 허용동종 조혈모세포를 이식한 소아청소년 중 표준치료에 저항성·불응성을 보이는 다중 바이러스 감염 또는 관련 감염증 환자를 대상으로 다중 바이러스 항원 특이적 면역세포인 T 세포(VST)를 투여하는 고위험 임상연구다.동종조혈모세포이식 과정에서 주로 발생하는 이식편대숙주병은 기증자의 면역세포가 환자의 조직을 공격하는 주요 중증 합병증이다.이를 관리하기 위해 강력한 면역억제제가 사용되며 그 부작용으로 환자 전반적인 면역력이 약화되어 감염에 취약해진다.이로 인해 환자 체내 잠복감염 바이러스들이 재활성화되어 감염을 일으키는데, 기존 치료제인 항바이러스제는 여러 바이러스를 동시에 억제하기 어렵고 장기 사용 시 내성이 생길 수 있으며 신장·간독성이 높다.해당 연구는 다중 바이러스 항원에 특이적인 T 세포를 이용하여 동시에 다중 바이러스를 억제하고 면역 기억을 통해 장기적으로 재발도 방지하는 것을 목표로 한다.식품의약품안전처장은 고위험 임상연구 신속·병합 검토를 통해 연구자의 제출 자료가 타당함을 심의위원회에 통보했다.절차에 따라 재생의료기관은 식약처장 승인 통보를 받은 후 임상연구를 실시하게 된다.김우기 첨단재생의료 및 첨단바이오의약품 심의위원회 사무국장은 "심의위원회는 임상연구 활성화를 위해 보완이 필요한 임상연구계획에 대해 재심의 결정을 통해 연구자가 보완할 수 있도록 기회를 부여하여 최종 적합 의결했다"고 설명했다.2025-05-23 11:31:53이정환 -
 한미-MSD, 임상협업 3건·기술수출...견고한 R&D 동맹[데일리팜=차지현 기자] 한미약품이 미국 머크(MSD)와 차세대 면역항암제 후보물질 개발을 위한 임상 협력 계약을 체결했다. 이로써 한미약품과 MSD 간 임상 협업은 총 세 건으로 확대됐다. 한미약품은 임상 협력뿐만 아니라 기술이전 등을 통해 MSD와 공고한 파트너십을 이어가고 있다.한미-MSD, 랩스 IL-2 아날로그 'HM16390'·항 PD-1 면역항암제 '키트루다' 병용 협력20일 제약 업계에 따르면 한미약품은 최근 MSD와 자사의 랩스 인터루킨-2(IL-2) 아날로그 차세대 면역항암제 후보물질 'HM16390'과 MSD 항 PD-1 면역항암제 '키트루다'(성분명 펨브롤리주맙) 병용요법을 평가하기 위한 임상시험 협력과 공급 계약을 체결했다.계약에 따라 한미약품은 임상 주관 기관으로서 HM16390과 키트루다 병용요법의 안전성과 유효성을 평가하기 위한 임상 1상을 총괄 진행하게 된다. MSD는 임상에 사용되는 키트루다를 공급할 예정이다.HM16390은 면역세포 활성화에 관여하는 IL- 기반 차세대 면역항암제 후보물질이다. HM16390은 T세포의 증식과 활성화를 유도해 종양 미세환경 내 면역반응을 강화하는 기전이다. 종양미세환경에서 면역관문억제제에 반응하는 종양침윤림프구(TIL) 수를 증가시켜 면역반응이 적은 종양(콜드 튜머)를 면역세포가 침투하는 종양(핫 튜머)으로 전환, 면역관문억제제와 병용 시 효과를 극대화하도록 설계했다.현재 유전자재조합 IL-2 치료제로는 '프로류킨'이 미국 식품의약국(FDA) 품목허가를 받았지만, 고용량 투여 시 부작용 위험이 있어 제한적으로 사용되고 있다. 또 현재 개발되고 있는 대부분 IL-2 아날로그는 항암 효과를 높이기 위해 IL-2 베타 수용체에 대한 결합력을 강화에 초점을 두는데, 이로 인해 전신 면역반응이 과도하게 유발되며 사이토카인 방출 증후군 등 심각한 부작용이 발생하는 문제가 있다.(자료: 한미약품) 한미약품은 IL-2 알파 수용체 결합력을 정밀하게 조절함으로써 이 같은 한계를 보완했다. 이를 통해 HM16390은 안전성을 확보하는 동시에 약물의 효능을 극대화하는 특징을 갖췄다는 게한미약품 측 설명이다. 특히 한미약품은 자사 독자적인 지속형 플랫폼 기술 랩스커버리를 적용, HM16390을 항암 약물 치료 주기당 1회 피하 투여(SC)가 가능한 지속형 치료제로 개발 중이다.HM16390은 현재 다국가 임상 1상 단계다. 앞서 한미약품은 지난해 11월 미국 면역항암학회(SITC)에서 HM16390 비임상 연구 결과 완전 관해를 달성했다고 발표한 바 있다.MSD가 개발한 면역 항암제 키트루다는 전 세계 매출 1위 의약품이다. 키트루다는 면역세포인 T세포 표면의 PD-1 단백질과 암세포의 PD-L1 수용체 간 결합을 막아 면역세포가 암세포를 공격하도록 돕는 면역관문억제제다.키트루다는 2014년 9월 FDA로부터 악성 흑색종 치료제로 처음 허가받은 후 적응증을 지속해서 추가, 시장 내 입지를 공고히 하고 있다. 유방암, 위암, 폐암 등 40개 이상 적응증을 확보하면서 작년 기준 면역관문억제제 중 가장 광범위한 암종에 사용 가능한 약물로 자리매김했다.다만 약물에 반응하는 환자가 제한적이라는 점이 한계점으로 꼽힌다. 키트루다는 PD-L1이 많이 발현되는 환자에겐 탁월한 항암 효과를 보이지만, PD-L1이 적게 발현되는 환자에겐 효과가 매우 낮다고 알려진다. MSD가 반응 환자군을 늘리거나 약효를 높이기 위해 병용요법에 적극적으로 나서는 배경이다. 한미약품은 이번 MSD와 협력을 통해 HM16390과 키트루다 병용요법이 치료 효과를 한층 높일 것으로 내다봤다.한미약품과 MSD 간 키트루다 병용요법 임상 협업 누적 3건, L/O 등 파트너십 '공고'이번 키트루다 임상 협력 계약 체결로 한미약품과 MSD 간 키트루다 병용요법 임상 협업은 총 세 건으로 확대됐다.한미약품은 MSD와 PD-L1/4-1BB 이중항체 후보물질 'BH3120'과 저분자 CCR4 길항제 후보물질 '티부메시르논'에 대해서도 키트루다 병용요법 임상을 진행 중이다.한미약품과 북경한미약품이 공동 개발 중인 BH3120은 하나의 항체가 서로 다른 두 표적에 동시 결합하는 이중항체 면역항암제 후보물질이다. 한미약품의 독자적 플랫폼 기술 펜탐바디를 적용해 면역세포를 활성화하는 면역항암 기전과 암세포만 선택적으로 공격하는 표적항암제 특성을 모두 지닌 게 특징이다. 특히 BH3120은 PD-L1과 4-1BB 각각 타깃에 다르게 반응토록 설계, 치료 효과는 높이면서 부작용을 줄였다는 게 한미약품 측 설명이다.한미약품은 BH3120과 키트루다 병용요법을 평가하는 임상 1상 중간 결과를 오는 하반기 발표할 예정이다. 앞서 한미약품은 면역항암제에 잘 반응하지 않는 종양쥐모델에서 BH3120과 키트루다 병용투여 시 경쟁 파이프라인(GEN1046) 병용투여 대비 동등 이상의 종양성장억제 효능을 확인했다고 밝힌 바 있다.(자료: 한미약품) 티부메시르논은 한미약품이 지난 2019년 미국 랩트테라퓨틱스로부터 도입한 먹는 면역항암제 후보물질로, 면역 반응을 억제하는 조절 T세포의 종양 내 이동을 유도하는 CCR4 수용체 단백질을 차단한다.한미약품은 지난 1월 미국 샌프란시스코에서 열린 미국임상종양학회 소화기암 심포지엄에서 티부메시르논의 2상 시험 1단계 결과를 포스터 발표했다. 해당 임상은 한미약품이 랩트, MSD와 공동으로 진행한 것으로, 엡스타인바 바이러스(EBV) 양성 위암 환자 10명을 대상으로 한 치료 결과 객관적반응률(ORR) 60%를 확인했다. ORR은 항암 치료 후 암이 완전히 사라지거나 일정 수준 이상 줄어든 환자의 비율을 의미하는 대표적인 치료 효과 지표다. 이 가운데 완전관해 1건과 부분관해 5건이 포함됐다.종양 반응까지의 중앙값(mTTR)은 2.7개월로 확인됐다. 반응 지속 기간의 중앙값(mDOR)은 17.3개월로 나타났다. 또 코호트 2에서 무진행 생존 기간(PFS)의 중앙값은 10.4개월로 나타났다. 한미약품은 임상에 참여한 총 20명의 환자에서 나타난 치료 관련 이상 반응은 대부분 관리 가능한 수준이었다고 설명했다.한미약품은 키트루다 병용요법을 중심으로 한 MSD와의 임상 협업 외에도, 기술수출 계약을 통한 파트너십도 이어가고 있다. 앞서 2020년 한미약품이 MSD에 총 8억6000만달러 규모로 기술수출한 '에피노페그듀타이드'가 그 대상이다. 에피노페그듀타이드는 인슐린 분비와 식욕 억제를 돕는 글루카곤 유사 펩타이드(GLP-1) 수용체와 에너지 대사량을 증가시키는 글루카곤 수용체를 동시에 활성화하는 이중 작용제다.한미약품은 2015년 에피노페그듀타이드를 비만·당뇨 치료제로 얀센에 기술수출했다가 2019년 권리를 반환받았는데, 이후 대사 이상 관련 지방간염(MASH)으로 적응증을 변경한 뒤 MSD에 다시 기수수출하는 데 성공했다.MSD는 현재 에피노페그듀타이드 임상 2상을 진행 중이다. 에피노페그듀타이드와 대조약물 노보노디스크의 '세마글루타이드', 위약을 비교하는 임상이다. 2023년 오스트리아 빈에서 열린 유럽간학회(EASL) 발표에 따르면 에피노페그듀타이드 임상 2a상 분석 결과 치료 24주 차에서 간지방함량 투약 전 대비 간경직도를 72.7% 줄였다. 같은 기간 42.3% 감소시킨 세마글루타이드를 훨씬 앞선 수치다. 섬유화 악화 없는 지방간 해소, 지방간 악화 없는 섬유화 개선은 FDA가 제시한 NASH 치료제 핵심 평가 지표다. MSD는 올 12월 에피노페그듀타이드 임상 2상 종료를 목표로 하고 있다.2025-05-20 06:18:25차지현
한미-MSD, 임상협업 3건·기술수출...견고한 R&D 동맹[데일리팜=차지현 기자] 한미약품이 미국 머크(MSD)와 차세대 면역항암제 후보물질 개발을 위한 임상 협력 계약을 체결했다. 이로써 한미약품과 MSD 간 임상 협업은 총 세 건으로 확대됐다. 한미약품은 임상 협력뿐만 아니라 기술이전 등을 통해 MSD와 공고한 파트너십을 이어가고 있다.한미-MSD, 랩스 IL-2 아날로그 'HM16390'·항 PD-1 면역항암제 '키트루다' 병용 협력20일 제약 업계에 따르면 한미약품은 최근 MSD와 자사의 랩스 인터루킨-2(IL-2) 아날로그 차세대 면역항암제 후보물질 'HM16390'과 MSD 항 PD-1 면역항암제 '키트루다'(성분명 펨브롤리주맙) 병용요법을 평가하기 위한 임상시험 협력과 공급 계약을 체결했다.계약에 따라 한미약품은 임상 주관 기관으로서 HM16390과 키트루다 병용요법의 안전성과 유효성을 평가하기 위한 임상 1상을 총괄 진행하게 된다. MSD는 임상에 사용되는 키트루다를 공급할 예정이다.HM16390은 면역세포 활성화에 관여하는 IL- 기반 차세대 면역항암제 후보물질이다. HM16390은 T세포의 증식과 활성화를 유도해 종양 미세환경 내 면역반응을 강화하는 기전이다. 종양미세환경에서 면역관문억제제에 반응하는 종양침윤림프구(TIL) 수를 증가시켜 면역반응이 적은 종양(콜드 튜머)를 면역세포가 침투하는 종양(핫 튜머)으로 전환, 면역관문억제제와 병용 시 효과를 극대화하도록 설계했다.현재 유전자재조합 IL-2 치료제로는 '프로류킨'이 미국 식품의약국(FDA) 품목허가를 받았지만, 고용량 투여 시 부작용 위험이 있어 제한적으로 사용되고 있다. 또 현재 개발되고 있는 대부분 IL-2 아날로그는 항암 효과를 높이기 위해 IL-2 베타 수용체에 대한 결합력을 강화에 초점을 두는데, 이로 인해 전신 면역반응이 과도하게 유발되며 사이토카인 방출 증후군 등 심각한 부작용이 발생하는 문제가 있다.(자료: 한미약품) 한미약품은 IL-2 알파 수용체 결합력을 정밀하게 조절함으로써 이 같은 한계를 보완했다. 이를 통해 HM16390은 안전성을 확보하는 동시에 약물의 효능을 극대화하는 특징을 갖췄다는 게한미약품 측 설명이다. 특히 한미약품은 자사 독자적인 지속형 플랫폼 기술 랩스커버리를 적용, HM16390을 항암 약물 치료 주기당 1회 피하 투여(SC)가 가능한 지속형 치료제로 개발 중이다.HM16390은 현재 다국가 임상 1상 단계다. 앞서 한미약품은 지난해 11월 미국 면역항암학회(SITC)에서 HM16390 비임상 연구 결과 완전 관해를 달성했다고 발표한 바 있다.MSD가 개발한 면역 항암제 키트루다는 전 세계 매출 1위 의약품이다. 키트루다는 면역세포인 T세포 표면의 PD-1 단백질과 암세포의 PD-L1 수용체 간 결합을 막아 면역세포가 암세포를 공격하도록 돕는 면역관문억제제다.키트루다는 2014년 9월 FDA로부터 악성 흑색종 치료제로 처음 허가받은 후 적응증을 지속해서 추가, 시장 내 입지를 공고히 하고 있다. 유방암, 위암, 폐암 등 40개 이상 적응증을 확보하면서 작년 기준 면역관문억제제 중 가장 광범위한 암종에 사용 가능한 약물로 자리매김했다.다만 약물에 반응하는 환자가 제한적이라는 점이 한계점으로 꼽힌다. 키트루다는 PD-L1이 많이 발현되는 환자에겐 탁월한 항암 효과를 보이지만, PD-L1이 적게 발현되는 환자에겐 효과가 매우 낮다고 알려진다. MSD가 반응 환자군을 늘리거나 약효를 높이기 위해 병용요법에 적극적으로 나서는 배경이다. 한미약품은 이번 MSD와 협력을 통해 HM16390과 키트루다 병용요법이 치료 효과를 한층 높일 것으로 내다봤다.한미약품과 MSD 간 키트루다 병용요법 임상 협업 누적 3건, L/O 등 파트너십 '공고'이번 키트루다 임상 협력 계약 체결로 한미약품과 MSD 간 키트루다 병용요법 임상 협업은 총 세 건으로 확대됐다.한미약품은 MSD와 PD-L1/4-1BB 이중항체 후보물질 'BH3120'과 저분자 CCR4 길항제 후보물질 '티부메시르논'에 대해서도 키트루다 병용요법 임상을 진행 중이다.한미약품과 북경한미약품이 공동 개발 중인 BH3120은 하나의 항체가 서로 다른 두 표적에 동시 결합하는 이중항체 면역항암제 후보물질이다. 한미약품의 독자적 플랫폼 기술 펜탐바디를 적용해 면역세포를 활성화하는 면역항암 기전과 암세포만 선택적으로 공격하는 표적항암제 특성을 모두 지닌 게 특징이다. 특히 BH3120은 PD-L1과 4-1BB 각각 타깃에 다르게 반응토록 설계, 치료 효과는 높이면서 부작용을 줄였다는 게 한미약품 측 설명이다.한미약품은 BH3120과 키트루다 병용요법을 평가하는 임상 1상 중간 결과를 오는 하반기 발표할 예정이다. 앞서 한미약품은 면역항암제에 잘 반응하지 않는 종양쥐모델에서 BH3120과 키트루다 병용투여 시 경쟁 파이프라인(GEN1046) 병용투여 대비 동등 이상의 종양성장억제 효능을 확인했다고 밝힌 바 있다.(자료: 한미약품) 티부메시르논은 한미약품이 지난 2019년 미국 랩트테라퓨틱스로부터 도입한 먹는 면역항암제 후보물질로, 면역 반응을 억제하는 조절 T세포의 종양 내 이동을 유도하는 CCR4 수용체 단백질을 차단한다.한미약품은 지난 1월 미국 샌프란시스코에서 열린 미국임상종양학회 소화기암 심포지엄에서 티부메시르논의 2상 시험 1단계 결과를 포스터 발표했다. 해당 임상은 한미약품이 랩트, MSD와 공동으로 진행한 것으로, 엡스타인바 바이러스(EBV) 양성 위암 환자 10명을 대상으로 한 치료 결과 객관적반응률(ORR) 60%를 확인했다. ORR은 항암 치료 후 암이 완전히 사라지거나 일정 수준 이상 줄어든 환자의 비율을 의미하는 대표적인 치료 효과 지표다. 이 가운데 완전관해 1건과 부분관해 5건이 포함됐다.종양 반응까지의 중앙값(mTTR)은 2.7개월로 확인됐다. 반응 지속 기간의 중앙값(mDOR)은 17.3개월로 나타났다. 또 코호트 2에서 무진행 생존 기간(PFS)의 중앙값은 10.4개월로 나타났다. 한미약품은 임상에 참여한 총 20명의 환자에서 나타난 치료 관련 이상 반응은 대부분 관리 가능한 수준이었다고 설명했다.한미약품은 키트루다 병용요법을 중심으로 한 MSD와의 임상 협업 외에도, 기술수출 계약을 통한 파트너십도 이어가고 있다. 앞서 2020년 한미약품이 MSD에 총 8억6000만달러 규모로 기술수출한 '에피노페그듀타이드'가 그 대상이다. 에피노페그듀타이드는 인슐린 분비와 식욕 억제를 돕는 글루카곤 유사 펩타이드(GLP-1) 수용체와 에너지 대사량을 증가시키는 글루카곤 수용체를 동시에 활성화하는 이중 작용제다.한미약품은 2015년 에피노페그듀타이드를 비만·당뇨 치료제로 얀센에 기술수출했다가 2019년 권리를 반환받았는데, 이후 대사 이상 관련 지방간염(MASH)으로 적응증을 변경한 뒤 MSD에 다시 기수수출하는 데 성공했다.MSD는 현재 에피노페그듀타이드 임상 2상을 진행 중이다. 에피노페그듀타이드와 대조약물 노보노디스크의 '세마글루타이드', 위약을 비교하는 임상이다. 2023년 오스트리아 빈에서 열린 유럽간학회(EASL) 발표에 따르면 에피노페그듀타이드 임상 2a상 분석 결과 치료 24주 차에서 간지방함량 투약 전 대비 간경직도를 72.7% 줄였다. 같은 기간 42.3% 감소시킨 세마글루타이드를 훨씬 앞선 수치다. 섬유화 악화 없는 지방간 해소, 지방간 악화 없는 섬유화 개선은 FDA가 제시한 NASH 치료제 핵심 평가 지표다. MSD는 올 12월 에피노페그듀타이드 임상 2상 종료를 목표로 하고 있다.2025-05-20 06:18:25차지현 -
 글로벌 매출 1위 '키트루다', 국내외 시밀러 개발 전쟁[데일리팜=차지현 기자] 전 세계 매출 1위 의약품 '키트루다'(펨브롤리주맙) 바이오시밀러 시장 선점을 위한 경쟁이 본격화하고 있다. 글로벌 빅파마는 물론 국내 기업까지 개발에 속도를 내면서 주도권 다툼이 치열해지는 분위기다.삼성에피스·셀트리온, 글로벌 3상 속도…"2027·2028년 임상 마무리 계획"30일 제약 업계에 따르면 셀트리온은 최근 식품의약품안전처로부터 키트루다 바이오시밀러로 개발 중인 'CT-P51'에 대한 임상 3상 임상시험계획(IND)을 승인받았다. 셀트리온은 과거 치료 이력이 없는 전이성 비편평 비소세포폐암 환자를 대상 606명을 대상으로 CT-P51과 키트루다 간 유효성과 안전성을 비교하기 위한 임상을 진행할 예정이다.앞서 셀트리온은 지난해 8월 미국 식품의약국(FDA)으로부터 CT-P51 다국가 임상 3상 IND 허가를 획득한 바 있다. 이어 셀트리온은 작년 12월 유럽의약품청(EMA)에서도 CT-P51 임상 3상 IND를 승인받았다. 이번에 국내 IND 허가를 획득하면서 셀트리온은 CT-P51 임상 3상에 더욱 박차를 가할 것으로 전망된다.삼성바이오에피스(왼), 셀트리온(오) 셀트리온과 함께 국내 바이오시밀러 양대산맥으로 꼽히는 삼성바이오에피스도 키트루다 바이오시밀러 'SB27'를 개발 중이다.삼성바이오에피스는 국내 업체 가운데 가장 먼저 키트루다 바이오시밀러 임상에 진입했다. 삼성바이오에피스는 지난해 2월 한국을 포함한 4개 국가에서 SB27 임상 1상을 개시했다. 비소세포폐암 환자 135명을 모집해 SB27과 오리지널 의약품의 약동학과 유효성, 안전성 등을 비교하는 임상이다.이어 삼성바이오에피스는 임상 1상에 착수한 지 두 달만에 임상 3상에 나섰다. 작년 4월 14개국 전이성 비소세포폐암 환자 616명을 대상으로 SB27과 키트루다를 비교하는 임상 3상에 돌입했다. 임상 1상과 3상을 동시 진행하는 '오버랩' 전략을 활용해 개발 속도를 높인다는 구상이다.임상정보 사이트 '클리니컬 트라이얼즈'에 따르면 삼성바이오로직스와 셀트리온은 키트루다 바이오시밀러 글로벌 임상 종료 시점을 각각 2027년과 2028년으로 예상하고 있다.머크의 항PD-1 면역항암제 '키트루다' 제품 사진키트루다는 미국 머크(MSD)가 개발한 면역 항암제다. 키트루다는 면역세포인 T세포 표면의 PD-1 단백질과 암세포의 PD-L1 수용체 간 결합을 막아 면역세포가 암세포를 공격하도록 돕는 면역관문억제제다.키트루다는 2014년 9월 FDA로부터 악성 흑색종 치료제로 처음 허가받은 후 적응증을 지속해서 추가, 시장 내 입지를 공고히 하고 있다. 유방암, 위암, 폐암 등 40개 이상 적응증을 확보하면서 작년 기준 면역관문억제제 중 가장 광범위한 암종에 사용 가능한 약물로 자리매김했다.이 같은 확장 전략을 통해 키트루다는 전 세계 매출 1위 의약품으로도 등극했다. 키트루다 지난해 매출은 294억8200만 달러(약 43조원)로 전년보다 18% 늘었다. 2020년 매출과 비교하면 105% 늘어난 수치다.2029년 이후 물질특허 만료…촘촘해진 방어 전략, MSD와 '합의' 관건키트루다의 물질특허는 미국에서 2029년 11월, 유럽에서 2031년 1월 만료된다. 이에 따라 키트루다 특허 만료 시점에 맞춰 바이오시밀러 제품을 출시하기 위한 국내외 제약바이오 업체들의 움직임도 분주해지는 모습이다.현재 키트루다 바이오시밀러 개발에 뛰어든 국내외 업체만 20여곳에 달한다.이 가운데 상용화에 가장 근접한 곳은 삼성바이오에피스와 셀트리온을 포함해 전 세계 8곳 정도로 추산된다. 해외에선 스페인 맵사이언스, 독일 프레지니우스 카비(MB-12), 러시아 바이오캐드(BCD-201), 중국 바이오테라솔루션스(BAT3306), 스위스 산도스(GME-751), 러시아 알팜(RPH-075), 미국 암젠(ABP 234) 등이 키트루다 바이오시밀러 임상 3상을 진행 중이다.이밖에 중국 치루제약과 독일 포미콘은 각각 키트루다 바이오시밀러 'QL-2107'와 'FYB-206'의 임상 1상을 진행하고 있다. 중국 헨리우스 바이오텍의 경우 키트루다 바이오시밀러 'HLX-17'에 대한 중국 임상에 나섰다. 이외 미국 리펠라 파마슈티컬스, 이란 페르시스젠 파, 캐나다 플랜트폼 등도 키트루다 바이오시밀러 개발을 위한 전임상 단계에 있는 상태다. 키트루다 바이오시밀러 개발 경쟁에 가세한 국내 바이오텍과 전통 제약사도 눈에 띈다. 프레스티지바이오파마는 키트루다 바이오시밀러 'PBP2102'의 세포주 개발 단계에 있다. 로피바이오는 키트루다 바이오시밀러 세포주 개발을 완료, 어밴터와 키트루다 바이오시밀러 공정개발을 위한 협약을 맺었다.종근당은 직접 바이오시밀러를 개발하는 게 아닌, 기술도입 방식으로 관련 시장에 참전을 선언했다. 종근당은 2022년 9월 싱가포르 파보렉스로부터 비임상 단계의 키트루다 바이오시밀러 국내 독점 공급·판매권을 도입했다.다만 오리지널 개발사가 장벽을 더욱 높이고 있다는 점은 부담 요소다. 키트루다의 경우 단순히 물질특허 외에도 적응증별 용도 특허, 제형 특허, 치료요법 특허, 공정 특허 등 다양한 후속 특허들이 여전히 유효하다.특히 키트루다는 허가받은 적응증만 30개 이상으로, 이와 관련된 부가 특허만 수십 건에 이른다. MSD는 특허 만료 이후에도 시장 독점을 최대한 연장하기 위해 사용하는 에버그리닝 전략을 통해 2040년 이후까지 특허를 보호하는 구조를 구축한 상황이다.MSD는 키트루다 시장을 최대한 지키기 위해 제형 변경도 꾀하고 있다. 정맥주사(IV) 제형인 키트루다를 피하주사(SC) 제형으로 바꾸는 전략이다. 피하주사로 바뀌면 투약시간을 10분의 1로 줄여 편의성을 높이는 동시에 투여용량과 용법 기준을 변화해 특허를 연장할 수 있다. MSD는 국내 알테오젠의 플랫폼 기술 'ALT-B4'를 적용해 키트루다 SC 제형을 개발 중이다.복잡하게 얽힌 특허망과 오리지널사의 방어 전략이 더욱 촘촘해지고 있다는 점에서 바이오시밀러 개발 업체의 기본 전략은 특허 극복 후 제품 발매보다 오리지널사와의 '합의'에 맞춰져 있다. 앞서 글로벌 블록버스터 의약품인 휴미라나 엔브렐 등의 사례에서도 바이오시밀러 개발 기업들은 오리지널사와의 합의를 통해 로열티 지급 혹은 출시일 조정을 거쳐 제품을 발매했다.이런 이유로 바이오시밀러 개발 기업들이 임상을 언제 마무리하느냐가 관건이 될 것이라는 분석이 나온다. 바이오시밀러 개발을 빠르게 완료할수록 오리지널사와의 로열티 지급 혹은 출시일 조정 협상 과정에서 경쟁 업체보다 유리한 고지를 점할 수 있기 때문이다.연 43조 시장 잡아라2025-04-30 06:00:00차지현
글로벌 매출 1위 '키트루다', 국내외 시밀러 개발 전쟁[데일리팜=차지현 기자] 전 세계 매출 1위 의약품 '키트루다'(펨브롤리주맙) 바이오시밀러 시장 선점을 위한 경쟁이 본격화하고 있다. 글로벌 빅파마는 물론 국내 기업까지 개발에 속도를 내면서 주도권 다툼이 치열해지는 분위기다.삼성에피스·셀트리온, 글로벌 3상 속도…"2027·2028년 임상 마무리 계획"30일 제약 업계에 따르면 셀트리온은 최근 식품의약품안전처로부터 키트루다 바이오시밀러로 개발 중인 'CT-P51'에 대한 임상 3상 임상시험계획(IND)을 승인받았다. 셀트리온은 과거 치료 이력이 없는 전이성 비편평 비소세포폐암 환자를 대상 606명을 대상으로 CT-P51과 키트루다 간 유효성과 안전성을 비교하기 위한 임상을 진행할 예정이다.앞서 셀트리온은 지난해 8월 미국 식품의약국(FDA)으로부터 CT-P51 다국가 임상 3상 IND 허가를 획득한 바 있다. 이어 셀트리온은 작년 12월 유럽의약품청(EMA)에서도 CT-P51 임상 3상 IND를 승인받았다. 이번에 국내 IND 허가를 획득하면서 셀트리온은 CT-P51 임상 3상에 더욱 박차를 가할 것으로 전망된다.삼성바이오에피스(왼), 셀트리온(오) 셀트리온과 함께 국내 바이오시밀러 양대산맥으로 꼽히는 삼성바이오에피스도 키트루다 바이오시밀러 'SB27'를 개발 중이다.삼성바이오에피스는 국내 업체 가운데 가장 먼저 키트루다 바이오시밀러 임상에 진입했다. 삼성바이오에피스는 지난해 2월 한국을 포함한 4개 국가에서 SB27 임상 1상을 개시했다. 비소세포폐암 환자 135명을 모집해 SB27과 오리지널 의약품의 약동학과 유효성, 안전성 등을 비교하는 임상이다.이어 삼성바이오에피스는 임상 1상에 착수한 지 두 달만에 임상 3상에 나섰다. 작년 4월 14개국 전이성 비소세포폐암 환자 616명을 대상으로 SB27과 키트루다를 비교하는 임상 3상에 돌입했다. 임상 1상과 3상을 동시 진행하는 '오버랩' 전략을 활용해 개발 속도를 높인다는 구상이다.임상정보 사이트 '클리니컬 트라이얼즈'에 따르면 삼성바이오로직스와 셀트리온은 키트루다 바이오시밀러 글로벌 임상 종료 시점을 각각 2027년과 2028년으로 예상하고 있다.머크의 항PD-1 면역항암제 '키트루다' 제품 사진키트루다는 미국 머크(MSD)가 개발한 면역 항암제다. 키트루다는 면역세포인 T세포 표면의 PD-1 단백질과 암세포의 PD-L1 수용체 간 결합을 막아 면역세포가 암세포를 공격하도록 돕는 면역관문억제제다.키트루다는 2014년 9월 FDA로부터 악성 흑색종 치료제로 처음 허가받은 후 적응증을 지속해서 추가, 시장 내 입지를 공고히 하고 있다. 유방암, 위암, 폐암 등 40개 이상 적응증을 확보하면서 작년 기준 면역관문억제제 중 가장 광범위한 암종에 사용 가능한 약물로 자리매김했다.이 같은 확장 전략을 통해 키트루다는 전 세계 매출 1위 의약품으로도 등극했다. 키트루다 지난해 매출은 294억8200만 달러(약 43조원)로 전년보다 18% 늘었다. 2020년 매출과 비교하면 105% 늘어난 수치다.2029년 이후 물질특허 만료…촘촘해진 방어 전략, MSD와 '합의' 관건키트루다의 물질특허는 미국에서 2029년 11월, 유럽에서 2031년 1월 만료된다. 이에 따라 키트루다 특허 만료 시점에 맞춰 바이오시밀러 제품을 출시하기 위한 국내외 제약바이오 업체들의 움직임도 분주해지는 모습이다.현재 키트루다 바이오시밀러 개발에 뛰어든 국내외 업체만 20여곳에 달한다.이 가운데 상용화에 가장 근접한 곳은 삼성바이오에피스와 셀트리온을 포함해 전 세계 8곳 정도로 추산된다. 해외에선 스페인 맵사이언스, 독일 프레지니우스 카비(MB-12), 러시아 바이오캐드(BCD-201), 중국 바이오테라솔루션스(BAT3306), 스위스 산도스(GME-751), 러시아 알팜(RPH-075), 미국 암젠(ABP 234) 등이 키트루다 바이오시밀러 임상 3상을 진행 중이다.이밖에 중국 치루제약과 독일 포미콘은 각각 키트루다 바이오시밀러 'QL-2107'와 'FYB-206'의 임상 1상을 진행하고 있다. 중국 헨리우스 바이오텍의 경우 키트루다 바이오시밀러 'HLX-17'에 대한 중국 임상에 나섰다. 이외 미국 리펠라 파마슈티컬스, 이란 페르시스젠 파, 캐나다 플랜트폼 등도 키트루다 바이오시밀러 개발을 위한 전임상 단계에 있는 상태다. 키트루다 바이오시밀러 개발 경쟁에 가세한 국내 바이오텍과 전통 제약사도 눈에 띈다. 프레스티지바이오파마는 키트루다 바이오시밀러 'PBP2102'의 세포주 개발 단계에 있다. 로피바이오는 키트루다 바이오시밀러 세포주 개발을 완료, 어밴터와 키트루다 바이오시밀러 공정개발을 위한 협약을 맺었다.종근당은 직접 바이오시밀러를 개발하는 게 아닌, 기술도입 방식으로 관련 시장에 참전을 선언했다. 종근당은 2022년 9월 싱가포르 파보렉스로부터 비임상 단계의 키트루다 바이오시밀러 국내 독점 공급·판매권을 도입했다.다만 오리지널 개발사가 장벽을 더욱 높이고 있다는 점은 부담 요소다. 키트루다의 경우 단순히 물질특허 외에도 적응증별 용도 특허, 제형 특허, 치료요법 특허, 공정 특허 등 다양한 후속 특허들이 여전히 유효하다.특히 키트루다는 허가받은 적응증만 30개 이상으로, 이와 관련된 부가 특허만 수십 건에 이른다. MSD는 특허 만료 이후에도 시장 독점을 최대한 연장하기 위해 사용하는 에버그리닝 전략을 통해 2040년 이후까지 특허를 보호하는 구조를 구축한 상황이다.MSD는 키트루다 시장을 최대한 지키기 위해 제형 변경도 꾀하고 있다. 정맥주사(IV) 제형인 키트루다를 피하주사(SC) 제형으로 바꾸는 전략이다. 피하주사로 바뀌면 투약시간을 10분의 1로 줄여 편의성을 높이는 동시에 투여용량과 용법 기준을 변화해 특허를 연장할 수 있다. MSD는 국내 알테오젠의 플랫폼 기술 'ALT-B4'를 적용해 키트루다 SC 제형을 개발 중이다.복잡하게 얽힌 특허망과 오리지널사의 방어 전략이 더욱 촘촘해지고 있다는 점에서 바이오시밀러 개발 업체의 기본 전략은 특허 극복 후 제품 발매보다 오리지널사와의 '합의'에 맞춰져 있다. 앞서 글로벌 블록버스터 의약품인 휴미라나 엔브렐 등의 사례에서도 바이오시밀러 개발 기업들은 오리지널사와의 합의를 통해 로열티 지급 혹은 출시일 조정을 거쳐 제품을 발매했다.이런 이유로 바이오시밀러 개발 기업들이 임상을 언제 마무리하느냐가 관건이 될 것이라는 분석이 나온다. 바이오시밀러 개발을 빠르게 완료할수록 오리지널사와의 로열티 지급 혹은 출시일 조정 협상 과정에서 경쟁 업체보다 유리한 고지를 점할 수 있기 때문이다.연 43조 시장 잡아라2025-04-30 06:00:00차지현 -
 텝메코·테빔브라 급여등재…자이티가 본인부담 축소텝메코정225mg(테포티닙, 한국머크). [데일리팜=이탁순 기자] 텝메코정과 테빔브라주 등 신규 항암제가 4월 1일부로 급여목록에 오른다.또한 자이티가정 등 아비라테론아세테이트 제제는 거세저항성 전립선암 1차 치료에 본인부담율이 축소되면서 환자의 경제적 부담이 크게 줄 전망이다.건강보험심사평가원은 이같은 내용의 암환자에게 처방·투여하는 약제에 따른 공고 개정안을 예고하며 의견조회에 들어갔다. 시행일은 4월 1일자이다.개정안에 따르면 텝메코정225mg(테포티닙, 한국머크)은 MET 엑손 14 결손이 확인된 국소 진행성 또는 전이성 비소세포폐암 환자에 요양급여가 인정된다.심평원은 "신청 야제는 타깃이 명확한 약제로 환자들에게 또 다른 치료 옵션을 제공할 수 있어 진료상 필요한 약제로 판단되는 점 등을 고려해 급여기준을 설정했다"고 전했다.국내에서 MET 돌연변이 항암제에 급여가 적용되는 건 텝메코정이 유일하다. 국내 비소세포폐암 환자 1020명의 진단 결과, 1.9%의 환자가 MET 엑손 14 결손으로 확인되고 있다.텝메코는 확증적 시험군이 추가된 2상 임상시험에서 ORR 51.4%(95% CI, 45.8-57.1), mPFS 11.2개월(95%CI, 9.5-13.8), mOS 19.6개월(95% CI, 16.2-22.9)로 높은 치료효과가 확인됐다. 주요 교과서와 해외 학회 가이드라인에서 이 약을 권고하고 있다. 텝메코의 상한금액은 정당 7만6500원으로 알려졌다. 재정 분담 차원에서 환급형과 총액제한형 RSA(위험분담제) 계약을 맺었다.테빔브라주(티슬렐리주맙, 베이진코리아)는 이전 백금 기반 화학요법 치료 도중 또는 이후에 재발 또는 진행된 절제 불가능, 재발성, 국소진행성 또는 전이성 식도편평세포암에 사용된다. 선행화학요법 또는 수술후보조요법 종료 후 6개월 이내 재발한 경우도 포함된다. 반면 이전 PD-1 inhibitor 등 면역관문억제제 치료를 받지 않은 경우에 급여가 적용된다.이 약은 PD-1저해 기전의 면역항암제로, 4월 급여 등재되면 면역항암제로는 최초로 식도암에 급여가 적용된다. 이 약의 상한금액은 병당 120만6000원이다. 텝메코와 같이 환급형, 총액제한형 RSA 계약을 맺었다.한편 자이티가정 등 아비라테론아세테이트 제제는 거세저항성 전립선암 1차 치료에 본인부담율이 30%에서 5%로 축소된다.아비라테론 제제는 오리지널 자이티가정(한국얀센)뿐만 아니라 한미약품, 에이스파마 등이 공급하는 제네릭약제도 있다.이번 본인부담율 축소는 제네릭 진입과도 관련돼 있다. 심평원은 "'차세대 호르몬 약제(ATRA)'가 전이성 호르몬 감수성 전립선암에 급여되며 해당 요법의 대상자가 점차적으로 줄어들 것으로 예상된다"면서 "제네릭 등재 등 기심의 대비 약가가 인하되어, 거세저항성 전립선암 1차에 '(아비라테론아세테이트(Abiraterone acetate) + (프레드니솔론)Prednisolone' 본인부담률을 30%에서 5%로 변경한다"고 전했다.ATRA 계열 차세대 호르몬 약제는 얀센의 얼리다정이다. 얼리다정은 2023년 4월 급여 등재됐다.2025-03-20 15:55:16이탁순
텝메코·테빔브라 급여등재…자이티가 본인부담 축소텝메코정225mg(테포티닙, 한국머크). [데일리팜=이탁순 기자] 텝메코정과 테빔브라주 등 신규 항암제가 4월 1일부로 급여목록에 오른다.또한 자이티가정 등 아비라테론아세테이트 제제는 거세저항성 전립선암 1차 치료에 본인부담율이 축소되면서 환자의 경제적 부담이 크게 줄 전망이다.건강보험심사평가원은 이같은 내용의 암환자에게 처방·투여하는 약제에 따른 공고 개정안을 예고하며 의견조회에 들어갔다. 시행일은 4월 1일자이다.개정안에 따르면 텝메코정225mg(테포티닙, 한국머크)은 MET 엑손 14 결손이 확인된 국소 진행성 또는 전이성 비소세포폐암 환자에 요양급여가 인정된다.심평원은 "신청 야제는 타깃이 명확한 약제로 환자들에게 또 다른 치료 옵션을 제공할 수 있어 진료상 필요한 약제로 판단되는 점 등을 고려해 급여기준을 설정했다"고 전했다.국내에서 MET 돌연변이 항암제에 급여가 적용되는 건 텝메코정이 유일하다. 국내 비소세포폐암 환자 1020명의 진단 결과, 1.9%의 환자가 MET 엑손 14 결손으로 확인되고 있다.텝메코는 확증적 시험군이 추가된 2상 임상시험에서 ORR 51.4%(95% CI, 45.8-57.1), mPFS 11.2개월(95%CI, 9.5-13.8), mOS 19.6개월(95% CI, 16.2-22.9)로 높은 치료효과가 확인됐다. 주요 교과서와 해외 학회 가이드라인에서 이 약을 권고하고 있다. 텝메코의 상한금액은 정당 7만6500원으로 알려졌다. 재정 분담 차원에서 환급형과 총액제한형 RSA(위험분담제) 계약을 맺었다.테빔브라주(티슬렐리주맙, 베이진코리아)는 이전 백금 기반 화학요법 치료 도중 또는 이후에 재발 또는 진행된 절제 불가능, 재발성, 국소진행성 또는 전이성 식도편평세포암에 사용된다. 선행화학요법 또는 수술후보조요법 종료 후 6개월 이내 재발한 경우도 포함된다. 반면 이전 PD-1 inhibitor 등 면역관문억제제 치료를 받지 않은 경우에 급여가 적용된다.이 약은 PD-1저해 기전의 면역항암제로, 4월 급여 등재되면 면역항암제로는 최초로 식도암에 급여가 적용된다. 이 약의 상한금액은 병당 120만6000원이다. 텝메코와 같이 환급형, 총액제한형 RSA 계약을 맺었다.한편 자이티가정 등 아비라테론아세테이트 제제는 거세저항성 전립선암 1차 치료에 본인부담율이 30%에서 5%로 축소된다.아비라테론 제제는 오리지널 자이티가정(한국얀센)뿐만 아니라 한미약품, 에이스파마 등이 공급하는 제네릭약제도 있다.이번 본인부담율 축소는 제네릭 진입과도 관련돼 있다. 심평원은 "'차세대 호르몬 약제(ATRA)'가 전이성 호르몬 감수성 전립선암에 급여되며 해당 요법의 대상자가 점차적으로 줄어들 것으로 예상된다"면서 "제네릭 등재 등 기심의 대비 약가가 인하되어, 거세저항성 전립선암 1차에 '(아비라테론아세테이트(Abiraterone acetate) + (프레드니솔론)Prednisolone' 본인부담률을 30%에서 5%로 변경한다"고 전했다.ATRA 계열 차세대 호르몬 약제는 얀센의 얼리다정이다. 얼리다정은 2023년 4월 급여 등재됐다.2025-03-20 15:55:16이탁순 -
 MSD 희귀암 치료제 '웰리렉' 급여 재도전 성공할까[데일리팜=어윤호 기자] 희귀 항암제 '웰리렉'이 보험급여 등재 재도전에 성공할지 관심이 모아진다.관련업계에 따르면 한국MSD 경구용 저산소증유도인자-2 알파(HIF-2α)억제제 웰리렉(벨주티판)이 오는 3월 건강보험심사평가원 암질환심의위원회에 상정될 전망이다.이 약물은 지난해 4월 급여 신청을 제출, 5월 국민동의청원에 오른 후 5만명 이상의 동의를 얻어냈지만 암질심의 벽을 넘지 못한 바 있다. 웰리렉의 재도전에서 관건은 역시 재정이 될 것으로 판단된다.웰리렉은 폰히펠-린다우(VHL, Von Hippel-Lindau)라는 희귀한 적응증에 대해 2023년 국내 희귀의약품으로 지정, 같은해 5월 최종 승인됐다.구체적인 적응증은 즉각적인 수술이 필요하지는 않으나 VHL 관련 신세포암, 중추신경계 혈관모세포종, 췌장 신경 내분비 종양에 대한 치료가 필요한 VHL 성인 환자의 치료 등이다.이 약은 세포 증식, 혈관신생, 종양 성장과 관련된 HIF-2α 표적 유전자의 전사 및 발현을 감소시키는 기전을 갖고 있다.웰리렉은 신장에 국한된 최소 하나 이상의 측정 가능한 고형종양이 있는 VHL 관련 신세포암 환자 61명을 대상으로 실시된 개방표지 임상시험 Study 004 연구를 통해 유효성을 입증했다.등록된 환자는 CNS 혈관모세포종, 췌장내분비종양을 포함해 다른 VHL 관련 종양이 있었다.임상시험의 주요 효능 평가변수는 독립적인 검토위원회가 RECIST v1.1을 사용해 평가한 방사선 평가로 측정된 객관적반응률(ORR)이었다. 다른 추가 효능 평가변수에는 반응 지속기간(DoR)과 최초 반응 획득까지의 기간(TTR)이 포함됐다.그 결과, 웰리렉은 VHL 관련 신세포암 환자에서 ORR 49%를 보였다. 모든 반응은 부분 반응이었다. 반응 지속기간은 아직 중앙값에 도달하지 않았으며 최소 12개월 이후 반응이 지속된 환자 비율은 56%로 집계됐다. 최초 반응 획득까지의 기간 중앙값은 8개월이었다.또한 VHL 관련 CNS 혈관모세포종이 있는 환자 24명에서 ORR은 63%로 나타났으며, 이 가운데 완전 반응률이 4%, 부분 반응률이 58%였다.웰리렉은 얼마 전 미국에서 신장암 적응증을 추가하기도 했다. 이 약은 PD-1 또는 PD-L1 억제제 및 VEGF-TKI 치료 후 질병이 진행된 진행성 신세포암 환자를 대상으로 진행된 임상 LITESPARK-005를 통해 유효성을 확인했다.그 결과, PD-1 또는 PD-L1 면역관문억제제 및 VEGF 수용체 표적 치료제를 순차적 또는 병용투여 받은 진행성 신세포암 환자에서 에베로리무스 대비 무진행생존율(PFS)을 개선했으며 질병 진행 또는 사망 위험을 25% 감소시켰다.2025-02-28 06:00:01어윤호
MSD 희귀암 치료제 '웰리렉' 급여 재도전 성공할까[데일리팜=어윤호 기자] 희귀 항암제 '웰리렉'이 보험급여 등재 재도전에 성공할지 관심이 모아진다.관련업계에 따르면 한국MSD 경구용 저산소증유도인자-2 알파(HIF-2α)억제제 웰리렉(벨주티판)이 오는 3월 건강보험심사평가원 암질환심의위원회에 상정될 전망이다.이 약물은 지난해 4월 급여 신청을 제출, 5월 국민동의청원에 오른 후 5만명 이상의 동의를 얻어냈지만 암질심의 벽을 넘지 못한 바 있다. 웰리렉의 재도전에서 관건은 역시 재정이 될 것으로 판단된다.웰리렉은 폰히펠-린다우(VHL, Von Hippel-Lindau)라는 희귀한 적응증에 대해 2023년 국내 희귀의약품으로 지정, 같은해 5월 최종 승인됐다.구체적인 적응증은 즉각적인 수술이 필요하지는 않으나 VHL 관련 신세포암, 중추신경계 혈관모세포종, 췌장 신경 내분비 종양에 대한 치료가 필요한 VHL 성인 환자의 치료 등이다.이 약은 세포 증식, 혈관신생, 종양 성장과 관련된 HIF-2α 표적 유전자의 전사 및 발현을 감소시키는 기전을 갖고 있다.웰리렉은 신장에 국한된 최소 하나 이상의 측정 가능한 고형종양이 있는 VHL 관련 신세포암 환자 61명을 대상으로 실시된 개방표지 임상시험 Study 004 연구를 통해 유효성을 입증했다.등록된 환자는 CNS 혈관모세포종, 췌장내분비종양을 포함해 다른 VHL 관련 종양이 있었다.임상시험의 주요 효능 평가변수는 독립적인 검토위원회가 RECIST v1.1을 사용해 평가한 방사선 평가로 측정된 객관적반응률(ORR)이었다. 다른 추가 효능 평가변수에는 반응 지속기간(DoR)과 최초 반응 획득까지의 기간(TTR)이 포함됐다.그 결과, 웰리렉은 VHL 관련 신세포암 환자에서 ORR 49%를 보였다. 모든 반응은 부분 반응이었다. 반응 지속기간은 아직 중앙값에 도달하지 않았으며 최소 12개월 이후 반응이 지속된 환자 비율은 56%로 집계됐다. 최초 반응 획득까지의 기간 중앙값은 8개월이었다.또한 VHL 관련 CNS 혈관모세포종이 있는 환자 24명에서 ORR은 63%로 나타났으며, 이 가운데 완전 반응률이 4%, 부분 반응률이 58%였다.웰리렉은 얼마 전 미국에서 신장암 적응증을 추가하기도 했다. 이 약은 PD-1 또는 PD-L1 억제제 및 VEGF-TKI 치료 후 질병이 진행된 진행성 신세포암 환자를 대상으로 진행된 임상 LITESPARK-005를 통해 유효성을 확인했다.그 결과, PD-1 또는 PD-L1 면역관문억제제 및 VEGF 수용체 표적 치료제를 순차적 또는 병용투여 받은 진행성 신세포암 환자에서 에베로리무스 대비 무진행생존율(PFS)을 개선했으며 질병 진행 또는 사망 위험을 25% 감소시켰다.2025-02-28 06:00:01어윤호 -
 조용준 동구바이오 대표, 큐리언트 이사회 의장 선임[데일리팜=이석준 기자] 조용준 동구바이오제약 대표가 큐리언트 이사회 의장에 선임됐다.큐리언트는 26일 진행된 임시주주총회에서 주요 안건들이 통과됨에 따라 새로운 지배구조에 따른 7인 이사회 구성을 완료했다고 밝혔다.이번 임총에서는 기존 최대 5인이었던 이사회의 정원을 7인으로 확대하는 정관 변경과 더불어 3인의 신규 기타비상무이사 선임이 주요 안건으로 상정됐다.안건들은 주주들의 높은 찬성으로 가결됐으며 이를 통해 큐리언트는 동구바이오제약의 조용준 대표, 이병걸 상무, 그리고 키스톤프라이빗에쿼티의 마영민 대표를 이사회에 새로 맞이했다.주총 직후 열린 이사회에서는 조용준 동구바이오제약 대표가 이사회 의장으로 선임됐다. 동구바이오제약은 지난 5월 큐리언트 최대주주로 올라섰다. 이번 이사회 재편은 양사의 시너지를 극대화하기 위한 중요한 진전으로 해석된다.큐리언트는 현재 결핵치료제 텔라세벡 허가 임상이 호주에서 부룰리궤양 환자 대상으로 진행중이며 항암제 'Q901' 1상은 마무리 단계다. 특히 Q901은 2상 투여 용량이 결정되면 항체약물접합체(ADC), 면역관문억제제 그리고 유방암에서의 항호르몬제 등과의 병용요법 임상이 본격적으로 시작된다.조용준 동구바이오제약 대표는 "이번 이사회 개편을 통해 큐리언트는 동구바이오제약과의 전략적 파트너십을 강화하고 연구개발 성과의 가속화를 위한 새로운 동력을 얻게 될 것"이라고 강조했다.2024-09-27 08:12:45이석준
조용준 동구바이오 대표, 큐리언트 이사회 의장 선임[데일리팜=이석준 기자] 조용준 동구바이오제약 대표가 큐리언트 이사회 의장에 선임됐다.큐리언트는 26일 진행된 임시주주총회에서 주요 안건들이 통과됨에 따라 새로운 지배구조에 따른 7인 이사회 구성을 완료했다고 밝혔다.이번 임총에서는 기존 최대 5인이었던 이사회의 정원을 7인으로 확대하는 정관 변경과 더불어 3인의 신규 기타비상무이사 선임이 주요 안건으로 상정됐다.안건들은 주주들의 높은 찬성으로 가결됐으며 이를 통해 큐리언트는 동구바이오제약의 조용준 대표, 이병걸 상무, 그리고 키스톤프라이빗에쿼티의 마영민 대표를 이사회에 새로 맞이했다.주총 직후 열린 이사회에서는 조용준 동구바이오제약 대표가 이사회 의장으로 선임됐다. 동구바이오제약은 지난 5월 큐리언트 최대주주로 올라섰다. 이번 이사회 재편은 양사의 시너지를 극대화하기 위한 중요한 진전으로 해석된다.큐리언트는 현재 결핵치료제 텔라세벡 허가 임상이 호주에서 부룰리궤양 환자 대상으로 진행중이며 항암제 'Q901' 1상은 마무리 단계다. 특히 Q901은 2상 투여 용량이 결정되면 항체약물접합체(ADC), 면역관문억제제 그리고 유방암에서의 항호르몬제 등과의 병용요법 임상이 본격적으로 시작된다.조용준 동구바이오제약 대표는 "이번 이사회 개편을 통해 큐리언트는 동구바이오제약과의 전략적 파트너십을 강화하고 연구개발 성과의 가속화를 위한 새로운 동력을 얻게 될 것"이라고 강조했다.2024-09-27 08:12:45이석준 -
 차바이오텍, 면역항암제 개발 속도...글로벌 주도권 확보[데일리팜=노병철 기자] 차바이오텍과 차백신연구소가 그룹사 간 오픈이노베이션을 통한 신약 모달리티에 도전하고 있어 주목된다.이들 기업이 새롭게 도전하고 있는 분야는 바로 NK세포와 면역증강제를 기술을 활용한 효과 높은 항암제다.차바이오텍은 차세대 항암제로 꼽히는 NK세포치료제 분야 국내 리딩기업으로 아직 글로벌 승자가 없는 유망 시장에서 주도권을 잡겠다는 전략이다.차바이오텍이 가진 경쟁력은 NK세포 배양 기술이다. 차바이오텍은 혈액에서 NK세포만 선별적으로 증식하는 기술의 특허를 가지고 있다.이 기술을 적용하면 2주 만에 NK세포가 최대 2000배까지 증가되고, 배양 전 5~20%인 활성도는 90% 이상으로 향상돼 높은 항암 효과를 나타낸다.기존 방식으로 NK세포를 증식하려면 혈액에서 NK세포를 분리한 뒤 배양하는 작업이 필요하다.그러나 차바이오텍의 특허 기술은 분리 절차를 생략하고 혈액에서 분리한 림프구를 항체와 사이토카인 등 단백질 성분을 투입하면 바로 NK세포가 선별 증식되는 방식이기 때문에 시간과 비용이 크게 줄어든다.차바이오텍은 이런 특허 기술과 NK세포를 활용해 고형암 면역세포치료제 CBT101을 개발하고 있다.CBT101은 환자 본인의 혈액에서 선천적 면역력에 중요한 역할을 하는 NK세포를 추출한 뒤 체외에서 증식해 제조한 면역세포치료제다. 차바이오텍은 상업화를 위해 임상 1상을 진행했고, 2022년 3월 안전성과 내약성을 확인했다.2024년 6월 정부의 국가신약개발사업 지원대상에 선정돼 임상 2상 진행을 위한 준비에 착수했다.다국가 임상은 동종 NK세포치료제로 할 계획이다.동종 NK세포치료제는 건강한 세포 기증자에게서 얻은 NK세포를 배양해 제조한다. 글로벌 기준에 맞춘 세포주로 경쟁력을 확보할 계획이다.차백신연구소는 독자 개발한 면역증강제 L-pampo™(엘-팜포)를 기반으로 한 면역항암제 CVI-CT-001을 개발 중이다.면역항암제는 기존 항암제의 한계를 극복했지만, 면역세포가 암세포에 침투하지 못하는 저면역원성(콜드 튜머, Cold Tumor) 상태에서는 치료 반응률이 30%에 불과하다.차백신연구소의 L-pampo를 종양에 투여하면 암세포를 죽여 암항원을 노출시키고, T세포를 비롯한 면역세포를 활성화한다.이 과정에서 종양미세환경은 저면역원성에서 고면역원성(핫 튜머, Hot Tumor) 상태로 바뀌며 면역관문억제제 효과가 높아진다.전임상연구에서 CVI-CT-001의 효과가 확인됐다. CVI-CT-001을 면역관문억제제(ICI)와 병용투여한 동물모델은 60일 이상 생존했는데, 이는 면역관문억제제만 투여한 개체의 47일 생존보다 더 오래 항암효과를 유지한 결과다.차백신연구소는 L-pampo™와 면역관문억제제의 병용요법에 대해 글로벌 기술이전 및 공동연구를 협의 중이다.mRNA 전달체 리포플렉스(Lipoplex)를 활용한 항암백신도 개발 중이다.리포플렉스는 리포좀(Liposome) 기반의 mRNA 전달체로, 차백신연구소가 독자 개발한 TLR2 기반의 면역증강제를 첨가했다.차백신연구소는 mRNA-리포플렉스 백신 제형을 동물에 주입했을 때 mRNA를 단독으로 투입했을 때보다 체액성 면역반응은 50배, 세포성 면역반응은 15배 증가한 것을 확인했다.피부암을 이식한 마우스 모델에 mRNA-리포플렉스 백신을 투여했을 때 mRNA 단독 투여보다 종양 형성을 막아 21일 차에서 mRNA를 단독 투여한 대조군 대비 종양 성장이 41% 억제됐다.또 LNP 사용 시 나타나는 간독성이나 다른 부작용도 관찰되지 않았다. 차백신연구는 이러한 연구결과를 2023년 독일 베를린에서 열린 제11회 국제 mRNA 헬스 컨퍼런스’에 발표했다. 에스티팜, 한국파스퇴르연구소 등과 백신과 치료제 개발을 위해 협력하고 있다.한편 세계보건기구(WHO) 산하 국제암연구소(IARC)의 보고서에 따르면 2050년 암 발생 건수는 2022년 2000만건보다 77% 증가한 3500만건 이상이 될 전망이다.전 세계 암 사망자는 2022년 970만명에서 2050년 1850만명으로 늘어날 것으로 예측된다.암 발병 및 사망이 증가하면서, 여러 제약∙바이오 기업이 항암제 개발에 박차를 가하고 있다. 우리나라의 경우, 2023년 기준 신약 파이프라인 중 항암제가 35%인 578개를 차지할 정도로 경쟁이 치열하다.2024-09-27 06:00:34노병철
차바이오텍, 면역항암제 개발 속도...글로벌 주도권 확보[데일리팜=노병철 기자] 차바이오텍과 차백신연구소가 그룹사 간 오픈이노베이션을 통한 신약 모달리티에 도전하고 있어 주목된다.이들 기업이 새롭게 도전하고 있는 분야는 바로 NK세포와 면역증강제를 기술을 활용한 효과 높은 항암제다.차바이오텍은 차세대 항암제로 꼽히는 NK세포치료제 분야 국내 리딩기업으로 아직 글로벌 승자가 없는 유망 시장에서 주도권을 잡겠다는 전략이다.차바이오텍이 가진 경쟁력은 NK세포 배양 기술이다. 차바이오텍은 혈액에서 NK세포만 선별적으로 증식하는 기술의 특허를 가지고 있다.이 기술을 적용하면 2주 만에 NK세포가 최대 2000배까지 증가되고, 배양 전 5~20%인 활성도는 90% 이상으로 향상돼 높은 항암 효과를 나타낸다.기존 방식으로 NK세포를 증식하려면 혈액에서 NK세포를 분리한 뒤 배양하는 작업이 필요하다.그러나 차바이오텍의 특허 기술은 분리 절차를 생략하고 혈액에서 분리한 림프구를 항체와 사이토카인 등 단백질 성분을 투입하면 바로 NK세포가 선별 증식되는 방식이기 때문에 시간과 비용이 크게 줄어든다.차바이오텍은 이런 특허 기술과 NK세포를 활용해 고형암 면역세포치료제 CBT101을 개발하고 있다.CBT101은 환자 본인의 혈액에서 선천적 면역력에 중요한 역할을 하는 NK세포를 추출한 뒤 체외에서 증식해 제조한 면역세포치료제다. 차바이오텍은 상업화를 위해 임상 1상을 진행했고, 2022년 3월 안전성과 내약성을 확인했다.2024년 6월 정부의 국가신약개발사업 지원대상에 선정돼 임상 2상 진행을 위한 준비에 착수했다.다국가 임상은 동종 NK세포치료제로 할 계획이다.동종 NK세포치료제는 건강한 세포 기증자에게서 얻은 NK세포를 배양해 제조한다. 글로벌 기준에 맞춘 세포주로 경쟁력을 확보할 계획이다.차백신연구소는 독자 개발한 면역증강제 L-pampo™(엘-팜포)를 기반으로 한 면역항암제 CVI-CT-001을 개발 중이다.면역항암제는 기존 항암제의 한계를 극복했지만, 면역세포가 암세포에 침투하지 못하는 저면역원성(콜드 튜머, Cold Tumor) 상태에서는 치료 반응률이 30%에 불과하다.차백신연구소의 L-pampo를 종양에 투여하면 암세포를 죽여 암항원을 노출시키고, T세포를 비롯한 면역세포를 활성화한다.이 과정에서 종양미세환경은 저면역원성에서 고면역원성(핫 튜머, Hot Tumor) 상태로 바뀌며 면역관문억제제 효과가 높아진다.전임상연구에서 CVI-CT-001의 효과가 확인됐다. CVI-CT-001을 면역관문억제제(ICI)와 병용투여한 동물모델은 60일 이상 생존했는데, 이는 면역관문억제제만 투여한 개체의 47일 생존보다 더 오래 항암효과를 유지한 결과다.차백신연구소는 L-pampo™와 면역관문억제제의 병용요법에 대해 글로벌 기술이전 및 공동연구를 협의 중이다.mRNA 전달체 리포플렉스(Lipoplex)를 활용한 항암백신도 개발 중이다.리포플렉스는 리포좀(Liposome) 기반의 mRNA 전달체로, 차백신연구소가 독자 개발한 TLR2 기반의 면역증강제를 첨가했다.차백신연구소는 mRNA-리포플렉스 백신 제형을 동물에 주입했을 때 mRNA를 단독으로 투입했을 때보다 체액성 면역반응은 50배, 세포성 면역반응은 15배 증가한 것을 확인했다.피부암을 이식한 마우스 모델에 mRNA-리포플렉스 백신을 투여했을 때 mRNA 단독 투여보다 종양 형성을 막아 21일 차에서 mRNA를 단독 투여한 대조군 대비 종양 성장이 41% 억제됐다.또 LNP 사용 시 나타나는 간독성이나 다른 부작용도 관찰되지 않았다. 차백신연구는 이러한 연구결과를 2023년 독일 베를린에서 열린 제11회 국제 mRNA 헬스 컨퍼런스’에 발표했다. 에스티팜, 한국파스퇴르연구소 등과 백신과 치료제 개발을 위해 협력하고 있다.한편 세계보건기구(WHO) 산하 국제암연구소(IARC)의 보고서에 따르면 2050년 암 발생 건수는 2022년 2000만건보다 77% 증가한 3500만건 이상이 될 전망이다.전 세계 암 사망자는 2022년 970만명에서 2050년 1850만명으로 늘어날 것으로 예측된다.암 발병 및 사망이 증가하면서, 여러 제약∙바이오 기업이 항암제 개발에 박차를 가하고 있다. 우리나라의 경우, 2023년 기준 신약 파이프라인 중 항암제가 35%인 578개를 차지할 정도로 경쟁이 치열하다.2024-09-27 06:00:34노병철 -
 희귀 항암제 '웰리렉' 급여 첫 관문서 좌절...다음 행보는[데일리팜=어윤호 기자] 희귀 항암제 '웰리렉'의 보험급여권 진입이 난항을 겪고 있다.관련업계에 따르면 한국MSD는 최근 경구용 저산소증유도인자-2 알파(HIF-2α)억제제 웰리렉(벨주티판)의 지난달 암질환심의위원회 실패 후 재신청을 준비 중이다.이 약물은 지난 4월 급여 신청을 제출, 5월 국민동의청원에 오른 후 5만명 이상의 동의를 얻어냈지만 암질심의 벽을 넘지 못했다. 관건은 역시 재정이 될 것으로 판단된다.웰리렉은 폰히펠-린다우(VHL, Von Hippel-Lindau)라는 희귀한 적응증에 대해 지난해 국내 희귀의약품으로 지정, 같은 해 5월 최종 승인됐다.구체적인 적응증은 즉각적인 수술이 필요하지는 않으나 VHL 관련 신세포암, 중추신경계 혈관모세포종, 췌장 신경 내분비 종양에 대한 치료가 필요한 VHL 성인 환자의 치료 등이다.이 약은 세포 증식, 혈관신생, 종양 성장과 관련된 HIF-2α 표적 유전자의 전사 및 발현을 감소시키는 기전을 갖고 있다.웰리렉은 신장에 국한된 최소 하나 이상의 측정 가능한 고형종양이 있는 VHL 관련 신세포암 환자 61명을 대상으로 실시된 개방표지 임상시험 Study 004 연구를 통해 유효성을 입증했다.등록된 환자는 CNS 혈관모세포종, 췌장내분비종양을 포함해 다른 VHL 관련 종양이 있었다.임상시험의 주요 효능 평가변수는 독립적인 검토위원회가 RECIST v1.1을 사용해 평가한 방사선 평가로 측정된 객관적반응률(ORR)이었다. 다른 추가 효능 평가변수에는 반응 지속기간(DoR)과 최초 반응 획득까지의 기간(TTR)이 포함됐다.그 결과, 웰리렉은 VHL 관련 신세포암 환자에서 ORR 49%를 보였다. 모든 반응은 부분 반응이었다. 반응 지속기간은 아직 중앙값에 도달하지 않았으며 최소 12개월 이후 반응이 지속된 환자 비율은 56%로 집계됐다. 최초 반응 획득까지의 기간 중앙값은 8개월이었다.또한 VHL 관련 CNS 혈관모세포종이 있는 환자 24명에서 ORR은 63%로 나타났으며, 이 가운데 완전 반응률이 4%, 부분 반응률이 58%였다.웰리렉은 얼마 전 미국에서 신장암 적응증을 추가하기도 했다. 이 약은 PD-1 또는 PD-L1 억제제 및 VEGF-TKI 치료 후 질병이 진행된 진행성 신세포암 환자를 대상으로 진행된 임상 LITESPARK-005를 통해 유효성을 확인했다.그 결과, PD-1 또는 PD-L1 면역관문억제제 및 VEGF 수용체 표적 치료제를 순차적 또는 병용투여 받은 진행성 신세포암 환자에서 에베로리무스 대비 무진행생존율(PFS)을 개선했으며 질병 진행 또는 사망 위험을 25% 감소시켰다.2024-09-19 06:00:08어윤호
희귀 항암제 '웰리렉' 급여 첫 관문서 좌절...다음 행보는[데일리팜=어윤호 기자] 희귀 항암제 '웰리렉'의 보험급여권 진입이 난항을 겪고 있다.관련업계에 따르면 한국MSD는 최근 경구용 저산소증유도인자-2 알파(HIF-2α)억제제 웰리렉(벨주티판)의 지난달 암질환심의위원회 실패 후 재신청을 준비 중이다.이 약물은 지난 4월 급여 신청을 제출, 5월 국민동의청원에 오른 후 5만명 이상의 동의를 얻어냈지만 암질심의 벽을 넘지 못했다. 관건은 역시 재정이 될 것으로 판단된다.웰리렉은 폰히펠-린다우(VHL, Von Hippel-Lindau)라는 희귀한 적응증에 대해 지난해 국내 희귀의약품으로 지정, 같은 해 5월 최종 승인됐다.구체적인 적응증은 즉각적인 수술이 필요하지는 않으나 VHL 관련 신세포암, 중추신경계 혈관모세포종, 췌장 신경 내분비 종양에 대한 치료가 필요한 VHL 성인 환자의 치료 등이다.이 약은 세포 증식, 혈관신생, 종양 성장과 관련된 HIF-2α 표적 유전자의 전사 및 발현을 감소시키는 기전을 갖고 있다.웰리렉은 신장에 국한된 최소 하나 이상의 측정 가능한 고형종양이 있는 VHL 관련 신세포암 환자 61명을 대상으로 실시된 개방표지 임상시험 Study 004 연구를 통해 유효성을 입증했다.등록된 환자는 CNS 혈관모세포종, 췌장내분비종양을 포함해 다른 VHL 관련 종양이 있었다.임상시험의 주요 효능 평가변수는 독립적인 검토위원회가 RECIST v1.1을 사용해 평가한 방사선 평가로 측정된 객관적반응률(ORR)이었다. 다른 추가 효능 평가변수에는 반응 지속기간(DoR)과 최초 반응 획득까지의 기간(TTR)이 포함됐다.그 결과, 웰리렉은 VHL 관련 신세포암 환자에서 ORR 49%를 보였다. 모든 반응은 부분 반응이었다. 반응 지속기간은 아직 중앙값에 도달하지 않았으며 최소 12개월 이후 반응이 지속된 환자 비율은 56%로 집계됐다. 최초 반응 획득까지의 기간 중앙값은 8개월이었다.또한 VHL 관련 CNS 혈관모세포종이 있는 환자 24명에서 ORR은 63%로 나타났으며, 이 가운데 완전 반응률이 4%, 부분 반응률이 58%였다.웰리렉은 얼마 전 미국에서 신장암 적응증을 추가하기도 했다. 이 약은 PD-1 또는 PD-L1 억제제 및 VEGF-TKI 치료 후 질병이 진행된 진행성 신세포암 환자를 대상으로 진행된 임상 LITESPARK-005를 통해 유효성을 확인했다.그 결과, PD-1 또는 PD-L1 면역관문억제제 및 VEGF 수용체 표적 치료제를 순차적 또는 병용투여 받은 진행성 신세포암 환자에서 에베로리무스 대비 무진행생존율(PFS)을 개선했으며 질병 진행 또는 사망 위험을 25% 감소시켰다.2024-09-19 06:00:08어윤호
오늘의 TOP 10
- 1상장 바이오 추정 순이익 '껑충'...비교군 한미약품 '최다'
- 2고환율에 복잡한 약가인하...사업계획 엄두 못내는 제약사들
- 3완강한 약무정책과장..."플랫폼 도매 허용 동의 힘들어"
- 4"근무약사 연봉 1억"...창고형약국, 파격 급여 제시
- 5플랫폼 도매금지법 간담회, 편파운영 논란…"복지부 협박하나"
- 6'마운자로', 당뇨병 급여 적정성 확인…약가협상 시험대
- 7"웰컴"...K-약국, 해외관광객 소비건수 1년새 67% 증가
- 8[2025 결산] 급여재평가 희비...건보재정 적자터널 진입
- 9사노피 '듀피젠트', 아토피피부염 넘어 천식 공략 눈앞
- 10"대통령, 중대사고 엄벌 주문…제약업계도 대비해야"
-
순위상품명횟수
-
1타이레놀정500mg(10정)30,426
-
2판콜에스내복액16,732
-
3텐텐츄정(10정)13,671
-
4까스활명수큐액12,867
-
5판피린큐액12,851












![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
