총 22건
-
 세계 첫 항체 무관 혈우병 A·B 치료제 '피투시란'큐피틀리아(Qfitlia, 성분명 피투시란, Fitusiran, 사노피)는 GalXC 기술 플랫폼을 기반으로 개발된 항트롬빈(antithrombin)을 표적으로 하는 소간섭 리보핵산(small interfering RNA, siRNA) 치료제다.이 약제는 2024년 유럽의약청(EMA) 에서, 이어 올해 3월 미국 식품의약국(FDA) 에서 제VIII인자 또는 제IX인자 억제인자(inhibitor)의 유무와 관계없이, 12세 이상 성인 및 소아 혈우병 A 또는 B 환자에서 출혈 에피소드의 발생을 예방하거나 빈도를 감소시키기 위한 정기적 예방요법(routine prophylaxis)에 ‘두 달에 한번 피하주사’로 승인되었다. 국내에서는 올해 5월 희귀의약품(Orphan drug) 으로 지정되었다.혈우병(hemophilia)은 X염색체 연관 열성 유전질환으로, 제Ⅷ인자(FVIII) 또는 제Ⅸ인자(FIX) 의 결핍으로 인해 혈액응고 연쇄반응(coagulation cascade) 이 정상적으로 진행되지 못하며, 그 결과 트롬빈(thrombin) 생성 부족으로 지혈(hemostasis) 이 저하된다. 이러한 병태생리적 이상은 반복적인 출혈, 특히 관절 출혈을 초래하여 만성 관절병증(chronic arthropathy) 및 삶의 질 저하로 이어진다.기존의 표준 치료는 응고인자제제(clotting factor concentrate, CFC) 의 정맥 내 투여를 통한 인자 보충요법(replacement therapy) 이었다. 그러나 이 방식은 정맥 투여의 불편성, 반복적 투여 부담, 그리고 항체(억제인자, inhibitor) 형성으로 인한 치료 저항성이라는 한계를 지닌다.이에 따라 최근에는 비(非)응고인자 기반 치료(non-factor therapy) 의 개발이 활발히 이루어지고 있으며, 그중에서도 RNA 간섭(RNA interference, RNAi) 기술을 이용한 피투시란(Fitusiran) 은 새로운 치료 옵션으로 주목 받고 있다.피투시란은 간세포 내에서 항트롬빈(antithrombin, AT) 합성을 억제하도록 설계된 siRNA 기반 치료제로, 내인성 응고 조절 인자의 발현을 조절함으로써 응고 균형(hemostatic balance) 을 회복시키는 새로운 접근법을 제시한다.피투시란의 승인은 다국가, 무작위배정, 대조, 3상 임상시험들로 구성된 ATLAS 임상 프로그램의 결과를 근거로 하였다.이 프로그램에는 ATLAS-A/B, ATLAS-INH, 그리고 ATLAS-PPX 연구가 포함되며, 각각 혈우병 A 또는 B 환자 중 인자 억제인자의 유무, 그리고 기존 예방요법(prophylaxis) 사용 여부에 따라 구분되었다.ATLAS-A/B 연구는 억제인자가 없는(non-inhibitor) 혈우병 A 또는 B 환자를 대상으로, ATLAS-INH 연구는 억제인자가 존재하는(inhibitor-positive) 환자를 대상으로 수행되었다. ATLAS-PPX 연구는 기존 예방요법을 받고 있던 환자에서 피투시란으로 전환했을 때의 출혈률 변화를 평가하였다.이들 연구에서 피투시란은 월 1회 피하주사(subcutaneous injection) 투여만으로도 연간 출혈률(annualized bleeding rate, ABR)을 기존 치료 대비 약 90% 이상 유의하게 감소시켰으며, 절반 이상의 환자에서 무출혈(ABR = 0)이 관찰되었다. 또한 억제인자 유무와 관계없이 일관된 출혈 억제 효과가 확인되었다.혈우병이란 무엇인가?혈우병(hemophilia)은 그리스어 ‘hemo(피)’와 ‘philia(사랑하다)’에서 유래한 용어로, 1828년 Schönlein에 의해 Hämophilie라 명명됐다. 19세기 말 유럽 왕실 내 근친혼으로 인해 영국, 스페인, 독일, 러시아 등 여러 나라에서 다수의 환자가 발생하면서 ‘왕실병(The Royal Disease)’이라는 별칭을 얻었다.혈우병은 혈액응고인자의 결핍으로 인해 발생하는 대표적인 선천성 출혈성 질환이다. 제VIII응고인자(FVIII)의 결핍은 혈우병 A로, 전체 환자의 약 80~85%를 차지하며 ‘고전적 혈우병(classic hemophilia)’이라 불린다. 제IX응고인자(FIX)의 결핍은 혈우병 B로 약 15%를 차지하며, 최초 환자의 이름을 따 ‘크리스마스병(Christmas disease)’으로도 알려져 있다. 제XI응고인자(FXI)의 결핍은 혈우병 C로 상대적으로 드물게 발생한다.혈우병 A와 B는 X 염색체 열성 유전 양식을 가지므로 주로 남성에서 발병하며, 여성은 보인자로 존재하거나 드물게 태아기에 사망하기도 한다. 반면 혈우병 C는 4번 염색체 이상에 기인하므로 성별에 관계없이 발생할 수 있으며, 일부 환자에서는 가족력 없이 자연 발생적 유전자 변이에 의해 발현되기도 한다.혈우병과 유사한 질환으로는 폰빌레브란트병(von Willebrand disease, vWD)이 있다. 이는 응고인자 VIII과 결합하는 폰빌레브란트인자(vWF)의 결핍으로 인해 혈우병과 유사한 임상 양상을 보인다.이외에도 프로트롬빈(II), 피브리노겐(I), V, VII, X, XII, XIII 응고인자의 결핍으로 인한 선천성 응고장애가 보고되어 있으나, 이러한 질환들은 혈우병의 범주에는 포함되지 않는다.혈액응고 과정은 어떻게 일어나는가?혈액응고는 인체의 항상성을 유지하기 위한 필수적인 생리적 방어기전으로, 외상이나 혈관 손상 시 과도한 출혈을 방지하는 역할을 한다. 이 과정은 혈관수축, 혈소판 기능, 그리고 혈액응고인자의 연속적인 활성화로 이루어지는 응고 연쇄(cascade)로 설명되며, 궁극적으로 안정적인 피브린 혈전(fibrin clot)을 형성한다.혈액응고인자(Coagulation factors)는 주로 간에서 합성되는 단백질로, 로마 숫자로 표기된 I번부터 XIII번까지의 인자가 알려져 있다. 이들은 각각 특정 효소 활성 또는 보조인자로 작용하면서 정교하고 단계적인 반응을 매개한다. 주요 응고인자로는 피브리노겐(Factor I), 프로트롬빈(Factor II), 그리고 프로트롬빈 복합체를 구성하는 V, VII, IX, X, XI, XII 인자, 마지막으로 XIII 인자 등이 있다. 응고 연쇄는 크게 내인성 경로(intrinsic pathway), 외인성 경로(extrinsic pathway), 그리고 두 경로가 합류하는 공통 경로(common pathway)로 구성된다.내인성 경로는 Factor XII의 활성화를 시작으로 XI, IX, VIII 인자가 순차적으로 활성화되며, 외인성 경로는 조직인자(tissue factor, TF)와 Factor VII의 상호작용을 통해 개시된다.두 경로는 Factor X의 활성화 단계에서 공통 경로로 수렴하며, 활성화된 Factor X는 Factor V와 결합하여 프로트롬비나제(prothrombinase) 복합체를 형성한다. 이 복합체는 프로트롬빈(Factor II)을 트롬빈(thrombin)으로 전환시키고, 생성된 트롬빈은 피브리노겐(Factor I)을 불용성 피브린(fibrin)으로 전환시켜 최종적으로 혈전을 완성한다.또한 트롬빈은 Factor V, VIII, XI 등을 다시 활성화시키는 양성 되먹임(positive feedback) 작용을 통해 응고 반응을 증폭시키며, Factor XIII을 활성화시켜 피브린 가교결합(fibrin cross-linking)을 형성함으로써 혈전의 안정성을 더욱 높인다.이러한 정교한 연쇄 반응은 항응고 단백질(antithrombin, protein C/S system 등)과 섬유소 용해(fibrinolysis) 기전 간의 정밀한 균형 속에서 조절된다. 이 균형이 깨질 경우 출혈성 질환이나 혈전성 질환으로 이어질 수 있다.항트롬빈(Antithrombin, AT, heparin cofactor I)은 어떤 물질인가?항트롬빈(AT)은 혈액응고 조절에서 가장 중요한 내인성 항응고인자로, 전체 생리적 응고 억제 작용의 약 70~80%를 담당하는 핵심 단백질이다. AT는 혈장에 존재하는 세린 단백질분해효소 억제제(serpin) 계열의 당단백질로, 주된 표적은 트롬빈(thrombin)이지만, Factor Xa, IXa, XIa, XIIa 및 칼리크레인(kallikrein) 등 다양한 혈액응고인자를 동시에 억제함으로써 응고 연쇄(cascade) 전반의 균형 유지에 기여한다.The Coagulation Cascade(출처: Ann Pharmacother . 2016 Sep;50(9):758-67). AT는 트롬빈의 활성 중심부에 위치한 세린(serine) 잔기와 1:1 비율로 결합하여 불활성 복합체를 형성함으로써 트롬빈 활성을 차단한다. 이를 통해 소규모 응고 반응이나 불필요한 혈전 형성을 신속히 억제하며, 정상적인 생리 상태에서 과도한 혈액응고를 방지하는 핵심 역할을 수행한다.그러나 대규모 혈관 손상이나 파종성 혈관내응고(Disseminated intravascular coagulation, DIC)와 같이 트롬빈 생성이 폭발적으로 증가하는 상황에서는 AT의 억제 능력이 상대적으로 부족해져, 생리적 항응고 메커니즘만으로는 병적 혈전 형성을 완전히 제어하기 어렵다.AT의 항응고 활성이 가장 강력하게 발휘되는 조건은 헤파린(heparin)의 존재 하에서이다. 헤파린은 AT에 결합하여 구조적 변화를 유도하고, AT와 트롬빈 및 Factor Xa 간의 결합 친화도를 수백 배 이상 증폭시킨다.이로 인해 헤파린은 AT의 촉매제(cofactor) 역할을 하며, 임상적으로 항응고 효과를 발휘하는 주요 기전이 바로 AT 매개 억제 반응이다. 이러한 이유로 AT 결핍 환자에서는 헤파린의 항응고 효과가 현저히 감소하며, 이는 선천성 또는 후천성 AT 결핍에서 혈전성 질환 발생 위험이 증가하는 중요한 근거가 된다.AT는 간에서 합성되며 혈중 농도는 약 0.15mg/mL로 유지되고, 정상 활성도는 80~120% 범위 내에 있다. 선천성 AT 결핍은 드문 질환이지만 정맥혈전증과 폐색전증 발생의 중요한 위험 요인으로 알려져 있으며, 후천성 결핍은 간질환, 신증후군, DIC, 항응고제 치료 등 다양한 상황에서 관찰된다. AT 농도의 감소는 항응고 균형을 무너뜨려 과도한 혈전 형성을 유발하므로, 임상적으로 AT 농축제제 보충 또는 헤파린·직접 트롬빈 억제제와 같은 항응고 요법을 병행하는 치료 전략이 고려된다.이처럼 AT는 단순한 혈액응고인자 억제 단백질을 넘어, 혈액응고와 항응고, 그리고 섬유소 용해(fibrinolysis) 시스템 사이의 미세한 균형을 유지하는 핵심 조절인자로서, 혈전성 질환의 병태생리 이해와 새로운 항응고 치료제 개발에 있어 중요한 연구 대상이 되고 있다.혈우병 A 치료제에는 어떤 약제가 있는가?1. 응고인자 보충요법(Factor Replacement Therapy) 혈우병 A의 전통적인 치료는 부족한 제Ⅷ인자(FVIII)를 직접 보충하는 방식이다. 초기에는 혈액 유래 FVIII 제제가 사용되었으나, 감염 위험 등 안전성 문제가 제기되면서 현재는 재조합 FVIII(rFVIII)이 표준으로 자리잡았다. 또한 최근에는 반감기를 연장한 FVIII 제제들이 개발되어 투여 빈도를 줄이고 환자 순응도를 높이는 데 기여하고 있다.1) 표준 반감기(Standard half-life, SHL) FVIII 제제 표준 반감기 제제는 혈액 유래 FVIII와 재조합 FVIII로 나눌 수 있다. 혈액 유래 제제는 감염 위험 관리가 필요하지만 여전히 일부에서 사용되고 있으며, 재조합 FVIII로 애드베이트(AdvateⓇ, 코지네이트 에프에스(Kogenate FSⓇ) 등은 안전성 측면에서 더 선호된다.2) 반감기 연장형(Extended half-life, EHL) FVIII 제제 반감기 연장형 제제는 투여 간격을 늘리기 위해 Fc-fusion(엘록테이트, EloctateⓇ), PEGylation(애디노베이트, AdynovateⓇ, 지비, JiviⓇ) 등 다양한 기술이 적용되었다. 이러한 약제들은 환자의 주사 횟수를 줄여 장기적인 치료 순응도를 개선하는 장점이 있다.3) VWF-independent EHL(VWF 비의존성 반감기 연장형) FVIII 제제 VWF 비의존성 반감기 연장형 제제인 알투비오(AltuviiioⓇ)는 주 1회 주사로 FVIII 활성을 더 오래 유지할 수 있도록 설계된 최신형 지속형 치료제(high sustained factor, HSF)로 2023년 미 FDA에서 승인되었고 국내에서는 진행중이다,2. 억제인자 환자 치료(Treatment for Patients with Inhibitors) 혈우병 A 환자의 약 20~30%는 치료 과정에서 FVIII에 대한 억제항체를 형성하게 되며, 이 경우 기존의 FVIII 보충요법은 효과가 제한적이다. 억제인자 환자의 치료에는 크게 두 가지 접근법이 있다.첫째, 우회제제(bypassing agents, BPA)를 사용하는 방법이다. 활성화 프로트롬빈 복합체(aPCC, 훼이바, FEIBAⓇ)와 재조합 활성 VIIa(rFVIIa, 노보세븐, NovoSevenⓇ)는 응고경로를 우회적으로 활성화하여 지혈 효과를 발휘하지만, 지혈 반응의 변동성과 혈전 위험이라는 한계가 존재한다.둘째, 에미시주맙(Emicizumab, HemlibraⓇ)는 FIXa와 FX를 연결하여 FVIII의 기능을 모방하는 이중특이성 항체로, 억제인자 환자뿐 아니라 비(非)억제인자 환자에서도 예방요법으로 사용 가능하다. 피하 주사로 1주~4주 간격 투여가 가능하여 투여 편의성이 획기적으로 개선되었다.3. 대체 인자제제(Replacement therapy) 재조합 돼지 유래 FVIII(r-pFVIII)인 오비주르(Obizur®, Susoctocog alfa)는 2014년 미 FDA, 2015년 EMA 그리고 2023년 국내에서 ‘성인 후천성 혈우병 A(Acquired Haemophilia A, AHA) 환자의 출혈 에피소드 치료’에 승인되었다. 후천성 혈우병 A는 선천성 혈우병과 다르게, 정상 혈액응고인자 VIII(FVIII) 수준을 가지고 있지만, 이에 대해 자가면역 항체(중화 항체)가 생겨 혈액 응고 기능이 저해되어 출혈 위험이 커지는 인구 100만 명당 약 1명꼴로 발생하는 초희귀 자가면역 응고질환이다.4. 비응고인자 기반 치료(Non-factor Therapy) 최근 혈우병 A 치료에서 가장 주목받는 변화는 FVIII를 직접 보충하지 않고, 다른 경로를 통해 응고 균형을 회복하는 비응고인자 기반 치료이다. 대표적인 약제가 에미시주맙(Emicizumab, HemlibraⓇ)으로, FIXa와 FX을 연결하여 FVIII의 보조인자 기능을 모방하는 이중특이성 항체이다. 피하 주사로 주 1회, 격주, 또는 4주 간격 투여가 가능해 환자의 치료 편의성이 획기적으로 개선되었다.이외에도 피투시란(Fitusiran)과 콘시주맙(Concizumab, Alhemo®)가 있다. 피투시란은 RNA 간섭(RNAi) 기술을 이용하여 간세포에서 항트롬빈 합성을 억제함으로써 응고 활성을 높인다. 월 1회 피하 주사가 가능하지만, 혈전 및 간독성 발생 위험으로 인해 항트롬빈 활성(15–35%)을 유지하는 개별화 용량조절(AT-DR)이 필요하다. 콘시주맙은 조직인자경로억제인자(TFPI)를 차단하여 내인성 응고를 촉진하는 약제이다.5. 유전자 치료(Gene Therapy) 혈우병 A에서 유전자 치료는 단회 정맥투여를 통해 간세포에 FVIII 유전자를 도입하여 장기간 발현을 유도하는 새로운 전략이다. 대표적인 약제가 록타비안(RoctavianⓇ, Valoctocogene roxaparvovec)으로, AAV5 벡터를 이용해 개발되었으며 2022년 유럽, 2023년 미국 FDA의 승인을 받았다.단일 투여로 FVIII 발현을 장기간 유지할 수 있어 치료 패러다임의 변화를 예고했으나, 발현 지속 기간의 불확실성, 간효소 상승, 재투여 불가 등의 문제점이 여전히 남아 있다.혈우병 B 치료제에는 어떤 약제가 있는가?1. 응고인자 보충요법(Factor IX Replacement Therapy) 혈우병 B의 가장 기본적인 치료는 부족한 제Ⅸ인자(FIX)를 직접 보충하는 방식이다. 과거에는 혈액 유래 제제가 널리 사용되었으나, 감염 위험 문제로 현재는 재조합 FIX(rFIX) 제제가 주로 사용된다. 여기에 더해 반감기를 연장한 제제들이 개발되면서 투여 간격이 길어지고 환자의 치료 순응도가 크게 향상되었다.1) 표준 반감기(Standard half-life, SHL) FIX 제제 표준 반감기 FIX 제제는 투여 후 약 18~24시간의 반감기를 가지며, 주 2~3회 정맥 주사가 필요하다. 혈액 유래 FIX 제제는 여전히 일부에서 사용되지만, 바이러스 감염에 대한 안전성 우려가 있었다. 이를 보완하기 위해 개발된 재조합 FIX 제제인 베네픽스(BeneFIXⓇ, Nonacog alfa)는 안전성이 확보되어 현재 임상에서 가장 널리 사용되고 있다.2) 반감기 연장(Extended half-life, EHL) FIX 제제 반감기 연장 제제는 기존 표준 제제보다 3~5배 긴 반감기를 가지며, 1~2주 간격으로 투여가 가능하다. 이들 약제에는 Fc-fusion 단백을 이용한 알프로릭스(Alprolix(Ⓡ, Eftrenonacog alfa), albumin-fusion 기술이 적용된 아이델비온(IdelvionⓇ Albutrepenonacog alfa) 등이 포함된다. 이러한 제제들은 주사 횟수를 줄여 환자의 삶의 질과 치료 순응도를 높이는 중요한 진보로 평가된다.2. 억제인자 환자 치료(Treatment for Patients with Inhibitors) 혈우병 B 환자에서 억제인자 발생은 상대적으로 드물지만, 일단 형성되면 치료가 매우 어렵다. 억제인자가 형성된 경우 기존 FIX 제제의 효과가 소실되므로 우회제제(bypassing agents)가 사용된다.활성화 프로트롬빈 복합체(aPCC, 훼이바, FEIBAⓇ)와 재조합 활성 VIIa(rFVIIa, 노보세븐, NovoSevenⓇ)가 대표적이다. 그러나 혈우병 A와 달리 에미시주맙은 FVIII 기능을 모방하는 기전이기 때문에 혈우병 B 환자에게는 효과가 없다. 따라서 억제인자 환자의 치료는 여전히 제한적이며, 새로운 치료 전략이 필요한 영역이다.3. 비응고인자 기반 치료(Non-factor Therapy) 혈우병 B에서도 비응고인자 기반 치료가 적용될 수 있다. 이들 약제는 특정 응고인자를 보충하지 않고 응고 균형 자체를 조절하는 기전을 갖는다. 대표적으로 RNA 간섭 기반의 피투시란(Fitusiran)은 간세포에서 항트롬빈 합성을 억제하여 응고 활성을 증가시키며, 혈우병 A와 B 모두에 승인되었다.또한 항 TFPI 항체인 콘시주맙(Concizumab, Alhemo®) 역시 혈우병 A와 B 모두에 적용 가능하며, 내인성 응고경로를 촉진하여 출혈을 억제한다. 이처럼 비응고인자 기반 치료는 억제인자 보유 여부와 관계없이 사용할 수 있는 장점이 있어, 혈우병 B 환자에서도 중요한 치료 대안으로 부상하고 있다.4. 유전자 치료(Gene Therapy) 혈우병 B는 유전자 치료 분야에서 가장 먼저 성과를 낸 질환 중 하나이다. FIX 유전자의 크기가 FVIII보다 작아 AAV 벡터 전달이 용이하기 때문에, 임상개발이 상대적으로 앞서 진행되었다.대표적인 약제는 헴제닉스(HemgenixⓇ, Etranacogene dezaparvovec)으로, 2022년 미국 FDA와 2023년 유럽 EMA에서 세계 최초로 혈우병 유전자 치료제로 승인되었다. 단회 정맥투여만으로 간세포에서 FIX 발현이 장기간 유지될 수 있으며, 환자의 치료 부담을 획기적으로 줄일 수 있다. 그러나 여전히 발현 지속 기간의 변동성, 간효소 상승, 재투여 불가 등의 문제점이 존재하며, 고가의 치료비용 역시 중요한 사회적 논의 대상이 되고 있다.피투시란은 어떤 약제인가?피투시란은 안티트롬빈(AT) mRNA를 절단·분해하여 AT 발현을 억제함으로써 혈중 AT 농도를 감소시키는 기전을 가진다. siRNA 치료제는 RNAi 과정을 활용하는 대표적인 플랫폼으로, 표적 mRNA를 인식하고 분해하도록 설계된 합성 RNA 이중가닥 구조를 기반으로 한다. 이 과정은 특정 단백질의 번역을 저해하여 표적 단백질의 합성을 효과적으로 억제한다.피투시란은 화학적으로 안정화된 이중가닥 siRNA로 설계되어 뉴클레아제에 의한 분해나 Toll-like receptor(TLR)3, TLR7 등 선천면역 수용체의 인식을 회피한다. 특히 리보뉴클레오티드의 2′-데옥시-2′-플루오로 치환, 2′-O-메틸 치환, 인산 골격의 선택적 변형이 적용되어 높은 안정성과 생체 내 지속성을 확보하였다.이 siRNA는 삼중 안테나(tri-antenna) 형태의 N-아세틸갈락토사민(GalNAc) 잔기와 결합되어 있으며, 간세포 표면의 아실글리코프로테인 수용체(asialoglycoprotein receptor, ASGPR)를 통해 효율적으로 간세포 내로 전달된다. 세포 내로 흡수된 후 산성 환경에서 siRNA는 ASGPR로부터 해리되고, 엔도솜을 탈출하여 세포질 내 RNA 유도 침묵 복합체(RNA-induced silencing complex, RISC)에 탑재된다.RISC는 siRNA의 안티센스(antisense) 가닥을 선택적으로 유지하고, 이를 이용해 표적 유전자인 SERPINC1 mRNA를 서열 특이적으로 절단·분해함으로써 AT 발현을 억제한다. 이 과정의 결과로 혈중 AT 농도가 감소하며, 그에 따라 트롬빈 생성이 증가하여 혈우병 환자의 응고능이 향상된다.RISC 내 안티센스 가닥은 세포 내에서 수 주간 안정적으로 존재하면서 반복적으로 전사체 절단을 매개하므로, 세포당 수백 개 수준의 siRNA 분자만으로도 강력하고 지속적인 knockdown 효과를 낸다. 이러한 특성 덕분에 피투시란은 임상시험에서 한 달에 한 번의 피하 투여만으로도 충분한 약효를 유지할 수 있는 장점을 보인다.Antithrombin Knockdown by Fitusiran(출처: Molecular Therapy Vol. 28 No 3 April 2020).피투시란의 약리 기전은?피투시란은 간에서 합성되는 AT(antithrombin) mRNA를 표적하는 siRNA로 개발된 약제로, 항트롬빈 발현을 효율적으로 억제함으로써 체내의 친응고 상태를 강화하는 새로운 치료 전략이다.즉, AT 억제 작용을 통해 내인성 및 외인성 경로 모두에서 Factor Xa와 트롬빈의 활성을 증가시켜 응고 연쇄의 효율성을 회복시키며, 그 결과 FVIII 또는 FIX 결핍이 있는 혈우병 환자에서도 출혈 위험을 효과적으로 감소시킨다.The Role of Thrombin and Antithrombin in Hemostasis, and the Mechanism of Action of Fitusiran(출처: Res Pract Thromb Haemost. 2023;7:e100179).피투시란은 혈우병 A 또는 B 환자의 출혈 예방을 위해 2개월에 한 번 피하 주사로 투여된다. 초기 권장 용량은 50mg이며, 이후 항트롬빈 활성도를 모니터링하여 용량과 투여 간격을 조정한다. 목표 AT 활성도는 15~35% 사이로 유지하는 것이 바람직하다.AT 활성도가 15% 미만으로 떨어질 경우 용량을 줄이고, 35% 이상으로 증가하면 용량을 늘릴 수 있다. 예를 들어, 50mg을 2개월 간격으로 투여하던 환자의 AT 활성도가 35%를 초과할 경우, 동일 용량을 매월 투여하도록 변경할 수 있다.약동학 연구에서 피투시란은 혈장에서 비교적 짧은 반감기(약 3~5시간)를 보였으나, 모든 임상시험 용량군에서 투여 중단 후에도 수개월간 AT 감소 효과가 지속되었다. 평균 AT 회복 속도는 한 달에 약 10~15% 수준이었으며, 이 기간 동안 트롬빈 생성은 억제되고 출혈 사건 발생 위험은 증가하는 경향을 보였다.투여 중단 후 약 5개월 시점에서 중앙값 AT 수치는 약 60% 이상으로 회복되었다. 약력학적 분석 결과, AT 억제 효과는 첫 투여 후 약 15~28일 사이에 나타났으며, 개인 간 AT 감소 정도에는 차이가 있으나 개인 내에서는 일정하게 유지되어 지속적인 지혈 보호 효과를 제공하는 것으로 확인되었다.피투시란은 또한 비인자(non-factor) 치료제 중 유일하게 특정 역전제(reversal agent)를 보유한 약제로, 이는 재조합 또는 혈장 유래 항트롬빈 제제 형태로 제공된다. 이러한 역전제는 돌파성 출혈 시 다른 지혈제와 병용할 경우 혈전증 위험을 조절할 수 있다는 점에서 임상적으로 중요한 의미를 갖는다.한편, 혈중 AT 감소가 표준 응고 검사에 직접적인 영향을 미치지 않는다는 점은, CFC(concentrated factor concentrate) 또는 BPA(bypassing agent)를 사용하는 상황이나 수술 시 지혈 상태 및 인자 수치를 보다 용이하게 모니터링할 수 있음을 시사한다.피투시란(QFITLIA)의 허가임상은 어떠한가?성인 및 12세 이상의 소아 환자에서 억제인자(inhibitors)의 존재 여부와 관계없이 혈우병 A 또는 B를 가진 환자에서 QFITLIA의 유효성과 안전성은 두 건의 임상시험에서 입증되었다.-억제인자가 있는 혈우병 A 또는 B: ATLAS-INH -억제인자가 없는 혈우병 A 또는 B: ATLAS-A/B위의 본 임상시험에 참여한 환자들은 장기 연장 연구인 ATLAS-OLE로 이월되었다.임상시험 ATLAS-INH 및 ATLAS-A/B에서는 QFITLIA 80mg 고정 월 1회 용량을 시험하였다. 그러나 이 용량에서 혈전성 사건(thrombotic events)이 발생하여, ATLAS-OLE에서는 항트롬빈(AT) 활성 15–35%를 목표로 하는 QFITLIA AT-DR 용법이 도입되었다.AT-DR 용법은 ATLAS-INH 및 ATLAS-A/B 연구가 거의 완료될 시점에 도입되었으므로, QFITLIA AT-DR 치료의 유효성은 장기 연장 연구 ATLAS-OLE에서 얻어진 AT-DR 치료 데이터를 ATLAS-INH 및 ATLAS-A/B 연구의 대조(control) 데이터와 비교하여 평가되었다.유효성 분석은 본 임상시험들의 무작위 배정(randomization)을 보존하면서, 부모 연구(parent studies)에서의 의도한 치료(intent-to-treat, ITT) 원칙에 따라 수행되었다.[ATLAS-INH] ATLAS-INH은 혈우병 A 또는 B 환자 중 FVIII(제8인자) 또는 FIX(제9인자)에 대한 억제항체를 가진 성인 및 소아 남성 환자(≥12세) 57명을 대상으로 실시된 다기관, 무작위배정, 공개(open-label) 임상시험이었다. 이들은 모두 과거에 출혈 시 우회제제(BPAs)를 필요에 따라(episodic, on-demand) 투여받은 병력이 있었다.대상 환자들은 2:1 비율로 무작위 배정되어, 월 1회 80mg 고정 용량의 QFITLIA 피하 주사(SC)를 예방요법(prophylaxis)으로 투여받은 군(N=38)과, 돌발 출혈(breakthrough bleeding) 발생 시 BPA를 필요에 따라 투여받은 군(N=19)으로 나뉘어 9개월간 치료를 받았다.그러나 QFITLIA 80mg 용량은 심각한 혈전성 사건(thrombotic events), 담낭 질환(담낭절제술 필요 포함), 간독성(hepatotoxicity) 위험 증가로 인해 승인되지 않았다. 현재 50mg과 20mg이 허가되어 있다.[ATLAS A/B] ATLAS A/B는 FVIII(제8인자) 또는 FIX(제9인자)에 대한 억제항체가 없는 혈우병 A 또는 B 환자를 대상으로 한 다기관, 무작위배정, 공개(open-label) 임상시험이었다. 대상자는 모두 성인 및 소아 남성(≥12세)으로, 과거에 출혈 시 응고인자제제(CFC)를 필요에 따라(on-demand, episodic) 투여받은 병력이 있었다.대상 환자 120명은 2:1 비율로 무작위 배정되어, 월 1회 80 mg 고정 용량의 QFITLIA 피하 주사(SC)를 예방요법(prophylaxis)으로 투여받은 군(N=80)과, 돌발 출혈 발생 시 CFC를 필요에 따라 투여받은 군(N=40)으로 나뉘어 9개월간 치료를 받았다.그러나 QFITLIA 80mg용량은 심각한 혈전성 사건(thrombotic events), 담낭 질환(담낭절제술 필요 포함), 간독성(hepatotoxicity) 위험 증가로 인해 승인되지 않았다.[ATLAS-OLE] 총 227명의 환자가 두 임상시험(ATLAS-INH 및 ATLAS-A/B)과, CFC 또는 BPA 예방요법을 받던 환자를 대상으로 한 교차 임상시험 ATLAS-PPX에서 이월되어 ATLAS-OLE 연구에서 QFITLIA 치료를 받았다. 이 다기관 공개 연장 임상시험은 FVIII 또는 FIX 억제항체 유무와 관계없이, 12세 이상의 성인 및 소아 남성 혈우병 A 또는 B 환자에서 QFITLIA의 장기적인 안전성과 유효성을 평가하였다.대상자는 초기에는 월 1회 80mg QFITLIA 피하 주사를 투여받았으나, 연구가 개정되어 AT-DR(항트롬빈 활성 15–35% 목표) 용법의 유효성과 안전성을 평가하도록 설계가 변경되었다. 이후 총 213명의 환자가 AT-DR로 전환되었다.AT-DR에서는 시작 용량이 50mg 격월(2개월 간격) 투여였으며, INNOVANCE Antithrombin 분석법을 이용해 측정한 AT 활성 수치에 따라 개별적으로 용량을 조정하였다. 용량은 50mg 월 1회 또는 80mg 월 1회로 증량하거나, 20mg 격월 또는 20mg 월 1회로 감량할 수 있었다.AT 활성 수치가 최저 용량에서도2025-10-23 23:25:17최병철 박사
세계 첫 항체 무관 혈우병 A·B 치료제 '피투시란'큐피틀리아(Qfitlia, 성분명 피투시란, Fitusiran, 사노피)는 GalXC 기술 플랫폼을 기반으로 개발된 항트롬빈(antithrombin)을 표적으로 하는 소간섭 리보핵산(small interfering RNA, siRNA) 치료제다.이 약제는 2024년 유럽의약청(EMA) 에서, 이어 올해 3월 미국 식품의약국(FDA) 에서 제VIII인자 또는 제IX인자 억제인자(inhibitor)의 유무와 관계없이, 12세 이상 성인 및 소아 혈우병 A 또는 B 환자에서 출혈 에피소드의 발생을 예방하거나 빈도를 감소시키기 위한 정기적 예방요법(routine prophylaxis)에 ‘두 달에 한번 피하주사’로 승인되었다. 국내에서는 올해 5월 희귀의약품(Orphan drug) 으로 지정되었다.혈우병(hemophilia)은 X염색체 연관 열성 유전질환으로, 제Ⅷ인자(FVIII) 또는 제Ⅸ인자(FIX) 의 결핍으로 인해 혈액응고 연쇄반응(coagulation cascade) 이 정상적으로 진행되지 못하며, 그 결과 트롬빈(thrombin) 생성 부족으로 지혈(hemostasis) 이 저하된다. 이러한 병태생리적 이상은 반복적인 출혈, 특히 관절 출혈을 초래하여 만성 관절병증(chronic arthropathy) 및 삶의 질 저하로 이어진다.기존의 표준 치료는 응고인자제제(clotting factor concentrate, CFC) 의 정맥 내 투여를 통한 인자 보충요법(replacement therapy) 이었다. 그러나 이 방식은 정맥 투여의 불편성, 반복적 투여 부담, 그리고 항체(억제인자, inhibitor) 형성으로 인한 치료 저항성이라는 한계를 지닌다.이에 따라 최근에는 비(非)응고인자 기반 치료(non-factor therapy) 의 개발이 활발히 이루어지고 있으며, 그중에서도 RNA 간섭(RNA interference, RNAi) 기술을 이용한 피투시란(Fitusiran) 은 새로운 치료 옵션으로 주목 받고 있다.피투시란은 간세포 내에서 항트롬빈(antithrombin, AT) 합성을 억제하도록 설계된 siRNA 기반 치료제로, 내인성 응고 조절 인자의 발현을 조절함으로써 응고 균형(hemostatic balance) 을 회복시키는 새로운 접근법을 제시한다.피투시란의 승인은 다국가, 무작위배정, 대조, 3상 임상시험들로 구성된 ATLAS 임상 프로그램의 결과를 근거로 하였다.이 프로그램에는 ATLAS-A/B, ATLAS-INH, 그리고 ATLAS-PPX 연구가 포함되며, 각각 혈우병 A 또는 B 환자 중 인자 억제인자의 유무, 그리고 기존 예방요법(prophylaxis) 사용 여부에 따라 구분되었다.ATLAS-A/B 연구는 억제인자가 없는(non-inhibitor) 혈우병 A 또는 B 환자를 대상으로, ATLAS-INH 연구는 억제인자가 존재하는(inhibitor-positive) 환자를 대상으로 수행되었다. ATLAS-PPX 연구는 기존 예방요법을 받고 있던 환자에서 피투시란으로 전환했을 때의 출혈률 변화를 평가하였다.이들 연구에서 피투시란은 월 1회 피하주사(subcutaneous injection) 투여만으로도 연간 출혈률(annualized bleeding rate, ABR)을 기존 치료 대비 약 90% 이상 유의하게 감소시켰으며, 절반 이상의 환자에서 무출혈(ABR = 0)이 관찰되었다. 또한 억제인자 유무와 관계없이 일관된 출혈 억제 효과가 확인되었다.혈우병이란 무엇인가?혈우병(hemophilia)은 그리스어 ‘hemo(피)’와 ‘philia(사랑하다)’에서 유래한 용어로, 1828년 Schönlein에 의해 Hämophilie라 명명됐다. 19세기 말 유럽 왕실 내 근친혼으로 인해 영국, 스페인, 독일, 러시아 등 여러 나라에서 다수의 환자가 발생하면서 ‘왕실병(The Royal Disease)’이라는 별칭을 얻었다.혈우병은 혈액응고인자의 결핍으로 인해 발생하는 대표적인 선천성 출혈성 질환이다. 제VIII응고인자(FVIII)의 결핍은 혈우병 A로, 전체 환자의 약 80~85%를 차지하며 ‘고전적 혈우병(classic hemophilia)’이라 불린다. 제IX응고인자(FIX)의 결핍은 혈우병 B로 약 15%를 차지하며, 최초 환자의 이름을 따 ‘크리스마스병(Christmas disease)’으로도 알려져 있다. 제XI응고인자(FXI)의 결핍은 혈우병 C로 상대적으로 드물게 발생한다.혈우병 A와 B는 X 염색체 열성 유전 양식을 가지므로 주로 남성에서 발병하며, 여성은 보인자로 존재하거나 드물게 태아기에 사망하기도 한다. 반면 혈우병 C는 4번 염색체 이상에 기인하므로 성별에 관계없이 발생할 수 있으며, 일부 환자에서는 가족력 없이 자연 발생적 유전자 변이에 의해 발현되기도 한다.혈우병과 유사한 질환으로는 폰빌레브란트병(von Willebrand disease, vWD)이 있다. 이는 응고인자 VIII과 결합하는 폰빌레브란트인자(vWF)의 결핍으로 인해 혈우병과 유사한 임상 양상을 보인다.이외에도 프로트롬빈(II), 피브리노겐(I), V, VII, X, XII, XIII 응고인자의 결핍으로 인한 선천성 응고장애가 보고되어 있으나, 이러한 질환들은 혈우병의 범주에는 포함되지 않는다.혈액응고 과정은 어떻게 일어나는가?혈액응고는 인체의 항상성을 유지하기 위한 필수적인 생리적 방어기전으로, 외상이나 혈관 손상 시 과도한 출혈을 방지하는 역할을 한다. 이 과정은 혈관수축, 혈소판 기능, 그리고 혈액응고인자의 연속적인 활성화로 이루어지는 응고 연쇄(cascade)로 설명되며, 궁극적으로 안정적인 피브린 혈전(fibrin clot)을 형성한다.혈액응고인자(Coagulation factors)는 주로 간에서 합성되는 단백질로, 로마 숫자로 표기된 I번부터 XIII번까지의 인자가 알려져 있다. 이들은 각각 특정 효소 활성 또는 보조인자로 작용하면서 정교하고 단계적인 반응을 매개한다. 주요 응고인자로는 피브리노겐(Factor I), 프로트롬빈(Factor II), 그리고 프로트롬빈 복합체를 구성하는 V, VII, IX, X, XI, XII 인자, 마지막으로 XIII 인자 등이 있다. 응고 연쇄는 크게 내인성 경로(intrinsic pathway), 외인성 경로(extrinsic pathway), 그리고 두 경로가 합류하는 공통 경로(common pathway)로 구성된다.내인성 경로는 Factor XII의 활성화를 시작으로 XI, IX, VIII 인자가 순차적으로 활성화되며, 외인성 경로는 조직인자(tissue factor, TF)와 Factor VII의 상호작용을 통해 개시된다.두 경로는 Factor X의 활성화 단계에서 공통 경로로 수렴하며, 활성화된 Factor X는 Factor V와 결합하여 프로트롬비나제(prothrombinase) 복합체를 형성한다. 이 복합체는 프로트롬빈(Factor II)을 트롬빈(thrombin)으로 전환시키고, 생성된 트롬빈은 피브리노겐(Factor I)을 불용성 피브린(fibrin)으로 전환시켜 최종적으로 혈전을 완성한다.또한 트롬빈은 Factor V, VIII, XI 등을 다시 활성화시키는 양성 되먹임(positive feedback) 작용을 통해 응고 반응을 증폭시키며, Factor XIII을 활성화시켜 피브린 가교결합(fibrin cross-linking)을 형성함으로써 혈전의 안정성을 더욱 높인다.이러한 정교한 연쇄 반응은 항응고 단백질(antithrombin, protein C/S system 등)과 섬유소 용해(fibrinolysis) 기전 간의 정밀한 균형 속에서 조절된다. 이 균형이 깨질 경우 출혈성 질환이나 혈전성 질환으로 이어질 수 있다.항트롬빈(Antithrombin, AT, heparin cofactor I)은 어떤 물질인가?항트롬빈(AT)은 혈액응고 조절에서 가장 중요한 내인성 항응고인자로, 전체 생리적 응고 억제 작용의 약 70~80%를 담당하는 핵심 단백질이다. AT는 혈장에 존재하는 세린 단백질분해효소 억제제(serpin) 계열의 당단백질로, 주된 표적은 트롬빈(thrombin)이지만, Factor Xa, IXa, XIa, XIIa 및 칼리크레인(kallikrein) 등 다양한 혈액응고인자를 동시에 억제함으로써 응고 연쇄(cascade) 전반의 균형 유지에 기여한다.The Coagulation Cascade(출처: Ann Pharmacother . 2016 Sep;50(9):758-67). AT는 트롬빈의 활성 중심부에 위치한 세린(serine) 잔기와 1:1 비율로 결합하여 불활성 복합체를 형성함으로써 트롬빈 활성을 차단한다. 이를 통해 소규모 응고 반응이나 불필요한 혈전 형성을 신속히 억제하며, 정상적인 생리 상태에서 과도한 혈액응고를 방지하는 핵심 역할을 수행한다.그러나 대규모 혈관 손상이나 파종성 혈관내응고(Disseminated intravascular coagulation, DIC)와 같이 트롬빈 생성이 폭발적으로 증가하는 상황에서는 AT의 억제 능력이 상대적으로 부족해져, 생리적 항응고 메커니즘만으로는 병적 혈전 형성을 완전히 제어하기 어렵다.AT의 항응고 활성이 가장 강력하게 발휘되는 조건은 헤파린(heparin)의 존재 하에서이다. 헤파린은 AT에 결합하여 구조적 변화를 유도하고, AT와 트롬빈 및 Factor Xa 간의 결합 친화도를 수백 배 이상 증폭시킨다.이로 인해 헤파린은 AT의 촉매제(cofactor) 역할을 하며, 임상적으로 항응고 효과를 발휘하는 주요 기전이 바로 AT 매개 억제 반응이다. 이러한 이유로 AT 결핍 환자에서는 헤파린의 항응고 효과가 현저히 감소하며, 이는 선천성 또는 후천성 AT 결핍에서 혈전성 질환 발생 위험이 증가하는 중요한 근거가 된다.AT는 간에서 합성되며 혈중 농도는 약 0.15mg/mL로 유지되고, 정상 활성도는 80~120% 범위 내에 있다. 선천성 AT 결핍은 드문 질환이지만 정맥혈전증과 폐색전증 발생의 중요한 위험 요인으로 알려져 있으며, 후천성 결핍은 간질환, 신증후군, DIC, 항응고제 치료 등 다양한 상황에서 관찰된다. AT 농도의 감소는 항응고 균형을 무너뜨려 과도한 혈전 형성을 유발하므로, 임상적으로 AT 농축제제 보충 또는 헤파린·직접 트롬빈 억제제와 같은 항응고 요법을 병행하는 치료 전략이 고려된다.이처럼 AT는 단순한 혈액응고인자 억제 단백질을 넘어, 혈액응고와 항응고, 그리고 섬유소 용해(fibrinolysis) 시스템 사이의 미세한 균형을 유지하는 핵심 조절인자로서, 혈전성 질환의 병태생리 이해와 새로운 항응고 치료제 개발에 있어 중요한 연구 대상이 되고 있다.혈우병 A 치료제에는 어떤 약제가 있는가?1. 응고인자 보충요법(Factor Replacement Therapy) 혈우병 A의 전통적인 치료는 부족한 제Ⅷ인자(FVIII)를 직접 보충하는 방식이다. 초기에는 혈액 유래 FVIII 제제가 사용되었으나, 감염 위험 등 안전성 문제가 제기되면서 현재는 재조합 FVIII(rFVIII)이 표준으로 자리잡았다. 또한 최근에는 반감기를 연장한 FVIII 제제들이 개발되어 투여 빈도를 줄이고 환자 순응도를 높이는 데 기여하고 있다.1) 표준 반감기(Standard half-life, SHL) FVIII 제제 표준 반감기 제제는 혈액 유래 FVIII와 재조합 FVIII로 나눌 수 있다. 혈액 유래 제제는 감염 위험 관리가 필요하지만 여전히 일부에서 사용되고 있으며, 재조합 FVIII로 애드베이트(AdvateⓇ, 코지네이트 에프에스(Kogenate FSⓇ) 등은 안전성 측면에서 더 선호된다.2) 반감기 연장형(Extended half-life, EHL) FVIII 제제 반감기 연장형 제제는 투여 간격을 늘리기 위해 Fc-fusion(엘록테이트, EloctateⓇ), PEGylation(애디노베이트, AdynovateⓇ, 지비, JiviⓇ) 등 다양한 기술이 적용되었다. 이러한 약제들은 환자의 주사 횟수를 줄여 장기적인 치료 순응도를 개선하는 장점이 있다.3) VWF-independent EHL(VWF 비의존성 반감기 연장형) FVIII 제제 VWF 비의존성 반감기 연장형 제제인 알투비오(AltuviiioⓇ)는 주 1회 주사로 FVIII 활성을 더 오래 유지할 수 있도록 설계된 최신형 지속형 치료제(high sustained factor, HSF)로 2023년 미 FDA에서 승인되었고 국내에서는 진행중이다,2. 억제인자 환자 치료(Treatment for Patients with Inhibitors) 혈우병 A 환자의 약 20~30%는 치료 과정에서 FVIII에 대한 억제항체를 형성하게 되며, 이 경우 기존의 FVIII 보충요법은 효과가 제한적이다. 억제인자 환자의 치료에는 크게 두 가지 접근법이 있다.첫째, 우회제제(bypassing agents, BPA)를 사용하는 방법이다. 활성화 프로트롬빈 복합체(aPCC, 훼이바, FEIBAⓇ)와 재조합 활성 VIIa(rFVIIa, 노보세븐, NovoSevenⓇ)는 응고경로를 우회적으로 활성화하여 지혈 효과를 발휘하지만, 지혈 반응의 변동성과 혈전 위험이라는 한계가 존재한다.둘째, 에미시주맙(Emicizumab, HemlibraⓇ)는 FIXa와 FX를 연결하여 FVIII의 기능을 모방하는 이중특이성 항체로, 억제인자 환자뿐 아니라 비(非)억제인자 환자에서도 예방요법으로 사용 가능하다. 피하 주사로 1주~4주 간격 투여가 가능하여 투여 편의성이 획기적으로 개선되었다.3. 대체 인자제제(Replacement therapy) 재조합 돼지 유래 FVIII(r-pFVIII)인 오비주르(Obizur®, Susoctocog alfa)는 2014년 미 FDA, 2015년 EMA 그리고 2023년 국내에서 ‘성인 후천성 혈우병 A(Acquired Haemophilia A, AHA) 환자의 출혈 에피소드 치료’에 승인되었다. 후천성 혈우병 A는 선천성 혈우병과 다르게, 정상 혈액응고인자 VIII(FVIII) 수준을 가지고 있지만, 이에 대해 자가면역 항체(중화 항체)가 생겨 혈액 응고 기능이 저해되어 출혈 위험이 커지는 인구 100만 명당 약 1명꼴로 발생하는 초희귀 자가면역 응고질환이다.4. 비응고인자 기반 치료(Non-factor Therapy) 최근 혈우병 A 치료에서 가장 주목받는 변화는 FVIII를 직접 보충하지 않고, 다른 경로를 통해 응고 균형을 회복하는 비응고인자 기반 치료이다. 대표적인 약제가 에미시주맙(Emicizumab, HemlibraⓇ)으로, FIXa와 FX을 연결하여 FVIII의 보조인자 기능을 모방하는 이중특이성 항체이다. 피하 주사로 주 1회, 격주, 또는 4주 간격 투여가 가능해 환자의 치료 편의성이 획기적으로 개선되었다.이외에도 피투시란(Fitusiran)과 콘시주맙(Concizumab, Alhemo®)가 있다. 피투시란은 RNA 간섭(RNAi) 기술을 이용하여 간세포에서 항트롬빈 합성을 억제함으로써 응고 활성을 높인다. 월 1회 피하 주사가 가능하지만, 혈전 및 간독성 발생 위험으로 인해 항트롬빈 활성(15–35%)을 유지하는 개별화 용량조절(AT-DR)이 필요하다. 콘시주맙은 조직인자경로억제인자(TFPI)를 차단하여 내인성 응고를 촉진하는 약제이다.5. 유전자 치료(Gene Therapy) 혈우병 A에서 유전자 치료는 단회 정맥투여를 통해 간세포에 FVIII 유전자를 도입하여 장기간 발현을 유도하는 새로운 전략이다. 대표적인 약제가 록타비안(RoctavianⓇ, Valoctocogene roxaparvovec)으로, AAV5 벡터를 이용해 개발되었으며 2022년 유럽, 2023년 미국 FDA의 승인을 받았다.단일 투여로 FVIII 발현을 장기간 유지할 수 있어 치료 패러다임의 변화를 예고했으나, 발현 지속 기간의 불확실성, 간효소 상승, 재투여 불가 등의 문제점이 여전히 남아 있다.혈우병 B 치료제에는 어떤 약제가 있는가?1. 응고인자 보충요법(Factor IX Replacement Therapy) 혈우병 B의 가장 기본적인 치료는 부족한 제Ⅸ인자(FIX)를 직접 보충하는 방식이다. 과거에는 혈액 유래 제제가 널리 사용되었으나, 감염 위험 문제로 현재는 재조합 FIX(rFIX) 제제가 주로 사용된다. 여기에 더해 반감기를 연장한 제제들이 개발되면서 투여 간격이 길어지고 환자의 치료 순응도가 크게 향상되었다.1) 표준 반감기(Standard half-life, SHL) FIX 제제 표준 반감기 FIX 제제는 투여 후 약 18~24시간의 반감기를 가지며, 주 2~3회 정맥 주사가 필요하다. 혈액 유래 FIX 제제는 여전히 일부에서 사용되지만, 바이러스 감염에 대한 안전성 우려가 있었다. 이를 보완하기 위해 개발된 재조합 FIX 제제인 베네픽스(BeneFIXⓇ, Nonacog alfa)는 안전성이 확보되어 현재 임상에서 가장 널리 사용되고 있다.2) 반감기 연장(Extended half-life, EHL) FIX 제제 반감기 연장 제제는 기존 표준 제제보다 3~5배 긴 반감기를 가지며, 1~2주 간격으로 투여가 가능하다. 이들 약제에는 Fc-fusion 단백을 이용한 알프로릭스(Alprolix(Ⓡ, Eftrenonacog alfa), albumin-fusion 기술이 적용된 아이델비온(IdelvionⓇ Albutrepenonacog alfa) 등이 포함된다. 이러한 제제들은 주사 횟수를 줄여 환자의 삶의 질과 치료 순응도를 높이는 중요한 진보로 평가된다.2. 억제인자 환자 치료(Treatment for Patients with Inhibitors) 혈우병 B 환자에서 억제인자 발생은 상대적으로 드물지만, 일단 형성되면 치료가 매우 어렵다. 억제인자가 형성된 경우 기존 FIX 제제의 효과가 소실되므로 우회제제(bypassing agents)가 사용된다.활성화 프로트롬빈 복합체(aPCC, 훼이바, FEIBAⓇ)와 재조합 활성 VIIa(rFVIIa, 노보세븐, NovoSevenⓇ)가 대표적이다. 그러나 혈우병 A와 달리 에미시주맙은 FVIII 기능을 모방하는 기전이기 때문에 혈우병 B 환자에게는 효과가 없다. 따라서 억제인자 환자의 치료는 여전히 제한적이며, 새로운 치료 전략이 필요한 영역이다.3. 비응고인자 기반 치료(Non-factor Therapy) 혈우병 B에서도 비응고인자 기반 치료가 적용될 수 있다. 이들 약제는 특정 응고인자를 보충하지 않고 응고 균형 자체를 조절하는 기전을 갖는다. 대표적으로 RNA 간섭 기반의 피투시란(Fitusiran)은 간세포에서 항트롬빈 합성을 억제하여 응고 활성을 증가시키며, 혈우병 A와 B 모두에 승인되었다.또한 항 TFPI 항체인 콘시주맙(Concizumab, Alhemo®) 역시 혈우병 A와 B 모두에 적용 가능하며, 내인성 응고경로를 촉진하여 출혈을 억제한다. 이처럼 비응고인자 기반 치료는 억제인자 보유 여부와 관계없이 사용할 수 있는 장점이 있어, 혈우병 B 환자에서도 중요한 치료 대안으로 부상하고 있다.4. 유전자 치료(Gene Therapy) 혈우병 B는 유전자 치료 분야에서 가장 먼저 성과를 낸 질환 중 하나이다. FIX 유전자의 크기가 FVIII보다 작아 AAV 벡터 전달이 용이하기 때문에, 임상개발이 상대적으로 앞서 진행되었다.대표적인 약제는 헴제닉스(HemgenixⓇ, Etranacogene dezaparvovec)으로, 2022년 미국 FDA와 2023년 유럽 EMA에서 세계 최초로 혈우병 유전자 치료제로 승인되었다. 단회 정맥투여만으로 간세포에서 FIX 발현이 장기간 유지될 수 있으며, 환자의 치료 부담을 획기적으로 줄일 수 있다. 그러나 여전히 발현 지속 기간의 변동성, 간효소 상승, 재투여 불가 등의 문제점이 존재하며, 고가의 치료비용 역시 중요한 사회적 논의 대상이 되고 있다.피투시란은 어떤 약제인가?피투시란은 안티트롬빈(AT) mRNA를 절단·분해하여 AT 발현을 억제함으로써 혈중 AT 농도를 감소시키는 기전을 가진다. siRNA 치료제는 RNAi 과정을 활용하는 대표적인 플랫폼으로, 표적 mRNA를 인식하고 분해하도록 설계된 합성 RNA 이중가닥 구조를 기반으로 한다. 이 과정은 특정 단백질의 번역을 저해하여 표적 단백질의 합성을 효과적으로 억제한다.피투시란은 화학적으로 안정화된 이중가닥 siRNA로 설계되어 뉴클레아제에 의한 분해나 Toll-like receptor(TLR)3, TLR7 등 선천면역 수용체의 인식을 회피한다. 특히 리보뉴클레오티드의 2′-데옥시-2′-플루오로 치환, 2′-O-메틸 치환, 인산 골격의 선택적 변형이 적용되어 높은 안정성과 생체 내 지속성을 확보하였다.이 siRNA는 삼중 안테나(tri-antenna) 형태의 N-아세틸갈락토사민(GalNAc) 잔기와 결합되어 있으며, 간세포 표면의 아실글리코프로테인 수용체(asialoglycoprotein receptor, ASGPR)를 통해 효율적으로 간세포 내로 전달된다. 세포 내로 흡수된 후 산성 환경에서 siRNA는 ASGPR로부터 해리되고, 엔도솜을 탈출하여 세포질 내 RNA 유도 침묵 복합체(RNA-induced silencing complex, RISC)에 탑재된다.RISC는 siRNA의 안티센스(antisense) 가닥을 선택적으로 유지하고, 이를 이용해 표적 유전자인 SERPINC1 mRNA를 서열 특이적으로 절단·분해함으로써 AT 발현을 억제한다. 이 과정의 결과로 혈중 AT 농도가 감소하며, 그에 따라 트롬빈 생성이 증가하여 혈우병 환자의 응고능이 향상된다.RISC 내 안티센스 가닥은 세포 내에서 수 주간 안정적으로 존재하면서 반복적으로 전사체 절단을 매개하므로, 세포당 수백 개 수준의 siRNA 분자만으로도 강력하고 지속적인 knockdown 효과를 낸다. 이러한 특성 덕분에 피투시란은 임상시험에서 한 달에 한 번의 피하 투여만으로도 충분한 약효를 유지할 수 있는 장점을 보인다.Antithrombin Knockdown by Fitusiran(출처: Molecular Therapy Vol. 28 No 3 April 2020).피투시란의 약리 기전은?피투시란은 간에서 합성되는 AT(antithrombin) mRNA를 표적하는 siRNA로 개발된 약제로, 항트롬빈 발현을 효율적으로 억제함으로써 체내의 친응고 상태를 강화하는 새로운 치료 전략이다.즉, AT 억제 작용을 통해 내인성 및 외인성 경로 모두에서 Factor Xa와 트롬빈의 활성을 증가시켜 응고 연쇄의 효율성을 회복시키며, 그 결과 FVIII 또는 FIX 결핍이 있는 혈우병 환자에서도 출혈 위험을 효과적으로 감소시킨다.The Role of Thrombin and Antithrombin in Hemostasis, and the Mechanism of Action of Fitusiran(출처: Res Pract Thromb Haemost. 2023;7:e100179).피투시란은 혈우병 A 또는 B 환자의 출혈 예방을 위해 2개월에 한 번 피하 주사로 투여된다. 초기 권장 용량은 50mg이며, 이후 항트롬빈 활성도를 모니터링하여 용량과 투여 간격을 조정한다. 목표 AT 활성도는 15~35% 사이로 유지하는 것이 바람직하다.AT 활성도가 15% 미만으로 떨어질 경우 용량을 줄이고, 35% 이상으로 증가하면 용량을 늘릴 수 있다. 예를 들어, 50mg을 2개월 간격으로 투여하던 환자의 AT 활성도가 35%를 초과할 경우, 동일 용량을 매월 투여하도록 변경할 수 있다.약동학 연구에서 피투시란은 혈장에서 비교적 짧은 반감기(약 3~5시간)를 보였으나, 모든 임상시험 용량군에서 투여 중단 후에도 수개월간 AT 감소 효과가 지속되었다. 평균 AT 회복 속도는 한 달에 약 10~15% 수준이었으며, 이 기간 동안 트롬빈 생성은 억제되고 출혈 사건 발생 위험은 증가하는 경향을 보였다.투여 중단 후 약 5개월 시점에서 중앙값 AT 수치는 약 60% 이상으로 회복되었다. 약력학적 분석 결과, AT 억제 효과는 첫 투여 후 약 15~28일 사이에 나타났으며, 개인 간 AT 감소 정도에는 차이가 있으나 개인 내에서는 일정하게 유지되어 지속적인 지혈 보호 효과를 제공하는 것으로 확인되었다.피투시란은 또한 비인자(non-factor) 치료제 중 유일하게 특정 역전제(reversal agent)를 보유한 약제로, 이는 재조합 또는 혈장 유래 항트롬빈 제제 형태로 제공된다. 이러한 역전제는 돌파성 출혈 시 다른 지혈제와 병용할 경우 혈전증 위험을 조절할 수 있다는 점에서 임상적으로 중요한 의미를 갖는다.한편, 혈중 AT 감소가 표준 응고 검사에 직접적인 영향을 미치지 않는다는 점은, CFC(concentrated factor concentrate) 또는 BPA(bypassing agent)를 사용하는 상황이나 수술 시 지혈 상태 및 인자 수치를 보다 용이하게 모니터링할 수 있음을 시사한다.피투시란(QFITLIA)의 허가임상은 어떠한가?성인 및 12세 이상의 소아 환자에서 억제인자(inhibitors)의 존재 여부와 관계없이 혈우병 A 또는 B를 가진 환자에서 QFITLIA의 유효성과 안전성은 두 건의 임상시험에서 입증되었다.-억제인자가 있는 혈우병 A 또는 B: ATLAS-INH -억제인자가 없는 혈우병 A 또는 B: ATLAS-A/B위의 본 임상시험에 참여한 환자들은 장기 연장 연구인 ATLAS-OLE로 이월되었다.임상시험 ATLAS-INH 및 ATLAS-A/B에서는 QFITLIA 80mg 고정 월 1회 용량을 시험하였다. 그러나 이 용량에서 혈전성 사건(thrombotic events)이 발생하여, ATLAS-OLE에서는 항트롬빈(AT) 활성 15–35%를 목표로 하는 QFITLIA AT-DR 용법이 도입되었다.AT-DR 용법은 ATLAS-INH 및 ATLAS-A/B 연구가 거의 완료될 시점에 도입되었으므로, QFITLIA AT-DR 치료의 유효성은 장기 연장 연구 ATLAS-OLE에서 얻어진 AT-DR 치료 데이터를 ATLAS-INH 및 ATLAS-A/B 연구의 대조(control) 데이터와 비교하여 평가되었다.유효성 분석은 본 임상시험들의 무작위 배정(randomization)을 보존하면서, 부모 연구(parent studies)에서의 의도한 치료(intent-to-treat, ITT) 원칙에 따라 수행되었다.[ATLAS-INH] ATLAS-INH은 혈우병 A 또는 B 환자 중 FVIII(제8인자) 또는 FIX(제9인자)에 대한 억제항체를 가진 성인 및 소아 남성 환자(≥12세) 57명을 대상으로 실시된 다기관, 무작위배정, 공개(open-label) 임상시험이었다. 이들은 모두 과거에 출혈 시 우회제제(BPAs)를 필요에 따라(episodic, on-demand) 투여받은 병력이 있었다.대상 환자들은 2:1 비율로 무작위 배정되어, 월 1회 80mg 고정 용량의 QFITLIA 피하 주사(SC)를 예방요법(prophylaxis)으로 투여받은 군(N=38)과, 돌발 출혈(breakthrough bleeding) 발생 시 BPA를 필요에 따라 투여받은 군(N=19)으로 나뉘어 9개월간 치료를 받았다.그러나 QFITLIA 80mg 용량은 심각한 혈전성 사건(thrombotic events), 담낭 질환(담낭절제술 필요 포함), 간독성(hepatotoxicity) 위험 증가로 인해 승인되지 않았다. 현재 50mg과 20mg이 허가되어 있다.[ATLAS A/B] ATLAS A/B는 FVIII(제8인자) 또는 FIX(제9인자)에 대한 억제항체가 없는 혈우병 A 또는 B 환자를 대상으로 한 다기관, 무작위배정, 공개(open-label) 임상시험이었다. 대상자는 모두 성인 및 소아 남성(≥12세)으로, 과거에 출혈 시 응고인자제제(CFC)를 필요에 따라(on-demand, episodic) 투여받은 병력이 있었다.대상 환자 120명은 2:1 비율로 무작위 배정되어, 월 1회 80 mg 고정 용량의 QFITLIA 피하 주사(SC)를 예방요법(prophylaxis)으로 투여받은 군(N=80)과, 돌발 출혈 발생 시 CFC를 필요에 따라 투여받은 군(N=40)으로 나뉘어 9개월간 치료를 받았다.그러나 QFITLIA 80mg용량은 심각한 혈전성 사건(thrombotic events), 담낭 질환(담낭절제술 필요 포함), 간독성(hepatotoxicity) 위험 증가로 인해 승인되지 않았다.[ATLAS-OLE] 총 227명의 환자가 두 임상시험(ATLAS-INH 및 ATLAS-A/B)과, CFC 또는 BPA 예방요법을 받던 환자를 대상으로 한 교차 임상시험 ATLAS-PPX에서 이월되어 ATLAS-OLE 연구에서 QFITLIA 치료를 받았다. 이 다기관 공개 연장 임상시험은 FVIII 또는 FIX 억제항체 유무와 관계없이, 12세 이상의 성인 및 소아 남성 혈우병 A 또는 B 환자에서 QFITLIA의 장기적인 안전성과 유효성을 평가하였다.대상자는 초기에는 월 1회 80mg QFITLIA 피하 주사를 투여받았으나, 연구가 개정되어 AT-DR(항트롬빈 활성 15–35% 목표) 용법의 유효성과 안전성을 평가하도록 설계가 변경되었다. 이후 총 213명의 환자가 AT-DR로 전환되었다.AT-DR에서는 시작 용량이 50mg 격월(2개월 간격) 투여였으며, INNOVANCE Antithrombin 분석법을 이용해 측정한 AT 활성 수치에 따라 개별적으로 용량을 조정하였다. 용량은 50mg 월 1회 또는 80mg 월 1회로 증량하거나, 20mg 격월 또는 20mg 월 1회로 감량할 수 있었다.AT 활성 수치가 최저 용량에서도2025-10-23 23:25:17최병철 박사 -
 피타바스타틴-페노피브레이트, 허가품목 20개 넘어[데일리팜=이혜경 기자] 피타바스타틴·페노피브레이트 복합제 후발주자가 늘어나면서 허가 품목수가 20개를 넘어섰다.지난 2019년 한림제약(스타펜캡슐)을 수탁사로 8개사가 개량신약을 허가 받은 이후, 올해부터 본격적으로 후발주자가 뛰어든 가운데 최근까지 총 21개 품목이 허가를 받았다.식품의약품안전처는 28일 에이프로젠바이오로직스의 '페타바정(피타바스타틴, 페노피브레이트)'과 아주약품의 '피타렛정2/160mg(피타바스타틴칼슘수화물, 페노피브레이트)' 등 2개 품목을 허가했다.피타바스타틴·페노피브레이트 복합제 허가 목록. 피타바스타틴·페노피브레이트 복합제는 고지혈증 치료제 성분 피타바스타틴과 중성지방 치료제 성분 페노피브레이트가 결합한 복합제다.관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰인다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐다.스타틴-중성지방 복합제 시장은 지속적으로 성장하면서 국내사에서 피타바스타틴·페노피브레이 복합제를 개발해 2019년부터 허가를 받았다.당시 한림제약(스타펜캡슐), 동광제약(피에프캡슐), 한국프라임제약(리페스틴캡슐), 삼진제약(뉴스타틴듀오캡슐), 동국제약(피타론에프캡슐), 지엘파마(리로우펜캡슐), 대원제약(업타바캡슐), 안국약품(페바로에프캡슐) 등 8개사가 개량신약이 승인됐다.유비스트에 따르면 허가된 8개 품목의 지난해 원외처방액 규모는 38억원 정도다.페바로가 9억1261만원으로 가장 처방이 많았으며, 업타바 7억2313만원, 리페스틴 5억3457만원, 스타펜 5억2528만원, 피에프 5억2405만원, 피타론에프 3억8710만원, 뉴스타틴듀오 1억6771만원의 원외처방금액을 보였다.해당 성분제제에 국내사들이 관심을 갖기 시작한건 2년전 부터다. 신풍제약과 서울제약 등이 생동성시험을 진행하면서 후발의약품 개발을 알렸다.특히 2019년 허가를 받은 선발 품목의 경우 등재 특허가 존재하지 않아 후발 주자들은 생동만으로 제제 개발 이후 출시까지 장벽이 높지 않았다는 분석이다.2019년 8개 품목의 개량신약 허가 이후, 올해만 13개 품목이 허가 목록에 이름을 올린 상태다.2025-08-28 18:22:29이혜경
피타바스타틴-페노피브레이트, 허가품목 20개 넘어[데일리팜=이혜경 기자] 피타바스타틴·페노피브레이트 복합제 후발주자가 늘어나면서 허가 품목수가 20개를 넘어섰다.지난 2019년 한림제약(스타펜캡슐)을 수탁사로 8개사가 개량신약을 허가 받은 이후, 올해부터 본격적으로 후발주자가 뛰어든 가운데 최근까지 총 21개 품목이 허가를 받았다.식품의약품안전처는 28일 에이프로젠바이오로직스의 '페타바정(피타바스타틴, 페노피브레이트)'과 아주약품의 '피타렛정2/160mg(피타바스타틴칼슘수화물, 페노피브레이트)' 등 2개 품목을 허가했다.피타바스타틴·페노피브레이트 복합제 허가 목록. 피타바스타틴·페노피브레이트 복합제는 고지혈증 치료제 성분 피타바스타틴과 중성지방 치료제 성분 페노피브레이트가 결합한 복합제다.관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰인다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐다.스타틴-중성지방 복합제 시장은 지속적으로 성장하면서 국내사에서 피타바스타틴·페노피브레이 복합제를 개발해 2019년부터 허가를 받았다.당시 한림제약(스타펜캡슐), 동광제약(피에프캡슐), 한국프라임제약(리페스틴캡슐), 삼진제약(뉴스타틴듀오캡슐), 동국제약(피타론에프캡슐), 지엘파마(리로우펜캡슐), 대원제약(업타바캡슐), 안국약품(페바로에프캡슐) 등 8개사가 개량신약이 승인됐다.유비스트에 따르면 허가된 8개 품목의 지난해 원외처방액 규모는 38억원 정도다.페바로가 9억1261만원으로 가장 처방이 많았으며, 업타바 7억2313만원, 리페스틴 5억3457만원, 스타펜 5억2528만원, 피에프 5억2405만원, 피타론에프 3억8710만원, 뉴스타틴듀오 1억6771만원의 원외처방금액을 보였다.해당 성분제제에 국내사들이 관심을 갖기 시작한건 2년전 부터다. 신풍제약과 서울제약 등이 생동성시험을 진행하면서 후발의약품 개발을 알렸다.특히 2019년 허가를 받은 선발 품목의 경우 등재 특허가 존재하지 않아 후발 주자들은 생동만으로 제제 개발 이후 출시까지 장벽이 높지 않았다는 분석이다.2019년 8개 품목의 개량신약 허가 이후, 올해만 13개 품목이 허가 목록에 이름을 올린 상태다.2025-08-28 18:22:29이혜경 -
 셀트리온·휴온스·바이넥스, '스타펜' 후발약 시장 진입[데일리팜=이혜경 기자] 이달부터 피타바스타틴·페노피브레이트 복합제 후발약 8개 품목이 급여목록에 등장한 가운데, 동일제제 3개 품목이 추가 허가됐다.식품의약품안전처는 11일 셀트리온제약의 '셀타펜캡슐', 휴온스의 '리바페논캡슐2/160mg', 바이넥스의 '피타뉴펜캡슐' 등 3개 품목을 허가했다.이번에 허가된 품목의 경우 피타바스타틴·페노피브레이트 선발품목인 '스타펜캡슐'을 생산하고 있는 한림제약이 위탁생산을 맡는다.스타펜 후발약은 모두 고지혈증 치료제 성분 피타바스타틴과 중성지방 치료제 성분 페노피브레이트가 결합한 복합제이다.피타바스타틴·페노피브레이트 복합제 허가 현황. 지난 2019년 4월 3일 8개 품목이 허가 된 이후, 올해 4월 30일 신풍제약의 '스타페노캡슐'과 제뉴파마의 '제피노정2/160mg', 대웅제약의 '바로페노정2/160mg', 위더스제약의 '타스페노캡슐', 종근당의 '피타로우에프정2/160mg', 대우제약 '피타스론정2/160mg', 위더스제약 '타스페노캡슐', 보령바이오파마 '리바펜캡슐', 이든파마 '피바펜캡슐'이 허가를 받으면서 눈길을 끈 바 있다.2019년 허가를 받은 선발 품목의 경우 등재 특허가 존재하지 않아 후발 주자들은 생동만으로 제제 개발 이후 출시까지 장벽이 높지 않은 상황이었기 때문이다.여기에 7월 1일자로 후발 8개 품목 모두 급여등재가 이뤄지면서 곧바로 출시가 이어질 것으로 보인다.지난 4월 허가 받은 품목의 경우 캡슐 제형은 신풍제약이, 정제 제형은 제뉴파마가 공급하며, 이들은 캡슐 또는 정당 872원으로 기존 품목과 동일한 약가가 책정됐다. 반면 위탁 업체 6곳은 캡슐 또는 정당 741원으로 약 15% 낮은 약가를 받아 가격 경쟁력을 확보했다.스타틴-중성지방 복합제 시장은 지속적으로 성장하고 있다.2012년 발매한 유영제약의 프라바페닉스(프라바스타틴나트륨-페노피브레이트)는 유비스트 기준 지난해 211억원의 원외처방액을 기록했고, 2017년 11월 출시한 건일제약의 로수메가(로수바스타틴칼슘-오메가3산에틸에스텔90)도 작년 69억원의 원외처방액으로 시장안착에 성공했다.피타바스타틴·페노피브레이트 성분제제는 관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰인다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐다.또한 페노피브레이트는 중성지방 감소 및 HDL 콜레스테롤 증가 효과를 보여 국내 가이드라인에서 중성지방 강하 약물로 권고하고 있으며, ACCORD 연구를 통해 고중성지방 및 저HDL 콜레스테롤 환자군에서 심혈관질환 발생 위험을 낮춘 것으로 알려졌다.유비스트에 따르면 처음 허가된 8개 품목의 지난해 원외처방액 규모는 38억원 정도다.페바로가 9억1261만원으로 가장 처방이 많았으며, 업타바 7억2313만원, 리페스틴 5억3457만원, 스타펜 5억2528만원, 피에프 5억2405만원, 피타론에프 3억8710만원, 뉴스타틴듀오 1억6771만원의 원외처방금액을 보였다.2025-07-11 17:42:42이혜경
셀트리온·휴온스·바이넥스, '스타펜' 후발약 시장 진입[데일리팜=이혜경 기자] 이달부터 피타바스타틴·페노피브레이트 복합제 후발약 8개 품목이 급여목록에 등장한 가운데, 동일제제 3개 품목이 추가 허가됐다.식품의약품안전처는 11일 셀트리온제약의 '셀타펜캡슐', 휴온스의 '리바페논캡슐2/160mg', 바이넥스의 '피타뉴펜캡슐' 등 3개 품목을 허가했다.이번에 허가된 품목의 경우 피타바스타틴·페노피브레이트 선발품목인 '스타펜캡슐'을 생산하고 있는 한림제약이 위탁생산을 맡는다.스타펜 후발약은 모두 고지혈증 치료제 성분 피타바스타틴과 중성지방 치료제 성분 페노피브레이트가 결합한 복합제이다.피타바스타틴·페노피브레이트 복합제 허가 현황. 지난 2019년 4월 3일 8개 품목이 허가 된 이후, 올해 4월 30일 신풍제약의 '스타페노캡슐'과 제뉴파마의 '제피노정2/160mg', 대웅제약의 '바로페노정2/160mg', 위더스제약의 '타스페노캡슐', 종근당의 '피타로우에프정2/160mg', 대우제약 '피타스론정2/160mg', 위더스제약 '타스페노캡슐', 보령바이오파마 '리바펜캡슐', 이든파마 '피바펜캡슐'이 허가를 받으면서 눈길을 끈 바 있다.2019년 허가를 받은 선발 품목의 경우 등재 특허가 존재하지 않아 후발 주자들은 생동만으로 제제 개발 이후 출시까지 장벽이 높지 않은 상황이었기 때문이다.여기에 7월 1일자로 후발 8개 품목 모두 급여등재가 이뤄지면서 곧바로 출시가 이어질 것으로 보인다.지난 4월 허가 받은 품목의 경우 캡슐 제형은 신풍제약이, 정제 제형은 제뉴파마가 공급하며, 이들은 캡슐 또는 정당 872원으로 기존 품목과 동일한 약가가 책정됐다. 반면 위탁 업체 6곳은 캡슐 또는 정당 741원으로 약 15% 낮은 약가를 받아 가격 경쟁력을 확보했다.스타틴-중성지방 복합제 시장은 지속적으로 성장하고 있다.2012년 발매한 유영제약의 프라바페닉스(프라바스타틴나트륨-페노피브레이트)는 유비스트 기준 지난해 211억원의 원외처방액을 기록했고, 2017년 11월 출시한 건일제약의 로수메가(로수바스타틴칼슘-오메가3산에틸에스텔90)도 작년 69억원의 원외처방액으로 시장안착에 성공했다.피타바스타틴·페노피브레이트 성분제제는 관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰인다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐다.또한 페노피브레이트는 중성지방 감소 및 HDL 콜레스테롤 증가 효과를 보여 국내 가이드라인에서 중성지방 강하 약물로 권고하고 있으며, ACCORD 연구를 통해 고중성지방 및 저HDL 콜레스테롤 환자군에서 심혈관질환 발생 위험을 낮춘 것으로 알려졌다.유비스트에 따르면 처음 허가된 8개 품목의 지난해 원외처방액 규모는 38억원 정도다.페바로가 9억1261만원으로 가장 처방이 많았으며, 업타바 7억2313만원, 리페스틴 5억3457만원, 스타펜 5억2528만원, 피에프 5억2405만원, 피타론에프 3억8710만원, 뉴스타틴듀오 1억6771만원의 원외처방금액을 보였다.2025-07-11 17:42:42이혜경 -
 혈우병 신약 '오비주르', 빅5 대형병원 처방권 안착[데일리팜=어윤호 기자] 혈우병A 출혈치료제 오비주르가 상급종합병원 처방권에 안착했다.관련 업계에 따르면 한국다케다제약의 성인 후천성 혈우병A(AHA, Acquired Hemophilia A) 환자의 출혈 치료제 오비주르(서스옥토코그알파)는 삼성서울병원, 서울대병원, 서울성모병원, 서울아산병원, 신촌세브란스병원 등 빅5 종합병원을 비롯해 경희대병원, 분당서울대병원 등 의료기관의 약사위원회(DC, Drug committee)를 통과했다.지난해 2월 보험급여 등재 후 꾸준하게 처방 영역을 넓혀가는 모습이다. 오비주르는 현재 성인 후천성 혈우병 A 환자의 출혈 치료에서 ▲항체 역가 5BU(Bethesda Unit) 초과인 경우 ▲항체 역가 5BU 이하인 환자가 항혈우인자를 고용량 투여한 후에도 반응이 없는 경우 ▲최근에 항체 역가 5BU 이하인 환자가 항혈우인자를 고용량 투여해도 반응이 없어 오비주르에 효과가 있었던 경우 급여 적용이 가능하다.오비주르는 2021년 7월 국내 희귀의약품으로 지정, 2023년 3월 국내 허가 직후 급여 평가에 돌입한 바 있다.이 약은 기존 우회인자 약제와는 달리 AHA 적응증을 가진 혈액응고 8인자를 대체하는 치료제이다.인간과 유사한 돼지 혈액응고 8인자에서 B-도메인을 제거하여 만든 유전자재조합 제제로, 자가 면역 항체에 의해 쉽게 인식되지 않기 때문에 비활성화된 인간 혈액응고 8인자를 대체하여 혈액응고를 돕고 출혈 조절에 도움을 줄 수 있다.이러한 기전으로 후천성 혈우병 A 치료제 중 유일하게 표준분석법을 통해 혈액응고 8인자 수치를 안정적으로 모니터링해 개별 맞춤 용량 치료가 가능하다.한편 후천성 혈우병A 환자 28명을 대상으로 오비주르의 유효성을 평가한 전향적, 비-무작위배정, 오픈-라벨 2/3상 연구 결과, 오비주르로 치료받은 환자는 모두 첫 투여 후 24시간 째 평가 시 모든 초기 출혈 에피소드에 대해 긍정적 반응(Positive response)을 보였다. 긍정적 반응은 출혈이 중단되거나 감소되고 임상적 개선이 있거나 혈액응고 8인자 활성이 목표치 이상으로 나타난 경우를 의미한다.최종 투약 시점에서(투여 후 2주 이내) 치료성공률은 85.7%(24/28명)였으며 치료 성공률은 오비주르를 1차치료제로 사용한 환자군에서 더 높았다.1차치료에 오비주르주를 투여 받은 환자군의 치료성공률은 94%(16/17명)였고 2차치료에 오비주르주를 투여 받은 환자군의 치료성공률은 73%(8/11명)였다. 오비주르와 관련된 중증 이상사례나 사망은 발생하지 않았다.2025-06-25 06:25:17어윤호
혈우병 신약 '오비주르', 빅5 대형병원 처방권 안착[데일리팜=어윤호 기자] 혈우병A 출혈치료제 오비주르가 상급종합병원 처방권에 안착했다.관련 업계에 따르면 한국다케다제약의 성인 후천성 혈우병A(AHA, Acquired Hemophilia A) 환자의 출혈 치료제 오비주르(서스옥토코그알파)는 삼성서울병원, 서울대병원, 서울성모병원, 서울아산병원, 신촌세브란스병원 등 빅5 종합병원을 비롯해 경희대병원, 분당서울대병원 등 의료기관의 약사위원회(DC, Drug committee)를 통과했다.지난해 2월 보험급여 등재 후 꾸준하게 처방 영역을 넓혀가는 모습이다. 오비주르는 현재 성인 후천성 혈우병 A 환자의 출혈 치료에서 ▲항체 역가 5BU(Bethesda Unit) 초과인 경우 ▲항체 역가 5BU 이하인 환자가 항혈우인자를 고용량 투여한 후에도 반응이 없는 경우 ▲최근에 항체 역가 5BU 이하인 환자가 항혈우인자를 고용량 투여해도 반응이 없어 오비주르에 효과가 있었던 경우 급여 적용이 가능하다.오비주르는 2021년 7월 국내 희귀의약품으로 지정, 2023년 3월 국내 허가 직후 급여 평가에 돌입한 바 있다.이 약은 기존 우회인자 약제와는 달리 AHA 적응증을 가진 혈액응고 8인자를 대체하는 치료제이다.인간과 유사한 돼지 혈액응고 8인자에서 B-도메인을 제거하여 만든 유전자재조합 제제로, 자가 면역 항체에 의해 쉽게 인식되지 않기 때문에 비활성화된 인간 혈액응고 8인자를 대체하여 혈액응고를 돕고 출혈 조절에 도움을 줄 수 있다.이러한 기전으로 후천성 혈우병 A 치료제 중 유일하게 표준분석법을 통해 혈액응고 8인자 수치를 안정적으로 모니터링해 개별 맞춤 용량 치료가 가능하다.한편 후천성 혈우병A 환자 28명을 대상으로 오비주르의 유효성을 평가한 전향적, 비-무작위배정, 오픈-라벨 2/3상 연구 결과, 오비주르로 치료받은 환자는 모두 첫 투여 후 24시간 째 평가 시 모든 초기 출혈 에피소드에 대해 긍정적 반응(Positive response)을 보였다. 긍정적 반응은 출혈이 중단되거나 감소되고 임상적 개선이 있거나 혈액응고 8인자 활성이 목표치 이상으로 나타난 경우를 의미한다.최종 투약 시점에서(투여 후 2주 이내) 치료성공률은 85.7%(24/28명)였으며 치료 성공률은 오비주르를 1차치료제로 사용한 환자군에서 더 높았다.1차치료에 오비주르주를 투여 받은 환자군의 치료성공률은 94%(16/17명)였고 2차치료에 오비주르주를 투여 받은 환자군의 치료성공률은 73%(8/11명)였다. 오비주르와 관련된 중증 이상사례나 사망은 발생하지 않았다.2025-06-25 06:25:17어윤호 -
 '피타바+페노피브릭산' 복합제 출격...3개 품목 동시허가피타바스타틴+페노피브레이트 선발품목인 스타펜캡슐. [데일리팜=이혜경 기자] 피타바스타틴과 페노피브릭산을 결합한 이상지질혈증 복합제가 처음 등장했다.식품의약품안전처는 29일 한국유나이트제약의 '피타릭캡슐'과 제이더블유중외제약의 '리바로페노캡슐2/110mg', 한국바이오켐제약의 '피타브릭캡슐' 등 3개 품목을 허가했다.그동안 한림제약(스타펜캡슐)을 수탁사로 동광제약(피에프캡슐), 한국프라임제약(리페스틴캡슐), 삼진제약(뉴스타틴듀오캡슐), 동국제약(피타론에프캡슐), 지엘파마(리로우펜캡슐), 대원제약(업타바캡슐), 안국약품(페바로에프캡슐) 등 피타바스타틴과 페노피브레이트 복합제 허가가 이어졌지만, 페노피브릭산을 조합한 복합제는 처음이다.페노피브릭산 성분의 오리지널 제제는 한미약품의 '페노시드캡슐'이다.페노피브릭산과 페노피브레이트는 같은 계열의 약물이지만, 화학 구조가 달라 작용방식에 있어 차이를 나타낸다. 페노피브레이트는 공복 및 식후 복용에 따라 흡수율 차이가 크므로, 효과를 높이기 위해서는 반드시 식후 복용해야 한다.반면 페노피브릭산은 페노피브레이트의 활성 성분으로, 식사 여부와 무관하게 복용 즉시 체내에서 흡수될 수 있다.이번에 허가 받은 피타바·페노피브릭산 복합제 또한 피타바·페노피브레이트 복합제와 달리 식후 상관없이 복용할 수 있다.피타바·중성지방 치료제 복합제 모두 관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰인다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐다.페노피브릭산은 아포지단백 C-III(지방분해 효소의 작용을 저해하는 단백질)의 기능을 저하시키는 PPAR-alpha 인자의 활성을 유도해 지방분해 효과를 증폭, 혈중 중성지방의 수치를 낮추는 기전이다.한편 피타바·페노피브레이트 복합제의 경우 지난 2019년 한림제약(스타펜캡슐)을 수탁사로 동광제약(피에프캡슐), 한국프라임제약(리페스틴캡슐), 삼진제약(뉴스타틴듀오캡슐), 동국제약(피타론에프캡슐), 지엘파마(리로우펜캡슐), 대원제약(업타바캡슐), 안국약품(페바로에프캡슐) 등 8개사가 개량신약으로 허가 받은 이후, 올해까지 16개 품목이 허가를 받은 상황이다.유비스트에 따르면 지난해까지 허가된 8개 품목의 지난해 원외처방액 규모는 38억원 정도다.페바로가 9억1261만원으로 가장 처방이 많았으며, 업타바 7억2313만원, 리페스틴 5억3457만원, 스타펜 5억2528만원, 피에프 5억2405만원, 피타론에프 3억8710만원, 뉴스타틴듀오 1억6771만원의 원외처방금액을 보였다.2025-05-30 10:43:01이혜경
'피타바+페노피브릭산' 복합제 출격...3개 품목 동시허가피타바스타틴+페노피브레이트 선발품목인 스타펜캡슐. [데일리팜=이혜경 기자] 피타바스타틴과 페노피브릭산을 결합한 이상지질혈증 복합제가 처음 등장했다.식품의약품안전처는 29일 한국유나이트제약의 '피타릭캡슐'과 제이더블유중외제약의 '리바로페노캡슐2/110mg', 한국바이오켐제약의 '피타브릭캡슐' 등 3개 품목을 허가했다.그동안 한림제약(스타펜캡슐)을 수탁사로 동광제약(피에프캡슐), 한국프라임제약(리페스틴캡슐), 삼진제약(뉴스타틴듀오캡슐), 동국제약(피타론에프캡슐), 지엘파마(리로우펜캡슐), 대원제약(업타바캡슐), 안국약품(페바로에프캡슐) 등 피타바스타틴과 페노피브레이트 복합제 허가가 이어졌지만, 페노피브릭산을 조합한 복합제는 처음이다.페노피브릭산 성분의 오리지널 제제는 한미약품의 '페노시드캡슐'이다.페노피브릭산과 페노피브레이트는 같은 계열의 약물이지만, 화학 구조가 달라 작용방식에 있어 차이를 나타낸다. 페노피브레이트는 공복 및 식후 복용에 따라 흡수율 차이가 크므로, 효과를 높이기 위해서는 반드시 식후 복용해야 한다.반면 페노피브릭산은 페노피브레이트의 활성 성분으로, 식사 여부와 무관하게 복용 즉시 체내에서 흡수될 수 있다.이번에 허가 받은 피타바·페노피브릭산 복합제 또한 피타바·페노피브레이트 복합제와 달리 식후 상관없이 복용할 수 있다.피타바·중성지방 치료제 복합제 모두 관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰인다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐다.페노피브릭산은 아포지단백 C-III(지방분해 효소의 작용을 저해하는 단백질)의 기능을 저하시키는 PPAR-alpha 인자의 활성을 유도해 지방분해 효과를 증폭, 혈중 중성지방의 수치를 낮추는 기전이다.한편 피타바·페노피브레이트 복합제의 경우 지난 2019년 한림제약(스타펜캡슐)을 수탁사로 동광제약(피에프캡슐), 한국프라임제약(리페스틴캡슐), 삼진제약(뉴스타틴듀오캡슐), 동국제약(피타론에프캡슐), 지엘파마(리로우펜캡슐), 대원제약(업타바캡슐), 안국약품(페바로에프캡슐) 등 8개사가 개량신약으로 허가 받은 이후, 올해까지 16개 품목이 허가를 받은 상황이다.유비스트에 따르면 지난해까지 허가된 8개 품목의 지난해 원외처방액 규모는 38억원 정도다.페바로가 9억1261만원으로 가장 처방이 많았으며, 업타바 7억2313만원, 리페스틴 5억3457만원, 스타펜 5억2528만원, 피에프 5억2405만원, 피타론에프 3억8710만원, 뉴스타틴듀오 1억6771만원의 원외처방금액을 보였다.2025-05-30 10:43:01이혜경 -
 '케이캡' 첫 제네릭 등장...국내 개발 탄저백신 허가[데일리팜=이혜경 기자] 경동제약이 '케이캡정'의 제네릭 '테고잔정'을 국내에서 처음으로 허가 받았습니다.케이캡 제네릭 허가를 위해 성분명 테고프라잔을 앞세워 '테고' 관련 상표권을 출원한 곳이 20여개사가 넘고 있어 앞으로 케이캡 제네릭 시장 경쟁이 더 치열해질 전망입니다.지난달에는 국내 개발 유전자재조합 탄저백신인 녹십자의 '배리트락스'가 국산신약 39호로 허가 받기도 했습니다.베리트락스는 탄저균으로 인한 감염을 예방하는 항체의 생성을 유도하기 위해 탄저균의 외독소 구성성분 중 방어항원 단백질을 유전자재조합 기술을 이용해 제조한 것으로, 성인에서 탄저균으로 인한 감염증의 노출 전 예방을 목적으로 하는 백신입니다.또 지난 4월에는 피타바스타틴·페노피브레이트 복합제 후발주자가 6년만에 대거 등장하기도 했습니다. 식약처의 4월 의약품 허가 현황을 보면, 일반의약품 63개 품목, 전문의약품 66개 품목 등 129개 품목이 허가를 받았습니다.식약처는 매달 의료제품 허가현황을 공개하고 있는데, 정보공개 대상은 신약, 자료제출의약품, 조건부 허가 의약품 등에 한정하고 있습니다. ◆일반의약품=올해 4월 허가(신고)된 일반약은 모두 63개 품목으로 나타났습니다.제조법을 공인한 표준제조기준 품목이 36개 품목, 제네릭 등 기타품목이 25개 품목을 보였습니다. 안·유 심사 제외 품목은 2개 품목으로 집계됐습니다.동아제약 '베나치오프로액' (4월 30일, 표준제조기준)동아제약이 소화제 '베나치오' 브랜드 라인업을 확대합니다. 이달에만 '베나치오엠액'과 '베나치오프로액' 등 2개 제품을 허가 받았습니다.'아픈 배가 낫지요'라는 의미를 담고 있는 베나치오는 기름진 음식·육류 소화에 좋은 회향, 창출 등 생약성분을 함유한 무탄산 소화제입니다.베나치오 브랜드는 연간 2860만병이 판매됩니다. 1.1초당 1병씩 판매되는 셈입니다.지난 2008년 '베나치오액'을 허가 받은 이후 지금까지 '베나치오엑스액', '베나치오에프액', '베나치오이지액', '베나치오키즈액'을 선보였으며, 이번에 '베나치오엠액'과 '베나치오프로액'을 브랜드에 포함시켰습니다.이번에 허가 받은 베나치오 프로액은 탄산이 없으며, 위장 운동을 촉진해 소화불량을 해소하는 효능효과를 갖고 있습니다. 동성제약 '펙소페틴정120mg' (4월 28일, 제네릭)동성제약이 처방전 없이 약국에서 구매 가능한 알레르기 비염약 '펙소페틴정'을 허가 받았습니다.펙소페틴은 펙소페나딘염산염 성분제제로 꽃가루 알레르기 또는 기타 상기도 알레르기 치료제입니다.펙소페나딘은 3세대 항히스타민 성분으로 30mg, 60mg, 120mg, 180mg 등 4개 용량으로 구성됐는데, 이 중 60mg과 120mg은 일반의약품으로 알레르기 치료에 쓰입니다.60mg 용량의 경우 지난 2022년 알피바이오가 120mg 용량을 절반으로 줄여 캡슐제형으로 개발해 허가 받은 '노즈알연질캡슐'에 이어 지난해 유유제약이 정제 형태의 '페소지엔정'을 허가 받으면서 지속적으로 국내 제약회사들이 개발을 이어가고 있습니다.펙소페나딘은 기존 항히스타민제 대비 졸음이 쏟아지고 몸이 늘어지는 현상을 유발하는 진정 작용 발생빈도가 낮아 복용 후 졸음 부작용이 적은 약물로 평가받고 있습니다.알레르기 비염 증상은 일반적으로 다양한 알레르기 항원, 꽃가루나 황사 등 외부 요인으로 발생하며 일시적인 증상에 그칠 수 있지만, 환절기의 경우 증상이 수일간 지속되기 쉽습니다.페소페나딘 120mg 정제는 졸음 걱정은 줄이고, 1시간 이내에 효과 발현, 최대 24시간 지속 등의 특징을 갖고 있습니다.◆전문의약품=올해 4월 허가 받은 전문의약품은 모두 66개 품목으로 나타났습니다.신약 1개 품목, 제네릭 등 기타 유형이 32개 품목을 차지했습니다.의약품이나 염기, 제형 따위의 변화로 안전성, 유효성 심사를 받아 기존 약을 다르게 만든 자료제출의약품은 33개 품목으로 나타났습니다. 경동제약 '테고잔정' (4월 1일, 제네릭)P-CAB 계열 위식도 역류질환 치료제 '케이캡(테고프라잔)'의 국내 첫 제네릭이 허가를 받았습니다.경동제약의 '테고잔(테고프라잔)' 25mg, 50mg 등 2개 용량이 주인공입니다.현재 케이캡을 보유하고 있는 HK이노엔과 제네릭사들이 결정형특허 분쟁을 진행 중인 만큼, 첫 제네릭이 허가를 받았지만 출시는 불투명한 상태입니다.하지만 케이캡 제네릭 허가를 위해 성분명 테고프라잔을 앞세워 '테고' 관련 상표권을 출원한 곳이 20여개사가 넘고 있어 경동제약에 이어 다른 제약사들도 미리 허가를 받아놓을 가능성도 높아졌습니다.현재 출원된 상표권을 보면 경동제약을 비롯해 한국휴텍스제약 '테고캡', 환인제약 '테고닌', 국제약품 '테고란', 삼일제약 '테고에스', 동구바이오제약 '테고톤', 팜젠사이언스 '테고맥스', 메디카코리아 '테고프라', GC녹십자 '네오테고', 진양제약 '케이프라', 라이트팜텍 '라이트프라잔', 삼아제약 '프라잔' 등이 있습니다.케이캡은 2개 특허가 등재돼 있습니다. 케이캡은 2031년 8월 만료되는 물질특허와 2036년 3월 만료되는 결정형특허로 보호됩니다. 여기에 미등재 특허로 2036년 6월과 12월 각각 만료되는 용도특허·제제특허가 있습니다.제네릭사들은 지난 2022년 12월 케이캡 결정형특허에 소극적 권리범위확인 심판을 청구했으며, 현재까지 80여개 기업이 같은 심판을 청구하며 특허 도전 대열에 합류했습니다.대원제약 '엠파메트서방정' (4월 3일, 자료제출의약품)대원제약이 SGLT-2 억제제 계열의 당뇨병치료제 '자디앙듀오(엠파글리플로진·메트포르민)'에는 없는 제형인 서방형 제제인 '엠파메트서방정' 10/1000mg, 25/1000mg을 허가 받았습니다.자디앙듀오 서방정의 경우 지난해 동광제약이 '엠플로엠서방정10/1000mg'을 허가 받은 데 이어, 올해 동구바이오제약, 에이프로젠바이오로직스, 대원제약 등이 잇따라 허가를 받고 있습니다.서방형 제형은 약물이 치료 혈중 농도에 도달 후 일정시간 지속되면서 일반 제형 약물보다 복용횟수가 적다는 장점이 있어, 자디앙듀오의 용법은 1일 2회이지만, 엠플로엠서방정은 1일 1회입니다.오리지널에는 없는 서방형 제제 개발이 늘어나는 이유는 이미 자디앙듀오에 대한 품목허가가 200여개에 달하고 있기 때문입니다.자디앙듀오는 SGLT-2 억제제 '자디앙'과 메트포르민을 결합한 당뇨병 복합제로 SGLT-2 억제제와 다른 기전으로 혈당을 조절하는 만큼, 혈당을 더욱 효과적으로 관리할 수 있다는 특징이 있습니다.자디앙듀오 후발약들은 후속특허를 회피해 우판권은 따냈지만, 아직 물질특허가 만료되지 않았습니다. 물질특허는 오는 2025년 10월 23일 만료될 예정으로, 자디앙듀오 제네릭은 특허가 만료된 이후 출시될 전망입니다.녹십자 '배리트락스주' (4월 7일, 신약)녹십자가 생물테러 등 국가 위기 상황 대비를 위해 질병관리청과 공동 개발한 탄저백신 '배리트락스주'를 허가 받았습니다.배리트락스는 국산 신약 39호로 이름을 올렸습니다.탄저균은 열악한 환경에서도 장기간 생존이 가능해 공기 중 살포가 용이한 1급 법정 감염병입니다. 치명률도 97%에 달해 테러에 생물학 무기로 악용될 가능성이 높습니다.배리트락스는 2종의 탄저균 독소인자를 세포 내로 전달해 주는 방어항원(PA) 단백질을 유전자 재조합 기술을 이용해 만들어 낸 백신입니다.백신을 접종함으로써 방어항원을 통한 면역반응을 일으켜 탄저병을 예방할 수 있습니다.기존 백신은 세균 배양을 통해 만들기 때문에 미량의 탄저균 독소인자가 남아 부작용을 유발할 수 있지만, 녹십자의 백신은 단백질 항원을 기반으로 해 이러한 부작용을 없앴습니다. 더 안전한 재조합 단백질 방식으로 탄저백신을 개발한 것은 세계 최초입니다.탄저균은 치명률이 높아 다수를 대상으로 하는 임상3상 시험이 수행되기 어렵습니다.질병청은 '공중보건 위기대응 의료제품의 개발 촉진 및 긴급 공급을 위한 특별법'에 따라 임상3상 대체 동물실험을 수행했으며, 그 결과 동물모델에서 백신 4회차 접종 후 6개월이 지나도 높은 탄저 독소 중화 항체가가 유지됐고 탄저균 포자에 대해서도 높은 생존율이 확인돼 뛰어난 효과를 입증했습니다.대웅제약 '바로페노정' (4월 30일, 자료제출의약품)피타바스타틴·페노피브레이트 복합제 후발주자가 6년만에 대거 등장했습니다.대웅제약의 '바로페노정2/160mg' 뿐 아니라 신풍제약의 '스타페노캡슐'과 제뉴파마의 '제피노정2/160mg', 위더스제약의 '타스페노캡슐', 종근당의 '피타로우에프정2/160mg', 대우제약 '피타스론정2/160mg', 보령바이오파마 '리바펜캡슐', 이든파마 '피바펜캡슐' 등 8개사가 피타바스타틴 복합제를 허가 받았습니다.이번에 허가된 품목의 경우 제뉴파마가 수탁사로 대웅제약, 종근당, 대우제약의 제품을 생산하게 되며 신풍제약이 위더스제약, 이든파마, 보령바이오파마의 제품을 위탁 생산합니다.이들 제품은 모두 고지혈증 치료제 성분 피타바스타틴과 중성지방 치료제 성분 페노피브레이트가 결합한 복합제입니다.피타바스타틴·페노피브레이트 성분제제는 관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰입니다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐습니다.또한 페노피브레이트는 중성지방 감소 및 HDL 콜레스테롤 증가 효과를 보여 국내 가이드라인에서 중성지방 강하 약물로 권고하고 있으며, ACCORD 연구를 통해 고중성지방 및 저HDL 콜레스테롤 환자군에서 심혈관질환 발생 위험을 낮춘 것으로 알려졌습니다.2025-05-06 10:56:13이혜경
'케이캡' 첫 제네릭 등장...국내 개발 탄저백신 허가[데일리팜=이혜경 기자] 경동제약이 '케이캡정'의 제네릭 '테고잔정'을 국내에서 처음으로 허가 받았습니다.케이캡 제네릭 허가를 위해 성분명 테고프라잔을 앞세워 '테고' 관련 상표권을 출원한 곳이 20여개사가 넘고 있어 앞으로 케이캡 제네릭 시장 경쟁이 더 치열해질 전망입니다.지난달에는 국내 개발 유전자재조합 탄저백신인 녹십자의 '배리트락스'가 국산신약 39호로 허가 받기도 했습니다.베리트락스는 탄저균으로 인한 감염을 예방하는 항체의 생성을 유도하기 위해 탄저균의 외독소 구성성분 중 방어항원 단백질을 유전자재조합 기술을 이용해 제조한 것으로, 성인에서 탄저균으로 인한 감염증의 노출 전 예방을 목적으로 하는 백신입니다.또 지난 4월에는 피타바스타틴·페노피브레이트 복합제 후발주자가 6년만에 대거 등장하기도 했습니다. 식약처의 4월 의약품 허가 현황을 보면, 일반의약품 63개 품목, 전문의약품 66개 품목 등 129개 품목이 허가를 받았습니다.식약처는 매달 의료제품 허가현황을 공개하고 있는데, 정보공개 대상은 신약, 자료제출의약품, 조건부 허가 의약품 등에 한정하고 있습니다. ◆일반의약품=올해 4월 허가(신고)된 일반약은 모두 63개 품목으로 나타났습니다.제조법을 공인한 표준제조기준 품목이 36개 품목, 제네릭 등 기타품목이 25개 품목을 보였습니다. 안·유 심사 제외 품목은 2개 품목으로 집계됐습니다.동아제약 '베나치오프로액' (4월 30일, 표준제조기준)동아제약이 소화제 '베나치오' 브랜드 라인업을 확대합니다. 이달에만 '베나치오엠액'과 '베나치오프로액' 등 2개 제품을 허가 받았습니다.'아픈 배가 낫지요'라는 의미를 담고 있는 베나치오는 기름진 음식·육류 소화에 좋은 회향, 창출 등 생약성분을 함유한 무탄산 소화제입니다.베나치오 브랜드는 연간 2860만병이 판매됩니다. 1.1초당 1병씩 판매되는 셈입니다.지난 2008년 '베나치오액'을 허가 받은 이후 지금까지 '베나치오엑스액', '베나치오에프액', '베나치오이지액', '베나치오키즈액'을 선보였으며, 이번에 '베나치오엠액'과 '베나치오프로액'을 브랜드에 포함시켰습니다.이번에 허가 받은 베나치오 프로액은 탄산이 없으며, 위장 운동을 촉진해 소화불량을 해소하는 효능효과를 갖고 있습니다. 동성제약 '펙소페틴정120mg' (4월 28일, 제네릭)동성제약이 처방전 없이 약국에서 구매 가능한 알레르기 비염약 '펙소페틴정'을 허가 받았습니다.펙소페틴은 펙소페나딘염산염 성분제제로 꽃가루 알레르기 또는 기타 상기도 알레르기 치료제입니다.펙소페나딘은 3세대 항히스타민 성분으로 30mg, 60mg, 120mg, 180mg 등 4개 용량으로 구성됐는데, 이 중 60mg과 120mg은 일반의약품으로 알레르기 치료에 쓰입니다.60mg 용량의 경우 지난 2022년 알피바이오가 120mg 용량을 절반으로 줄여 캡슐제형으로 개발해 허가 받은 '노즈알연질캡슐'에 이어 지난해 유유제약이 정제 형태의 '페소지엔정'을 허가 받으면서 지속적으로 국내 제약회사들이 개발을 이어가고 있습니다.펙소페나딘은 기존 항히스타민제 대비 졸음이 쏟아지고 몸이 늘어지는 현상을 유발하는 진정 작용 발생빈도가 낮아 복용 후 졸음 부작용이 적은 약물로 평가받고 있습니다.알레르기 비염 증상은 일반적으로 다양한 알레르기 항원, 꽃가루나 황사 등 외부 요인으로 발생하며 일시적인 증상에 그칠 수 있지만, 환절기의 경우 증상이 수일간 지속되기 쉽습니다.페소페나딘 120mg 정제는 졸음 걱정은 줄이고, 1시간 이내에 효과 발현, 최대 24시간 지속 등의 특징을 갖고 있습니다.◆전문의약품=올해 4월 허가 받은 전문의약품은 모두 66개 품목으로 나타났습니다.신약 1개 품목, 제네릭 등 기타 유형이 32개 품목을 차지했습니다.의약품이나 염기, 제형 따위의 변화로 안전성, 유효성 심사를 받아 기존 약을 다르게 만든 자료제출의약품은 33개 품목으로 나타났습니다. 경동제약 '테고잔정' (4월 1일, 제네릭)P-CAB 계열 위식도 역류질환 치료제 '케이캡(테고프라잔)'의 국내 첫 제네릭이 허가를 받았습니다.경동제약의 '테고잔(테고프라잔)' 25mg, 50mg 등 2개 용량이 주인공입니다.현재 케이캡을 보유하고 있는 HK이노엔과 제네릭사들이 결정형특허 분쟁을 진행 중인 만큼, 첫 제네릭이 허가를 받았지만 출시는 불투명한 상태입니다.하지만 케이캡 제네릭 허가를 위해 성분명 테고프라잔을 앞세워 '테고' 관련 상표권을 출원한 곳이 20여개사가 넘고 있어 경동제약에 이어 다른 제약사들도 미리 허가를 받아놓을 가능성도 높아졌습니다.현재 출원된 상표권을 보면 경동제약을 비롯해 한국휴텍스제약 '테고캡', 환인제약 '테고닌', 국제약품 '테고란', 삼일제약 '테고에스', 동구바이오제약 '테고톤', 팜젠사이언스 '테고맥스', 메디카코리아 '테고프라', GC녹십자 '네오테고', 진양제약 '케이프라', 라이트팜텍 '라이트프라잔', 삼아제약 '프라잔' 등이 있습니다.케이캡은 2개 특허가 등재돼 있습니다. 케이캡은 2031년 8월 만료되는 물질특허와 2036년 3월 만료되는 결정형특허로 보호됩니다. 여기에 미등재 특허로 2036년 6월과 12월 각각 만료되는 용도특허·제제특허가 있습니다.제네릭사들은 지난 2022년 12월 케이캡 결정형특허에 소극적 권리범위확인 심판을 청구했으며, 현재까지 80여개 기업이 같은 심판을 청구하며 특허 도전 대열에 합류했습니다.대원제약 '엠파메트서방정' (4월 3일, 자료제출의약품)대원제약이 SGLT-2 억제제 계열의 당뇨병치료제 '자디앙듀오(엠파글리플로진·메트포르민)'에는 없는 제형인 서방형 제제인 '엠파메트서방정' 10/1000mg, 25/1000mg을 허가 받았습니다.자디앙듀오 서방정의 경우 지난해 동광제약이 '엠플로엠서방정10/1000mg'을 허가 받은 데 이어, 올해 동구바이오제약, 에이프로젠바이오로직스, 대원제약 등이 잇따라 허가를 받고 있습니다.서방형 제형은 약물이 치료 혈중 농도에 도달 후 일정시간 지속되면서 일반 제형 약물보다 복용횟수가 적다는 장점이 있어, 자디앙듀오의 용법은 1일 2회이지만, 엠플로엠서방정은 1일 1회입니다.오리지널에는 없는 서방형 제제 개발이 늘어나는 이유는 이미 자디앙듀오에 대한 품목허가가 200여개에 달하고 있기 때문입니다.자디앙듀오는 SGLT-2 억제제 '자디앙'과 메트포르민을 결합한 당뇨병 복합제로 SGLT-2 억제제와 다른 기전으로 혈당을 조절하는 만큼, 혈당을 더욱 효과적으로 관리할 수 있다는 특징이 있습니다.자디앙듀오 후발약들은 후속특허를 회피해 우판권은 따냈지만, 아직 물질특허가 만료되지 않았습니다. 물질특허는 오는 2025년 10월 23일 만료될 예정으로, 자디앙듀오 제네릭은 특허가 만료된 이후 출시될 전망입니다.녹십자 '배리트락스주' (4월 7일, 신약)녹십자가 생물테러 등 국가 위기 상황 대비를 위해 질병관리청과 공동 개발한 탄저백신 '배리트락스주'를 허가 받았습니다.배리트락스는 국산 신약 39호로 이름을 올렸습니다.탄저균은 열악한 환경에서도 장기간 생존이 가능해 공기 중 살포가 용이한 1급 법정 감염병입니다. 치명률도 97%에 달해 테러에 생물학 무기로 악용될 가능성이 높습니다.배리트락스는 2종의 탄저균 독소인자를 세포 내로 전달해 주는 방어항원(PA) 단백질을 유전자 재조합 기술을 이용해 만들어 낸 백신입니다.백신을 접종함으로써 방어항원을 통한 면역반응을 일으켜 탄저병을 예방할 수 있습니다.기존 백신은 세균 배양을 통해 만들기 때문에 미량의 탄저균 독소인자가 남아 부작용을 유발할 수 있지만, 녹십자의 백신은 단백질 항원을 기반으로 해 이러한 부작용을 없앴습니다. 더 안전한 재조합 단백질 방식으로 탄저백신을 개발한 것은 세계 최초입니다.탄저균은 치명률이 높아 다수를 대상으로 하는 임상3상 시험이 수행되기 어렵습니다.질병청은 '공중보건 위기대응 의료제품의 개발 촉진 및 긴급 공급을 위한 특별법'에 따라 임상3상 대체 동물실험을 수행했으며, 그 결과 동물모델에서 백신 4회차 접종 후 6개월이 지나도 높은 탄저 독소 중화 항체가가 유지됐고 탄저균 포자에 대해서도 높은 생존율이 확인돼 뛰어난 효과를 입증했습니다.대웅제약 '바로페노정' (4월 30일, 자료제출의약품)피타바스타틴·페노피브레이트 복합제 후발주자가 6년만에 대거 등장했습니다.대웅제약의 '바로페노정2/160mg' 뿐 아니라 신풍제약의 '스타페노캡슐'과 제뉴파마의 '제피노정2/160mg', 위더스제약의 '타스페노캡슐', 종근당의 '피타로우에프정2/160mg', 대우제약 '피타스론정2/160mg', 보령바이오파마 '리바펜캡슐', 이든파마 '피바펜캡슐' 등 8개사가 피타바스타틴 복합제를 허가 받았습니다.이번에 허가된 품목의 경우 제뉴파마가 수탁사로 대웅제약, 종근당, 대우제약의 제품을 생산하게 되며 신풍제약이 위더스제약, 이든파마, 보령바이오파마의 제품을 위탁 생산합니다.이들 제품은 모두 고지혈증 치료제 성분 피타바스타틴과 중성지방 치료제 성분 페노피브레이트가 결합한 복합제입니다.피타바스타틴·페노피브레이트 성분제제는 관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰입니다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐습니다.또한 페노피브레이트는 중성지방 감소 및 HDL 콜레스테롤 증가 효과를 보여 국내 가이드라인에서 중성지방 강하 약물로 권고하고 있으며, ACCORD 연구를 통해 고중성지방 및 저HDL 콜레스테롤 환자군에서 심혈관질환 발생 위험을 낮춘 것으로 알려졌습니다.2025-05-06 10:56:13이혜경 -
 피타바스타틴-페노피브레이트 후발약 대거 허가피타바스타틴+페노피브레이트 선발품목인 스타펜캡슐[데일리팜=이혜경 기자] 피타바스타틴·페노피브레이트 복합제 후발주자가 6년만에 대거 등장했다.식품의약품안전처는 30일 신풍제약의 '스타페노캡슐'과 제뉴파마의 '제피노정2/160mg', 대웅제약의 '바로페노정2/160mg', 위더스제약의 '타스페노캡슐', 종근당의 '피타로우에프정2/160mg', 대우제약 '피타스론정2/160mg', 위더스제약 '타스페노캡슐', 보령바이오파마 '리바펜캡슐', 이든파마 '피바펜캡슐'을 허가했다.모두 고지혈증 치료제 성분 피타바스타틴과 중성지방 치료제 성분 페노피브레이트가 결합한 복합제이다.이번에 허가된 품목의 경우 제뉴파마가 수탁사로 대웅제약, 종근당, 대우제약의 제품을 생산하게 되며 신풍제약이 위더스제약, 이든파마, 보령바이오파마의 제품을 위탁 생산한다.스타틴-중성지방 복합제 시장은 지속적으로 성장하고 있다.2012년 발매한 유영제약의 프라바페닉스(프라바스타틴나트륨-페노피브레이트)는 유비스트 기준 지난해 211억원의 원외처방액을 기록했고, 2017년 11월 출시한 건일제약의 로수메가(로수바스타틴칼슘-오메가3산에틸에스텔90)도 작년 69억원의 원외처방액으로 시장안착에 성공했다.피타바스타틴·페노피브레이트 성분제제는 관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰인다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐다.또한 페노피브레이트는 중성지방 감소 및 HDL 콜레스테롤 증가 효과를 보여 국내 가이드라인에서 중성지방 강하 약물로 권고하고 있으며, ACCORD 연구를 통해 고중성지방 및 저HDL 콜레스테롤 환자군에서 심혈관질환 발생 위험을 낮춘 것으로 알려졌다.지난 2019년 한림제약(스타펜캡슐)을 수탁사로 동광제약(피에프캡슐), 한국프라임제약(리페스틴캡슐), 삼진제약(뉴스타틴듀오캡슐), 동국제약(피타론에프캡슐), 지엘파마(리로우펜캡슐), 대원제약(업타바캡슐), 안국약품(페바로에프캡슐) 등 8개사가 개량신약으로 허가 받은바 있다.유비스트에 따르면 허가된 8개 품목의 지난해 원외처방액 규모는 38억원 정도다.페바로가 9억1261만원으로 가장 처방이 많았으며, 업타바 7억2313만원, 리페스틴 5억3457만원, 스타펜 5억2528만원, 피에프 5억2405만원, 피타론에프 3억8710만원, 뉴스타틴듀오 1억6771만원의 원외처방금액을 보였다.해당 성분제제에 국내사들이 관심을 갖기 시작한건 2년전 부터다. 신풍제약과 서울제약 등이 생동성시험을 진행하면서 후발의약품 개발을 알렸다.특히 2019년 허가를 받은 선발 품목의 경우 등재 특허가 존재하지 않아 후발 주자들은 생동만으로 제제 개발 이후 출시까지 장벽이 높지 않았다는 분석이다.고지혈증 복합제 시장 쟁탈전2025-04-30 16:58:21이혜경
피타바스타틴-페노피브레이트 후발약 대거 허가피타바스타틴+페노피브레이트 선발품목인 스타펜캡슐[데일리팜=이혜경 기자] 피타바스타틴·페노피브레이트 복합제 후발주자가 6년만에 대거 등장했다.식품의약품안전처는 30일 신풍제약의 '스타페노캡슐'과 제뉴파마의 '제피노정2/160mg', 대웅제약의 '바로페노정2/160mg', 위더스제약의 '타스페노캡슐', 종근당의 '피타로우에프정2/160mg', 대우제약 '피타스론정2/160mg', 위더스제약 '타스페노캡슐', 보령바이오파마 '리바펜캡슐', 이든파마 '피바펜캡슐'을 허가했다.모두 고지혈증 치료제 성분 피타바스타틴과 중성지방 치료제 성분 페노피브레이트가 결합한 복합제이다.이번에 허가된 품목의 경우 제뉴파마가 수탁사로 대웅제약, 종근당, 대우제약의 제품을 생산하게 되며 신풍제약이 위더스제약, 이든파마, 보령바이오파마의 제품을 위탁 생산한다.스타틴-중성지방 복합제 시장은 지속적으로 성장하고 있다.2012년 발매한 유영제약의 프라바페닉스(프라바스타틴나트륨-페노피브레이트)는 유비스트 기준 지난해 211억원의 원외처방액을 기록했고, 2017년 11월 출시한 건일제약의 로수메가(로수바스타틴칼슘-오메가3산에틸에스텔90)도 작년 69억원의 원외처방액으로 시장안착에 성공했다.피타바스타틴·페노피브레이트 성분제제는 관상동맥심질환(CHD) 고위험이 있는 성인환자에서 피타바스타틴 2mg 단일치료 요법시 LDL-콜레스테롤 수치는 적절히 조절되지만 트리글리세라이드 수치는 높고 HDL-콜레스테롤 수치는 낮은 복합형이상지질혈증의 치료 사용에 쓰인다.피타바스타틴은 ACC/AHA 가이드라인에서 분류하는 대표적인 중간 강도 스타틴으로 LDL 콜레스테롤을 개선시켜주며 J-PREDICT 등의 임상 연구들을 통해 신규 당뇨병의 발생 위험을 높이지 않는 것으로 보고됐다.또한 페노피브레이트는 중성지방 감소 및 HDL 콜레스테롤 증가 효과를 보여 국내 가이드라인에서 중성지방 강하 약물로 권고하고 있으며, ACCORD 연구를 통해 고중성지방 및 저HDL 콜레스테롤 환자군에서 심혈관질환 발생 위험을 낮춘 것으로 알려졌다.지난 2019년 한림제약(스타펜캡슐)을 수탁사로 동광제약(피에프캡슐), 한국프라임제약(리페스틴캡슐), 삼진제약(뉴스타틴듀오캡슐), 동국제약(피타론에프캡슐), 지엘파마(리로우펜캡슐), 대원제약(업타바캡슐), 안국약품(페바로에프캡슐) 등 8개사가 개량신약으로 허가 받은바 있다.유비스트에 따르면 허가된 8개 품목의 지난해 원외처방액 규모는 38억원 정도다.페바로가 9억1261만원으로 가장 처방이 많았으며, 업타바 7억2313만원, 리페스틴 5억3457만원, 스타펜 5억2528만원, 피에프 5억2405만원, 피타론에프 3억8710만원, 뉴스타틴듀오 1억6771만원의 원외처방금액을 보였다.해당 성분제제에 국내사들이 관심을 갖기 시작한건 2년전 부터다. 신풍제약과 서울제약 등이 생동성시험을 진행하면서 후발의약품 개발을 알렸다.특히 2019년 허가를 받은 선발 품목의 경우 등재 특허가 존재하지 않아 후발 주자들은 생동만으로 제제 개발 이후 출시까지 장벽이 높지 않았다는 분석이다.고지혈증 복합제 시장 쟁탈전2025-04-30 16:58:21이혜경 -
 혈우병A 치료제 '오비주르', 주요 처방 의료기관 입성[데일리팜=어윤호 기자] 혈우병A 출혈치료제 오비주르가 종합병원 처방권에 입성했다.관련 업계에 따르면 한국다케다제약의 성인 후천성 혈우병A(AHA, Acquired Hemophilia A) 환자의 출혈 치료제 오비주르(서스옥토코그알파)는 삼성서울병원, 서울성모병원, 신촌세브란스병원 등 상급종합병원을 비롯해 경희대병원, 분당서울대병원 등 의료기관의 약사위원회(DC, Drug committee)를 통과했다.지난해 2월 보험급여 등재 후 꾸준하게 처방 영역을 넓혀가는 모습이다.오비주르는 2021년 7월 국내 희귀의약품으로 지정, 2023년 3월 국내 허가 직후 급여 평가에 돌입한 바 있다.이 약은 기존 우회인자 약제와는 달리 AHA 적응증을 가진 혈액응고 8인자를 대체하는 치료제이다.인간과 유사한 돼지 혈액응고 8인자에서 B-도메인을 제거하여 만든 유전자재조합 제제로, 자가 면역 항체에 의해 쉽게 인식되지 않기 때문에 비활성화된 인간 혈액응고 8인자를 대체하여 혈액응고를 돕고 출혈 조절에 도움을 줄 수 있다.이러한 기전으로 후천성 혈우병 A 치료제 중 유일하게 표준분석법을 통해 혈액응고 8인자 수치를 안정적으로 모니터링해 개별 맞춤 용량 치료가 가능하다.한편 후천성 혈우병A 환자 28명을 대상으로 오비주르의 유효성을 평가한 전향적, 비-무작위배정, 오픈-라벨 2/3상 연구 결과, 오비주르로 치료받은 환자는 모두 첫 투여 후 24시간 째 평가 시 모든 초기 출혈 에피소드에 대해 긍정적 반응(Positive response)을 보였다. 긍정적 반응은 출혈이 중단되거나 감소되고 임상적 개선이 있거나 혈액응고 8인자 활성이 목표치 이상으로 나타난 경우를 의미한다.최종 투약 시점에서(투여 후 2주 이내) 치료성공률은 85.7%(24/28명)였으며 치료 성공률은 오비주르를 1차치료제로 사용한 환자군에서 더 높았다.1차치료에 오비주르주를 투여 받은 환자군의 치료성공률은 94%(16/17명)였고 2차치료에 오비주르주를 투여 받은 환자군의 치료성공률은 73%(8/11명)였다. 오비주르와 관련된 중증 이상사례나 사망은 발생하지 않았다.2025-04-26 06:00:00어윤호
혈우병A 치료제 '오비주르', 주요 처방 의료기관 입성[데일리팜=어윤호 기자] 혈우병A 출혈치료제 오비주르가 종합병원 처방권에 입성했다.관련 업계에 따르면 한국다케다제약의 성인 후천성 혈우병A(AHA, Acquired Hemophilia A) 환자의 출혈 치료제 오비주르(서스옥토코그알파)는 삼성서울병원, 서울성모병원, 신촌세브란스병원 등 상급종합병원을 비롯해 경희대병원, 분당서울대병원 등 의료기관의 약사위원회(DC, Drug committee)를 통과했다.지난해 2월 보험급여 등재 후 꾸준하게 처방 영역을 넓혀가는 모습이다.오비주르는 2021년 7월 국내 희귀의약품으로 지정, 2023년 3월 국내 허가 직후 급여 평가에 돌입한 바 있다.이 약은 기존 우회인자 약제와는 달리 AHA 적응증을 가진 혈액응고 8인자를 대체하는 치료제이다.인간과 유사한 돼지 혈액응고 8인자에서 B-도메인을 제거하여 만든 유전자재조합 제제로, 자가 면역 항체에 의해 쉽게 인식되지 않기 때문에 비활성화된 인간 혈액응고 8인자를 대체하여 혈액응고를 돕고 출혈 조절에 도움을 줄 수 있다.이러한 기전으로 후천성 혈우병 A 치료제 중 유일하게 표준분석법을 통해 혈액응고 8인자 수치를 안정적으로 모니터링해 개별 맞춤 용량 치료가 가능하다.한편 후천성 혈우병A 환자 28명을 대상으로 오비주르의 유효성을 평가한 전향적, 비-무작위배정, 오픈-라벨 2/3상 연구 결과, 오비주르로 치료받은 환자는 모두 첫 투여 후 24시간 째 평가 시 모든 초기 출혈 에피소드에 대해 긍정적 반응(Positive response)을 보였다. 긍정적 반응은 출혈이 중단되거나 감소되고 임상적 개선이 있거나 혈액응고 8인자 활성이 목표치 이상으로 나타난 경우를 의미한다.최종 투약 시점에서(투여 후 2주 이내) 치료성공률은 85.7%(24/28명)였으며 치료 성공률은 오비주르를 1차치료제로 사용한 환자군에서 더 높았다.1차치료에 오비주르주를 투여 받은 환자군의 치료성공률은 94%(16/17명)였고 2차치료에 오비주르주를 투여 받은 환자군의 치료성공률은 73%(8/11명)였다. 오비주르와 관련된 중증 이상사례나 사망은 발생하지 않았다.2025-04-26 06:00:00어윤호 -
 10년간 40배 늘었는데…미 의약품 관세 검토에 우려↑도널드 트럼프 미국 대통령은 10일(현지시간) 백악관에서 미국에 수입되는 철강·알루미늄 제품에 25%의 관세를 부과하는 내용의 포고문에 서명하며 의약품 관세 가능성도 언급했다. [데일리팜=김진구 기자] 도널드 트럼프 미국 대통령이 자국 수입 의약품에 관세를 부과하는 방안을 검토 중이라고 밝혀 국내 제약바이오업계의 우려가 커지는 모습이다.국산 의약품의 미국 수출액은 2015년부터 지난해까지 10년간 40배 이상 급증했다. 2022년부터는 최대 수출국으로 자리 잡고 있다. 이런 상황에서 미국이 의약품에 관세를 부과할 경우 적잖은 타격이 불가피하다는 분석이 나온다.작년 국산 의약품 미국 수출액 13.6억 달러…관세 적용 검토 먹구름12일 주요 외신에 따르면 트럼프 미국 대통령은 지난 10일(현지시간) “미국에 수입되는 자동차·반도체·의약품에도 관세 부과를 검토 중”이라고 밝혔다. 그는 이날 철강·알루미늄 제품에 25%의 관세 부과 내용을 담은 포고문에 서명하면서 이같이 말했다.제약업계에선 미국의 관세 부과가 국산 의약품 수출에 부정적으로 작용할 것이란 전망이 지배적이다. 국산 의약품의 최대 수출국이 미국이며, 연 2조원 규모로 수출실적이 확대됐기 때문이다.실제 관세청 수출입 실적에 따르면 지난해 국산 의약품의 미국 수출액은 13억5900만 달러(약 1조9700억원)에 달한다.국산 의약품의 미국 수출액은 최근 10년간 급격히 증가했다. 2015년 3300만 달러에 그쳤던 미국 수출액은 2019년 4억3500만 달러로 4년 새 13배 이상 늘었다. 이어 코로나 팬데믹 사태를 겪으며 수출액은 더욱 늘었고, 2021년엔 10억 달러 이상으로 확대됐다.엔데믹 이후로는 다소 주춤했으나, 지난해엔 전년대비 50% 증가하며 역대 최대 수출실적을 달성했다. 삼성바이오로직스를 중심으로 한 의약품 CDMO 물량과 셀트리온·삼성바이오에피스 등의 바이오시밀러가 수출 확대에 기여한 것으로 분석된다.최근 10년간 국산 의약품의 미국 수출액·수출비중(단위 백만 달러, 자료 관세청) 국산 의약품의 미국 수출 비중도 점차 확대됐다. 전체 의약품 수출액에서 미국이 차지하는 비중은 2017년 10%를 넘어섰다. 2022년엔 독일을 제치고 최대 수출국으로 올라섰다. 이어 2023년엔 15% 이상으로 확대됐고, 지난해엔 18%로 더욱 높아졌다.이런 상황에서 미국이 실제로 의약품 관세 부과를 강행할 경우 국산 의약품 수출에도 적잖은 타격이 불가피할 것으로 예상된다.제약업계에선 특히 중소형제약사에 타격이 클 것이란 우려가 제기된다. 한국의약품수출입협회장은 "대형제약사의 경우 미국 내 생산시설 확대와 재고 확보로 대응할 수 있지만, 완제의약품을 직수출하는 중소제약사의 경우 타격이 불가피할 것"이라고 우려했다.한국 관세 맞대응 땐 미국 손실↑…“미국 내 의약품 부족” 현지서 우려 제기일각에선 트럼프 행정부가 의약품 관세 부과에 대해 신중할 것이란 전망도 제기된다.한국이 동일한 수준으로 상호 관세를 부과할 경우, 한국과의 의약품 무역에서 이익보다 손실이 더 크게 나타날 수 있기 때문이다. 또한 의약품에 대한 관세가 미국 내 필수의약품 부족으로 이어질 것이란 우려도 현지에서 제기된다.통상적으로 한 국가가 관세를 부과하면 무역 상호주의에 따라 상대국가도 동일한 수준의 관세를 부과한다. 이땐 대체로 수출 규모가 더 큰 쪽의 손해가 두드러진다. 미국 입장에선 상호 관세로 인한 이득보다 손실이 더 크게 나타나는 셈이다.실제 한국과 미국 간 의약품 무역에서 한국은 한 번도 흑자를 기록한 적이 없다. 미국을 상대로 한 한국의 의약품 무역수지는 2023년까지 꾸준히 7억~11억 달러 적자를 기록했다. 지난해엔 수출이 늘고 수입이 감소하면서 무역수지 적자 폭이 2억9200만 달러로 감소했다. 의약품에 대한 관세가 미국 내 의약품 부족과 가격 상승을 초래할 것이란 현지의 우려도 나온다.실제 미국병원협회(AHA)는 트럼프 대통령이 중국산 모든 제품에 10%의 관세를 부과하자 “암과 심장치료제는 물론 중국산 아목시실린과 같은 항생제에도 영향을 미칠 것"이라는 서한을 전달했다.제네릭 의약품 로비 단체인 '접근가능의약품협회(AAM)'도 트럼프 행정부에 의약품 관세 면제를 요청한 것으로 전해진다. 이들은 저가 의약품 제조업체들의 이윤 감소와 의약품 부족을 우려하고 있다.2025-02-12 06:17:46김진구
10년간 40배 늘었는데…미 의약품 관세 검토에 우려↑도널드 트럼프 미국 대통령은 10일(현지시간) 백악관에서 미국에 수입되는 철강·알루미늄 제품에 25%의 관세를 부과하는 내용의 포고문에 서명하며 의약품 관세 가능성도 언급했다. [데일리팜=김진구 기자] 도널드 트럼프 미국 대통령이 자국 수입 의약품에 관세를 부과하는 방안을 검토 중이라고 밝혀 국내 제약바이오업계의 우려가 커지는 모습이다.국산 의약품의 미국 수출액은 2015년부터 지난해까지 10년간 40배 이상 급증했다. 2022년부터는 최대 수출국으로 자리 잡고 있다. 이런 상황에서 미국이 의약품에 관세를 부과할 경우 적잖은 타격이 불가피하다는 분석이 나온다.작년 국산 의약품 미국 수출액 13.6억 달러…관세 적용 검토 먹구름12일 주요 외신에 따르면 트럼프 미국 대통령은 지난 10일(현지시간) “미국에 수입되는 자동차·반도체·의약품에도 관세 부과를 검토 중”이라고 밝혔다. 그는 이날 철강·알루미늄 제품에 25%의 관세 부과 내용을 담은 포고문에 서명하면서 이같이 말했다.제약업계에선 미국의 관세 부과가 국산 의약품 수출에 부정적으로 작용할 것이란 전망이 지배적이다. 국산 의약품의 최대 수출국이 미국이며, 연 2조원 규모로 수출실적이 확대됐기 때문이다.실제 관세청 수출입 실적에 따르면 지난해 국산 의약품의 미국 수출액은 13억5900만 달러(약 1조9700억원)에 달한다.국산 의약품의 미국 수출액은 최근 10년간 급격히 증가했다. 2015년 3300만 달러에 그쳤던 미국 수출액은 2019년 4억3500만 달러로 4년 새 13배 이상 늘었다. 이어 코로나 팬데믹 사태를 겪으며 수출액은 더욱 늘었고, 2021년엔 10억 달러 이상으로 확대됐다.엔데믹 이후로는 다소 주춤했으나, 지난해엔 전년대비 50% 증가하며 역대 최대 수출실적을 달성했다. 삼성바이오로직스를 중심으로 한 의약품 CDMO 물량과 셀트리온·삼성바이오에피스 등의 바이오시밀러가 수출 확대에 기여한 것으로 분석된다.최근 10년간 국산 의약품의 미국 수출액·수출비중(단위 백만 달러, 자료 관세청) 국산 의약품의 미국 수출 비중도 점차 확대됐다. 전체 의약품 수출액에서 미국이 차지하는 비중은 2017년 10%를 넘어섰다. 2022년엔 독일을 제치고 최대 수출국으로 올라섰다. 이어 2023년엔 15% 이상으로 확대됐고, 지난해엔 18%로 더욱 높아졌다.이런 상황에서 미국이 실제로 의약품 관세 부과를 강행할 경우 국산 의약품 수출에도 적잖은 타격이 불가피할 것으로 예상된다.제약업계에선 특히 중소형제약사에 타격이 클 것이란 우려가 제기된다. 한국의약품수출입협회장은 "대형제약사의 경우 미국 내 생산시설 확대와 재고 확보로 대응할 수 있지만, 완제의약품을 직수출하는 중소제약사의 경우 타격이 불가피할 것"이라고 우려했다.한국 관세 맞대응 땐 미국 손실↑…“미국 내 의약품 부족” 현지서 우려 제기일각에선 트럼프 행정부가 의약품 관세 부과에 대해 신중할 것이란 전망도 제기된다.한국이 동일한 수준으로 상호 관세를 부과할 경우, 한국과의 의약품 무역에서 이익보다 손실이 더 크게 나타날 수 있기 때문이다. 또한 의약품에 대한 관세가 미국 내 필수의약품 부족으로 이어질 것이란 우려도 현지에서 제기된다.통상적으로 한 국가가 관세를 부과하면 무역 상호주의에 따라 상대국가도 동일한 수준의 관세를 부과한다. 이땐 대체로 수출 규모가 더 큰 쪽의 손해가 두드러진다. 미국 입장에선 상호 관세로 인한 이득보다 손실이 더 크게 나타나는 셈이다.실제 한국과 미국 간 의약품 무역에서 한국은 한 번도 흑자를 기록한 적이 없다. 미국을 상대로 한 한국의 의약품 무역수지는 2023년까지 꾸준히 7억~11억 달러 적자를 기록했다. 지난해엔 수출이 늘고 수입이 감소하면서 무역수지 적자 폭이 2억9200만 달러로 감소했다. 의약품에 대한 관세가 미국 내 의약품 부족과 가격 상승을 초래할 것이란 현지의 우려도 나온다.실제 미국병원협회(AHA)는 트럼프 대통령이 중국산 모든 제품에 10%의 관세를 부과하자 “암과 심장치료제는 물론 중국산 아목시실린과 같은 항생제에도 영향을 미칠 것"이라는 서한을 전달했다.제네릭 의약품 로비 단체인 '접근가능의약품협회(AAM)'도 트럼프 행정부에 의약품 관세 면제를 요청한 것으로 전해진다. 이들은 저가 의약품 제조업체들의 이윤 감소와 의약품 부족을 우려하고 있다.2025-02-12 06:17:46김진구 -
 미국 제약업계, 트럼프 행정부에 '의약품 관세 제외' 요청[데일리팜=김진구 기자] 미국 제약업계가 트럼프 행정부에 수입 의약품의 관세를 제외해달라고 요청했다. 이들은 의약품에 대한 관세가 미국 내 의약품 부족과 가격 상승을 초래할 것이란 우려를 제기했다.한국바이오협회는 7일 이슈브리핑을 통해 이같이 전했다. 바이오협회에 따르면 트럼프 행정부는 지난 4일 미국으로 수입되는 모든 모든 중국산 제품에 10%의 관세를 부과한다고 발표했다. 멕시코와 캐나다산 제품에 대한 25%의 관세 부과는 30일간 유예됐다. 트럼프 대통령은 유럽연합(EU)을 다음 목표로 삼고 있다.이러한 조치에 미국병원협회(AHA)는 트럼프 대통령에게 "이번 관세가 암과 심장치료제는 물론 중국산 아목시실린과 같은 항생제에도 영향을 미칠 것"이라는 서한을 전달했다.미국병원협회는 핵심 의약품을 만드는 데 사용되는 원료의 30%가 중국에서 생산되며, 일회용 안면 마스크의 3분의 1과 의료 분야에 사용되는 거의 모든 비닐장갑도 중국에서 생산된다고 설명했다.제네릭 의약품 로비 단체인 '접근가능의약품협회(AAM)'도 트럼프 행정부에 의약품 관세 면제를 제공할 것을 요청하고 있는 것으로 전해진다. 저가 의약품 제조업체들이 직면한 이윤 마진의 부족과 의약품 부족의 역사가 되풀이될 것으로 이들은 우려하고 있다.실제 미국 무역데이터에 따르면 미국은 2023년에 해외에서 1760억 달러 이상의 의약품을 수입했으며, 이 가운데 약 60억 달러가 중국에서 수입됐다.미국은 1994년 체결된 WTO 의약품 협정(WTO Pharmaceutical Agreement)에 따라 의약품과 의약품 생산에 사용되는 물질에 대한 관세 및 기타 관세 부과를 없앴다. 협정 가입국들은 모든 완제의약품뿐 아니라 의약품 공급에 사용되는 7000개 이상의 제약 활성성분·화학성분에 대한 관세를 폐지키로 했다. 이 협정에는 미국을 포함해 유럽연합, 일본, 캐나다, 마카오, 노르웨이, 스위스, 영국 등 대부분 의약품 선진국들이 참여하고 있다.미국은 케미컬의약품과 바이오의약품의 생산·공급 구조가 이원화돼 있다. 케미컬의약품의 경우 중국·인도 등에서 저가의 원료의약품을 수입해 고가의 완제의약품으로 생산·판매한다. 반면 고가의 바이오의약품의 경우에 자체적으로 생산하거나 유럽 등에서 수입한다.이러한 구조로 인해 미국의 의약품 수입에서 금액으로는 중국의 비중이 낮지만, 물량에선 높은 비중을 차지한다. 특히 제네릭의약품을 판매하는 미국 기업 입장에선 원료의약품의 수입 단가가 중요하기 때문에 중국산 의약품에 대한 관세 인상이 매우 부정적인 영향을 미칠 것으로 전망된다.반면, 케미컬 완제의약품을 판매하거나 바이오의약품을 판매하는 브랜드 제약사에게는 중국산 수입의약품에 대한 10% 관세 인상이 최종 판매 가격에 큰 영향을 미치지 않을 것으로 전망된다.오히려 유럽에 대한 관세 부과 여부가 관건이다. 유럽에 제조기반을 둔 바이오의약품의 경우에는 상대적으로 큰 리스크로 다가올 수 있다는 점에서 바이오의약품 판매 제약사들은 트럼프 대통령의 유럽에 대한 관세 인상 추진에 대해 우려하고 있다.한국바이오협회는 "세계 1위 의약품 시장인 미국이 실제 의약품에 대한 관세를 부과할지, 부과한다면 어느 정도 할지, 대상은 수입량 의존도가 높은 원료의약품이 될지 또는 모든 의약품이 될지, 특정 국가에만 관세를 부과할지 또는 모든 국가에 부과할지 등 전 세계가 지켜보고 있다"고 설명했다.2025-02-07 12:00:00김진구
미국 제약업계, 트럼프 행정부에 '의약품 관세 제외' 요청[데일리팜=김진구 기자] 미국 제약업계가 트럼프 행정부에 수입 의약품의 관세를 제외해달라고 요청했다. 이들은 의약품에 대한 관세가 미국 내 의약품 부족과 가격 상승을 초래할 것이란 우려를 제기했다.한국바이오협회는 7일 이슈브리핑을 통해 이같이 전했다. 바이오협회에 따르면 트럼프 행정부는 지난 4일 미국으로 수입되는 모든 모든 중국산 제품에 10%의 관세를 부과한다고 발표했다. 멕시코와 캐나다산 제품에 대한 25%의 관세 부과는 30일간 유예됐다. 트럼프 대통령은 유럽연합(EU)을 다음 목표로 삼고 있다.이러한 조치에 미국병원협회(AHA)는 트럼프 대통령에게 "이번 관세가 암과 심장치료제는 물론 중국산 아목시실린과 같은 항생제에도 영향을 미칠 것"이라는 서한을 전달했다.미국병원협회는 핵심 의약품을 만드는 데 사용되는 원료의 30%가 중국에서 생산되며, 일회용 안면 마스크의 3분의 1과 의료 분야에 사용되는 거의 모든 비닐장갑도 중국에서 생산된다고 설명했다.제네릭 의약품 로비 단체인 '접근가능의약품협회(AAM)'도 트럼프 행정부에 의약품 관세 면제를 제공할 것을 요청하고 있는 것으로 전해진다. 저가 의약품 제조업체들이 직면한 이윤 마진의 부족과 의약품 부족의 역사가 되풀이될 것으로 이들은 우려하고 있다.실제 미국 무역데이터에 따르면 미국은 2023년에 해외에서 1760억 달러 이상의 의약품을 수입했으며, 이 가운데 약 60억 달러가 중국에서 수입됐다.미국은 1994년 체결된 WTO 의약품 협정(WTO Pharmaceutical Agreement)에 따라 의약품과 의약품 생산에 사용되는 물질에 대한 관세 및 기타 관세 부과를 없앴다. 협정 가입국들은 모든 완제의약품뿐 아니라 의약품 공급에 사용되는 7000개 이상의 제약 활성성분·화학성분에 대한 관세를 폐지키로 했다. 이 협정에는 미국을 포함해 유럽연합, 일본, 캐나다, 마카오, 노르웨이, 스위스, 영국 등 대부분 의약품 선진국들이 참여하고 있다.미국은 케미컬의약품과 바이오의약품의 생산·공급 구조가 이원화돼 있다. 케미컬의약품의 경우 중국·인도 등에서 저가의 원료의약품을 수입해 고가의 완제의약품으로 생산·판매한다. 반면 고가의 바이오의약품의 경우에 자체적으로 생산하거나 유럽 등에서 수입한다.이러한 구조로 인해 미국의 의약품 수입에서 금액으로는 중국의 비중이 낮지만, 물량에선 높은 비중을 차지한다. 특히 제네릭의약품을 판매하는 미국 기업 입장에선 원료의약품의 수입 단가가 중요하기 때문에 중국산 의약품에 대한 관세 인상이 매우 부정적인 영향을 미칠 것으로 전망된다.반면, 케미컬 완제의약품을 판매하거나 바이오의약품을 판매하는 브랜드 제약사에게는 중국산 수입의약품에 대한 10% 관세 인상이 최종 판매 가격에 큰 영향을 미치지 않을 것으로 전망된다.오히려 유럽에 대한 관세 부과 여부가 관건이다. 유럽에 제조기반을 둔 바이오의약품의 경우에는 상대적으로 큰 리스크로 다가올 수 있다는 점에서 바이오의약품 판매 제약사들은 트럼프 대통령의 유럽에 대한 관세 인상 추진에 대해 우려하고 있다.한국바이오협회는 "세계 1위 의약품 시장인 미국이 실제 의약품에 대한 관세를 부과할지, 부과한다면 어느 정도 할지, 대상은 수입량 의존도가 높은 원료의약품이 될지 또는 모든 의약품이 될지, 특정 국가에만 관세를 부과할지 또는 모든 국가에 부과할지 등 전 세계가 지켜보고 있다"고 설명했다.2025-02-07 12:00:00김진구 -
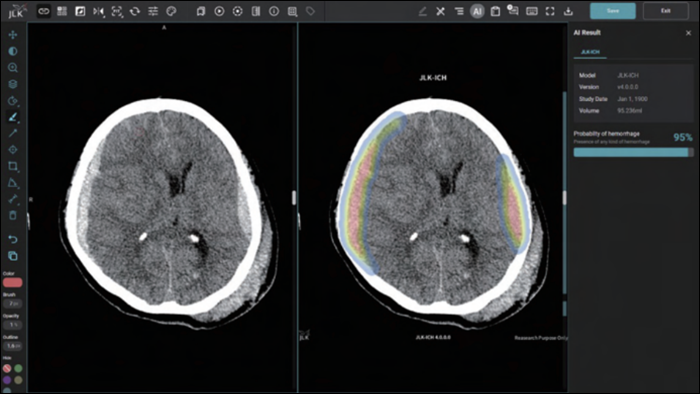 제이엘케이, 두개내출혈 검출 솔루션 FDA 승인[데일리팜=노병철 기자] 의료 AI 1호 상장기업 제이엘케이(대표 김동민)는 지난해 미국 FDA(식품의약국) 인허가를 신청했던 JLK-ICH(두개내출혈 검출 솔루션)가 보완사항 없이 승인(FDA 510(k))을 완료했다고 6일 밝혔다.지난해 이미 한 해동안 전립선암 솔루션 1개 획득에 이어 뇌졸중 솔루션에서만 3개 솔루션(JLK-LVO, JLK-CTP, JLK-PWI)의 승인을 획득한 제이엘케이는 이번 승인이 전체 5번째 FDA 획득으로 뇌졸중 분야에서만 4개 솔루션에 대한 FDA 인허가를 확보하게 됐다.특히, 이번 인허가는 미국 FDA 별도 추가보완 없이 단번에 승인받아 그 의미가 남다르다. 업계에서는 그동안 다수의 해외 인허가 진행으로 포트폴리오를 쌓아왔던 제이엘케이의 자체 인허가 역량이 인정받고 있음을 보여주는 지표라고 평가했다.JLK-ICH는 제이엘케이가 주력하고 있는 뇌졸중 AI 솔루션으로 환자의 뇌 CT 영상을 분석해 뇌출혈 영역을 검출하는 AI 솔루션이다. 통상 뇌졸중 의심환자가 응급실에 도착하면 가장 먼저 뇌 CT를 촬영해 뇌출혈 여부를 확인하는데 이 과정에서 JLK-ICH가 빈번히 쓰일 것으로 예측된다. 특히 기존에 획득한 JLK-LVO, JLK-CTP, JLK-PWI와 함께 연동돼 전주기에 걸친 뇌졸중 진단과 치료 결정 활용 시너지는 물론 미국 병원에서의 시장 차별성과 경쟁력이 매우 커질 것으로 기대된다.더욱이, 혈관이 막히는 뇌경색 대비 중증도가 높은 뇌출혈은 출혈 크기 증가 우려와 재출혈 위험으로 치료까지 걸리는 시간을 단축하는 것이 환자 예후개선에 필수적이다. JLK-ICH는 임상연구를 통해 발생 특징이 다른 5가지 뇌출혈 유형에 대해 편차 없는 높은 검출 성능을 입증한 만큼 골든타임 확보에 큰 역할을 할 것으로 기대된다.이번 FDA 승인으로 매출 확대를 위한 기반도 견고히 다졌다는 평가다. 미국의 연간 CT 촬상 수가 약 8600만 건에 이를 정도로 빈도가 매우 높아 CT 영상을 기반으로 하는 해당 솔루션의 미국 내 시장성이 높을 것으로 기대하고 있다.회사 관계자는 “지난해부터 글로벌 선진국 시장 진출을 위하여 공격적인 미국 FDA와 일본 PMDA 인허가 활동들이 빠른 결실을 맺고 있는 만큼 남은 솔루션들에 대한 인허가도 조속히 진행할 예정”이라고 전했다.제이엘케이는 올해 인허가 신청과 승인 그리고 보험수가 획득에 집중해 해외 매출 확대에 포석을 마련한다는 목표를 세웠다. 미국 FDA의 경우 올해 총 6개의 인허가를 추가로 신청하고 일본 PMDA는 8개 솔루션의 인허가 신청을 마친다는 계획이다.아울러, 각국 보험수가 진입도 전념해 해외 매출도 발생시킨다는 방침이다. 뇌졸중 종합 플랫폼 메디허브 스트로크(Medihub Stroke)의 각 구성 제품들이 연속적인 FDA 신청과 획득 성공을 통해 전 세계적으로 경쟁력을 인정받고 있으며, AI 의료 플랫폼(AI Medical Platform)의 비즈니스 기반이 형성되고 있기 때문이다. 특히 제이엘케이는 모든 솔루션 개발에 세계적 표준인 ASA/AHA 가이드라인을 준용해 시간이 지남에 따라 글로벌 가치가 더욱 올라갈 것으로 확신되고 있다.김동민 제이엘케이 대표는 “JLK-ICH를 통해 올해 첫 해외 인허가 획득 소식을 전할 수 있어 기쁘다”라며 “보완사항 없이 단번에 승인을 마친 이번 FDA 획득으로 제이엘케이가 자체적으로 구축한 인허가 역량의 우수성을 입증한 만큼 남은 인허가와 현지 보험수가 획득에 주력해 성공적인 해외 진출 성과를 가져오는 최선을 다하겠다”라고 말했다.2025-01-06 10:30:03노병철
제이엘케이, 두개내출혈 검출 솔루션 FDA 승인[데일리팜=노병철 기자] 의료 AI 1호 상장기업 제이엘케이(대표 김동민)는 지난해 미국 FDA(식품의약국) 인허가를 신청했던 JLK-ICH(두개내출혈 검출 솔루션)가 보완사항 없이 승인(FDA 510(k))을 완료했다고 6일 밝혔다.지난해 이미 한 해동안 전립선암 솔루션 1개 획득에 이어 뇌졸중 솔루션에서만 3개 솔루션(JLK-LVO, JLK-CTP, JLK-PWI)의 승인을 획득한 제이엘케이는 이번 승인이 전체 5번째 FDA 획득으로 뇌졸중 분야에서만 4개 솔루션에 대한 FDA 인허가를 확보하게 됐다.특히, 이번 인허가는 미국 FDA 별도 추가보완 없이 단번에 승인받아 그 의미가 남다르다. 업계에서는 그동안 다수의 해외 인허가 진행으로 포트폴리오를 쌓아왔던 제이엘케이의 자체 인허가 역량이 인정받고 있음을 보여주는 지표라고 평가했다.JLK-ICH는 제이엘케이가 주력하고 있는 뇌졸중 AI 솔루션으로 환자의 뇌 CT 영상을 분석해 뇌출혈 영역을 검출하는 AI 솔루션이다. 통상 뇌졸중 의심환자가 응급실에 도착하면 가장 먼저 뇌 CT를 촬영해 뇌출혈 여부를 확인하는데 이 과정에서 JLK-ICH가 빈번히 쓰일 것으로 예측된다. 특히 기존에 획득한 JLK-LVO, JLK-CTP, JLK-PWI와 함께 연동돼 전주기에 걸친 뇌졸중 진단과 치료 결정 활용 시너지는 물론 미국 병원에서의 시장 차별성과 경쟁력이 매우 커질 것으로 기대된다.더욱이, 혈관이 막히는 뇌경색 대비 중증도가 높은 뇌출혈은 출혈 크기 증가 우려와 재출혈 위험으로 치료까지 걸리는 시간을 단축하는 것이 환자 예후개선에 필수적이다. JLK-ICH는 임상연구를 통해 발생 특징이 다른 5가지 뇌출혈 유형에 대해 편차 없는 높은 검출 성능을 입증한 만큼 골든타임 확보에 큰 역할을 할 것으로 기대된다.이번 FDA 승인으로 매출 확대를 위한 기반도 견고히 다졌다는 평가다. 미국의 연간 CT 촬상 수가 약 8600만 건에 이를 정도로 빈도가 매우 높아 CT 영상을 기반으로 하는 해당 솔루션의 미국 내 시장성이 높을 것으로 기대하고 있다.회사 관계자는 “지난해부터 글로벌 선진국 시장 진출을 위하여 공격적인 미국 FDA와 일본 PMDA 인허가 활동들이 빠른 결실을 맺고 있는 만큼 남은 솔루션들에 대한 인허가도 조속히 진행할 예정”이라고 전했다.제이엘케이는 올해 인허가 신청과 승인 그리고 보험수가 획득에 집중해 해외 매출 확대에 포석을 마련한다는 목표를 세웠다. 미국 FDA의 경우 올해 총 6개의 인허가를 추가로 신청하고 일본 PMDA는 8개 솔루션의 인허가 신청을 마친다는 계획이다.아울러, 각국 보험수가 진입도 전념해 해외 매출도 발생시킨다는 방침이다. 뇌졸중 종합 플랫폼 메디허브 스트로크(Medihub Stroke)의 각 구성 제품들이 연속적인 FDA 신청과 획득 성공을 통해 전 세계적으로 경쟁력을 인정받고 있으며, AI 의료 플랫폼(AI Medical Platform)의 비즈니스 기반이 형성되고 있기 때문이다. 특히 제이엘케이는 모든 솔루션 개발에 세계적 표준인 ASA/AHA 가이드라인을 준용해 시간이 지남에 따라 글로벌 가치가 더욱 올라갈 것으로 확신되고 있다.김동민 제이엘케이 대표는 “JLK-ICH를 통해 올해 첫 해외 인허가 획득 소식을 전할 수 있어 기쁘다”라며 “보완사항 없이 단번에 승인을 마친 이번 FDA 획득으로 제이엘케이가 자체적으로 구축한 인허가 역량의 우수성을 입증한 만큼 남은 인허가와 현지 보험수가 획득에 주력해 성공적인 해외 진출 성과를 가져오는 최선을 다하겠다”라고 말했다.2025-01-06 10:30:03노병철 -
 심근병증 신약 '캄지오스' 급여 성공...환자 혜택 기대[데일리팜=어윤호 기자] 폐색성비대성심근병증 신약 '캄지오스'가 보험급여 목록에 이름을 올리게 됐다.보건복지부는 이달 28일 제23차 건강보험정책심의위원회를 열고 한국BMS제약의 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)에 대한 급여 적용을 예고했다.이에 따라, 캄지오스는 내달(12월)부터 원활한 처방이 이뤄질 것으로 예상된다.2023년 5월 국내 허가된 캄지오스는 건강보험심사평가원 약제급여평가위원회 단계에서부터 재논의 판정 등으로 인해 어려움을 겪었다. 이후 약평위를 통과하고 지난 8월 약가협상에 돌입했지만 협상 기일(60일) 동안 결론을 내지 못했다. 이후 연장협상에서 빠르게 합의하면서 이번 건정심에 상정됐다.캄지오스는 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-11-29 06:00:09어윤호
심근병증 신약 '캄지오스' 급여 성공...환자 혜택 기대[데일리팜=어윤호 기자] 폐색성비대성심근병증 신약 '캄지오스'가 보험급여 목록에 이름을 올리게 됐다.보건복지부는 이달 28일 제23차 건강보험정책심의위원회를 열고 한국BMS제약의 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)에 대한 급여 적용을 예고했다.이에 따라, 캄지오스는 내달(12월)부터 원활한 처방이 이뤄질 것으로 예상된다.2023년 5월 국내 허가된 캄지오스는 건강보험심사평가원 약제급여평가위원회 단계에서부터 재논의 판정 등으로 인해 어려움을 겪었다. 이후 약평위를 통과하고 지난 8월 약가협상에 돌입했지만 협상 기일(60일) 동안 결론을 내지 못했다. 이후 연장협상에서 빠르게 합의하면서 이번 건정심에 상정됐다.캄지오스는 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-11-29 06:00:09어윤호 -
 폐색성비대성심근병증 신약 '캄지오스' 약가협상 타결[데일리팜=어윤호 기자] 폐색성비대성심근병증 신약 '캄지오스'가 보험급여 등재를 향한 9부 능선을 넘었다.취재 결과, 한국BMS제약과 국민건강보험공단의 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)에 대한 약가협상을 타결했다. 한번의 연장 결정 후 빠르게 합의를 이룬 모습이다.캄지오스는 이에 따라, 연내 등재 고시도 기대할 수 있게 됐다.이 약은 건강보험심사평가원 약제급여평가위원회 단계에서부터 재논의 판정 등으로 인해 어려움을 겪었다. 이후 약평위를 통과하고 지난 8월 약가협상에 돌입했지만 협상 기일(60일) 동안 결론을 내지 못했다.캄지오스는 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-11-05 05:59:35어윤호
폐색성비대성심근병증 신약 '캄지오스' 약가협상 타결[데일리팜=어윤호 기자] 폐색성비대성심근병증 신약 '캄지오스'가 보험급여 등재를 향한 9부 능선을 넘었다.취재 결과, 한국BMS제약과 국민건강보험공단의 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)에 대한 약가협상을 타결했다. 한번의 연장 결정 후 빠르게 합의를 이룬 모습이다.캄지오스는 이에 따라, 연내 등재 고시도 기대할 수 있게 됐다.이 약은 건강보험심사평가원 약제급여평가위원회 단계에서부터 재논의 판정 등으로 인해 어려움을 겪었다. 이후 약평위를 통과하고 지난 8월 약가협상에 돌입했지만 협상 기일(60일) 동안 결론을 내지 못했다.캄지오스는 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-11-05 05:59:35어윤호 -
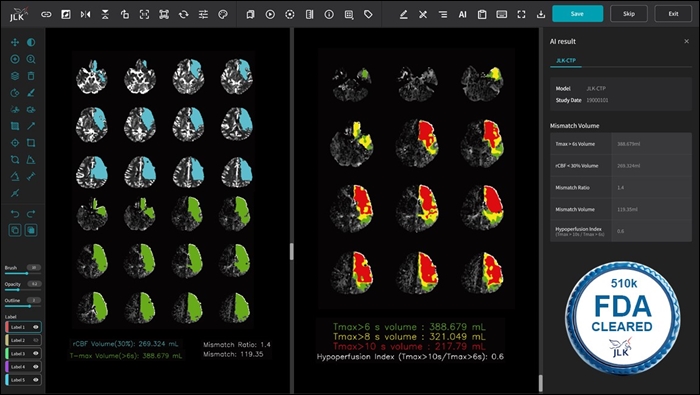 제이엘케이, 뇌 CT AI 솔루션 'JLK-CTP' FDA 승인뇌 CT 관류영상 분석 AI 솔루션 JLK-CTP. [데일리팜=노병철 기자] 의료 AI 1호 상장기업 제이엘케이(대표 김동민)는 뇌졸중 솔루션 JLK-CTP가 미국 FDA 510(k) 승인을 획득했다고 17일 발표했다.JLK-CTP는 뇌 CT 관류영상(CT Perfusion)에서 뇌혈류(CBF : Cerebral blood flow) 분석 결과를 기반으로 뇌경색 중심(Infarct core)과 뇌관류(Perfusion) 저하 영역의 부피를 자동으로 계산해 주는 솔루션이다.이 솔루션을 활용하면 뇌경색 발병 부위는 물론 손상 정도를 정밀하게 파악할 수 있고, 회복 가능한 뇌의 범위와 뇌경색 부피(ischemic core)를 제공해 촌각을 다투는 뇌졸중 환자의 수술∙시술 시행 여부를 빠르게 판단할 수 있다.JLK-CTP는 지난 5월 국제 의료 학술지 프론티어스(Frontiers)에 발표된 ‘CT 관류영상 AI 솔루션 성능 비교 논문’에서 정밀도∙일치도에서 우수한 성능을 보였고, 미국 Rapid AI 제품과의 비교에서도 더 정확한 뇌경색 중심 부피예측률을 나타낸 바 있다.이번 승인은 JLK-PROSTATE(전립선), JLK-LVO(대혈관폐색)에 이은 올해 세번째 FDA 승인 건으로 회사 측은 추가로 신청했던 뇌졸중 솔루션들의 인허가 승인도 탄력 받을 것으로 전망하고 있다.제이엘케이는 지난 8월 JLK-PWI(뇌관류MR) 제품의 FDA 인허가 신청을 마친 상황으로 올해 내 3개의 뇌졸중 솔루션을 추가 신청할 계획을 가지고 있다.회사는 이번 FDA 승인이 올해 진행 중인 미국을 비롯한 세계 시장 진출에기반이 될 것으로 관측했다. JLK-CTP가 이미 FDA 승인을 받은 JLK-LVO와 함께 연결되는 제품으로 2가지 제품의 시너지를 통한 매출 효과가 기대되기 때문이다.또 유연하고 뛰어난 기술을 바탕으로 미국 경쟁사인 Rapid AI 제품보다 우수한 성능을 입증한 만큼 Rapid AI가 독식 해오던 미국 의료 인공지능 시장에서 제이엘케이가 새로운 시장을 열 것으로 전망했다.회사는 미국, 일본을 중심으로 세계 진출을 동시에 추진 중이다.일본의 경우CTP(CT관류영상)을 활용한 뇌졸중 치료 보험수가가 적극적으로 논의되고 있어 제이엘케이의 시장 진출이 더 빨라질 것으로 전망된다. 회사는 의약품의료기기종합기구(PMDA)를 통해 JLK-CTP, JLK-PWI의 인허가 신청을 마친 상황으로 승인 여부에 촉각을 곤두세우고 있다.제이엘케이 김동민 대표는 “제이엘케이의 AI 솔루션은 모두 글로벌 스탠다드 규격(ASA/AHA)에 맞게 개발돼 모든 제품들이 연결성을 가지고 있고, 각 솔루션들은 실질 임상과 연결돼 시너지 효과를 낼 수 있는 것이 특징”라고 말했다.또 “앞으로도 남은 FDA 인허가 신청을 차질 없이 진행해 빠른 승인과 상용화로 미국 시장에서의 안정적 매출원을 확보하는 데 더욱 주력하겠다”라면서 “다양하게 조화를 이루는 인공지능 솔루션으로 시장 선점 및 매출 확장을 적극적으로 추진하겠다”라고 말했다.2024-10-17 09:43:15노병철
제이엘케이, 뇌 CT AI 솔루션 'JLK-CTP' FDA 승인뇌 CT 관류영상 분석 AI 솔루션 JLK-CTP. [데일리팜=노병철 기자] 의료 AI 1호 상장기업 제이엘케이(대표 김동민)는 뇌졸중 솔루션 JLK-CTP가 미국 FDA 510(k) 승인을 획득했다고 17일 발표했다.JLK-CTP는 뇌 CT 관류영상(CT Perfusion)에서 뇌혈류(CBF : Cerebral blood flow) 분석 결과를 기반으로 뇌경색 중심(Infarct core)과 뇌관류(Perfusion) 저하 영역의 부피를 자동으로 계산해 주는 솔루션이다.이 솔루션을 활용하면 뇌경색 발병 부위는 물론 손상 정도를 정밀하게 파악할 수 있고, 회복 가능한 뇌의 범위와 뇌경색 부피(ischemic core)를 제공해 촌각을 다투는 뇌졸중 환자의 수술∙시술 시행 여부를 빠르게 판단할 수 있다.JLK-CTP는 지난 5월 국제 의료 학술지 프론티어스(Frontiers)에 발표된 ‘CT 관류영상 AI 솔루션 성능 비교 논문’에서 정밀도∙일치도에서 우수한 성능을 보였고, 미국 Rapid AI 제품과의 비교에서도 더 정확한 뇌경색 중심 부피예측률을 나타낸 바 있다.이번 승인은 JLK-PROSTATE(전립선), JLK-LVO(대혈관폐색)에 이은 올해 세번째 FDA 승인 건으로 회사 측은 추가로 신청했던 뇌졸중 솔루션들의 인허가 승인도 탄력 받을 것으로 전망하고 있다.제이엘케이는 지난 8월 JLK-PWI(뇌관류MR) 제품의 FDA 인허가 신청을 마친 상황으로 올해 내 3개의 뇌졸중 솔루션을 추가 신청할 계획을 가지고 있다.회사는 이번 FDA 승인이 올해 진행 중인 미국을 비롯한 세계 시장 진출에기반이 될 것으로 관측했다. JLK-CTP가 이미 FDA 승인을 받은 JLK-LVO와 함께 연결되는 제품으로 2가지 제품의 시너지를 통한 매출 효과가 기대되기 때문이다.또 유연하고 뛰어난 기술을 바탕으로 미국 경쟁사인 Rapid AI 제품보다 우수한 성능을 입증한 만큼 Rapid AI가 독식 해오던 미국 의료 인공지능 시장에서 제이엘케이가 새로운 시장을 열 것으로 전망했다.회사는 미국, 일본을 중심으로 세계 진출을 동시에 추진 중이다.일본의 경우CTP(CT관류영상)을 활용한 뇌졸중 치료 보험수가가 적극적으로 논의되고 있어 제이엘케이의 시장 진출이 더 빨라질 것으로 전망된다. 회사는 의약품의료기기종합기구(PMDA)를 통해 JLK-CTP, JLK-PWI의 인허가 신청을 마친 상황으로 승인 여부에 촉각을 곤두세우고 있다.제이엘케이 김동민 대표는 “제이엘케이의 AI 솔루션은 모두 글로벌 스탠다드 규격(ASA/AHA)에 맞게 개발돼 모든 제품들이 연결성을 가지고 있고, 각 솔루션들은 실질 임상과 연결돼 시너지 효과를 낼 수 있는 것이 특징”라고 말했다.또 “앞으로도 남은 FDA 인허가 신청을 차질 없이 진행해 빠른 승인과 상용화로 미국 시장에서의 안정적 매출원을 확보하는 데 더욱 주력하겠다”라면서 “다양하게 조화를 이루는 인공지능 솔루션으로 시장 선점 및 매출 확장을 적극적으로 추진하겠다”라고 말했다.2024-10-17 09:43:15노병철 -
 심근병증 신약 '캄지오스', 급여 마지막 관문서 '발목'[데일리팜=어윤호 기자] 보험급여 등재를 노리는 '캄지오스'의 여정이 마지막까지 험난하다.관련 업계에 따르면 한국BMS제약과 국민건강보험공단의 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)에 대한 약가협상이 기한내 마무리되지 못하고 연장됐다.캄지오스는 건강보험심사평가원 약제급여평가위원회 단계에서부터 재논의 판정 등으로 인해 어려움을 겪었다.이후 약평위를 통과하고 지난 8월 약가협상에 돌입했지만 협상 기일(60일) 동안 결론을 내지 못했다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.김형관 서울대병원 순환기내과 교수는 "마땅한 치료제가 없었던 질환이기에 많은 비후성 심근증 환자들이 신약을 애타게 기다리고 있다. 특히 지난 7월 약평위 통과후 연내 급여 등재에 대한 기대감이 더욱 커진 상황인데 기다리고 있는 환자분들과 보호자들을 위해 잔여 절차가 조속히 마무리돼 우리나라 비후성 심근증 환자들이 신약의 혜택을 봤으면 한다"고 말했다.2024-10-15 06:00:45어윤호
심근병증 신약 '캄지오스', 급여 마지막 관문서 '발목'[데일리팜=어윤호 기자] 보험급여 등재를 노리는 '캄지오스'의 여정이 마지막까지 험난하다.관련 업계에 따르면 한국BMS제약과 국민건강보험공단의 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)에 대한 약가협상이 기한내 마무리되지 못하고 연장됐다.캄지오스는 건강보험심사평가원 약제급여평가위원회 단계에서부터 재논의 판정 등으로 인해 어려움을 겪었다.이후 약평위를 통과하고 지난 8월 약가협상에 돌입했지만 협상 기일(60일) 동안 결론을 내지 못했다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.김형관 서울대병원 순환기내과 교수는 "마땅한 치료제가 없었던 질환이기에 많은 비후성 심근증 환자들이 신약을 애타게 기다리고 있다. 특히 지난 7월 약평위 통과후 연내 급여 등재에 대한 기대감이 더욱 커진 상황인데 기다리고 있는 환자분들과 보호자들을 위해 잔여 절차가 조속히 마무리돼 우리나라 비후성 심근증 환자들이 신약의 혜택을 봤으면 한다"고 말했다.2024-10-15 06:00:45어윤호 -
 심근병증 신약 '캄지오스', 급여 마지막 관문 돌입[데일리팜=어윤호 기자] 폐색성비대성심근병증 신약 '캄지오스'가 보험급여 등재를 향한 마지막 관문에 돌입한다.관련 업계에 따르면 보건복지부는 최근 국민건강보험공단에 한국BMS제약의 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy)치료제 캄지오스(마바캄텐)에 대한 약가협상 명령을 내렸다.건강보험심사평가원 단계에서부터 재논의 판정 등 어려움을 겪었던 캄지오스가 급여 등재를 이룰수 있을지 지켜 볼 부분이다.캄지오스는 경제성평가소위원회 통과 후 예상보다 빠르게 약평위에 상정됐지만 한번 보류 판정을 받았다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-08-02 06:31:42어윤호
심근병증 신약 '캄지오스', 급여 마지막 관문 돌입[데일리팜=어윤호 기자] 폐색성비대성심근병증 신약 '캄지오스'가 보험급여 등재를 향한 마지막 관문에 돌입한다.관련 업계에 따르면 보건복지부는 최근 국민건강보험공단에 한국BMS제약의 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy)치료제 캄지오스(마바캄텐)에 대한 약가협상 명령을 내렸다.건강보험심사평가원 단계에서부터 재논의 판정 등 어려움을 겪었던 캄지오스가 급여 등재를 이룰수 있을지 지켜 볼 부분이다.캄지오스는 경제성평가소위원회 통과 후 예상보다 빠르게 약평위에 상정됐지만 한번 보류 판정을 받았다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-08-02 06:31:42어윤호 -
 최초 심근병증치료제 '캄지오스', 상급종합병원 안착[데일리팜=어윤호 기자] 보험급여 등재를 노리는 '캄지오스'의 처방 환경 조성이 한창이다.관련 업계에 따르면 한국BMS제약 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)는 현재 삼성서울병원, 서울대병원, 서울아산병원, 신촌세브란스병원 등 빅5 종합병원을 비롯해 강원대병원, 경북대병원, 계명대병원, 부산대병원, 분당서울대병원, 전남대병원 등 전국 약 50개 의료기관의 약사위원회(DC, drug commitee)를 통과했다.이에 따라 캄지오스가 급여 등재에 성공하고 활발한 처방을 확보할 수 있을지 지켜 볼 부분이다. 현재 캄지오스는 지난 4일 건강보험심사평가원 약제급여평가위원회를 통과하고 건강보험공단과 약가협상을 앞두고 있다.캄지오스는 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적 의약품(BTD)으로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-07-22 06:23:17어윤호
최초 심근병증치료제 '캄지오스', 상급종합병원 안착[데일리팜=어윤호 기자] 보험급여 등재를 노리는 '캄지오스'의 처방 환경 조성이 한창이다.관련 업계에 따르면 한국BMS제약 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)는 현재 삼성서울병원, 서울대병원, 서울아산병원, 신촌세브란스병원 등 빅5 종합병원을 비롯해 강원대병원, 경북대병원, 계명대병원, 부산대병원, 분당서울대병원, 전남대병원 등 전국 약 50개 의료기관의 약사위원회(DC, drug commitee)를 통과했다.이에 따라 캄지오스가 급여 등재에 성공하고 활발한 처방을 확보할 수 있을지 지켜 볼 부분이다. 현재 캄지오스는 지난 4일 건강보험심사평가원 약제급여평가위원회를 통과하고 건강보험공단과 약가협상을 앞두고 있다.캄지오스는 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적 의약품(BTD)으로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-07-22 06:23:17어윤호 -
 BMS 심근병증 신약 '캄지오스', 약평위 재상정[데일리팜=어윤호 기자] 재논의 판정을 받았던 폐색성비대성심근병증 신약 '캄지오스'가 오늘 다시 심판대에 오른다.관련 업계에 따르면 한국BMS제약 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)가 4일 건강보험심사평가원 약제급여평가위원회에 상정된다.이에 따라 캄지오스가 급여 적정성을 인정받고 건강보험공단과 약가협상 단계로 넘어갈 수 있을지 지켜 볼 부분이다.캄지오스는 경제성평가소위원회 통과 후 예상보다 빠르게 약평위에 상정됐지만 한번 보류 판정을 받았다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-07-04 06:00:33어윤호
BMS 심근병증 신약 '캄지오스', 약평위 재상정[데일리팜=어윤호 기자] 재논의 판정을 받았던 폐색성비대성심근병증 신약 '캄지오스'가 오늘 다시 심판대에 오른다.관련 업계에 따르면 한국BMS제약 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)가 4일 건강보험심사평가원 약제급여평가위원회에 상정된다.이에 따라 캄지오스가 급여 적정성을 인정받고 건강보험공단과 약가협상 단계로 넘어갈 수 있을지 지켜 볼 부분이다.캄지오스는 경제성평가소위원회 통과 후 예상보다 빠르게 약평위에 상정됐지만 한번 보류 판정을 받았다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-07-04 06:00:33어윤호 -
 심근병증 혁신신약 '캄지오스', 약평위 재논의 판정[데일리팜=어윤호 기자] 역시 한번에 결론은 나지 않았다. 최초의 폐색성비대성심근병증 신약 '캄지오스'의 보험급여 등재 논의가 순탄치 않은 모습이다.관련 업계에 따르면 한국BMS제약 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)는 최근 건강보험심사평가원 약제급여평가위원회에 상정됐지만 '재논의' 판정을 받았다.경제성평가소위원회 통과 후 예상보다 빠르게 약평위에 상정됐지만 약물 자체가 해당 질환에서 최초 치료옵션인 만큼, 단번에 결과를 도출하진 못한 것으로 판단된다.다만 정부가 혁신신약 우대방안을 비롯 신약 가치산정에 대한 개선 의지를 보이고 있는 만큼, 다음 약평위에서 캄지오스의 평가에도 영향을 미칠지 지켜 볼 부분이다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-06-22 06:00:20어윤호
심근병증 혁신신약 '캄지오스', 약평위 재논의 판정[데일리팜=어윤호 기자] 역시 한번에 결론은 나지 않았다. 최초의 폐색성비대성심근병증 신약 '캄지오스'의 보험급여 등재 논의가 순탄치 않은 모습이다.관련 업계에 따르면 한국BMS제약 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)는 최근 건강보험심사평가원 약제급여평가위원회에 상정됐지만 '재논의' 판정을 받았다.경제성평가소위원회 통과 후 예상보다 빠르게 약평위에 상정됐지만 약물 자체가 해당 질환에서 최초 치료옵션인 만큼, 단번에 결과를 도출하진 못한 것으로 판단된다.다만 정부가 혁신신약 우대방안을 비롯 신약 가치산정에 대한 개선 의지를 보이고 있는 만큼, 다음 약평위에서 캄지오스의 평가에도 영향을 미칠지 지켜 볼 부분이다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.2024-06-22 06:00:20어윤호 -
 경제성 평가 마친 '캄지오스', 약평위 상정 기대[데일리팜=어윤호 기자] 최초의 폐색성비대성심근병증 신약 '캄지오스'의 보험급여 등재 논의에 진전이 생길지 주목된다.관련 업계에 따르면, 한국BMS제약 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)는 최근 건강보험심사평가원 경제성평가소위원회를 통과, 약제급여평가위원회 상정 일정을 조율 중이다. 이르면 오는 6월 약평위 상정 가능성도 점쳐진다.캄지오스가 해당 질환에서 최초 치료옵션이기 때문에 첫번째 도전에서 어떤 결과가 도출될지 지켜 볼 부분이다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.김형관 서울대병원 순환기내과 교수는 "근시안적으로 보면 캄지오스의 급여 등재가 건강보험 재정에 부담으로 느껴질 수 있지만, 거시적으로 시야를 확장해보면 그렇지 않다고 본다. oHCM 환자들을 제대로 치료하지 않고 방치하면 심부전 발생 위험이 높아져 이로 인해 소요되는 직간접적 의료비용이 증가할 수밖에 없다"고 말했다.2024-05-29 06:00:12어윤호
경제성 평가 마친 '캄지오스', 약평위 상정 기대[데일리팜=어윤호 기자] 최초의 폐색성비대성심근병증 신약 '캄지오스'의 보험급여 등재 논의에 진전이 생길지 주목된다.관련 업계에 따르면, 한국BMS제약 폐색성비대성심근병증(oHCM, obstructive hypertrophic cardiomyopathy) 신약 캄지오스(마바캄텐)는 최근 건강보험심사평가원 경제성평가소위원회를 통과, 약제급여평가위원회 상정 일정을 조율 중이다. 이르면 오는 6월 약평위 상정 가능성도 점쳐진다.캄지오스가 해당 질환에서 최초 치료옵션이기 때문에 첫번째 도전에서 어떤 결과가 도출될지 지켜 볼 부분이다.이 약은 폐색성비대성심근병증의 발생 원인인 심장 마이오신과 액틴의 과도한 교차결합을 선택적으로 억제하는 유일한 치료제다. 마이오신을 액틴으로부터 분리시켜 과도하게 수축했던 심장 근육을 이완시켜, 비대해진 좌심실 구조와 좌심실 유출로 폐색을 개선하는 기전을 갖고 있다.폐색성비대성심근병증은 오랜 시간 치료제가 전무해 오프라벨 약제로 증상관리가 이뤄져 왔다.실제 캄지오스의 등장으로 지난해 유럽심장학회(ESC)는 9년 만에 가이드라인은 업데이트했다. 과거 HCM 가이드라인은 개별 기관에서 보고된 소규모 관찰 데이터, 후향적 분석 결과 또는 전문가 합의 의견(consensus opinion) 정도의 근거만을 바탕으로 가이드라인을 구성할 수밖에 없었다.그런데 캄지오스가 상황을 완전히 바꿨다. 대규모 3상 무작위대조시험(RCT) 임상 연구 2건에서 캄지오스의 유의한 효과를 확인하면서 ESC 가이드라인에서 캄지오스는 치료옵션 중 최초로 가장 높은 근거 수준인 A로 권고됐다. 현재 미국심장학회(ACC)와 미국심장협회(AHA)에서도 가이드라인 업데이트를 준비 중이다.여기에 3상 근거를 바탕으로 캄지오스는 미국 FDA서 획기적의약품지정(BTD)로 지정·허가됐다.이 같은 요소들을 살펴보면 캄지오스는 지난해 정부가 발표한 혁신신약 기준인 ▲대체 가능하거나 치료적 위치가 동등한 제품 또는 치료법이 없는 경우 ▲생존기간의 상당기간 연장 등 임상적으로 의미있는 개선이 입증된 경우 ▲식약처 GIFT(우선심사 대상 지정)-미국 FDA 획기적의약품지정(BTD)-유럽 EMA 신속심사(PRIME)로 허가된 경우 등을 충족하는 것으로 보여진다.한편 캄지오스는 3상 EXPLORER-HCM 연구를 통해 유효성을 확인했다. 해당 임상에서 캄지오스는 1차평가변수인 환자 증상(NYHA 등급)과 운동능력(최고산소섭취량, pVO2) 위약 대비 두 배 이상 개선했다.이중 캄지오스 투약군의 20%는 NYHA 등급과 pVO2 개선을 모두 달성했다. 운동 후 좌심실 유출로 폐색 지표도 4배 이상 감소했다. 캄지오스 치료를 받은 10명 중 7명은 수술을 고려하지 않을 정도로 지표가 개선됐으며, 30주간 일관된 효과를 유지했다.김형관 서울대병원 순환기내과 교수는 "근시안적으로 보면 캄지오스의 급여 등재가 건강보험 재정에 부담으로 느껴질 수 있지만, 거시적으로 시야를 확장해보면 그렇지 않다고 본다. oHCM 환자들을 제대로 치료하지 않고 방치하면 심부전 발생 위험이 높아져 이로 인해 소요되는 직간접적 의료비용이 증가할 수밖에 없다"고 말했다.2024-05-29 06:00:12어윤호
오늘의 TOP 10
- 1개설허가 7개월 만에 제1호 창고형약국 개설자 변경
- 2급여 생존의 대가...애엽 위염약 약가인하 손실 연 150억
- 3약국서 카드 15만원+현금 5만원 결제, 현금영수증은?
- 4부광, 유니온제약 인수…공장은 얻었지만 부채는 부담
- 51호 창고형약국 불법 전용 논란 일단락…위반건축물 해제
- 6P-CAB 3종 경쟁력 제고 박차…자큐보, 구강붕해정 탑재
- 7발사르탄 원료 사기 사건 2심으로...민사소송 확전될까
- 8국내제약, 결핵치료제 '서튜러' 특허도전 1심 승리
- 9카나프테라퓨틱스, 코스닥 상장 예비심사 통과
- 10대전시약, 공공심야약국 점검…내년 동구에도 개설
-
순위상품명횟수
-
1타이레놀정500mg(10정)30,426
-
2판콜에스내복액16,732
-
3텐텐츄정(10정)13,671
-
4까스활명수큐액12,867
-
5판피린큐액12,851












![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
