총 151건
-
 강원도약, 첫 스크린 골프대회…‘춘천분회 팀’ 우승 차지[데일리팜=김지은 기자] 강원특별자치도약사회(회장 이효선)는 지난 14일 춘천 골프존파크 퇴계남춘천점에서 ‘제1회 강원특별자치도약사회장배 셀로맥스 약업인 스크린 골프대회’를 진행했다.이효선 회장은 개회사에서 “회원 약사, 약업인 화합과 친목을 위해 처음으로 대회를 개최하게 됐는데 추운날씨에도 참석하신 모든 분들께 감사드린다”며 “우리 약사회는 앞으로도 회원간 소통을 위해 노력할 것이다. 내년에도 함께 하길 기원한다”고 말했다. 이어 이번 대회 후원사인 셀로맥스 서정민 대표의 축사를 김원준 총무이사가 대독했다.이날 대회는 단체전에서 춘천분회2(김원준, 최영준, 윤일훈, 이효빈)팀이 우승을, 원주분회1(윤주해, 곽정근, 진용근, 김호찬)팀이 준우승을, 강릉분회(최상순, 이기석, 최홍필, 김진만)팀이 3위를 차지했다. 개인전에서는 최영준 메달리스트, 곽정근 롱기스트, 서성민 니어리스트, 진용근, 김호찬 이글상을 받았다. 도약사회는 “이번 대회는 회원 간 유대와 약업인들과의 교류를 확대하는 의미있는 자리가 됐다”고 평가했다.2025-12-16 11:45:53김지은 기자
강원도약, 첫 스크린 골프대회…‘춘천분회 팀’ 우승 차지[데일리팜=김지은 기자] 강원특별자치도약사회(회장 이효선)는 지난 14일 춘천 골프존파크 퇴계남춘천점에서 ‘제1회 강원특별자치도약사회장배 셀로맥스 약업인 스크린 골프대회’를 진행했다.이효선 회장은 개회사에서 “회원 약사, 약업인 화합과 친목을 위해 처음으로 대회를 개최하게 됐는데 추운날씨에도 참석하신 모든 분들께 감사드린다”며 “우리 약사회는 앞으로도 회원간 소통을 위해 노력할 것이다. 내년에도 함께 하길 기원한다”고 말했다. 이어 이번 대회 후원사인 셀로맥스 서정민 대표의 축사를 김원준 총무이사가 대독했다.이날 대회는 단체전에서 춘천분회2(김원준, 최영준, 윤일훈, 이효빈)팀이 우승을, 원주분회1(윤주해, 곽정근, 진용근, 김호찬)팀이 준우승을, 강릉분회(최상순, 이기석, 최홍필, 김진만)팀이 3위를 차지했다. 개인전에서는 최영준 메달리스트, 곽정근 롱기스트, 서성민 니어리스트, 진용근, 김호찬 이글상을 받았다. 도약사회는 “이번 대회는 회원 간 유대와 약업인들과의 교류를 확대하는 의미있는 자리가 됐다”고 평가했다.2025-12-16 11:45:53김지은 기자 -
 1300억 애엽 위염약 퇴출 모면...제네릭·개량신약 기사회생[데일리팜=천승현 기자] 애엽 추출물 성분 위염치료제가 건강보험 급여목록에서 퇴출 위기에서 벗어날 전망이다. 급여 재평가 결과 급여 삭제 위기에 놓였지만 약가인하를 통한 생존에 무게가 실린다. 제약사들은 연간 1300억원 규모 대형 캐시카우의 상실 위기에서 기사회생하는 분위기다. 100억원 이상을 투입해 애엽 추출물의 동등성 평가 임상시험을 추진 중인 제네릭 업체들도 한숨을 돌리게 됐다. 동아에스티가 2년 동안 수백명의 피험자를 대상으로 개발한 개량신약도 좌초 위기를 모면하게 됐다. 5일 업계에 따르면 건강보험심사평가원은 애엽 추출물의 급여 적정성 평가 결과 ‘비용효과성 충족시 급여적정성 있음’이라고 제약사들의 이의신청 결과를 공개했다. 애엽 성분 의약품은 쑥을 기반으로 만드는 천연물의약품이다. 동아에스티의 ‘스티렌’이 오리지널 제품으로 급성위염과 만성위염의 위점막 병변, 출혈, 발적, 부종 등의 개선에 사용된다. ‘비스테로이드소염진통제(NSAID) 투여로 인한 위염 예방’ 적응증도 보유 중이다. 심평원은 지난 8월 약제급여평가위원회에서 심의한 결과 애엽 추출물에 대해 임상적 유용성 근거가 없다는 이유로 급여 적정성이 없다는 결론을 내렸다. 제약사들은 급여 재평가 결과를 수용할 수 없다며 이의신청을 제기했고 10%대 약가인하를 수용하면 비용효과성을 충족해 급여 적정성이 있다는 게 심평원의 판단이다. 의약품 조사기관 유비스트에 따르면 애엽 추출물은 지난해 1298억원의 외래 처방시장을 형성했다. 올해 3분기 누적 처방액은 918억원에 달했다.제약사들 입장에선 약가인하를 수용하면 1000억원 이상의 캐시카우의 퇴출을 저지할 수 있게 된다. 애엽 추출물이 급여목록에 잔류하면 제네릭 업체들이 추진하는 대규모 동등성 재평가 임상시험도 좌초 위기에서 벗어날 수 있다. 제약사 50여곳은 지난 6월 말 식품의약품안전처에 애엽 성분 위염치료제의 임상시험 계획서를 제출했다. 오리지널 의약품 스티렌과 스티렌투엑스를 각각 대조약으로 위염치료제 효능을 비교하는 내용의 임상시험이다. 식약처의 동등성 재평가 지시에 따른 임상시험 수행 계획이다. 식약처는 지난해 12월 한약·생약제제 전문의약품 212개 품목에 대해 동등성 재평가를 지시했다. 오리지널 의약품과의 동등성을 입증하면 허가를 인정해주겠다는 의미다. 애엽 성분 의약품 135개 품목이 동등성 재평가 대상에 포함됐다. 제약사들은 동등성 재평가 대상 애엽 추출물 의약품을 스티렌과 스티렌투엑스와 각각 비교 임상시험하는 방식으로 동등성을 입증할 계획이다. 생약제제 특성상 유효 성분의 혈중농도를 비교하는 생물학적동등성시험으로 동등성을 입증하기 어렵다는 이유에서다. 스티렌과 스티렌투엑스 제네릭 제품들은 비교 용출과 비교 붕해 방식으로 허가받았다. 동등성 평가 임상시험은 애엽 성분 의약품을 생산하는 수탁사를 중심으로 진행된다. 풍림무약이 애엽 성분 60mg와 90mg 2건의 임상시험을 별도로 진행하고, 마더스제약이 애엽 성분 60mg의 임상시험을 수행하는 방식이다. 임상시험 1건당 모집 피험자는 400명 이상 설정한 것으로 전해졌다. 3건의 임상시험 비용은 총 150억원으로 책정된 것으로 알려졌다. 제약사들은 식약처의 보완 지시로 임상 디자인을 재설계하고 있다. 이미 스티렌 제네릭의 용량과 제조업체별로 별도의 임상시험을 설계하면서 임상시험 규모와 비용이 커졌고 시장 철수 제품이 속출했다. 올해 들어 애엽 성분 위염치료제 60개 제품이 시장에서 철수했다. 지난 6월부터 한달 동안 애엽 성분 위염치료제 47개 품목이 동시다발로 시장에서 사라졌다. 동아에스티가 개발한 애엽추출물 개량신약도 좌초 위기에서 벗어날 전망이다. 동아에스티는 DA-5219 임상3상시험을 지난 7월 종료했다. DA-5219은 애엽 추출물 성분 스티렌을 복용 횟수를 1일 3회에서 1회로 줄인 서방형 제제다. 애엽 추출물의 용량이 스티렌 60mg보다 3배 많은 180mg 함유한 것으로 추정된다. 지난 2023년 10월 DA-5219의 급만성 위염에 대한 임상3상시험 계획을 승인 받은 이후 2년 만에 임상시험이 마무리됐다. 급성 또는 만성 위염 환자에서 DA-5219을 스티렌과 비교해 유효성 및 안전성을 평가하기 위한 임상시험이다. 임상시험은 현대병원, 인하대의과대학부속병원, 건국대병원, 강동경희대의대병원, 아산사회복지재단서울아산병원, 가톨릭대여의도성모병원, 가톨릭대인천성모병원, 고신대 복음병원, 부산대병원, 분당서울대병원, 삼성서울병원, 서울대병원, 원주세브란스기독병원, 연세대의과대학세브란스병원, 영남대병원, 이화여자대의과대학부속서울병원, 예수병원유지재단 예수병원, 전북대병원, 중앙대병원, 충남대병원, 칠곡경북대병원, 가톨릭대서울성모병원, 건양대병원, 춘천성심병원, 한림대성심병원 등 26곳에서 진행됐다. 임상시험 기간은 2023년 12월부터 올해 12월로 설계됐다. 지난 7월 목표 시험 대상자 452명에 대한 최종 시험대상자 관찰이 종료됐다. 임상시험에는 수십억원이 투입된 것으로 전해졌다. 동아에스티는 지난달 DA-5219의 주 유효성 평가변수인 ‘상부위장관 내시경 검사상 위점막 미란의 유효율’에 대해 스티렌에 비해 열등하지 않다고 판단했다는 임상 결과를 공개했다. 동아에스티는 “유효성 및 안전성 상세 분석 진행 후 식품의약품안전처(MFDS)에 최종 결과보고서 제출 및 품목허가 신청 예정이다”라고 밝혔다. 동아에스티는 지난 2015년 10월 스티렌 주 성분의 용량을 60mg에서 90mg으로 늘려 1일 2회 복용하는 스티렌투엑스를 허가받은 바 있다. DA-5219가 식약처 허가를 받으면 스티렌투엑스에 이어 10년 만에 복용 편의성을 개선한 개량신약이 등장하는 셈이다. 하지만 애엽 추출물이 급여 퇴출되면 DA-5219가 식약처 허가를 통과하더라도 급여 등재를 장담하기 쉽지 않은 상황이다. 1일 복용 횟수를 줄여 복용 편의성을 높였지만 애엽 추출물의 급여 적정성이 인정받지 못했다는 이유로 급여 등재를 낙관할 수 없다. 보건당국의 급여재평가 결과 제약사들의 연구개발 노력이 수포로 돌아갈 수 있다는 우려가 제기됐다. 애엽 추출물의 약가인하로 급여가 유지되면 DA-5219도 약가비교를 통해 급여진입 가능성이 높아질 것으로 보인다. 다만 애엽 추출물의 약가인하로 급여목록에 잔류하더라도 약가제도 개편으로 또 다시 약가가 내려갈 수 있다는 점이 변수다. 내년 7월 시행 예정인 개편 약가제도에서 제네릭의 약가 산정기준은 특허만료 전 신약의 53.55%에서 40%대로 내려간다. 정부는 기등재 제네릭을 개편 약가제도 산정 기준에 맞춰 내리는 방안을 추진할 예정이다. 제약사 한 관계자는 “애엽추출물의 약가가 인하되고 약가제도 개편으로 또 다시 내려가면 열악한 원가구조로 시장에서 철수하는 제품이 속출할 수 있다”라고 우려했다.2025-12-05 12:05:59천승현 기자
1300억 애엽 위염약 퇴출 모면...제네릭·개량신약 기사회생[데일리팜=천승현 기자] 애엽 추출물 성분 위염치료제가 건강보험 급여목록에서 퇴출 위기에서 벗어날 전망이다. 급여 재평가 결과 급여 삭제 위기에 놓였지만 약가인하를 통한 생존에 무게가 실린다. 제약사들은 연간 1300억원 규모 대형 캐시카우의 상실 위기에서 기사회생하는 분위기다. 100억원 이상을 투입해 애엽 추출물의 동등성 평가 임상시험을 추진 중인 제네릭 업체들도 한숨을 돌리게 됐다. 동아에스티가 2년 동안 수백명의 피험자를 대상으로 개발한 개량신약도 좌초 위기를 모면하게 됐다. 5일 업계에 따르면 건강보험심사평가원은 애엽 추출물의 급여 적정성 평가 결과 ‘비용효과성 충족시 급여적정성 있음’이라고 제약사들의 이의신청 결과를 공개했다. 애엽 성분 의약품은 쑥을 기반으로 만드는 천연물의약품이다. 동아에스티의 ‘스티렌’이 오리지널 제품으로 급성위염과 만성위염의 위점막 병변, 출혈, 발적, 부종 등의 개선에 사용된다. ‘비스테로이드소염진통제(NSAID) 투여로 인한 위염 예방’ 적응증도 보유 중이다. 심평원은 지난 8월 약제급여평가위원회에서 심의한 결과 애엽 추출물에 대해 임상적 유용성 근거가 없다는 이유로 급여 적정성이 없다는 결론을 내렸다. 제약사들은 급여 재평가 결과를 수용할 수 없다며 이의신청을 제기했고 10%대 약가인하를 수용하면 비용효과성을 충족해 급여 적정성이 있다는 게 심평원의 판단이다. 의약품 조사기관 유비스트에 따르면 애엽 추출물은 지난해 1298억원의 외래 처방시장을 형성했다. 올해 3분기 누적 처방액은 918억원에 달했다.제약사들 입장에선 약가인하를 수용하면 1000억원 이상의 캐시카우의 퇴출을 저지할 수 있게 된다. 애엽 추출물이 급여목록에 잔류하면 제네릭 업체들이 추진하는 대규모 동등성 재평가 임상시험도 좌초 위기에서 벗어날 수 있다. 제약사 50여곳은 지난 6월 말 식품의약품안전처에 애엽 성분 위염치료제의 임상시험 계획서를 제출했다. 오리지널 의약품 스티렌과 스티렌투엑스를 각각 대조약으로 위염치료제 효능을 비교하는 내용의 임상시험이다. 식약처의 동등성 재평가 지시에 따른 임상시험 수행 계획이다. 식약처는 지난해 12월 한약·생약제제 전문의약품 212개 품목에 대해 동등성 재평가를 지시했다. 오리지널 의약품과의 동등성을 입증하면 허가를 인정해주겠다는 의미다. 애엽 성분 의약품 135개 품목이 동등성 재평가 대상에 포함됐다. 제약사들은 동등성 재평가 대상 애엽 추출물 의약품을 스티렌과 스티렌투엑스와 각각 비교 임상시험하는 방식으로 동등성을 입증할 계획이다. 생약제제 특성상 유효 성분의 혈중농도를 비교하는 생물학적동등성시험으로 동등성을 입증하기 어렵다는 이유에서다. 스티렌과 스티렌투엑스 제네릭 제품들은 비교 용출과 비교 붕해 방식으로 허가받았다. 동등성 평가 임상시험은 애엽 성분 의약품을 생산하는 수탁사를 중심으로 진행된다. 풍림무약이 애엽 성분 60mg와 90mg 2건의 임상시험을 별도로 진행하고, 마더스제약이 애엽 성분 60mg의 임상시험을 수행하는 방식이다. 임상시험 1건당 모집 피험자는 400명 이상 설정한 것으로 전해졌다. 3건의 임상시험 비용은 총 150억원으로 책정된 것으로 알려졌다. 제약사들은 식약처의 보완 지시로 임상 디자인을 재설계하고 있다. 이미 스티렌 제네릭의 용량과 제조업체별로 별도의 임상시험을 설계하면서 임상시험 규모와 비용이 커졌고 시장 철수 제품이 속출했다. 올해 들어 애엽 성분 위염치료제 60개 제품이 시장에서 철수했다. 지난 6월부터 한달 동안 애엽 성분 위염치료제 47개 품목이 동시다발로 시장에서 사라졌다. 동아에스티가 개발한 애엽추출물 개량신약도 좌초 위기에서 벗어날 전망이다. 동아에스티는 DA-5219 임상3상시험을 지난 7월 종료했다. DA-5219은 애엽 추출물 성분 스티렌을 복용 횟수를 1일 3회에서 1회로 줄인 서방형 제제다. 애엽 추출물의 용량이 스티렌 60mg보다 3배 많은 180mg 함유한 것으로 추정된다. 지난 2023년 10월 DA-5219의 급만성 위염에 대한 임상3상시험 계획을 승인 받은 이후 2년 만에 임상시험이 마무리됐다. 급성 또는 만성 위염 환자에서 DA-5219을 스티렌과 비교해 유효성 및 안전성을 평가하기 위한 임상시험이다. 임상시험은 현대병원, 인하대의과대학부속병원, 건국대병원, 강동경희대의대병원, 아산사회복지재단서울아산병원, 가톨릭대여의도성모병원, 가톨릭대인천성모병원, 고신대 복음병원, 부산대병원, 분당서울대병원, 삼성서울병원, 서울대병원, 원주세브란스기독병원, 연세대의과대학세브란스병원, 영남대병원, 이화여자대의과대학부속서울병원, 예수병원유지재단 예수병원, 전북대병원, 중앙대병원, 충남대병원, 칠곡경북대병원, 가톨릭대서울성모병원, 건양대병원, 춘천성심병원, 한림대성심병원 등 26곳에서 진행됐다. 임상시험 기간은 2023년 12월부터 올해 12월로 설계됐다. 지난 7월 목표 시험 대상자 452명에 대한 최종 시험대상자 관찰이 종료됐다. 임상시험에는 수십억원이 투입된 것으로 전해졌다. 동아에스티는 지난달 DA-5219의 주 유효성 평가변수인 ‘상부위장관 내시경 검사상 위점막 미란의 유효율’에 대해 스티렌에 비해 열등하지 않다고 판단했다는 임상 결과를 공개했다. 동아에스티는 “유효성 및 안전성 상세 분석 진행 후 식품의약품안전처(MFDS)에 최종 결과보고서 제출 및 품목허가 신청 예정이다”라고 밝혔다. 동아에스티는 지난 2015년 10월 스티렌 주 성분의 용량을 60mg에서 90mg으로 늘려 1일 2회 복용하는 스티렌투엑스를 허가받은 바 있다. DA-5219가 식약처 허가를 받으면 스티렌투엑스에 이어 10년 만에 복용 편의성을 개선한 개량신약이 등장하는 셈이다. 하지만 애엽 추출물이 급여 퇴출되면 DA-5219가 식약처 허가를 통과하더라도 급여 등재를 장담하기 쉽지 않은 상황이다. 1일 복용 횟수를 줄여 복용 편의성을 높였지만 애엽 추출물의 급여 적정성이 인정받지 못했다는 이유로 급여 등재를 낙관할 수 없다. 보건당국의 급여재평가 결과 제약사들의 연구개발 노력이 수포로 돌아갈 수 있다는 우려가 제기됐다. 애엽 추출물의 약가인하로 급여가 유지되면 DA-5219도 약가비교를 통해 급여진입 가능성이 높아질 것으로 보인다. 다만 애엽 추출물의 약가인하로 급여목록에 잔류하더라도 약가제도 개편으로 또 다시 약가가 내려갈 수 있다는 점이 변수다. 내년 7월 시행 예정인 개편 약가제도에서 제네릭의 약가 산정기준은 특허만료 전 신약의 53.55%에서 40%대로 내려간다. 정부는 기등재 제네릭을 개편 약가제도 산정 기준에 맞춰 내리는 방안을 추진할 예정이다. 제약사 한 관계자는 “애엽추출물의 약가가 인하되고 약가제도 개편으로 또 다시 내려가면 열악한 원가구조로 시장에서 철수하는 제품이 속출할 수 있다”라고 우려했다.2025-12-05 12:05:59천승현 기자 -
심평원, 디지털클라우드센터 개소..."빅데이터 고도화 전환점"[데일리팜=정흥준 기자]건강보험심사평가원(원장 강중구, 이하 심평원)은 2일 본원 2사옥에서 디지털클라우드센터 개소식을 개최했다.이날 개소식에는 보건복지부, 원주시 관계자와 강원 혁신도시 공공기관 관계자 등 200여명이 참석한 가운데 성황리에 진행됐다.심평원 디지털클라우드센터는 인공지능(AI), 빅데이터, 클라우드 기반의 첨단 인프라를 갖춘 통합 플랫폼이다. 건강보험·의료데이터를 안전하고 효율적으로 관리함으로써 국민 맞춤형 건강관리와 보건의료 정책 고도화의 핵심 기반이 될 전망이다.특히 이번 개소를 통해 방대한 건강보험 데이터를 안전하게 저장하고 분석할 수 있는 첨단 인프라 환경을 구축했다.심평원은 기후변화에 능동적으로 대처할 수 있는 공조시설과 사이버 위협에 대한 대비 태세도 한층 강화했다는 설명이다.강중구 원장은 “이번 디지털클라우드센터 개소는 단순한 시설 확충을 넘어, 국민의 건강정보를 과학적으로 분석하고 활용할 수 있는 새로운 전환점”이라며 “데이터를 중심으로 한 정책 혁신을 통해 ‘가치있는 심사·평가, 같이가는 국민건강’을 실현하겠다”고 전했다.심평원은 앞으로 디지털클라우드센터를 기반으로 ▲AI 기반 질병 예측 모델 개발 ▲의료비 효율화 ▲공공데이터 개방 및 민·관 협력 강화 등 디지털 보건의료 생태계 조성에 앞장설 계획이다.2025-12-02 22:04:20정흥준 기자
-
 강원 원주시약, 겨울나기 연탄 기부·배달 봉사 진행[데일리팜=김지은 기자] 강원도 원주시약사회(회장 엄일훈)는 23일 연말을 앞두고 난방 지원이 필요한 이웃의 따뜻한 겨울나기를 위해 연탄 기부·배달 봉사를 진행했다고 밝혔다.시약사회는 올해 총 2500장의 연탄을 밥상공동체 연탄은행을 통해 후원하고 이 중 1500장을 우산동 일대 에너지 취약 5가구에 직접 전달했다.이번 봉사에는 지역 내 회원 약사와 강원지오영 원주센터, 동원약품 원주지점, 광동제약, 녹십자, 동국제약, 제일헬스사이언스 등 지역 약업인, 그 가족들이 함께 참여했다.엄일훈 회장은 “추운 날씨에도 힘을 모아 연탄을 나르며 따뜻한 마음을 함께해 주셔서 감사하다”며 “덕분에 올해도 이웃들에 실질적 도움을 드릴 수 있었다. 앞으로도 지역사회를 위한 사회공헌 활동을 지속적으로 이어가겠다”고 말했다.시약사회는 매년 난방 취약계층을 위한 연탄 나눔 뿐만 아니라 다양한 사회 활동을 통해 지역 공동체 상생에 앞장서고 있다고 밝혔다.2025-11-24 14:50:33김지은
강원 원주시약, 겨울나기 연탄 기부·배달 봉사 진행[데일리팜=김지은 기자] 강원도 원주시약사회(회장 엄일훈)는 23일 연말을 앞두고 난방 지원이 필요한 이웃의 따뜻한 겨울나기를 위해 연탄 기부·배달 봉사를 진행했다고 밝혔다.시약사회는 올해 총 2500장의 연탄을 밥상공동체 연탄은행을 통해 후원하고 이 중 1500장을 우산동 일대 에너지 취약 5가구에 직접 전달했다.이번 봉사에는 지역 내 회원 약사와 강원지오영 원주센터, 동원약품 원주지점, 광동제약, 녹십자, 동국제약, 제일헬스사이언스 등 지역 약업인, 그 가족들이 함께 참여했다.엄일훈 회장은 “추운 날씨에도 힘을 모아 연탄을 나르며 따뜻한 마음을 함께해 주셔서 감사하다”며 “덕분에 올해도 이웃들에 실질적 도움을 드릴 수 있었다. 앞으로도 지역사회를 위한 사회공헌 활동을 지속적으로 이어가겠다”고 말했다.시약사회는 매년 난방 취약계층을 위한 연탄 나눔 뿐만 아니라 다양한 사회 활동을 통해 지역 공동체 상생에 앞장서고 있다고 밝혔다.2025-11-24 14:50:33김지은 -
 방광암 면역치료 최초 IL-15 초작용제 '안크티바'안크티바(Anktiva®, 성분명: 노가펜데킨 알파 인바키셉트-pmln, nogapendekin alfa inbakicept-pmln, ImmunityBio)는 IL-15 초작용제(superagonist) 복합체로 개발된 최초의 방광 내 면역치료제다.2024년 4월 미국 FDA에서 유두종 유무와 관계없이 상피내암(CIS)을 동반한 BCG-불응성 비근육침윤성 방광암(non-muscle invasive bladder cancer, NMIBC) 성인 환자를 대상으로 BCG와 병용 사용하는 치료제로 승인됐다.방광암은 전 세계적으로 흔한 악성 종양 중 하나다. 국내에서도 발생 빈도가 높은 암종으로 알려져 있다. 이 중 약 75%는 비근육침윤성 방광암(NMIBC)으로 분류되며, 초기 치료는 대개 경요도 방광 종양 절제술(transurethral resection of bladder tumor, TURBT)로 시작된다.그러나 NMIBC는 60–70%의 재발률을 보이므로, TURBT 이후 방광 내 치료(intravesical therapy)가 질병의 재발을 억제하고 진행을 지연시키는 데 핵심적인 역할을 한다.현재 방광 내 치료는 크게 두 가지로 구분되며, 하나는 BCG 요법을 기반으로 하는 면역치료, 다른 하나는 미토마이신 C, 젬시타빈, 에피루비신, 독소루비신 등으로 구성되는 화학요법이다.BCG는 NMIBC의 표준 치료 중 하나이지만, 약 40%의 환자에서는 충분한 치료 효과를 보이지 못한다. 안크티바는 이러한 BCG-불응성 환자에서 방광 절제술을 피할 수 있는 새로운 치료 대안으로 개발됐다.IL-15는 NK 세포와 CD8⁺ T 세포의 활성, 증식, 기억 형성에 관여하는 중요한 사이토카인이다. 안크티바는 IL-15 변형체와 IL-15Rα의 sushi(반복 단백질 구조) domain이 결합한 IL-15 초작용제(superagonist) 복합체를 통해 NK 세포, CD4⁺ T 세포, CD8⁺ T 세포의 활성을 강력하게 유도하며, 특히 종양 특이적 기억 T 세포 반응을 증폭시켜 항종양 면역반응을 강화한다.임상시험에서 BCG 유지요법과 함께 안크티바를 투여받은 77명의 환자 중 62%(95% CI, 51–73)가 완전관해에 도달했다. 이 반응은 일부 환자에서 최대 47개월까지 지속됐다. 완전관해가 12개월 이상 유지된 비율은 58%, 24개월 이상 유지된 비율은 40%였다.치료 스케줄은 방광 내 카테터를 통한 유도요법(6주간 주 1회) 후, 4, 7, 10, 13, 19개월째의 유지요법(각 3주간 주 1회)으로 구성된다. 3개월 시점에 완전 반응이 확인되지 않으면 두 번째 유도요법을 시행할 수 있으며, 25개월 이후에도 완전 반응이 지속되는 경우에는 25, 31, 37개월째에 추가 BCG 유지투여를 실시할 수 있다. 투여 시 약물 혼합액은 방광 내에 2시간 동안 유지한 뒤 배출한다.안크티바 치료에는 몇 가지 중요한 주의사항이 있다. 방광절제술을 지연함으로써 전이성 방광암으로 진행할 위험이 존재하며, 배아–태아 독성 가능성이 보고되어 가임기 여성은 치료 중과 마지막 투여 후 최소 1주일 동안 피임이 필요하다.흔하게 보고되는 이상반응으로는 배뇨곤란, 혈뇨, 빈뇨, 절박뇨, 요로감염, 근골격계 통증, 발열 및 오한 등이 있으며, 실험실 검사에서는 크레아티닌 상승과 칼륨 상승이 비교적 흔하게 관찰된다.방광암(Bladder Cancer)이란 무엇인가?방광암은 요로계에서 가장 흔히 발생하는 악성 종양 중 하나로, 소변을 저장하는 장기인 방광의 점막 상피세포에서 주로 기원한다.전 세계적으로 방광암은 발생률과 사망률 측면에서 중요한 건강 문제를 야기하고 있으며, 특히 남성에서 높은 발생 빈도를 보인다. 방광암의 발생에는 흡연이 가장 강력한 위험 요인으로 작용하는 것으로 알려져 있다. 이 외에도 직업적 발암물질 노출, 만성 요로 감염 및 요로 결석 등이 발병과 연관돼 있다.조직학적으로 방광암의 대다수는 요로상피암(urothelial carcinoma)으로, 전체 방광암의 약 90%를 차지한다. 요로상피암은 방광뿐 아니라 요관, 신우, 요도 등 요로 전반에 걸쳐 발생할 수 있는 특성을 지니고 있다.이 외에도 만성 자극이나 염증과 관련된 편평세포암(squamous cell carcinoma), 드물게 선종 양상의 조직학적 특징을 보이는 선암(adenocarcinoma), 그리고 고도로 공격적인 생물학적 특성을 나타내는 소세포암(small cell carcinoma) 등 다양한 형태가 존재한다. 이러한 조직형의 차이는 임상적 경과, 치료 전략 및 예후와 밀접하게 연관되어 있어 진단 시 정확한 병리학적 분류가 필수적이다.방광암의 병기 결정은 치료 방침 수립과 예후 평가에 있어 핵심적인 요소이다. 국제적으로 널리 사용되는 TNM 병기 체계는 종양의 침윤 정도(T), 국소 림프절 전이 여부(N), 및 원격 전이 여부(M)에 기반하여 병기를 구분한다.특히 방광벽의 근육층 침윤 여부는 임상적 의사결정에서 매우 중요한 기준으로 작용한다. 종양이 점막층에 국한된 Ta 병기, 상피 내에서 편평하게 확산되는 상피내암(carcinoma in situ, CIS), 그리고 점막하층을 침범하나 근육층에는 도달하지 않은 T1 병기는 비근침윤성 방광암(non–muscle invasive bladder cancer, NMIBC)으로 분류된다.반면, 종양이 방광 근육층을 침범하는 T2 병기부터는 근침윤성 방광암(muscle invasive bladder cancer, MIBC)으로 정의되며, 이후 주변 지방조직(T3) 및 인접 장기(T4)로의 침윤 여부에 따라 병기가 상승한다. 림프절 전이(N1–N3)와 원격 전이(M1)의 존재는 질병의 진행을 시사하며 전신적 치료 전략이 요구된다.Non–Muscle Invasive Bladder Cancer(NMIBC) and Muscle Invasive Bladder Cancer(출처: https://cgoncology.com/science/).이와 같이 방광암은 조직학적 이질성과 침윤 정도에 따른 이분화된 임상 양상을 보이며, 병기 및 조직형은 환자의 치료 선택과 예후에 결정적인 영향을 미친다.비근침윤성 방광암(Non–muscle invasive bladder cancer, NMIBC)은 무엇인가?비근육 침습성 방광암(NMIBC)은 새로 진단되는 방광암의 약 75%를 차지하며, 병변이 주로 요로상피의 표층(Ta), 점막하층(T1) 또는 상피내암(CIS)에 국한되는 질환이다.NMIBC는 즉각적으로 생명을 위협하는 경우는 드물지만, 높은 재발률과 적지 않은 진행 위험으로 인해 임상적으로 중요한 도전 과제로 여겨진다. 실제로 환자의 약 50~70%가 초기 치료 이후 재발을 경험하며, 최대 30%는 근육 침습성 또는 전이성 방광암으로 진행한다.수십 년 동안 고위험군 NMIBC 환자에서 경요도 방광 종양 절제술(transurethral resection of bladder tumor, TURBT) 후 시행되는 BCG(Bacillus Calmette–Guérin) 치료는 재발과 진행을 효과적으로 억제하는 표준 치료로 자리매김해 왔다.그러나 BCG 치료의 임상적 이점에도 불구하고 약 40%의 환자에서 실패가 발생하며, 이 경우 추가적인 치료 전략이 필요하다. 이러한 환자군에서 전통적으로 가장 선호된 치료는 근치적 방광절제술(radical cystectomy)이었으나, 이 수술은 상당한 이환율과 삶의 질 저하를 초래하는 고난도 치료로, 실제 임상 적용에는 한계가 적지 않다.NMIBC의 위험도 분류—저위험군, 중간위험군, 고위험군—는 종양의 병기, 등급, 크기, 다초점성, 재발력 등의 임상·병리학적 지표를 종합해 이루어지며, 특히 고위험군 환자, 그중에서도 CIS 또는 T1 병변을 가진 환자는 진행 위험이 높아 보다 적극적인 치료가 요구된다.근치적 방광절제술은 BCG 불응 NMIBC에서 높은 질병 조절 효과를 보이지만, 그 침습성과 장기적인 기능 상실로 인해 방광을 보존하면서도 충분한 종양 조절을 달성할 수 있는 새로운 치료 전략의 필요성이 크게 대두되고 있다.이에 따라 면역관문억제제, 종양용해성 바이러스(oncolytic virus) 치료, 방광내 약물전달 플랫폼, 표적 치료제 등 다양한 신기술 기반 치료법이 개발되고 있으며, 이들 접근법은 방광 기능을 유지하면서도 지속적이고 임상적으로 의미 있는 치료 효과를 달성하는 것을 목표로 한다.최근 NMIBC 치료 환경은 과거와 달리 빠르게 확장되고 있으며, 새로운 약제의 등장, 기존 약물의 새로운 적응증 또는 약물 전달 방식의 진화, 그리고 완전히 새로운 치료 플랫폼의 출현 등 혁신적 변화가 지속되고 있다.초기에는 대부분의 신약 개발이 BCG 불응성 고위험군 NMIBC 환자를 대상으로 이루어졌으나, 점차 고위험군뿐 아니라 중간위험군 환자에서도 BCG와 직접 경쟁 가능한 후보 약제가 등장하면서 치료 선택지는 더욱 다양해지고 있다.비근침윤성 방광암(NMIBC)은 어떻게 치료하고, 치료 성적은 어떠한가?비근침윤성 방광암(NMIBC)은 대부분 경요도 방광 종양 절제술(TURBT) 후 시행되는 보조요법을 통해 관리된다. 이 질환의 임상적 특징은 높은 재발률과 상대적으로 낮은 진행률로 요약된다.실제로 5년 재발률은 50~70%에 이르며, 진행률은 10~20% 수준으로 보고된다. 이러한 자연경과는 단순 TURBT만으로는 장기적인 종양 조절이 어렵다는 점을 시사하며, 보조적 방광내 치료의 중요성을 부각시킨다.TURBT 직후 시행되는 단회 방광내 항암제 주입요법은 저위험군 및 일부 중위험군에서 재발률을 유의하게 낮추는 것으로 입증됐다. 특히 mitomycin C(MMC)는 절제 후 잔존 암세포를 제거하고 세포 재부착을 방지하는 작용을 통해 초기 재발 감소 전략의 표준요법으로 자리잡았다. 그러나 MMC를 포함한 기존 화학요법은 병변의 진행 억제 효과가 제한적이어서 고위험군에서는 단독 치료만으로는 충분하지 않다.고위험군 NMIBC, 특히 고등급 Ta/T1 병변 및 상피내암(CIS)의 경우 BCG 면역요법이 여전히 가장 강력하고 일관된 치료 효과를 제공한다. BCG의 초기 완전반응률은 유두종양에서 55~65%, CIS에서 70~75%로 보고되며, 재발 억제와 진행 위험 감소를 동시에 입증한 유일한 방광내 치료법이다.그럼에도 불구하고 전체 환자의 약 30~40%는 BCG에 초기 반응을 보이지 않는다. 초기 완전반응을 얻더라도 약 절반은 결국 재발한다. 여기에 장기화된 BCG 공급 부족 문제까지 겹치면서 고위험군 외의 환자에게 BCG 사용을 제한해야 하는 현실적인 어려움도 지속되고 있다.이러한 한계를 보완하기 위해 다양한 대체 전략이 개발되고 있다. Gemcitabine, Epirubicin, MMC 등 기존 항암제의 방광내 투여는 BCG 불응성 또는 BCG 금기 환자에서 활용되고 있으며, 특히 gemcitabine–docetaxel 병용요법은 BCG 불응 환자에서 1년 완전반응률 50~60%를 보이며 salvage therapy로 임상적 관심이 높아지고 있다.최근에는 방광보존 치료 옵션이 기존 면역요법을 넘어 유전자치료 영역으로까지 확장되고 있다. Nadofaragene firadenovec(AdstiladrinⓇ)은 IFN-α2b 유전자를 방광 점막에 전달하여 국소 면역반응을 활성화하는 비증식성 아데노바이러스 벡터 기반 치료제로, 고위험 BCG 불응성 NMIBC에서 2022년 미국 FDA 승인을 받았다. 주요 임상시험에서는 3개월 완전반응률 53%, 12개월 지속반응률 24~30%가 보고되며, BCG 불응성 환자에서 새로운 치료 기전의 확립이라는 의의를 가진다.종합하면 NMIBC 치료 전략은 위험군에 따라 크게 달라지며, 저위험군에서는 TURBT와 단회 항암제 주입만으로도 비교적 양호한 성적을 기대할 수 있다. 반면 고위험군에서는 BCG를 중심으로 한 적극적 면역치료가 필수적이며, BCG 불응성 증가와 공급 제한 문제로 인해 새로운 치료제 개발이 더욱 활발히 이루어지고 있다.Bacillus Calmette-Guérin(BCG)는 어떤 치료 방법인가?BCG는 1990년 미국 FDA에서 승인된 비특이적 면역요법으로, 비근육침윤성 방광암(NMIBC) 치료에 널리 사용돼 왔다.BCG의 항종양 효과는 Th1 중심의 면역 반응을 유도하는 기전에 기반한다. BCG가 요로상피세포에 부착되면 IL-1, IL-6, IL-8, TNF-α 등 다양한 사이토카인과 케모카인이 분비되며, 이로 인해 면역세포들이 방광 점막으로 집중된다. 이어서 대식세포, 호중구, 수지상세포 등 항원제시세포가 활성화되고, 변화된 사이토카인 환경 속에서 미성숙 CD4+ T 세포는 Th1 또는 Th2 세포로 분화한다.이 중 Th1 반응은 IFN-γ를 포함한 사이토카인 분비를 통해 BCG 치료 효과와 밀접히 연관되며, 반대로 IL-10을 중심으로 한 Th2 반응은 BCG 실패와 관련된다. 실제로 IL-10 억제 또는 IFN-γ 증가가 Th1 우세 상태를 유도하며, 이는 BCG 매개 종양 퇴행에 필수적인 요소로 알려져 있다.이처럼 BCG는 Th1 면역 반응을 활성화함으로써 방광암이 유발하는 면역 억제 환경을 극복하는 데 효과적이지만, 환자 예후를 더 향상시키기 위해서는 보다 강력한 면역조절 능력을 가진 새로운 치료제의 개발이 필요하다.특히 BCG에 반응하지 않는 NMIBC는 예후가 불량하고 전통적으로 치료 옵션이 제한적이었다. 고위험 BCG-불응성 질환의 경우 근치적 방광 절제술이 표준 치료로 권고되지만, 모든 환자가 수술을 감내할 수 있는 것은 아니다.임상시험 기준으로 BCG의 초기 완전반응률은 유두종양에서 약 55~65%, CIS에서 70~75% 수준이다. 그러나 전체 NMIBC 환자의 약 3분의 1은 BCG에 전혀 반응하지 않으며, 초기 반응을 보인 환자의 약 절반도 결국 재발하거나 진행을 경험한다.미국 FDA는 BCG-불응성 NMIBC를 다음과 같이 정의한다: ▲ 적절한 BCG 요법 후 12개월 이내 지속성 또는 재발성 CIS, 또는 재발성 Ta/T1 질환이 있는 경우(초기 유도 6회 중 ≥5회, 유지 3회 중 ≥2회 또는 2차 유도 6회 중 ≥2회 투여 완료를 ‘적절한 요법’으로 정의), ▲ 적절한 BCG 요법 후 6개월 이내 재발한 고등급 Ta/T1 질환, ▲ 유도요법 후 첫 평가에서 고등급 T1 질환이 확인된 경우이다.Bacillus Calmette-Guérin(BCG)-불응성은 왜 일어나는가?BCG-불응성은 단일 요인보다는 종양 미세환경, 면역반응의 왜곡, 종양세포의 생물학적 저항성이 복합적으로 작용하여 발생한다. 일부 NMIBC는 이미 강한 면역억제 환경을 형성하고 있어, BCG가 유도하는 Th1 중심 면역 반응이 충분히 활성화되지 못한다.이들 종양에서는 IL-10과 TGF-β 같은 면역억제성 사이토카인이 증가하고, Treg와 MDSC가 축적되며, 종양세포의 PD-L1 발현도 높아져 T 세포 기능이 억제된다. 이러한 환경에서는 BCG가 방출시키는 사이토카인이 존재하더라도 Th1 분화보다는 Th2 또는 억제성 면역반응이 우세해져 IFN-γ 중심의 항종양 면역이 제대로 형성되지 않는다.또한 종양세포 자체가 BCG에 대한 내성을 가지는 경우도 있다. 상피세포 표면의 BCG 부착·내재화에 필요한 integrin 등 분자의 발현이 낮거나, BCG가 유도하는 세포사멸 신호(TRAIL, Fas 등)에 저항성을 나타내는 경우가 이에 해당한다. 일부 NMIBC는 특정 유전자 변이나 생존 신호의 과활성화로 인해 BCG 면역 반응에 본질적으로 둔감하다.여기에 고령, 기저질환, 면역노화 등 환자 요인이 더해지면 APC 활성 및 T 세포 반응성이 감소해 BCG가 충분한 면역 강화 효과를 내지 못한다. 균주 간 면역원성 차이, BCG 부족으로 인한 불충분한 치료 역시 면역반응 축적을 방해해 불응 위험을 높인다.결국 BCG 불응성은 종양 미세환경의 면역억제성, Th1 면역 활성화의 실패, 종양세포의 내재적 저항성, 그리고 숙주 면역 기능 저하가 상호 작용하여 나타나는 복합적 면역치료 실패 현상으로 이해된다. 이러한 이유로 BCG 불응성 NMIBC에서는 보다 강력한 면역조절 능력을 갖춘 새로운 치료 전략이 필요하다.인터루킨-15(IL-15)는 어떤 역할을 하는가?IL-15는 공통 γ사슬(γc) 사이토카인 패밀리에 속하는 면역 조절 인자로, 선천 면역과 적응 면역의 경계를 연결하며 항종양 면역을 강화하는 데 핵심적인 역할을 수행한다. IL-2, IL-4, IL-7, IL-9, IL-21과 함께 γc 계열을 이루는 IL-15는 특히 CD8+ T 세포와 자연살해(NK) 세포의 발달, 생존, 증식, 그리고 기능적 활성화 전반을 조절하는 중심적 사이토카인이다.Pleiotropic Effects of IL-15(출처: Cells 2023, 12, 1611).이러한 생물학적 중요성은 다양한 전임상·임상 연구에서 반복적으로 입증되어 왔으며, IL-15가 항암 면역을 유지하는 데 필수적인 조절자로 작용함을 뚜렷하게 보여준다.생리학적으로 IL-15는 IL-15 수용체 α(IL-15Rα)와 함께 이종이량체 형태로 합성된다. IL-15Rα는 자체적으로 신호 전달 기능을 갖고 있지는 않지만 IL-15에 높은 친화도로 결합하여 내질망에서 안정적인 복합체를 형성하고 이를 세포 표면까지 운반함으로써 생물학적 기능 발현을 위한 핵심적인 플랫폼을 제공한다.이 복합체는 생산 세포 표면에 제시된 뒤 인접한 수용 세포의 IL-2/IL-15Rβ와 공통 γ사슬과 결합하여 신호를 전달하는데, 이러한 ‘트랜스제시(trans-presentation)’는 IL-15 생물학을 규정하는 대표적 기전이자 IL-2와 구별되는 가장 특징적인 작동 방식이다.따라서 IL-15와 IL-15Rα는 단핵구, 대식세포, 수지상세포, 혈관내피세포, 골수 및 림프절의 기질세포 등 다양한 세포 유형에서 발현되며, 특히 수지상세포와 대식세포가 주요 생산자인 것으로 보고되었다. 이들 세포는 항원 제시뿐 아니라 IL-15 제시 기능을 통해 CD8+ T 세포와 NK 세포의 생존 신호를 제공함으로써 면역계의 항상성을 유지하는 데 기여한다.IL-15 초작용제(superagonist) 복합체는 무엇인가?최근 면역조절 치료제 개발은 기존 사이토카인 신호 경로를 선택적으로 증폭하여 항종양 면역 반응을 극대화하는 방향으로 진화하고 있으며, 그 중심에는 IL-15 경로 기반의 차세대 초작용제(superagonist) 기술이 있다.IL-15는 본래 NK 세포와 CD8⁺ T 세포의 생존, 증식, 기억 형성에 핵심적인 사이토카인이지만, 생체 내 반감기가 짧고 수용체 결합 효율이 낮아 단독 활용에는 한계가 있었다.이러한 제약을 극복하기 위해 고안된 IL-15 초작용제 복합체는 IL-15의 생물학적 활성을 비약적으로 증폭하도록 설계된 구조적 혁신체로, 대표적인 예가 IL-15N72D 변형체와 IL-15Rα의 sushi 도메인을 융합한 노가펜데킨 알파 인바키셉트이다.IL-15N72D는 아스파라긴(N)에서 아스파트산(D)으로의 단일 아미노산 치환을 통해 수용체 친화성과 신호전달 강도를 향상시킨 기능적 변형체이며, IL-15Rα의 sushi 도메인 결합을 통해 자연적인 trans-presentation 기전을 모사하도록 설계되었다.이 두 구성요소는 IgG1 Fc 영역과 융합되어 약물의 안정성, 체내 반감기, 조직 내 지속 시간을 획기적으로 개선하며, 그 결과 NK 세포와 CD8⁺ T 세포의 활성화 및 항종양 세포독성 반응을 장기간 유도하는 강력한 IL-15 신호 증폭체를 형성한다.이러한 기전은 기존 BCG 치료로 유도되는 국소 면역 반응을 효과적으로 증폭시키며, BCG-불응성 비근육침윤성 방광암에서 관찰되는 높은 완전관해율과 반응 지속성을 설명하는 면역학적 기반을 제공한다.결과적으로 IL-15 변형체와 IL-15Rα가 융합된 초작용제 플랫폼은 단순한 사이토카인 보충을 넘어, 정밀하게 설계된 면역 신호 조절을 통해 종양 미세환경 내에서 효과적인 항암 면역을 재활성화하려는 현대 면역항암제 개발의 중요한 패러다임을 제시한다노가펜데킨 알파 인바키셉트의 약리 기전은?노가펜데킨 알파 인바키셉트는 IL-15 돌연변이체(IL-15N72D)와 IL-15Rα를 융합한 복합체로, 자연 면역세포가 제공하는 IL-15 제시 기전을 모방한다. 이를 통해 CD8+ T 세포, NK 세포, 기억 T 세포의 증식·활성화를 강하게 유도하면서도, 면역억제성 조절 T 세포의 확장은 최소화한다.전임상 모델에서 방광 내 투여된 노가펜데킨 알파 인바키셉트는 단독 또는 BCG와 병용 시 BCG 단독보다 우수한 항종양 효과를 보였다. 또한 비융합(native) IL-15에 비해 림프조직 내 지속시간이 길고, 약동학적 안정성이 크게 향상되어 보다 강력하고 지속적인 항종양 면역반응을 유발한다.결과적으로 노가펜데킨 알파 인바키셉트는 IL-15 신호를 증폭해 킬러 T 세포 중심의 면역반응을 재가동시키는 기전적 특성을 기반으로, BCG-불응성 NMIBC에서 의미 있는 치료적 이점을 제공하는 IL-15 기반 면역증강제이다.Immune Effects of nogapendekin alfa inbakicept(출처: Cells 2023, 12, 1611).위 사진자료에 대해 설명하면, A. 노가펜데킨 알파 인바키셉트는 인간 IgG1 Fc와 융합된 IL15Rα에 결합된 돌연변이(N72D) 인간 IL-15로 구성된다. B. 노가펜데킨 알파 인바키셉트는 IL-15 수용체를 통해 순환 면역 세포에 결합한다. C. 노가펜데킨 알파 인바키셉트가 림프구에 결합하면 자연 살해(NK) 세포와 CD8+ T 세포 집단이 활성화된다되고 확장되어 고효과 CD56 dim 및 CD56 bright NK 세포와 중앙 기억 T 세포(TCM)가 확장된다. D. 비장 CD8+ T 세포 표면의 CXCR3가 상향 조절되면 종양 미세 환경(TME)으로 이동할 가능성이 높아집니다. 활성화된 NK 세포도 종양으로 이동한다. E. 활성화된 종양 침윤 CD8+ T 림프구(TIL)는 MHC 클래스 I 복합체가 제시하는 종양 관련 항원 에피토프를 인식하여 암세포를 인식한다. 활성화된 CD8+ T 세포와 NK 세포는 세포독성이 증가하여 암세포 사멸을 유도한다.CD8+ T 세포는 IFNγ 및 TNF⍺와 같은 Th1 사이토카인을 분비하여 염증성 TME를 촉진하고 과립구 및 단핵구 골수유래 억제 세포(MDSC)의 PD-L1을 상향 조절합니다. 노가펜데킨 알파 인바키셉트는 NK TIL이 TGF-β의 영향에 저항성을 갖도록 하고 항체 의존성 세포독성(ADCC)을 증가시킬 수 있도록 한다.노가펜데킨 알파 인바키셉트의 치료적 위치는?비근육침윤성 방광암(NMIBC)은 초기 치료로 경요도 방광종양절제술(TURBT)이 시행되지만, 재발률이 높고 병변이 지속·활성화되는 경우가 많아 반복적 치료가 필요하다. 특히 CIS를 동반한 고위험군에서는 BCG 치료가 표준으로 자리잡아 있으나, 충분한 BCG 노출에도 불구하고 재발·지속·진행이 나타나는 BCG-불응성 환자군이 적지 않다.이러한 환자에서 근치적 방광적출술(radical cystectomy)은 표준 치료로 권고되지만, 고령, 동반질환, 삶의 질 저하에 대한 우려, 환자 선호 등의 이유로 수술 적용이 어려운 경우가 많다. 이에 따라 방광을 보존하면서도 충분한 항종양 효과를 제공할 수 있는 새로운 치료 전략의 필요성이 지속적으로 제기되어 왔다.노가펜데킨 알파 인바키셉트는 IL-15/IL-15Rα 복합체 기반의 IL-15 초작동제로, CD8+ T 세포와 NK 세포의 증식·활성화를 강력하게 유도하는 면역 증강형 생물학적 제제이다. NMIBC에서 BCG 치료는 국소 면역활성에 의존하지만, BCG-불응성 환자에서는 방광 내 면역 미세환경의 소진, T/NK 세포 감소, BCG 반응 저하 등이 주요 병태생리로 지적된다.이러한 맥락에서 노가펜데킨 알파 인바키셉트는 고갈된 면역계를 다시 활성화하여 기존 BCG 효과를 강화하고, 단독 BCG로는 확보하기 어려운 항종양 면역반응을 확대하는 기전적 장점을 가진다.전신 면역관문억제제인 pembrolizumab(키트루다)은 일부 환자에서 의미 있는 완전반응을 유도하지만, 전신 면역 관련 부작용과 장기 치료에 따른 독성·비용 부담이 중요한 제약으로 남아 있다. 반면 노가펜데킨 알파 인바키셉트는 방광 내 국소 투여를 기반으로 하여 전신 독성이 극히 낮으며, 고령 또는 동반질환이 많은 실제 진료 환경에서 사용하기 용이하다.또한 바이러스 벡터를 이용하는 AAV 기반 유전자치료제(nadofaragene firadenovec)와 달리 벡터 노출에 따른 안전성 우려가 없고, 기존 BCG 치료 패턴과 자연스럽게 연계되어 임상적 채택성이 높다는 점도 장점이다.노가펜데킨 알파 인바키셉트의 임상적 의미는 단순한 반응률 개선을 넘어, BCG-불응성 CIS 환자에서 방광적출술을 지연하거나 회피할 수 있는 실질적 치료 대안을 제공한다는 데에 있다.실제 임상에서 의미 있는 완전반응률과 지속기간이 확인되었으며, 이는 방광적출술을 바로 시행하기 어려운 환자에게 중요한 시간적 여유와 치료 선택권을 제공한다. 전신 독성의 부담이 거의 없고, BCG 기반 면역작동 기전을 확장하는 방식이라는 점 또한 치료적 위치를 공고히 한다.노가펜데킨 알파 인바키셉트(ANKTIVA)의 허가임상은 어떠한가?ANKTIVA의 효능은 QUILT-3.032(NCT03022825) 시험에서 평가되었다. 이 연구는 경요도 방광종양절제술(TURBT) 이후 BCG에 반응하지 않는 고위험 비근육침윤성 방광암(NMIBC) 중 상피내암(CIS)을 동반한 성인 환자 77명을 대상으로 한 단일군, 다기관 임상시험이었다. 여기에는 Ta/T1 유두상 병변의 동반 여부와 상관없이 CIS를 가진 환자들이 포함되었다.BCG 불응성 고위험군 NMIBC의 CIS는, 충분한 BCG 치료를 완료한 후 12개월 이내에 CIS가 단독으로 또는 Ta/T1 병변과 함께 지속되거나 재발한 경우로 정의되었다. 충분한 BCG 치료는 초기 유도요법 6회 중 최소 5회를 투여하고, 이어서 유지요법 3회 중 최소 2회 또는 두 번째 유도요법 6회 중 최소 2회를 투여한 경우로 정의되었다.치료 전 Ta 또는 T1 병변 환자들은 절제가 가능한 모든 병변을 제거하기 위해 TURBT를 시행받았다. 절제, 소작 또는 전기소작이 불가능한 잔여 CIS는 허용되었다. 한편 근침윤성 방광암(T2~T4), 국소 진행성, 전이성 또는 방광 외부(요도, 요관, 신우) 침범이 있거나 그 병력이 있는 환자는 시험에서 제외되었다.환자들은 유도요법 동안 ANKTIVA 400mcg와 BCG를 주 1회, 6주 연속 투여받았다. 이후 질병이 없거나 저등급 질환을 가진 경우 4, 7, 10, 13, 19개월째에 3주 간격으로 주 1회 추가 투여를 받았다. 치료 3개월 시점에 CIS가 지속되거나 고등급 Ta 병변이 남아 있는 경우에는 두 번째 유도요법을 받을 수 있었다. 치료 25개월 시점에 완전반응(CR)이 유지되는 환자는 25, 31, 37개월째에 동일한 방식으로 추가 투여가 가능했다.종양 상태 평가는 최대 2년 동안 3개월마다 시행되었다. 24개월 이후의 반응 평가는 각 기관의 진료 기준에 따라 시행되었다. 치료 시작 후 첫 6개월 동안은 무작위 또는 방광경 유도 조직검사가 필수적으로 시행되었다. 주요 효능 평가지표는 어느 시점에서든 완전반응을 달성했는지와(방광경 검사 및 필요 시 TURBT/조직검사 결과 음성, 요세포검사 음성 기준) 그 반응의 지속기간이었다.등록 환자의 중앙 연령은 73세(범위 50~91세)였고, 86%가 남성이었다. 인종 분포는 백인 90%, 흑인 6%, 아시아인 1%, 아메리칸 인디언/알래스카 원주민 1%, 미상 1%였다. ECOG 수행능력은 0점이 83%, 1점이 17%였다.연구 등록 시 종양 특성은 CIS 단독 69%, CIS + Ta 병변 21%, CIS + T1(±Ta) 병변 10%였다. 기저 질환 상태는 불응성 43%, 재발성 57%였다. 이전 BCG 투여 횟수의 중앙값은 12회(범위 8~45회)였고, 13%는 분할 용량 BCG를 받은 경험이 있었다. 방광경 영상 방식은 백색광 57%, 청색광 또는 협대역 영상 40%, 미상 3%였다.효능 결과는 표 3에 제시되어 있으며, 전체 환자의 31%(24명)는 두 번째 유도요법을 받았다.노가펜데킨 알파 인바키셉트의 쟁점을 무엇인가?노가펜데킨 알파 인바키셉트는 IL-15의 생물학적 활성을 기반으로 설계된 차세대 면역작용제로, 고위험 BCG 불응성 비근침윤성 방광암(NMIBC) 치료에서 새로운 치료적 가능성을 제시하고 있다.IL-15는 CD8⁺ T 세포와 NK 세포의 생존과 기능을 강화하는 핵심 사이토카인으로 알려져 있으나, 자연 상태의 IL-15는 짧은 반감기, 불안정한 구조, 수용체 결합의 가변성 등으로 인해 치료제로 활용하는 데 본질적인 제약이 존재해왔다.노가펜데킨 알파 인바키셉트는 IL-15와 IL-15Rα 수용체 도메인을 결합해 형성한 안정적 이종이량체 기반의 IL-15 초작용제로, 내재 IL-15에 비해 우수한 생체 내 안정성과 장기적 면역 활성 유도가 가능하다는 점에서 임상적 의미가 크다.특히 BCG 치료에 반응하지 않는 NMIBC 환자는 방광적출술이 표준 치료임에도 불구하고, 고령 및 동반질환 등으로 수술이 어려운 경우가 많아 실질적인 치료 공백이 존재해왔다. 이러한 점에서 BCG와 병용하여 국소 종양 미세환경을 재활성화할 수 있는 약제의 개발은 방광보존 전략을 확장할 수 있는 새로운 치료 패러다임이라 할 수 있다.노가펜데킨 알파 인바키셉트의 주요 장점은 BCG와 병용 시 강력한 상승효과를 보인다는 점이다. IL-15Rα와의 결합을 통해 강화된 생물학적 활성은 APC, NK 세포, CD8⁺ T 세포의 집적과 기능을 촉진하여 항종양 면역반응을 증폭시키며, 이는 허가 근거가 된 QUILT-3.032 연구에서 3개월 완전반응률 53%, 12개월 반응 지속률 24~30%로 나타났다.이러한 치료 성적은 기존 BCG 불응 환자에서 보고된 방광내 요법의 성적을 상회하는 결과이며, 이 약제가 임상적으로 의미 있는 반응을 유도하는 면역치료제로 기능함을 보여준다.그러나 노가펜데킨 알파 인바키셉트는의 개발과 허가 과정에는 여러 한계와 도전이 병존한다. 가장 큰 문제는 근거 임상이 무작위 대조군이 없는 단일군(single-arm) 연구로 수행되었다는 점으로, 이는 약제의 효과를 BCG 재투여 효과와 명확히 구분하기 어렵게 만들며, 역사적 대조(historical control)와의 비교에서 발생할 수 있는 해석의 변이를 피하기 어렵다.또한 환자군 내 BCG 노출량, CIS 단독 여부, 종양 특성 등에서 이질성이 존재하여 반응률과 반응 지속성의 정확한 비교가 제한된다. 반응의 지속성 역시 완전반응을 보인 환자의 일부에서만 장기적으로 유지되는 경향이 관찰되었고, 12개월 이후 장기 추적자료는 아직 충분히 축적되지 않아 방광보존 전략의 장기적 안전성과 유효성에 대한 확정적 결론을 내리기 어렵다.더불어 치료효과의 기저에 있는 종양면역미세환경의 상태가 환자별로 크게 달라, 이 약제가 NK/T 세포 결핍 또는 극도로 억제된 미세환경을 충분히 회복시키지 못하는 경우가 존재할 것으로 예상되며, 이러한 점은 향후 바이오마커 기반 환자선택 전략의 필요성을 시사한다.이처럼 노가펜데킨 알파 인바키셉트는 IL-15 생물학을 임상적으로 구현한 최초의 치료제로서 BCG 불응성 NMIBC라는 미충족 의료수요 영역에서 실질적인 치료 옵션을 제공하고 있다.초기 반응률과 독성 프로파일은 고무적이지만, 단일군 연구 설계, 병용요법의 기여도 분리 문제, 반응 지속성의 제한, 장기 추적자료 부족 등은 여전히 해결해야 할 과제로 남아 있다.그럼에도 불구하고 노가펜데킨 알파 인바키셉트는 기존 치료제와는 차별화된 기전을 바탕으로 난치성 NMIBC에서 방광보존 전력을 확장할 수 있는 중요한 면역치료제로 자리매김할 가능성이 높으며, 향후 병용 전략, 내성 기전 규명, 예측 바이오마커 개발 등을 통해 그 임상적 가치가 더욱 강화될 것으로 기대된다.참고문헌 1. Grace Lui et al. “Exploiting an Interleukin-15 Heterodimeric Agonist (N803) for Effective Immunotherapy of Solid Malignancies” Cells 2023, 12(12), 1611. 3. Richard S et al. “Non–muscle-invasive Bladder Cancer: Overview and Contemporary Treatment Landscape of Neoadjuvant Chemoablative Therapies” Reviews in Urology, Vol. 22 No. 2 2020. 3. Jong Ho Park et al. “The Emerging Treatment of BCG (Bacillus Calmette-Guérin)- Unresponsive Non–Muscle-Invasive Bladder Cancer“ Journal of Urologic Oncology 2024;22(3):246-255. 4. Aiman Waheed et al. “Nogapendekin alfa inbakicept-PMLN: first approval milestone for BCG-unresponsive noninvasive bladder cancer: editorial” Annals of Medicine & Surgery (2024) 86:6386–6388. 5. Brian L. Heiss et al. “FDA Approval Summary: Nogapendekin Alfa Inbakicept-pmln with BCG for BCG-unresponsive carcinoma in situ” Clin Cancer Res. 2025 October 15; 31(20): 4223–4229. 6. Vikram M et al. “Mechanism of action of nadofaragene firadenovec-vncg” Front. Oncol. 14:1359725. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-11-20 17:29:43최병철 박사
방광암 면역치료 최초 IL-15 초작용제 '안크티바'안크티바(Anktiva®, 성분명: 노가펜데킨 알파 인바키셉트-pmln, nogapendekin alfa inbakicept-pmln, ImmunityBio)는 IL-15 초작용제(superagonist) 복합체로 개발된 최초의 방광 내 면역치료제다.2024년 4월 미국 FDA에서 유두종 유무와 관계없이 상피내암(CIS)을 동반한 BCG-불응성 비근육침윤성 방광암(non-muscle invasive bladder cancer, NMIBC) 성인 환자를 대상으로 BCG와 병용 사용하는 치료제로 승인됐다.방광암은 전 세계적으로 흔한 악성 종양 중 하나다. 국내에서도 발생 빈도가 높은 암종으로 알려져 있다. 이 중 약 75%는 비근육침윤성 방광암(NMIBC)으로 분류되며, 초기 치료는 대개 경요도 방광 종양 절제술(transurethral resection of bladder tumor, TURBT)로 시작된다.그러나 NMIBC는 60–70%의 재발률을 보이므로, TURBT 이후 방광 내 치료(intravesical therapy)가 질병의 재발을 억제하고 진행을 지연시키는 데 핵심적인 역할을 한다.현재 방광 내 치료는 크게 두 가지로 구분되며, 하나는 BCG 요법을 기반으로 하는 면역치료, 다른 하나는 미토마이신 C, 젬시타빈, 에피루비신, 독소루비신 등으로 구성되는 화학요법이다.BCG는 NMIBC의 표준 치료 중 하나이지만, 약 40%의 환자에서는 충분한 치료 효과를 보이지 못한다. 안크티바는 이러한 BCG-불응성 환자에서 방광 절제술을 피할 수 있는 새로운 치료 대안으로 개발됐다.IL-15는 NK 세포와 CD8⁺ T 세포의 활성, 증식, 기억 형성에 관여하는 중요한 사이토카인이다. 안크티바는 IL-15 변형체와 IL-15Rα의 sushi(반복 단백질 구조) domain이 결합한 IL-15 초작용제(superagonist) 복합체를 통해 NK 세포, CD4⁺ T 세포, CD8⁺ T 세포의 활성을 강력하게 유도하며, 특히 종양 특이적 기억 T 세포 반응을 증폭시켜 항종양 면역반응을 강화한다.임상시험에서 BCG 유지요법과 함께 안크티바를 투여받은 77명의 환자 중 62%(95% CI, 51–73)가 완전관해에 도달했다. 이 반응은 일부 환자에서 최대 47개월까지 지속됐다. 완전관해가 12개월 이상 유지된 비율은 58%, 24개월 이상 유지된 비율은 40%였다.치료 스케줄은 방광 내 카테터를 통한 유도요법(6주간 주 1회) 후, 4, 7, 10, 13, 19개월째의 유지요법(각 3주간 주 1회)으로 구성된다. 3개월 시점에 완전 반응이 확인되지 않으면 두 번째 유도요법을 시행할 수 있으며, 25개월 이후에도 완전 반응이 지속되는 경우에는 25, 31, 37개월째에 추가 BCG 유지투여를 실시할 수 있다. 투여 시 약물 혼합액은 방광 내에 2시간 동안 유지한 뒤 배출한다.안크티바 치료에는 몇 가지 중요한 주의사항이 있다. 방광절제술을 지연함으로써 전이성 방광암으로 진행할 위험이 존재하며, 배아–태아 독성 가능성이 보고되어 가임기 여성은 치료 중과 마지막 투여 후 최소 1주일 동안 피임이 필요하다.흔하게 보고되는 이상반응으로는 배뇨곤란, 혈뇨, 빈뇨, 절박뇨, 요로감염, 근골격계 통증, 발열 및 오한 등이 있으며, 실험실 검사에서는 크레아티닌 상승과 칼륨 상승이 비교적 흔하게 관찰된다.방광암(Bladder Cancer)이란 무엇인가?방광암은 요로계에서 가장 흔히 발생하는 악성 종양 중 하나로, 소변을 저장하는 장기인 방광의 점막 상피세포에서 주로 기원한다.전 세계적으로 방광암은 발생률과 사망률 측면에서 중요한 건강 문제를 야기하고 있으며, 특히 남성에서 높은 발생 빈도를 보인다. 방광암의 발생에는 흡연이 가장 강력한 위험 요인으로 작용하는 것으로 알려져 있다. 이 외에도 직업적 발암물질 노출, 만성 요로 감염 및 요로 결석 등이 발병과 연관돼 있다.조직학적으로 방광암의 대다수는 요로상피암(urothelial carcinoma)으로, 전체 방광암의 약 90%를 차지한다. 요로상피암은 방광뿐 아니라 요관, 신우, 요도 등 요로 전반에 걸쳐 발생할 수 있는 특성을 지니고 있다.이 외에도 만성 자극이나 염증과 관련된 편평세포암(squamous cell carcinoma), 드물게 선종 양상의 조직학적 특징을 보이는 선암(adenocarcinoma), 그리고 고도로 공격적인 생물학적 특성을 나타내는 소세포암(small cell carcinoma) 등 다양한 형태가 존재한다. 이러한 조직형의 차이는 임상적 경과, 치료 전략 및 예후와 밀접하게 연관되어 있어 진단 시 정확한 병리학적 분류가 필수적이다.방광암의 병기 결정은 치료 방침 수립과 예후 평가에 있어 핵심적인 요소이다. 국제적으로 널리 사용되는 TNM 병기 체계는 종양의 침윤 정도(T), 국소 림프절 전이 여부(N), 및 원격 전이 여부(M)에 기반하여 병기를 구분한다.특히 방광벽의 근육층 침윤 여부는 임상적 의사결정에서 매우 중요한 기준으로 작용한다. 종양이 점막층에 국한된 Ta 병기, 상피 내에서 편평하게 확산되는 상피내암(carcinoma in situ, CIS), 그리고 점막하층을 침범하나 근육층에는 도달하지 않은 T1 병기는 비근침윤성 방광암(non–muscle invasive bladder cancer, NMIBC)으로 분류된다.반면, 종양이 방광 근육층을 침범하는 T2 병기부터는 근침윤성 방광암(muscle invasive bladder cancer, MIBC)으로 정의되며, 이후 주변 지방조직(T3) 및 인접 장기(T4)로의 침윤 여부에 따라 병기가 상승한다. 림프절 전이(N1–N3)와 원격 전이(M1)의 존재는 질병의 진행을 시사하며 전신적 치료 전략이 요구된다.Non–Muscle Invasive Bladder Cancer(NMIBC) and Muscle Invasive Bladder Cancer(출처: https://cgoncology.com/science/).이와 같이 방광암은 조직학적 이질성과 침윤 정도에 따른 이분화된 임상 양상을 보이며, 병기 및 조직형은 환자의 치료 선택과 예후에 결정적인 영향을 미친다.비근침윤성 방광암(Non–muscle invasive bladder cancer, NMIBC)은 무엇인가?비근육 침습성 방광암(NMIBC)은 새로 진단되는 방광암의 약 75%를 차지하며, 병변이 주로 요로상피의 표층(Ta), 점막하층(T1) 또는 상피내암(CIS)에 국한되는 질환이다.NMIBC는 즉각적으로 생명을 위협하는 경우는 드물지만, 높은 재발률과 적지 않은 진행 위험으로 인해 임상적으로 중요한 도전 과제로 여겨진다. 실제로 환자의 약 50~70%가 초기 치료 이후 재발을 경험하며, 최대 30%는 근육 침습성 또는 전이성 방광암으로 진행한다.수십 년 동안 고위험군 NMIBC 환자에서 경요도 방광 종양 절제술(transurethral resection of bladder tumor, TURBT) 후 시행되는 BCG(Bacillus Calmette–Guérin) 치료는 재발과 진행을 효과적으로 억제하는 표준 치료로 자리매김해 왔다.그러나 BCG 치료의 임상적 이점에도 불구하고 약 40%의 환자에서 실패가 발생하며, 이 경우 추가적인 치료 전략이 필요하다. 이러한 환자군에서 전통적으로 가장 선호된 치료는 근치적 방광절제술(radical cystectomy)이었으나, 이 수술은 상당한 이환율과 삶의 질 저하를 초래하는 고난도 치료로, 실제 임상 적용에는 한계가 적지 않다.NMIBC의 위험도 분류—저위험군, 중간위험군, 고위험군—는 종양의 병기, 등급, 크기, 다초점성, 재발력 등의 임상·병리학적 지표를 종합해 이루어지며, 특히 고위험군 환자, 그중에서도 CIS 또는 T1 병변을 가진 환자는 진행 위험이 높아 보다 적극적인 치료가 요구된다.근치적 방광절제술은 BCG 불응 NMIBC에서 높은 질병 조절 효과를 보이지만, 그 침습성과 장기적인 기능 상실로 인해 방광을 보존하면서도 충분한 종양 조절을 달성할 수 있는 새로운 치료 전략의 필요성이 크게 대두되고 있다.이에 따라 면역관문억제제, 종양용해성 바이러스(oncolytic virus) 치료, 방광내 약물전달 플랫폼, 표적 치료제 등 다양한 신기술 기반 치료법이 개발되고 있으며, 이들 접근법은 방광 기능을 유지하면서도 지속적이고 임상적으로 의미 있는 치료 효과를 달성하는 것을 목표로 한다.최근 NMIBC 치료 환경은 과거와 달리 빠르게 확장되고 있으며, 새로운 약제의 등장, 기존 약물의 새로운 적응증 또는 약물 전달 방식의 진화, 그리고 완전히 새로운 치료 플랫폼의 출현 등 혁신적 변화가 지속되고 있다.초기에는 대부분의 신약 개발이 BCG 불응성 고위험군 NMIBC 환자를 대상으로 이루어졌으나, 점차 고위험군뿐 아니라 중간위험군 환자에서도 BCG와 직접 경쟁 가능한 후보 약제가 등장하면서 치료 선택지는 더욱 다양해지고 있다.비근침윤성 방광암(NMIBC)은 어떻게 치료하고, 치료 성적은 어떠한가?비근침윤성 방광암(NMIBC)은 대부분 경요도 방광 종양 절제술(TURBT) 후 시행되는 보조요법을 통해 관리된다. 이 질환의 임상적 특징은 높은 재발률과 상대적으로 낮은 진행률로 요약된다.실제로 5년 재발률은 50~70%에 이르며, 진행률은 10~20% 수준으로 보고된다. 이러한 자연경과는 단순 TURBT만으로는 장기적인 종양 조절이 어렵다는 점을 시사하며, 보조적 방광내 치료의 중요성을 부각시킨다.TURBT 직후 시행되는 단회 방광내 항암제 주입요법은 저위험군 및 일부 중위험군에서 재발률을 유의하게 낮추는 것으로 입증됐다. 특히 mitomycin C(MMC)는 절제 후 잔존 암세포를 제거하고 세포 재부착을 방지하는 작용을 통해 초기 재발 감소 전략의 표준요법으로 자리잡았다. 그러나 MMC를 포함한 기존 화학요법은 병변의 진행 억제 효과가 제한적이어서 고위험군에서는 단독 치료만으로는 충분하지 않다.고위험군 NMIBC, 특히 고등급 Ta/T1 병변 및 상피내암(CIS)의 경우 BCG 면역요법이 여전히 가장 강력하고 일관된 치료 효과를 제공한다. BCG의 초기 완전반응률은 유두종양에서 55~65%, CIS에서 70~75%로 보고되며, 재발 억제와 진행 위험 감소를 동시에 입증한 유일한 방광내 치료법이다.그럼에도 불구하고 전체 환자의 약 30~40%는 BCG에 초기 반응을 보이지 않는다. 초기 완전반응을 얻더라도 약 절반은 결국 재발한다. 여기에 장기화된 BCG 공급 부족 문제까지 겹치면서 고위험군 외의 환자에게 BCG 사용을 제한해야 하는 현실적인 어려움도 지속되고 있다.이러한 한계를 보완하기 위해 다양한 대체 전략이 개발되고 있다. Gemcitabine, Epirubicin, MMC 등 기존 항암제의 방광내 투여는 BCG 불응성 또는 BCG 금기 환자에서 활용되고 있으며, 특히 gemcitabine–docetaxel 병용요법은 BCG 불응 환자에서 1년 완전반응률 50~60%를 보이며 salvage therapy로 임상적 관심이 높아지고 있다.최근에는 방광보존 치료 옵션이 기존 면역요법을 넘어 유전자치료 영역으로까지 확장되고 있다. Nadofaragene firadenovec(AdstiladrinⓇ)은 IFN-α2b 유전자를 방광 점막에 전달하여 국소 면역반응을 활성화하는 비증식성 아데노바이러스 벡터 기반 치료제로, 고위험 BCG 불응성 NMIBC에서 2022년 미국 FDA 승인을 받았다. 주요 임상시험에서는 3개월 완전반응률 53%, 12개월 지속반응률 24~30%가 보고되며, BCG 불응성 환자에서 새로운 치료 기전의 확립이라는 의의를 가진다.종합하면 NMIBC 치료 전략은 위험군에 따라 크게 달라지며, 저위험군에서는 TURBT와 단회 항암제 주입만으로도 비교적 양호한 성적을 기대할 수 있다. 반면 고위험군에서는 BCG를 중심으로 한 적극적 면역치료가 필수적이며, BCG 불응성 증가와 공급 제한 문제로 인해 새로운 치료제 개발이 더욱 활발히 이루어지고 있다.Bacillus Calmette-Guérin(BCG)는 어떤 치료 방법인가?BCG는 1990년 미국 FDA에서 승인된 비특이적 면역요법으로, 비근육침윤성 방광암(NMIBC) 치료에 널리 사용돼 왔다.BCG의 항종양 효과는 Th1 중심의 면역 반응을 유도하는 기전에 기반한다. BCG가 요로상피세포에 부착되면 IL-1, IL-6, IL-8, TNF-α 등 다양한 사이토카인과 케모카인이 분비되며, 이로 인해 면역세포들이 방광 점막으로 집중된다. 이어서 대식세포, 호중구, 수지상세포 등 항원제시세포가 활성화되고, 변화된 사이토카인 환경 속에서 미성숙 CD4+ T 세포는 Th1 또는 Th2 세포로 분화한다.이 중 Th1 반응은 IFN-γ를 포함한 사이토카인 분비를 통해 BCG 치료 효과와 밀접히 연관되며, 반대로 IL-10을 중심으로 한 Th2 반응은 BCG 실패와 관련된다. 실제로 IL-10 억제 또는 IFN-γ 증가가 Th1 우세 상태를 유도하며, 이는 BCG 매개 종양 퇴행에 필수적인 요소로 알려져 있다.이처럼 BCG는 Th1 면역 반응을 활성화함으로써 방광암이 유발하는 면역 억제 환경을 극복하는 데 효과적이지만, 환자 예후를 더 향상시키기 위해서는 보다 강력한 면역조절 능력을 가진 새로운 치료제의 개발이 필요하다.특히 BCG에 반응하지 않는 NMIBC는 예후가 불량하고 전통적으로 치료 옵션이 제한적이었다. 고위험 BCG-불응성 질환의 경우 근치적 방광 절제술이 표준 치료로 권고되지만, 모든 환자가 수술을 감내할 수 있는 것은 아니다.임상시험 기준으로 BCG의 초기 완전반응률은 유두종양에서 약 55~65%, CIS에서 70~75% 수준이다. 그러나 전체 NMIBC 환자의 약 3분의 1은 BCG에 전혀 반응하지 않으며, 초기 반응을 보인 환자의 약 절반도 결국 재발하거나 진행을 경험한다.미국 FDA는 BCG-불응성 NMIBC를 다음과 같이 정의한다: ▲ 적절한 BCG 요법 후 12개월 이내 지속성 또는 재발성 CIS, 또는 재발성 Ta/T1 질환이 있는 경우(초기 유도 6회 중 ≥5회, 유지 3회 중 ≥2회 또는 2차 유도 6회 중 ≥2회 투여 완료를 ‘적절한 요법’으로 정의), ▲ 적절한 BCG 요법 후 6개월 이내 재발한 고등급 Ta/T1 질환, ▲ 유도요법 후 첫 평가에서 고등급 T1 질환이 확인된 경우이다.Bacillus Calmette-Guérin(BCG)-불응성은 왜 일어나는가?BCG-불응성은 단일 요인보다는 종양 미세환경, 면역반응의 왜곡, 종양세포의 생물학적 저항성이 복합적으로 작용하여 발생한다. 일부 NMIBC는 이미 강한 면역억제 환경을 형성하고 있어, BCG가 유도하는 Th1 중심 면역 반응이 충분히 활성화되지 못한다.이들 종양에서는 IL-10과 TGF-β 같은 면역억제성 사이토카인이 증가하고, Treg와 MDSC가 축적되며, 종양세포의 PD-L1 발현도 높아져 T 세포 기능이 억제된다. 이러한 환경에서는 BCG가 방출시키는 사이토카인이 존재하더라도 Th1 분화보다는 Th2 또는 억제성 면역반응이 우세해져 IFN-γ 중심의 항종양 면역이 제대로 형성되지 않는다.또한 종양세포 자체가 BCG에 대한 내성을 가지는 경우도 있다. 상피세포 표면의 BCG 부착·내재화에 필요한 integrin 등 분자의 발현이 낮거나, BCG가 유도하는 세포사멸 신호(TRAIL, Fas 등)에 저항성을 나타내는 경우가 이에 해당한다. 일부 NMIBC는 특정 유전자 변이나 생존 신호의 과활성화로 인해 BCG 면역 반응에 본질적으로 둔감하다.여기에 고령, 기저질환, 면역노화 등 환자 요인이 더해지면 APC 활성 및 T 세포 반응성이 감소해 BCG가 충분한 면역 강화 효과를 내지 못한다. 균주 간 면역원성 차이, BCG 부족으로 인한 불충분한 치료 역시 면역반응 축적을 방해해 불응 위험을 높인다.결국 BCG 불응성은 종양 미세환경의 면역억제성, Th1 면역 활성화의 실패, 종양세포의 내재적 저항성, 그리고 숙주 면역 기능 저하가 상호 작용하여 나타나는 복합적 면역치료 실패 현상으로 이해된다. 이러한 이유로 BCG 불응성 NMIBC에서는 보다 강력한 면역조절 능력을 갖춘 새로운 치료 전략이 필요하다.인터루킨-15(IL-15)는 어떤 역할을 하는가?IL-15는 공통 γ사슬(γc) 사이토카인 패밀리에 속하는 면역 조절 인자로, 선천 면역과 적응 면역의 경계를 연결하며 항종양 면역을 강화하는 데 핵심적인 역할을 수행한다. IL-2, IL-4, IL-7, IL-9, IL-21과 함께 γc 계열을 이루는 IL-15는 특히 CD8+ T 세포와 자연살해(NK) 세포의 발달, 생존, 증식, 그리고 기능적 활성화 전반을 조절하는 중심적 사이토카인이다.Pleiotropic Effects of IL-15(출처: Cells 2023, 12, 1611).이러한 생물학적 중요성은 다양한 전임상·임상 연구에서 반복적으로 입증되어 왔으며, IL-15가 항암 면역을 유지하는 데 필수적인 조절자로 작용함을 뚜렷하게 보여준다.생리학적으로 IL-15는 IL-15 수용체 α(IL-15Rα)와 함께 이종이량체 형태로 합성된다. IL-15Rα는 자체적으로 신호 전달 기능을 갖고 있지는 않지만 IL-15에 높은 친화도로 결합하여 내질망에서 안정적인 복합체를 형성하고 이를 세포 표면까지 운반함으로써 생물학적 기능 발현을 위한 핵심적인 플랫폼을 제공한다.이 복합체는 생산 세포 표면에 제시된 뒤 인접한 수용 세포의 IL-2/IL-15Rβ와 공통 γ사슬과 결합하여 신호를 전달하는데, 이러한 ‘트랜스제시(trans-presentation)’는 IL-15 생물학을 규정하는 대표적 기전이자 IL-2와 구별되는 가장 특징적인 작동 방식이다.따라서 IL-15와 IL-15Rα는 단핵구, 대식세포, 수지상세포, 혈관내피세포, 골수 및 림프절의 기질세포 등 다양한 세포 유형에서 발현되며, 특히 수지상세포와 대식세포가 주요 생산자인 것으로 보고되었다. 이들 세포는 항원 제시뿐 아니라 IL-15 제시 기능을 통해 CD8+ T 세포와 NK 세포의 생존 신호를 제공함으로써 면역계의 항상성을 유지하는 데 기여한다.IL-15 초작용제(superagonist) 복합체는 무엇인가?최근 면역조절 치료제 개발은 기존 사이토카인 신호 경로를 선택적으로 증폭하여 항종양 면역 반응을 극대화하는 방향으로 진화하고 있으며, 그 중심에는 IL-15 경로 기반의 차세대 초작용제(superagonist) 기술이 있다.IL-15는 본래 NK 세포와 CD8⁺ T 세포의 생존, 증식, 기억 형성에 핵심적인 사이토카인이지만, 생체 내 반감기가 짧고 수용체 결합 효율이 낮아 단독 활용에는 한계가 있었다.이러한 제약을 극복하기 위해 고안된 IL-15 초작용제 복합체는 IL-15의 생물학적 활성을 비약적으로 증폭하도록 설계된 구조적 혁신체로, 대표적인 예가 IL-15N72D 변형체와 IL-15Rα의 sushi 도메인을 융합한 노가펜데킨 알파 인바키셉트이다.IL-15N72D는 아스파라긴(N)에서 아스파트산(D)으로의 단일 아미노산 치환을 통해 수용체 친화성과 신호전달 강도를 향상시킨 기능적 변형체이며, IL-15Rα의 sushi 도메인 결합을 통해 자연적인 trans-presentation 기전을 모사하도록 설계되었다.이 두 구성요소는 IgG1 Fc 영역과 융합되어 약물의 안정성, 체내 반감기, 조직 내 지속 시간을 획기적으로 개선하며, 그 결과 NK 세포와 CD8⁺ T 세포의 활성화 및 항종양 세포독성 반응을 장기간 유도하는 강력한 IL-15 신호 증폭체를 형성한다.이러한 기전은 기존 BCG 치료로 유도되는 국소 면역 반응을 효과적으로 증폭시키며, BCG-불응성 비근육침윤성 방광암에서 관찰되는 높은 완전관해율과 반응 지속성을 설명하는 면역학적 기반을 제공한다.결과적으로 IL-15 변형체와 IL-15Rα가 융합된 초작용제 플랫폼은 단순한 사이토카인 보충을 넘어, 정밀하게 설계된 면역 신호 조절을 통해 종양 미세환경 내에서 효과적인 항암 면역을 재활성화하려는 현대 면역항암제 개발의 중요한 패러다임을 제시한다노가펜데킨 알파 인바키셉트의 약리 기전은?노가펜데킨 알파 인바키셉트는 IL-15 돌연변이체(IL-15N72D)와 IL-15Rα를 융합한 복합체로, 자연 면역세포가 제공하는 IL-15 제시 기전을 모방한다. 이를 통해 CD8+ T 세포, NK 세포, 기억 T 세포의 증식·활성화를 강하게 유도하면서도, 면역억제성 조절 T 세포의 확장은 최소화한다.전임상 모델에서 방광 내 투여된 노가펜데킨 알파 인바키셉트는 단독 또는 BCG와 병용 시 BCG 단독보다 우수한 항종양 효과를 보였다. 또한 비융합(native) IL-15에 비해 림프조직 내 지속시간이 길고, 약동학적 안정성이 크게 향상되어 보다 강력하고 지속적인 항종양 면역반응을 유발한다.결과적으로 노가펜데킨 알파 인바키셉트는 IL-15 신호를 증폭해 킬러 T 세포 중심의 면역반응을 재가동시키는 기전적 특성을 기반으로, BCG-불응성 NMIBC에서 의미 있는 치료적 이점을 제공하는 IL-15 기반 면역증강제이다.Immune Effects of nogapendekin alfa inbakicept(출처: Cells 2023, 12, 1611).위 사진자료에 대해 설명하면, A. 노가펜데킨 알파 인바키셉트는 인간 IgG1 Fc와 융합된 IL15Rα에 결합된 돌연변이(N72D) 인간 IL-15로 구성된다. B. 노가펜데킨 알파 인바키셉트는 IL-15 수용체를 통해 순환 면역 세포에 결합한다. C. 노가펜데킨 알파 인바키셉트가 림프구에 결합하면 자연 살해(NK) 세포와 CD8+ T 세포 집단이 활성화된다되고 확장되어 고효과 CD56 dim 및 CD56 bright NK 세포와 중앙 기억 T 세포(TCM)가 확장된다. D. 비장 CD8+ T 세포 표면의 CXCR3가 상향 조절되면 종양 미세 환경(TME)으로 이동할 가능성이 높아집니다. 활성화된 NK 세포도 종양으로 이동한다. E. 활성화된 종양 침윤 CD8+ T 림프구(TIL)는 MHC 클래스 I 복합체가 제시하는 종양 관련 항원 에피토프를 인식하여 암세포를 인식한다. 활성화된 CD8+ T 세포와 NK 세포는 세포독성이 증가하여 암세포 사멸을 유도한다.CD8+ T 세포는 IFNγ 및 TNF⍺와 같은 Th1 사이토카인을 분비하여 염증성 TME를 촉진하고 과립구 및 단핵구 골수유래 억제 세포(MDSC)의 PD-L1을 상향 조절합니다. 노가펜데킨 알파 인바키셉트는 NK TIL이 TGF-β의 영향에 저항성을 갖도록 하고 항체 의존성 세포독성(ADCC)을 증가시킬 수 있도록 한다.노가펜데킨 알파 인바키셉트의 치료적 위치는?비근육침윤성 방광암(NMIBC)은 초기 치료로 경요도 방광종양절제술(TURBT)이 시행되지만, 재발률이 높고 병변이 지속·활성화되는 경우가 많아 반복적 치료가 필요하다. 특히 CIS를 동반한 고위험군에서는 BCG 치료가 표준으로 자리잡아 있으나, 충분한 BCG 노출에도 불구하고 재발·지속·진행이 나타나는 BCG-불응성 환자군이 적지 않다.이러한 환자에서 근치적 방광적출술(radical cystectomy)은 표준 치료로 권고되지만, 고령, 동반질환, 삶의 질 저하에 대한 우려, 환자 선호 등의 이유로 수술 적용이 어려운 경우가 많다. 이에 따라 방광을 보존하면서도 충분한 항종양 효과를 제공할 수 있는 새로운 치료 전략의 필요성이 지속적으로 제기되어 왔다.노가펜데킨 알파 인바키셉트는 IL-15/IL-15Rα 복합체 기반의 IL-15 초작동제로, CD8+ T 세포와 NK 세포의 증식·활성화를 강력하게 유도하는 면역 증강형 생물학적 제제이다. NMIBC에서 BCG 치료는 국소 면역활성에 의존하지만, BCG-불응성 환자에서는 방광 내 면역 미세환경의 소진, T/NK 세포 감소, BCG 반응 저하 등이 주요 병태생리로 지적된다.이러한 맥락에서 노가펜데킨 알파 인바키셉트는 고갈된 면역계를 다시 활성화하여 기존 BCG 효과를 강화하고, 단독 BCG로는 확보하기 어려운 항종양 면역반응을 확대하는 기전적 장점을 가진다.전신 면역관문억제제인 pembrolizumab(키트루다)은 일부 환자에서 의미 있는 완전반응을 유도하지만, 전신 면역 관련 부작용과 장기 치료에 따른 독성·비용 부담이 중요한 제약으로 남아 있다. 반면 노가펜데킨 알파 인바키셉트는 방광 내 국소 투여를 기반으로 하여 전신 독성이 극히 낮으며, 고령 또는 동반질환이 많은 실제 진료 환경에서 사용하기 용이하다.또한 바이러스 벡터를 이용하는 AAV 기반 유전자치료제(nadofaragene firadenovec)와 달리 벡터 노출에 따른 안전성 우려가 없고, 기존 BCG 치료 패턴과 자연스럽게 연계되어 임상적 채택성이 높다는 점도 장점이다.노가펜데킨 알파 인바키셉트의 임상적 의미는 단순한 반응률 개선을 넘어, BCG-불응성 CIS 환자에서 방광적출술을 지연하거나 회피할 수 있는 실질적 치료 대안을 제공한다는 데에 있다.실제 임상에서 의미 있는 완전반응률과 지속기간이 확인되었으며, 이는 방광적출술을 바로 시행하기 어려운 환자에게 중요한 시간적 여유와 치료 선택권을 제공한다. 전신 독성의 부담이 거의 없고, BCG 기반 면역작동 기전을 확장하는 방식이라는 점 또한 치료적 위치를 공고히 한다.노가펜데킨 알파 인바키셉트(ANKTIVA)의 허가임상은 어떠한가?ANKTIVA의 효능은 QUILT-3.032(NCT03022825) 시험에서 평가되었다. 이 연구는 경요도 방광종양절제술(TURBT) 이후 BCG에 반응하지 않는 고위험 비근육침윤성 방광암(NMIBC) 중 상피내암(CIS)을 동반한 성인 환자 77명을 대상으로 한 단일군, 다기관 임상시험이었다. 여기에는 Ta/T1 유두상 병변의 동반 여부와 상관없이 CIS를 가진 환자들이 포함되었다.BCG 불응성 고위험군 NMIBC의 CIS는, 충분한 BCG 치료를 완료한 후 12개월 이내에 CIS가 단독으로 또는 Ta/T1 병변과 함께 지속되거나 재발한 경우로 정의되었다. 충분한 BCG 치료는 초기 유도요법 6회 중 최소 5회를 투여하고, 이어서 유지요법 3회 중 최소 2회 또는 두 번째 유도요법 6회 중 최소 2회를 투여한 경우로 정의되었다.치료 전 Ta 또는 T1 병변 환자들은 절제가 가능한 모든 병변을 제거하기 위해 TURBT를 시행받았다. 절제, 소작 또는 전기소작이 불가능한 잔여 CIS는 허용되었다. 한편 근침윤성 방광암(T2~T4), 국소 진행성, 전이성 또는 방광 외부(요도, 요관, 신우) 침범이 있거나 그 병력이 있는 환자는 시험에서 제외되었다.환자들은 유도요법 동안 ANKTIVA 400mcg와 BCG를 주 1회, 6주 연속 투여받았다. 이후 질병이 없거나 저등급 질환을 가진 경우 4, 7, 10, 13, 19개월째에 3주 간격으로 주 1회 추가 투여를 받았다. 치료 3개월 시점에 CIS가 지속되거나 고등급 Ta 병변이 남아 있는 경우에는 두 번째 유도요법을 받을 수 있었다. 치료 25개월 시점에 완전반응(CR)이 유지되는 환자는 25, 31, 37개월째에 동일한 방식으로 추가 투여가 가능했다.종양 상태 평가는 최대 2년 동안 3개월마다 시행되었다. 24개월 이후의 반응 평가는 각 기관의 진료 기준에 따라 시행되었다. 치료 시작 후 첫 6개월 동안은 무작위 또는 방광경 유도 조직검사가 필수적으로 시행되었다. 주요 효능 평가지표는 어느 시점에서든 완전반응을 달성했는지와(방광경 검사 및 필요 시 TURBT/조직검사 결과 음성, 요세포검사 음성 기준) 그 반응의 지속기간이었다.등록 환자의 중앙 연령은 73세(범위 50~91세)였고, 86%가 남성이었다. 인종 분포는 백인 90%, 흑인 6%, 아시아인 1%, 아메리칸 인디언/알래스카 원주민 1%, 미상 1%였다. ECOG 수행능력은 0점이 83%, 1점이 17%였다.연구 등록 시 종양 특성은 CIS 단독 69%, CIS + Ta 병변 21%, CIS + T1(±Ta) 병변 10%였다. 기저 질환 상태는 불응성 43%, 재발성 57%였다. 이전 BCG 투여 횟수의 중앙값은 12회(범위 8~45회)였고, 13%는 분할 용량 BCG를 받은 경험이 있었다. 방광경 영상 방식은 백색광 57%, 청색광 또는 협대역 영상 40%, 미상 3%였다.효능 결과는 표 3에 제시되어 있으며, 전체 환자의 31%(24명)는 두 번째 유도요법을 받았다.노가펜데킨 알파 인바키셉트의 쟁점을 무엇인가?노가펜데킨 알파 인바키셉트는 IL-15의 생물학적 활성을 기반으로 설계된 차세대 면역작용제로, 고위험 BCG 불응성 비근침윤성 방광암(NMIBC) 치료에서 새로운 치료적 가능성을 제시하고 있다.IL-15는 CD8⁺ T 세포와 NK 세포의 생존과 기능을 강화하는 핵심 사이토카인으로 알려져 있으나, 자연 상태의 IL-15는 짧은 반감기, 불안정한 구조, 수용체 결합의 가변성 등으로 인해 치료제로 활용하는 데 본질적인 제약이 존재해왔다.노가펜데킨 알파 인바키셉트는 IL-15와 IL-15Rα 수용체 도메인을 결합해 형성한 안정적 이종이량체 기반의 IL-15 초작용제로, 내재 IL-15에 비해 우수한 생체 내 안정성과 장기적 면역 활성 유도가 가능하다는 점에서 임상적 의미가 크다.특히 BCG 치료에 반응하지 않는 NMIBC 환자는 방광적출술이 표준 치료임에도 불구하고, 고령 및 동반질환 등으로 수술이 어려운 경우가 많아 실질적인 치료 공백이 존재해왔다. 이러한 점에서 BCG와 병용하여 국소 종양 미세환경을 재활성화할 수 있는 약제의 개발은 방광보존 전략을 확장할 수 있는 새로운 치료 패러다임이라 할 수 있다.노가펜데킨 알파 인바키셉트의 주요 장점은 BCG와 병용 시 강력한 상승효과를 보인다는 점이다. IL-15Rα와의 결합을 통해 강화된 생물학적 활성은 APC, NK 세포, CD8⁺ T 세포의 집적과 기능을 촉진하여 항종양 면역반응을 증폭시키며, 이는 허가 근거가 된 QUILT-3.032 연구에서 3개월 완전반응률 53%, 12개월 반응 지속률 24~30%로 나타났다.이러한 치료 성적은 기존 BCG 불응 환자에서 보고된 방광내 요법의 성적을 상회하는 결과이며, 이 약제가 임상적으로 의미 있는 반응을 유도하는 면역치료제로 기능함을 보여준다.그러나 노가펜데킨 알파 인바키셉트는의 개발과 허가 과정에는 여러 한계와 도전이 병존한다. 가장 큰 문제는 근거 임상이 무작위 대조군이 없는 단일군(single-arm) 연구로 수행되었다는 점으로, 이는 약제의 효과를 BCG 재투여 효과와 명확히 구분하기 어렵게 만들며, 역사적 대조(historical control)와의 비교에서 발생할 수 있는 해석의 변이를 피하기 어렵다.또한 환자군 내 BCG 노출량, CIS 단독 여부, 종양 특성 등에서 이질성이 존재하여 반응률과 반응 지속성의 정확한 비교가 제한된다. 반응의 지속성 역시 완전반응을 보인 환자의 일부에서만 장기적으로 유지되는 경향이 관찰되었고, 12개월 이후 장기 추적자료는 아직 충분히 축적되지 않아 방광보존 전략의 장기적 안전성과 유효성에 대한 확정적 결론을 내리기 어렵다.더불어 치료효과의 기저에 있는 종양면역미세환경의 상태가 환자별로 크게 달라, 이 약제가 NK/T 세포 결핍 또는 극도로 억제된 미세환경을 충분히 회복시키지 못하는 경우가 존재할 것으로 예상되며, 이러한 점은 향후 바이오마커 기반 환자선택 전략의 필요성을 시사한다.이처럼 노가펜데킨 알파 인바키셉트는 IL-15 생물학을 임상적으로 구현한 최초의 치료제로서 BCG 불응성 NMIBC라는 미충족 의료수요 영역에서 실질적인 치료 옵션을 제공하고 있다.초기 반응률과 독성 프로파일은 고무적이지만, 단일군 연구 설계, 병용요법의 기여도 분리 문제, 반응 지속성의 제한, 장기 추적자료 부족 등은 여전히 해결해야 할 과제로 남아 있다.그럼에도 불구하고 노가펜데킨 알파 인바키셉트는 기존 치료제와는 차별화된 기전을 바탕으로 난치성 NMIBC에서 방광보존 전력을 확장할 수 있는 중요한 면역치료제로 자리매김할 가능성이 높으며, 향후 병용 전략, 내성 기전 규명, 예측 바이오마커 개발 등을 통해 그 임상적 가치가 더욱 강화될 것으로 기대된다.참고문헌 1. Grace Lui et al. “Exploiting an Interleukin-15 Heterodimeric Agonist (N803) for Effective Immunotherapy of Solid Malignancies” Cells 2023, 12(12), 1611. 3. Richard S et al. “Non–muscle-invasive Bladder Cancer: Overview and Contemporary Treatment Landscape of Neoadjuvant Chemoablative Therapies” Reviews in Urology, Vol. 22 No. 2 2020. 3. Jong Ho Park et al. “The Emerging Treatment of BCG (Bacillus Calmette-Guérin)- Unresponsive Non–Muscle-Invasive Bladder Cancer“ Journal of Urologic Oncology 2024;22(3):246-255. 4. Aiman Waheed et al. “Nogapendekin alfa inbakicept-PMLN: first approval milestone for BCG-unresponsive noninvasive bladder cancer: editorial” Annals of Medicine & Surgery (2024) 86:6386–6388. 5. Brian L. Heiss et al. “FDA Approval Summary: Nogapendekin Alfa Inbakicept-pmln with BCG for BCG-unresponsive carcinoma in situ” Clin Cancer Res. 2025 October 15; 31(20): 4223–4229. 6. Vikram M et al. “Mechanism of action of nadofaragene firadenovec-vncg” Front. Oncol. 14:1359725. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-11-20 17:29:43최병철 박사 -
 "심부전 치료 4제요법 필수…ARNI 조기 도입이 예후 좌우"[데일리팜=손형민 기자] 심부전은 여전히 심장병 중 가장 위험한 질환으로 꼽힌다. 단순 피로감이나 호흡곤란으로 대표되는 질환이 아니라, 심장의 구조적·기능적 이상으로 인해 혈류 공급이 떨어지고 전신 장기의 기능 저하를 초래하는 전신성 질환이다.특히 우리나라처럼 고령화 속도가 빠른 국가에서는 유병률 증가 속도가 더욱 가파르다. 실제 국내 심부전 유병률은 20년 만에 약 4.5배 증가했고, 80세 이상에서는 유병률이 26%를 넘어선다.더 주목해야 할 점은 심부전의 5년 생존율이 유방암·전립선암 등 주요 암보다 낮다는 사실이다. 더 이상 단순한 만성질환이 아닌, 생존과 직결되는 중증질환임을 보여준다.이처럼 심부전이 중증질환화하는 가운데, 데일리팜은 유럽심장학회(ESC) 과학프로그램 위원장 미하엘 뵘 자를란트대학병원 내과 교수, 대한심부전학회 이사장 유병수 원주기독병원 심장내과 교수와 함께 심부전의 현재와 한국 치료환경의 과제를 짚어봤다.왼쪽부터 미하엘 뵘 교수, 유병수 교수 두 전문가는 특히 박출률 감소 심부전(HFrEF)의 악화 속도와 재입원 위험성을 강조하며 "초기 치료가 생존을 결정한다"고 입을 모았다.심부전 중에서도 박출률 감소 심부전(HFrEF)은 악화 속도가 빠르고, 퇴원 후 1년 내 재입원율이 20% 이상으로 보고되는 대표 고위험 질환이다. 재입원은 예후 악화를 의미할 뿐 아니라 사망률 증가로 직결되기 때문에, 전 세계 가이드라인은 ‘HFrEF 치료의 성패는 초기 치료전략에 달려 있다’고 명시하고 있다.진단 즉시 4 가지 기둥 약제(pillars) ACE 억제제 혹은 안지오텐신수용체 네프릴리신억제제, 베타차단제, 비스테로이드성 무기질코르티코이드 길항제, SGLT-2 억제제를 신속히 도입하고, 가능한 빠른 시점에 목표 용량까지 증량하는 것이 생존율을 개선하는 유일한 근거 기반 전략이라는 의미다.이 가운데 대표적인 ARNI 계열 치료제인 '엔트레스토(사쿠비트릴·발사르탄)'는 HFrEF 치료의 가장 중요한 축이다. 대표 임상인 PARADIGM-HF 연구에서 엔트레스토는 기존 ACE 억제제 ‘에날라프릴’ 대비 심혈관 사망·심부전 입원을 20% 감소시키며 HFrEF 치료 패러다임을 완전히 뒤바꿨다.돌연사 위험과 응급실 방문까지 줄어드는 일관된 결과는 RAAS 단일 억제 시대에서 ARNI 중심의 새로운 표준치료로 넘어가야 한다는 근거가 됐다.독일은 이러한 변화가 실제 진료 현장에 신속히 반영된 대표 국가다. 엔트레스토를 포함한 표준치료가 대부분의 HFrEF 환자에게 초기부터 적용되고, 목표 용량 도달을 원칙으로 하는 표준화된 심부전 진료경로가 이미 자리 잡았다.반면 국내는 여전히 초기 4제 적용률이 낮고, 약물 용량 증량이 미흡해 치료 격차가 발생한다는 지적이 끊이지 않는다. 전문가들은 이 같은 격차는 결국 환자의 생존 격차로 이어진다며 조기 치료 최적화의 필요성을 강조하고 있다.Q. 박출률 감소 심부전(HFrEF)의 환자 비중과 질환적인 특징은?유병수 교수유 교수: 데이터에 따라 다르지만, 상급종합병원 중심의 Korean Heart Failure III Registry에서는 약 55% 이상이 HFrEF로 나타난다. 이는 중증 환자가 많은 3차 병원 환자군 특성 때문이다.실제 임상 현장에서는 박출률 보존(HFpEF) 또는 경도 감소(HFmrEF) 환자가 더 많을 것으로 추정된다. 최근 고령·비만 환자 증가로 이러한 분포는 더욱 뚜렷해지는 경향을 보인다. HFrEF는 심장의 수축 기능이 크게 떨어지는 형태로 악화 속도가 빠르며, 호흡곤란·부종·피로감 등 증상이 더 심하게 나타난다.미하엘 교수: 유럽에서도 HFrEF는 약 50% 정도로 설명되지만 실제 비율은 더 높을 가능성이 있다. 고혈압, 심방세동, 뇌졸중, 당뇨를 가진 여성 환자들은 과거 HFpEF로 분류되는 경우가 많았는데, 최신 기준에서는 이들이 HFrEF 또는 HFmrEF로 재분류될 수 있다. 이 변화는 박출률을 기준으로 한 심부전 분류가 향후 수정될 가능성을 시사한다.Q. 심부전 치료에서 4제요법이 표준요법으로 확립된 근거는 무엇인가?유 교수: 심부전 표준치료는 수십 년 동안 축적된 임상 연구를 기반으로 확립된 치료 전략이다. 베타차단제, ACE 억제제, ARB, MRA 등 기존 약제들은 모두 사망률과 재입원을 감소시키는 효과가 대규모 연구를 통해 일관되게 입증됐다. 여기에 최근 SGLT-2 억제제가 추가되면서 네 가지 기둥 약제가 완성됐고, RAAS 억제제는 ARNI 계열로 대체되는 흐름이 자리 잡았다. 특히 4제요법을 모두 적용할 경우 사망·입원 위험을 70% 이상 줄일 수 있다는 근거가 확보돼 있어, 특별한 금기가 없는 한 초기부터 적극적으로 사용하는 것이 예후 개선의 핵심이다.주요 사건 발생(hard outcome)을 개선시키는 명확한 효과가 있기 때문에 특별한 이유를 제외하고는 반드시 지켜야 하는 표준 치료라고 정립하고 있다. 말씀드린 표준치료는 이미 그 효과가 너무 많이 입증돼 있다. 특히 이 4가지 표준 약제를 사용하면 상대적으로 약 70% 이상의 사망률과 입원율을 줄일 수 있고 이 효과를 4명 당 1명의 환자가 볼 수 있는 것으로 나와 있다.미하엘 교수: 심부전 약물치료는 오랜 기간 신경·내분비 축을 조절하는 방향으로 발전해 왔다. ACE 억제제와 MRA가 먼저 개발됐고, 주요 대규모 임상들이 지금의 치료 기반을 만들었다. 이 연구들이 축적되면서 심부전 환자의 사망률이 점차 낮아졌다.실제로 메타 분석에서도 이러한 사망률이나 입원율이 4개 제제를 함께 시작했을 때 65%정도 감소한다는 분석이 있다.Q. 엔트레스토가 RAAS 억제제 계열 약제 중 우선 권고되는 이유는 무엇인가?유 교수: 엔트레스토(ARNI)가 우선 권고되는 근거는 PARADIGM-HF 연구에서 명확하게 제시된다.이 연구에서 엔트레스토는 기존 ACE 억제제인 에날라프릴 대비 사망과 입원을 포함한 주요 hard outcome을 약 20% 감소시켰다. 특히 이 임상은 일반적인 위약 대비 연구가 아니라, 당시의 강력한 표준치료인 ACE 억제제와 직접 비교해 우월성을 입증했다는 점에서 의미가 크다.기전 측면에서는 ARB(발사르탄)에 네프릴리신 억제제(사쿠비트릴)라는 새로운 작용기전이 더해져 나트륨 배출, 혈관 확장, 심근 보호 효과가 상승적으로 작용한다. 이러한 생물학적 효과가 실제 임상 결과로 이어졌고, ARNI가 기존 RAAS 억제제를 대체하는 새로운 표준으로 자리 잡게 된 배경이 됐다.미하엘 뵘 교수미하엘 교수: PARADIGM-HF는 심부전 치료 패러다임을 바꾼 연구로 평가할 수 있다. 기존 표준요법이던 ACE 억제제를 대체할 수 있는 새로운 기전을 제시했고, 대규모 무작위 배정 연구로서 장기 데이터를 확보해 높은 안정성과 신뢰도를 가진다. 이러한 규모의 컨트롤 그룹을 다시 모집하는 것은 사실상 어렵기 때문에 동급 연구가 재현되기 힘들 것이라고 본다.엔트레스토는 단순히 1차 평가변수뿐 아니라 환자의 삶의 질(QoL)에서도 뚜렷한 개선을 보였다. 설문 기반 평가에서도 환자의 전반적 웰빙과 증상 부담이 크게 완화된 것으로 나타났으며, 이는 심부전 특히 HFrEF 환자에게 매우 중요한 임상적 의미를 갖는다.또 신기능 보존 효과가 ACE 억제제보다 우수하게 나타났고, 장기적으로 당뇨 발생 위험을 줄이는 이점까지 확인되었다. 이러한 부가적 혜택은 사쿠비트릴과 발사르탄 조합의 상호보완적 특성이 가져온 결과로 볼 수 있으며, 심부전 치료 전반에서 환자에게 더 나은 임상적 경험을 제공할 수 있다는 점에서 큰 의의를 갖는다.Q. 표준치료 네 가지 약제를 ‘가능한 한 빨리’ 도입해야 한다고 강조되는 이유는 무엇인가?유 교수: HFrEF는 진단 초기의 예후가 특히 나쁜 질환으로, 첫 3개월 동안 예후가 급격히 나빠지는 환자가 많다. 초기 사망률과 재입원 위험이 집중되는 시기이기 때문에, 네 가지 표준치료 약제를 가능한 한 빠르게 도입해야 한다.이 약제들의 효과는 단순히 증상 완화가 아니라 사망률·입원률을 빠르게 낮추는 방향으로 나타나기 때문에, 치료 시기가 늦어지면 해당 이득을 바로 잃게 된다. 특히 HFrEF 환자에서 초기에 약제를 적용할수록 예후 개선이 크다는 여러 연구 결과가 축적되면서 국내외 가이드라인 모두 조기 개입을 강조하고 있다.미하엘 교수: 초기 집중 치료가 중요한 이유는 심부전의 임상적 골든타임이 존재하기 때문이다. HFrEF 환자는 처음 진단된 시점부터 심근 스트레스가 급격히 증가하고 이 과정에서 구조적·기능적 손상이 빠르게 진행된다. 따라서 치료제의 이점이 누적되기 전에 가능한 빨리 네 가지 약제를 투입해야 한다.또 약제를 순차적으로 늦게 도입하는 방식은 환자의 임상적 위험을 그대로 방치하는 결과를 초래할 수 있다. 대규모 환자 자료에서도 신속한 병용도입이 단독·지연 도입보다 생존율을 높이고 입원 위험을 줄이는 것으로 일관되게 제시된다. 이러한 이유로 유럽에서도 가능하면 4제요법 조기 완성을 목표로 치료 전략을 운영하고 있다.Q. 한국은 여전히 4제 요법의 초기 적용률이 낮다. 개선을 위해 필요한 과제는 무엇인가?유 교수: 국내에서 초기 치료 최적화가 잘 이루어지지 않는 이유로, 의료진의 시간적·환경적 제약, 다약제에 대한 환자 우려, 진료현장의 인력 부담 등이 복합적으로 작용하고 있다. 하지만 4제요법의 임상적 이득이 매우 크기 때문에, 이를 공통된 진료경로로 만드는 것이 필요하다.심부전 센터와 전문클리닉의 역할 강화, 초진 단계부터 적용 가능한 통합 치료 알고리즘 마련, 진료현장에서 적극적인 용량 증량(titration)을 도울 수 있는 구조가 중요하다. 환자의 약제 순응도를 높이기 위한 교육, 그리고 지역 의료기관에서도 동일한 기준으로 치료가 이뤄질 수 있도록 정책적 지원이 동반돼야 한다.임상적 관성(clinical inertia) 차원에서 특히 한국의 특별한 상황은 의료진이 외래 환자를 볼 때 너무 짧은 시간이 주어지고 많은 환자를 봐야 한다는 점이다. 그래서 실제로 표준치료나 환자에 대한 개인 맞춤형 치료를 적용하기가 굉장히 어려운 부분이 있다.정리하자면 국내의 표준치료 목표 수준은 많이 올라온 상태이다. 하지만 여전히 심부전 환자를 보는 특별한 전문의를 제외한 많은 분들은 아직 개선의 여지가 있다고 말씀드릴 수 있겠다.미하엘 교수: 독일의 사례에서도 확인되듯, 초기 치료 도입률을 높이기 위해서는 ‘표준화된 진료경로(clinical pathway)’가 핵심이다. 의료진의 경험과 숙련도에 의존하는 방식이 아니라, 누구라도 동일한 기준으로 치료를 설계할 수 있게 만드는 체계가 필요하다.또 약제의 최대 내약용량에 도달하도록 관리하는 과정에서, 임상현장에 시간적 여유·지속적 모니터링 체계가 마련되는 것이 중요하다. 실제로 엔트레스토를 포함한 표준 4제 요법은 용량을 충분히 올렸을 때 최적 효과가 나타나므로, 이를 위한 외래·간호·교육 체계의 확충이 반드시 필요하다.결국 국가 차원의 관리모델이 도입될 때 치료 격차가 좁아지고, 한국에서도 많은 환자가 더 나은 예후를 기대할 수 있을 것이라고 강조했다.2025-11-20 06:07:34손형민
"심부전 치료 4제요법 필수…ARNI 조기 도입이 예후 좌우"[데일리팜=손형민 기자] 심부전은 여전히 심장병 중 가장 위험한 질환으로 꼽힌다. 단순 피로감이나 호흡곤란으로 대표되는 질환이 아니라, 심장의 구조적·기능적 이상으로 인해 혈류 공급이 떨어지고 전신 장기의 기능 저하를 초래하는 전신성 질환이다.특히 우리나라처럼 고령화 속도가 빠른 국가에서는 유병률 증가 속도가 더욱 가파르다. 실제 국내 심부전 유병률은 20년 만에 약 4.5배 증가했고, 80세 이상에서는 유병률이 26%를 넘어선다.더 주목해야 할 점은 심부전의 5년 생존율이 유방암·전립선암 등 주요 암보다 낮다는 사실이다. 더 이상 단순한 만성질환이 아닌, 생존과 직결되는 중증질환임을 보여준다.이처럼 심부전이 중증질환화하는 가운데, 데일리팜은 유럽심장학회(ESC) 과학프로그램 위원장 미하엘 뵘 자를란트대학병원 내과 교수, 대한심부전학회 이사장 유병수 원주기독병원 심장내과 교수와 함께 심부전의 현재와 한국 치료환경의 과제를 짚어봤다.왼쪽부터 미하엘 뵘 교수, 유병수 교수 두 전문가는 특히 박출률 감소 심부전(HFrEF)의 악화 속도와 재입원 위험성을 강조하며 "초기 치료가 생존을 결정한다"고 입을 모았다.심부전 중에서도 박출률 감소 심부전(HFrEF)은 악화 속도가 빠르고, 퇴원 후 1년 내 재입원율이 20% 이상으로 보고되는 대표 고위험 질환이다. 재입원은 예후 악화를 의미할 뿐 아니라 사망률 증가로 직결되기 때문에, 전 세계 가이드라인은 ‘HFrEF 치료의 성패는 초기 치료전략에 달려 있다’고 명시하고 있다.진단 즉시 4 가지 기둥 약제(pillars) ACE 억제제 혹은 안지오텐신수용체 네프릴리신억제제, 베타차단제, 비스테로이드성 무기질코르티코이드 길항제, SGLT-2 억제제를 신속히 도입하고, 가능한 빠른 시점에 목표 용량까지 증량하는 것이 생존율을 개선하는 유일한 근거 기반 전략이라는 의미다.이 가운데 대표적인 ARNI 계열 치료제인 '엔트레스토(사쿠비트릴·발사르탄)'는 HFrEF 치료의 가장 중요한 축이다. 대표 임상인 PARADIGM-HF 연구에서 엔트레스토는 기존 ACE 억제제 ‘에날라프릴’ 대비 심혈관 사망·심부전 입원을 20% 감소시키며 HFrEF 치료 패러다임을 완전히 뒤바꿨다.돌연사 위험과 응급실 방문까지 줄어드는 일관된 결과는 RAAS 단일 억제 시대에서 ARNI 중심의 새로운 표준치료로 넘어가야 한다는 근거가 됐다.독일은 이러한 변화가 실제 진료 현장에 신속히 반영된 대표 국가다. 엔트레스토를 포함한 표준치료가 대부분의 HFrEF 환자에게 초기부터 적용되고, 목표 용량 도달을 원칙으로 하는 표준화된 심부전 진료경로가 이미 자리 잡았다.반면 국내는 여전히 초기 4제 적용률이 낮고, 약물 용량 증량이 미흡해 치료 격차가 발생한다는 지적이 끊이지 않는다. 전문가들은 이 같은 격차는 결국 환자의 생존 격차로 이어진다며 조기 치료 최적화의 필요성을 강조하고 있다.Q. 박출률 감소 심부전(HFrEF)의 환자 비중과 질환적인 특징은?유병수 교수유 교수: 데이터에 따라 다르지만, 상급종합병원 중심의 Korean Heart Failure III Registry에서는 약 55% 이상이 HFrEF로 나타난다. 이는 중증 환자가 많은 3차 병원 환자군 특성 때문이다.실제 임상 현장에서는 박출률 보존(HFpEF) 또는 경도 감소(HFmrEF) 환자가 더 많을 것으로 추정된다. 최근 고령·비만 환자 증가로 이러한 분포는 더욱 뚜렷해지는 경향을 보인다. HFrEF는 심장의 수축 기능이 크게 떨어지는 형태로 악화 속도가 빠르며, 호흡곤란·부종·피로감 등 증상이 더 심하게 나타난다.미하엘 교수: 유럽에서도 HFrEF는 약 50% 정도로 설명되지만 실제 비율은 더 높을 가능성이 있다. 고혈압, 심방세동, 뇌졸중, 당뇨를 가진 여성 환자들은 과거 HFpEF로 분류되는 경우가 많았는데, 최신 기준에서는 이들이 HFrEF 또는 HFmrEF로 재분류될 수 있다. 이 변화는 박출률을 기준으로 한 심부전 분류가 향후 수정될 가능성을 시사한다.Q. 심부전 치료에서 4제요법이 표준요법으로 확립된 근거는 무엇인가?유 교수: 심부전 표준치료는 수십 년 동안 축적된 임상 연구를 기반으로 확립된 치료 전략이다. 베타차단제, ACE 억제제, ARB, MRA 등 기존 약제들은 모두 사망률과 재입원을 감소시키는 효과가 대규모 연구를 통해 일관되게 입증됐다. 여기에 최근 SGLT-2 억제제가 추가되면서 네 가지 기둥 약제가 완성됐고, RAAS 억제제는 ARNI 계열로 대체되는 흐름이 자리 잡았다. 특히 4제요법을 모두 적용할 경우 사망·입원 위험을 70% 이상 줄일 수 있다는 근거가 확보돼 있어, 특별한 금기가 없는 한 초기부터 적극적으로 사용하는 것이 예후 개선의 핵심이다.주요 사건 발생(hard outcome)을 개선시키는 명확한 효과가 있기 때문에 특별한 이유를 제외하고는 반드시 지켜야 하는 표준 치료라고 정립하고 있다. 말씀드린 표준치료는 이미 그 효과가 너무 많이 입증돼 있다. 특히 이 4가지 표준 약제를 사용하면 상대적으로 약 70% 이상의 사망률과 입원율을 줄일 수 있고 이 효과를 4명 당 1명의 환자가 볼 수 있는 것으로 나와 있다.미하엘 교수: 심부전 약물치료는 오랜 기간 신경·내분비 축을 조절하는 방향으로 발전해 왔다. ACE 억제제와 MRA가 먼저 개발됐고, 주요 대규모 임상들이 지금의 치료 기반을 만들었다. 이 연구들이 축적되면서 심부전 환자의 사망률이 점차 낮아졌다.실제로 메타 분석에서도 이러한 사망률이나 입원율이 4개 제제를 함께 시작했을 때 65%정도 감소한다는 분석이 있다.Q. 엔트레스토가 RAAS 억제제 계열 약제 중 우선 권고되는 이유는 무엇인가?유 교수: 엔트레스토(ARNI)가 우선 권고되는 근거는 PARADIGM-HF 연구에서 명확하게 제시된다.이 연구에서 엔트레스토는 기존 ACE 억제제인 에날라프릴 대비 사망과 입원을 포함한 주요 hard outcome을 약 20% 감소시켰다. 특히 이 임상은 일반적인 위약 대비 연구가 아니라, 당시의 강력한 표준치료인 ACE 억제제와 직접 비교해 우월성을 입증했다는 점에서 의미가 크다.기전 측면에서는 ARB(발사르탄)에 네프릴리신 억제제(사쿠비트릴)라는 새로운 작용기전이 더해져 나트륨 배출, 혈관 확장, 심근 보호 효과가 상승적으로 작용한다. 이러한 생물학적 효과가 실제 임상 결과로 이어졌고, ARNI가 기존 RAAS 억제제를 대체하는 새로운 표준으로 자리 잡게 된 배경이 됐다.미하엘 뵘 교수미하엘 교수: PARADIGM-HF는 심부전 치료 패러다임을 바꾼 연구로 평가할 수 있다. 기존 표준요법이던 ACE 억제제를 대체할 수 있는 새로운 기전을 제시했고, 대규모 무작위 배정 연구로서 장기 데이터를 확보해 높은 안정성과 신뢰도를 가진다. 이러한 규모의 컨트롤 그룹을 다시 모집하는 것은 사실상 어렵기 때문에 동급 연구가 재현되기 힘들 것이라고 본다.엔트레스토는 단순히 1차 평가변수뿐 아니라 환자의 삶의 질(QoL)에서도 뚜렷한 개선을 보였다. 설문 기반 평가에서도 환자의 전반적 웰빙과 증상 부담이 크게 완화된 것으로 나타났으며, 이는 심부전 특히 HFrEF 환자에게 매우 중요한 임상적 의미를 갖는다.또 신기능 보존 효과가 ACE 억제제보다 우수하게 나타났고, 장기적으로 당뇨 발생 위험을 줄이는 이점까지 확인되었다. 이러한 부가적 혜택은 사쿠비트릴과 발사르탄 조합의 상호보완적 특성이 가져온 결과로 볼 수 있으며, 심부전 치료 전반에서 환자에게 더 나은 임상적 경험을 제공할 수 있다는 점에서 큰 의의를 갖는다.Q. 표준치료 네 가지 약제를 ‘가능한 한 빨리’ 도입해야 한다고 강조되는 이유는 무엇인가?유 교수: HFrEF는 진단 초기의 예후가 특히 나쁜 질환으로, 첫 3개월 동안 예후가 급격히 나빠지는 환자가 많다. 초기 사망률과 재입원 위험이 집중되는 시기이기 때문에, 네 가지 표준치료 약제를 가능한 한 빠르게 도입해야 한다.이 약제들의 효과는 단순히 증상 완화가 아니라 사망률·입원률을 빠르게 낮추는 방향으로 나타나기 때문에, 치료 시기가 늦어지면 해당 이득을 바로 잃게 된다. 특히 HFrEF 환자에서 초기에 약제를 적용할수록 예후 개선이 크다는 여러 연구 결과가 축적되면서 국내외 가이드라인 모두 조기 개입을 강조하고 있다.미하엘 교수: 초기 집중 치료가 중요한 이유는 심부전의 임상적 골든타임이 존재하기 때문이다. HFrEF 환자는 처음 진단된 시점부터 심근 스트레스가 급격히 증가하고 이 과정에서 구조적·기능적 손상이 빠르게 진행된다. 따라서 치료제의 이점이 누적되기 전에 가능한 빨리 네 가지 약제를 투입해야 한다.또 약제를 순차적으로 늦게 도입하는 방식은 환자의 임상적 위험을 그대로 방치하는 결과를 초래할 수 있다. 대규모 환자 자료에서도 신속한 병용도입이 단독·지연 도입보다 생존율을 높이고 입원 위험을 줄이는 것으로 일관되게 제시된다. 이러한 이유로 유럽에서도 가능하면 4제요법 조기 완성을 목표로 치료 전략을 운영하고 있다.Q. 한국은 여전히 4제 요법의 초기 적용률이 낮다. 개선을 위해 필요한 과제는 무엇인가?유 교수: 국내에서 초기 치료 최적화가 잘 이루어지지 않는 이유로, 의료진의 시간적·환경적 제약, 다약제에 대한 환자 우려, 진료현장의 인력 부담 등이 복합적으로 작용하고 있다. 하지만 4제요법의 임상적 이득이 매우 크기 때문에, 이를 공통된 진료경로로 만드는 것이 필요하다.심부전 센터와 전문클리닉의 역할 강화, 초진 단계부터 적용 가능한 통합 치료 알고리즘 마련, 진료현장에서 적극적인 용량 증량(titration)을 도울 수 있는 구조가 중요하다. 환자의 약제 순응도를 높이기 위한 교육, 그리고 지역 의료기관에서도 동일한 기준으로 치료가 이뤄질 수 있도록 정책적 지원이 동반돼야 한다.임상적 관성(clinical inertia) 차원에서 특히 한국의 특별한 상황은 의료진이 외래 환자를 볼 때 너무 짧은 시간이 주어지고 많은 환자를 봐야 한다는 점이다. 그래서 실제로 표준치료나 환자에 대한 개인 맞춤형 치료를 적용하기가 굉장히 어려운 부분이 있다.정리하자면 국내의 표준치료 목표 수준은 많이 올라온 상태이다. 하지만 여전히 심부전 환자를 보는 특별한 전문의를 제외한 많은 분들은 아직 개선의 여지가 있다고 말씀드릴 수 있겠다.미하엘 교수: 독일의 사례에서도 확인되듯, 초기 치료 도입률을 높이기 위해서는 ‘표준화된 진료경로(clinical pathway)’가 핵심이다. 의료진의 경험과 숙련도에 의존하는 방식이 아니라, 누구라도 동일한 기준으로 치료를 설계할 수 있게 만드는 체계가 필요하다.또 약제의 최대 내약용량에 도달하도록 관리하는 과정에서, 임상현장에 시간적 여유·지속적 모니터링 체계가 마련되는 것이 중요하다. 실제로 엔트레스토를 포함한 표준 4제 요법은 용량을 충분히 올렸을 때 최적 효과가 나타나므로, 이를 위한 외래·간호·교육 체계의 확충이 반드시 필요하다.결국 국가 차원의 관리모델이 도입될 때 치료 격차가 좁아지고, 한국에서도 많은 환자가 더 나은 예후를 기대할 수 있을 것이라고 강조했다.2025-11-20 06:07:34손형민 -
 제일약품 '자큐보 비전 선포식'…내년 1700억 목표[데일리팜=이석준 기자] 제일약품은 11월 13일부터 14일까지 원주 오크밸리에서 ‘2025 자큐보 비전 선포식’을 개최했다고 17일 밝혔따.이번 행사에는 영업·마케팅·학술·R&D 등 임직원 약 600여 명이 참석해 회사의 미래 성장 동력에 대한 비전과 로드맵을 함께 논의했다. 특히 하고, 자사의 핵심 전략 품목인 자큐보정의 중장기 목표와 영업·마케팅 방향성을 전사적으로 공유하는 시간을 가졌다.자큐보는 올해 700억 원 매출 달성이 예상되고, 내년에는 1700억 원이라는 공격적인 목표를 제시하며 시장에서 확고한 위치를 차지하기 위한 방향을 명확히 했다.선포식은 자큐보정의 성공적인 출시와 강력한 시장 반응을 바탕으로 향후 시장 확대 전략을 본격적으로 실행하기 위한 조직별 계획 공유에 초점을 맞췄다.행사는 △마케팅 브랜드 캠페인 및 시장 분석 공유 △2025년 영업 실적 리마인드 및 주요 성과 브리핑 △2026년 영업 목표 및 전략 발표 순으로 이어지며 본격적인 비즈니스 세션이 진행됐다.특히 2025년 영업 리마인드 세션에서는 자큐보정 출시 이후 병원 코드 오픈·DC 승인 현황, 채널별 성과 지표 등 실제 데이터를 기반으로 구체적인 결과 브리핑이 이루어졌다. 이를 통해 지난 1년간의 성과를 객관적으로 점검하고, 2026년 시장 확대 전략을 보다 정교하게 수립하는 계기가 마련됐다.또 △의사소통 역량 강화를 위한 명사 특강 △팀빌딩 및 레크레이션이 진행됐다. 명사 특강에서는 프로파일러 권일용 교수가 ‘프로파일러가 보는 마음을 읽는 소통법’을 주제로 상대의 심리를 이해하고 조직 내 협업을 강화하는 실질적인 소통 기법을 강연했다. 임직원이 참여한 팀빌딩 및 레크레이션 프로그램을 통해 부서 간 소통을 강화하고 공통의 목표로 결집하는 조직 문화를 다지는 시간도 마련됐다.제일약품 관계자는 “자큐보는 제일약품 65년 역사 속에서 만들어낸 가장 의미 있는 성과 중 하나이며, 회사의 미래 성장을 이끌 핵심 엔진이다. 부문 간 긴밀한 협업과 현장에서의 실행력이 강화된다면 자큐보는 국내를 넘어 글로벌 블록버스터 신약으로 성장할 것”이라고 말했다.2025-11-17 14:59:07이석준
제일약품 '자큐보 비전 선포식'…내년 1700억 목표[데일리팜=이석준 기자] 제일약품은 11월 13일부터 14일까지 원주 오크밸리에서 ‘2025 자큐보 비전 선포식’을 개최했다고 17일 밝혔따.이번 행사에는 영업·마케팅·학술·R&D 등 임직원 약 600여 명이 참석해 회사의 미래 성장 동력에 대한 비전과 로드맵을 함께 논의했다. 특히 하고, 자사의 핵심 전략 품목인 자큐보정의 중장기 목표와 영업·마케팅 방향성을 전사적으로 공유하는 시간을 가졌다.자큐보는 올해 700억 원 매출 달성이 예상되고, 내년에는 1700억 원이라는 공격적인 목표를 제시하며 시장에서 확고한 위치를 차지하기 위한 방향을 명확히 했다.선포식은 자큐보정의 성공적인 출시와 강력한 시장 반응을 바탕으로 향후 시장 확대 전략을 본격적으로 실행하기 위한 조직별 계획 공유에 초점을 맞췄다.행사는 △마케팅 브랜드 캠페인 및 시장 분석 공유 △2025년 영업 실적 리마인드 및 주요 성과 브리핑 △2026년 영업 목표 및 전략 발표 순으로 이어지며 본격적인 비즈니스 세션이 진행됐다.특히 2025년 영업 리마인드 세션에서는 자큐보정 출시 이후 병원 코드 오픈·DC 승인 현황, 채널별 성과 지표 등 실제 데이터를 기반으로 구체적인 결과 브리핑이 이루어졌다. 이를 통해 지난 1년간의 성과를 객관적으로 점검하고, 2026년 시장 확대 전략을 보다 정교하게 수립하는 계기가 마련됐다.또 △의사소통 역량 강화를 위한 명사 특강 △팀빌딩 및 레크레이션이 진행됐다. 명사 특강에서는 프로파일러 권일용 교수가 ‘프로파일러가 보는 마음을 읽는 소통법’을 주제로 상대의 심리를 이해하고 조직 내 협업을 강화하는 실질적인 소통 기법을 강연했다. 임직원이 참여한 팀빌딩 및 레크레이션 프로그램을 통해 부서 간 소통을 강화하고 공통의 목표로 결집하는 조직 문화를 다지는 시간도 마련됐다.제일약품 관계자는 “자큐보는 제일약품 65년 역사 속에서 만들어낸 가장 의미 있는 성과 중 하나이며, 회사의 미래 성장을 이끌 핵심 엔진이다. 부문 간 긴밀한 협업과 현장에서의 실행력이 강화된다면 자큐보는 국내를 넘어 글로벌 블록버스터 신약으로 성장할 것”이라고 말했다.2025-11-17 14:59:07이석준 -
 약제사후관리 공급 중심 강화...의무위반 패널티 실행[데일리팜=정흥준 기자] 건강보험공단이 내년 의약품 안정적 공급 관리에 방점을 찍고 약가협상과 약제사후관리 제도를 손본다.건보공단과 제약사의 약가 협의 내용과 달리 일방적인 의약품 공급 중단을 결정할 경우, 규정상의 패널티를 적극 실행할 방침이다.올해 국정감사에서 ‘약가-요양급여합의서’에도 불구하고 의약품 공급의무 관리가 되지 않고 있다는 지적에 따른 후속조치다.오세림 약제관리실 협상사후관리부장.11일 공단은 원주 본원에서 ‘약가협상 및 약제 사후관리 제도 설명회’를 열고 업계 관계자들과 내년도 관리 강화 방향성을 공유했다.만약 불가피한 사정으로 합의 내용과 달리 공급을 중단하기 위해서는 환자보호방안을 마련해 공단과 사전 협의해야 한다고 강조했다.오세림 약제관리실 협상사후관리부장은 “내년에는 공급 중심으로 관리를 강화할 예정이다. 허가 취하하고 공급 중단을 하려면 학회에 물어보고, 환자들에게 다른 약으로 대체해도 되는지 확인해 공단과 환자보호방안을 협의해달라”고 당부했다.내년부터 공급의무 위반 업체는 정해진 산식에 따라 패널티 적용을 적극 검토한다. 현재 정해진 산식은 위반기간 1일당 ‘위반 약제의 직전년도 연간 청구액 X 1/n X1/365X50%’에 해당하는 금액이라고 정하고 있다.또 공급의무 이행 확인을 위해 분기 종료 후 40일 이내 공단에 자료제출(월별 생산량, 수입량, 공급요청량과 실제 공급량 등)을 해야 하고, 이를 어길 시 100만원을 지급해야 한다는 문구도 있다.국감에서 해당 조항이 시행되지 않고 있다는 지적을 받았는데, 마찬가지로 내년부터는 적극 적용할 방침이다.오세림 부장은 “합의서 이행이 어려운 경우에는 사전에 공단과 소통해서 협의를 해야 한다. 실제로 일부 업체는 위탁사의 사정에 따라 협의를 사전에 진행해서 패널티 조항을 합의한 경우도 있었다”고 설명했다.이어 “(자료제출)미이행 업체는 100만원씩 지급해야 하지만 작동하지 않았다. 공단도 인지하고 있다. 앞으로는 지켜달라”며 업계 협조를 당부했다.신약 효능효과 추가 보고 없앤다..함량추가도 간소화 검토현재 신약은 공단과 계열 체결 후 해외에서 효능효과가 추가되는 경우 보고 의무가 있는데, 내년 상반기부터는 면제할 계획이다.함량 추가 시 보고 의무도 간소화한다. 대신 국내 도입이 필요할 경우 세부사항을 합의서에 명시할 예정이다.오 부장은 “합의서에는 효능효과 추가 시 보고 의무 내용이 들어있다. 내년 상반기부터 보고 의무 면제를 검토하고 있다”면서 “또 함량 추가 시 보고의무도 간소화를 고민하고 있다. 다만 해외에는 급여 등재돼있는 함량의 국내 도입이 필요한 경우 합의서에 세부사항을 명시하는 방향으로 풀어갈 예정이다. 의견 수렴을 하겠다”고 밝혔다.위험분담계약 의약품의 일부 정보 공개도 검토하고 있다. 환급형 적용 약제 목록을 공개하는 방안을 놓고 의견조회를 진행 중이다.오 부장은 “심평원에 급여결정신청을 하면 환급률에 대한 정보 제공이 가능하도록 할 것이다. 단 비밀유지각서 등을 작성해야 한다”면서 “또 위험분담약제 환급형 적용 약제 목록은 공개하는 방향으로 의견 조회를 진행하고 있다”고 했다. PVA ‘일회성환급’ 내년 제한적 운영...사용범위 확대 협상 가이드 신설문해희 사용량관리부장.공단은 내년 의약품 사용량관리 방안도 개선한다. 코로나로 인해 적용했던 ‘일회성 환급’을 제한적 운영하고, 사용범위 확대 협상에 대한 가이드라인도 신설한다.문해희 약제관리실 사용량관리부장은 “내년부터는 일회성 환급 계약 대상을 제한적으로 운영할 계획이다. 복지부와 논의 중에 있다. 이후 제약협회를 통해 의견을 수렴할 계획”이라고 전했다.문 부장은 “또 사용범위 확대 협상 과정의 명문화된 지침 필요성에 따라 가이드라인을 마련한다. 이번 주에 의견수렴을 진행할 예정이다. 내년에는 이를 고도화할 것”이라고 설명했다.복지부와 이중약가제도 도입 방안에 대해서도 검토하고 있다. 문 부장은 “미국 MFN 정책 추진으로 이중약가제도 도입에 대한 제약사 요청이 있다. 복지부와 제도 개선과 실행방안에 대해 검토중”이라고 밝혔다. 약가협상 상한금액 조정 가이드라인 개정...긴급도입 약은 별도 조정김형민 신약관리부장.약가 협상에서 상한금액을 조정할 때의 가이드라인도 일부 개정한다.예상청구금액 고려사항은 ‘기존 협상 약제의 3~5년간의 청구량 및 증가율’이었는데, ‘협상 약제의 최근 3년에서 5년간 발생한 청구금액’으로 바뀐다.또 희귀필수의약품센터 공급 긴급도입 의약품의 경우 별도의 조정정차를 운영한다는 문구가 생긴다.이외에도 약가조정 이후 3년 신청 제한 조건에서 ‘공공의료적 필요성이 있는 경우’를 명시하고 있는데, 이를 구체화한다.김형민 신약관리부장은 “공공의료 필요성의 정의를 중앙행정기관 등의 협조요청이라고 명시하고, 약평위에 재조정 신청 사실을 공단에 통보하도록 개정한다”면서 “또 의무생산 계약에 미달 시 환급 등 조치 요구가 가능하다는 문구가 들어간다”면서 안정적 공급에 대한 의지가 녹아있다고 부연했다.2025-11-11 21:38:06정흥준
약제사후관리 공급 중심 강화...의무위반 패널티 실행[데일리팜=정흥준 기자] 건강보험공단이 내년 의약품 안정적 공급 관리에 방점을 찍고 약가협상과 약제사후관리 제도를 손본다.건보공단과 제약사의 약가 협의 내용과 달리 일방적인 의약품 공급 중단을 결정할 경우, 규정상의 패널티를 적극 실행할 방침이다.올해 국정감사에서 ‘약가-요양급여합의서’에도 불구하고 의약품 공급의무 관리가 되지 않고 있다는 지적에 따른 후속조치다.오세림 약제관리실 협상사후관리부장.11일 공단은 원주 본원에서 ‘약가협상 및 약제 사후관리 제도 설명회’를 열고 업계 관계자들과 내년도 관리 강화 방향성을 공유했다.만약 불가피한 사정으로 합의 내용과 달리 공급을 중단하기 위해서는 환자보호방안을 마련해 공단과 사전 협의해야 한다고 강조했다.오세림 약제관리실 협상사후관리부장은 “내년에는 공급 중심으로 관리를 강화할 예정이다. 허가 취하하고 공급 중단을 하려면 학회에 물어보고, 환자들에게 다른 약으로 대체해도 되는지 확인해 공단과 환자보호방안을 협의해달라”고 당부했다.내년부터 공급의무 위반 업체는 정해진 산식에 따라 패널티 적용을 적극 검토한다. 현재 정해진 산식은 위반기간 1일당 ‘위반 약제의 직전년도 연간 청구액 X 1/n X1/365X50%’에 해당하는 금액이라고 정하고 있다.또 공급의무 이행 확인을 위해 분기 종료 후 40일 이내 공단에 자료제출(월별 생산량, 수입량, 공급요청량과 실제 공급량 등)을 해야 하고, 이를 어길 시 100만원을 지급해야 한다는 문구도 있다.국감에서 해당 조항이 시행되지 않고 있다는 지적을 받았는데, 마찬가지로 내년부터는 적극 적용할 방침이다.오세림 부장은 “합의서 이행이 어려운 경우에는 사전에 공단과 소통해서 협의를 해야 한다. 실제로 일부 업체는 위탁사의 사정에 따라 협의를 사전에 진행해서 패널티 조항을 합의한 경우도 있었다”고 설명했다.이어 “(자료제출)미이행 업체는 100만원씩 지급해야 하지만 작동하지 않았다. 공단도 인지하고 있다. 앞으로는 지켜달라”며 업계 협조를 당부했다.신약 효능효과 추가 보고 없앤다..함량추가도 간소화 검토현재 신약은 공단과 계열 체결 후 해외에서 효능효과가 추가되는 경우 보고 의무가 있는데, 내년 상반기부터는 면제할 계획이다.함량 추가 시 보고 의무도 간소화한다. 대신 국내 도입이 필요할 경우 세부사항을 합의서에 명시할 예정이다.오 부장은 “합의서에는 효능효과 추가 시 보고 의무 내용이 들어있다. 내년 상반기부터 보고 의무 면제를 검토하고 있다”면서 “또 함량 추가 시 보고의무도 간소화를 고민하고 있다. 다만 해외에는 급여 등재돼있는 함량의 국내 도입이 필요한 경우 합의서에 세부사항을 명시하는 방향으로 풀어갈 예정이다. 의견 수렴을 하겠다”고 밝혔다.위험분담계약 의약품의 일부 정보 공개도 검토하고 있다. 환급형 적용 약제 목록을 공개하는 방안을 놓고 의견조회를 진행 중이다.오 부장은 “심평원에 급여결정신청을 하면 환급률에 대한 정보 제공이 가능하도록 할 것이다. 단 비밀유지각서 등을 작성해야 한다”면서 “또 위험분담약제 환급형 적용 약제 목록은 공개하는 방향으로 의견 조회를 진행하고 있다”고 했다. PVA ‘일회성환급’ 내년 제한적 운영...사용범위 확대 협상 가이드 신설문해희 사용량관리부장.공단은 내년 의약품 사용량관리 방안도 개선한다. 코로나로 인해 적용했던 ‘일회성 환급’을 제한적 운영하고, 사용범위 확대 협상에 대한 가이드라인도 신설한다.문해희 약제관리실 사용량관리부장은 “내년부터는 일회성 환급 계약 대상을 제한적으로 운영할 계획이다. 복지부와 논의 중에 있다. 이후 제약협회를 통해 의견을 수렴할 계획”이라고 전했다.문 부장은 “또 사용범위 확대 협상 과정의 명문화된 지침 필요성에 따라 가이드라인을 마련한다. 이번 주에 의견수렴을 진행할 예정이다. 내년에는 이를 고도화할 것”이라고 설명했다.복지부와 이중약가제도 도입 방안에 대해서도 검토하고 있다. 문 부장은 “미국 MFN 정책 추진으로 이중약가제도 도입에 대한 제약사 요청이 있다. 복지부와 제도 개선과 실행방안에 대해 검토중”이라고 밝혔다. 약가협상 상한금액 조정 가이드라인 개정...긴급도입 약은 별도 조정김형민 신약관리부장.약가 협상에서 상한금액을 조정할 때의 가이드라인도 일부 개정한다.예상청구금액 고려사항은 ‘기존 협상 약제의 3~5년간의 청구량 및 증가율’이었는데, ‘협상 약제의 최근 3년에서 5년간 발생한 청구금액’으로 바뀐다.또 희귀필수의약품센터 공급 긴급도입 의약품의 경우 별도의 조정정차를 운영한다는 문구가 생긴다.이외에도 약가조정 이후 3년 신청 제한 조건에서 ‘공공의료적 필요성이 있는 경우’를 명시하고 있는데, 이를 구체화한다.김형민 신약관리부장은 “공공의료 필요성의 정의를 중앙행정기관 등의 협조요청이라고 명시하고, 약평위에 재조정 신청 사실을 공단에 통보하도록 개정한다”면서 “또 의무생산 계약에 미달 시 환급 등 조치 요구가 가능하다는 문구가 들어간다”면서 안정적 공급에 대한 의지가 녹아있다고 부연했다.2025-11-11 21:38:06정흥준 -
 제도부터 한약까지…강원도약, 올해 2차 연수교육 진행[데일리팜=김지은 기자] 강원특별자치도약사회(회장 이효선)는 9일 원주 시티호텔 기업도시점 사우나동 3층에서 ‘2025년도 강원특별자치도약사회 2차 연수교육’을 진행했다.이번 연수교육은 지난 6월 15일 평창 한화리조트에서 실시한 1차 연수교육에 참석하지 못한 회원 약사를 대상으로 진행된 것이다. 이효선 회장은 교육에 앞서 참석한 회원 약사들과 교육을 준비한 이사진, 사무국 직원들의 노고에 고마움을 전했다.이 회장은 “우리 지부는 회원의 권익 향상과 도민의 건강 증진을 위해 더 노력하겠다”고 말했다.이날 연수교육은 ▲최해륭 덕성여자대학 약학대학 겸임교수 ‘약국 한약(약국 고급 보약용 한약제제와 생약 건기식 완전정복)’ ▲노수진 대한약사회 총무·홍보이사 ‘보건의료제도(동일성분조제에 대한 이해)’ ▲김우림 강원대 약대 교수 ‘복약지도(약사의 다제약물 관리 전략과 실제 적용)’ ▲오성곤 약학 커뮤니케이터 ‘건강기능식품(증상별 영양제 상담 핵심 포인트 및 FAQ )’등으로 이어졌다.2025-11-10 12:59:37김지은
제도부터 한약까지…강원도약, 올해 2차 연수교육 진행[데일리팜=김지은 기자] 강원특별자치도약사회(회장 이효선)는 9일 원주 시티호텔 기업도시점 사우나동 3층에서 ‘2025년도 강원특별자치도약사회 2차 연수교육’을 진행했다.이번 연수교육은 지난 6월 15일 평창 한화리조트에서 실시한 1차 연수교육에 참석하지 못한 회원 약사를 대상으로 진행된 것이다. 이효선 회장은 교육에 앞서 참석한 회원 약사들과 교육을 준비한 이사진, 사무국 직원들의 노고에 고마움을 전했다.이 회장은 “우리 지부는 회원의 권익 향상과 도민의 건강 증진을 위해 더 노력하겠다”고 말했다.이날 연수교육은 ▲최해륭 덕성여자대학 약학대학 겸임교수 ‘약국 한약(약국 고급 보약용 한약제제와 생약 건기식 완전정복)’ ▲노수진 대한약사회 총무·홍보이사 ‘보건의료제도(동일성분조제에 대한 이해)’ ▲김우림 강원대 약대 교수 ‘복약지도(약사의 다제약물 관리 전략과 실제 적용)’ ▲오성곤 약학 커뮤니케이터 ‘건강기능식품(증상별 영양제 상담 핵심 포인트 및 FAQ )’등으로 이어졌다.2025-11-10 12:59:37김지은 -
 건보공단, 사회공헌활동 인정받아 복지부장관 표창[데일리팜=정흥준 기자] 국민건강보험공단(이사장 정기석)은 지난 6일 여의도 한국방송공사(KBS)에서 열린 ‘제14회 대한민국 나눔국민대상’ 시상식에서 보건복지부 장관 표창을 수상했다.‘대한민국 나눔국민대상’은 보건복지부·한국방송공사(KBS)·사회복지공동모금회가 공동 주최하는 사회공헌 분야의 권위 있는 상이다. 인적·물적·생명나눔·희망멘토링 4개 분야에서 나눔문화 확산에 기여한 개인 또는 단체를 선정해 시상하고 있다.공단은 지난 2005년 6월 공공기관 최초 임직원 봉사단 발족 이후, 찾아가는 의료봉사, 빨래봉사, 집수리 봉사 등 다양한 사회공헌 활동으로 나눔문화 확산에 기여한 공로를 인정받았다. ‘인적나눔’ 부문에서 보건복지부 장관 표창을 수상했다.특히 올해는 원주시 대표 문화재인 반계리 은행나무 광장 새단장, 재난 지역(산불, 폭우피해) 지원, 의료폐기물 관리 및 폐의약품 수거 등 사회공헌 뿐만 아니라 지역사회와 환경까지 아우르는 다양한 환경·사회·투명(ESG) 경영 활동을 지속 추진해오고 있다.공단 관계자는 “지속적으로 진행해온 사회공헌 활동을 인정받게 되어 영광이다”라며, “앞으로도 지역사회와 소통하고 어려운 이웃을 배려하여 나눔문화 확산을 위해 노력하겠다”고 밝혔다.2025-11-07 15:38:06정흥준
건보공단, 사회공헌활동 인정받아 복지부장관 표창[데일리팜=정흥준 기자] 국민건강보험공단(이사장 정기석)은 지난 6일 여의도 한국방송공사(KBS)에서 열린 ‘제14회 대한민국 나눔국민대상’ 시상식에서 보건복지부 장관 표창을 수상했다.‘대한민국 나눔국민대상’은 보건복지부·한국방송공사(KBS)·사회복지공동모금회가 공동 주최하는 사회공헌 분야의 권위 있는 상이다. 인적·물적·생명나눔·희망멘토링 4개 분야에서 나눔문화 확산에 기여한 개인 또는 단체를 선정해 시상하고 있다.공단은 지난 2005년 6월 공공기관 최초 임직원 봉사단 발족 이후, 찾아가는 의료봉사, 빨래봉사, 집수리 봉사 등 다양한 사회공헌 활동으로 나눔문화 확산에 기여한 공로를 인정받았다. ‘인적나눔’ 부문에서 보건복지부 장관 표창을 수상했다.특히 올해는 원주시 대표 문화재인 반계리 은행나무 광장 새단장, 재난 지역(산불, 폭우피해) 지원, 의료폐기물 관리 및 폐의약품 수거 등 사회공헌 뿐만 아니라 지역사회와 환경까지 아우르는 다양한 환경·사회·투명(ESG) 경영 활동을 지속 추진해오고 있다.공단 관계자는 “지속적으로 진행해온 사회공헌 활동을 인정받게 되어 영광이다”라며, “앞으로도 지역사회와 소통하고 어려운 이웃을 배려하여 나눔문화 확산을 위해 노력하겠다”고 밝혔다.2025-11-07 15:38:06정흥준 -
 "17년 전통"…경북·전북·강원도약, 원주서 친선교류회[데일리팜=김지은 기자] 경상북도약사회(회장 고영일)·전북특별자지도(회장 전용근), 강원특별자치도약사회(회장 이효선)는 2일 강원도 원주 일원에서 3도 약사회의 상호 교류와 화합의 한마당 자리를 마련해 협력하는 시간을 가졌다고 밝혔다.오전에는 권영희 대한약사회장이 방문해 회원 약사들을 격려하고 최근 약사사회 이슈인 한약사 문제, 돌봄통합 등에 대해 각 지부 협조와 관심을 당부했다. 이후 3개 지부 회원 약사들은 소금산 케이블카를 타고 출렁다리, 스카이워크, 울렁다리를 등반하고, 오후에는 오크밸리 뮤지엄산을 관람하며 화합하는 시간을 가졌다.이날 행사의 저녁만찬을 주관한 이효선 강원도약사회장은 “단풍이 한창인 요즘 강원도를 찾아 주셔서 진심으로 감사드린다”며 “열심히 준비한 만큼 모쪼록 즐거운 시간이셨길 바라고, 앞으로도 3도 약사회의 친선교류가 계속되길 바란다”고 말했다.고영일 경북약사회장은 “강원, 경북, 전북 3도 약사회 친선교류회가 오랫동안 지속돼 너무 감사드린다”며 “인연을 중요시 하는데 특히 강원, 전북은 오랜 교류로 더 의미가 깊다. 좋은 인연 오래 갔으면 한다”고 했다.전용근 전북약사회장도 “올해 3도 약사회 친선교류회를 준비하신 이효선 회장님 노고에 감사하다는 말씀드린다”면서 “즐거운 시간이었고, 내년에도 여기 모인 모든 분들 꼭 뵐 수 있길 바란다”고 말했다.한편 경북, 전북, 강원 3개 지부의 친선교류회는 지난 2008년부터 현재까지 이어지고 있다.2025-11-03 10:41:13김지은
"17년 전통"…경북·전북·강원도약, 원주서 친선교류회[데일리팜=김지은 기자] 경상북도약사회(회장 고영일)·전북특별자지도(회장 전용근), 강원특별자치도약사회(회장 이효선)는 2일 강원도 원주 일원에서 3도 약사회의 상호 교류와 화합의 한마당 자리를 마련해 협력하는 시간을 가졌다고 밝혔다.오전에는 권영희 대한약사회장이 방문해 회원 약사들을 격려하고 최근 약사사회 이슈인 한약사 문제, 돌봄통합 등에 대해 각 지부 협조와 관심을 당부했다. 이후 3개 지부 회원 약사들은 소금산 케이블카를 타고 출렁다리, 스카이워크, 울렁다리를 등반하고, 오후에는 오크밸리 뮤지엄산을 관람하며 화합하는 시간을 가졌다.이날 행사의 저녁만찬을 주관한 이효선 강원도약사회장은 “단풍이 한창인 요즘 강원도를 찾아 주셔서 진심으로 감사드린다”며 “열심히 준비한 만큼 모쪼록 즐거운 시간이셨길 바라고, 앞으로도 3도 약사회의 친선교류가 계속되길 바란다”고 말했다.고영일 경북약사회장은 “강원, 경북, 전북 3도 약사회 친선교류회가 오랫동안 지속돼 너무 감사드린다”며 “인연을 중요시 하는데 특히 강원, 전북은 오랜 교류로 더 의미가 깊다. 좋은 인연 오래 갔으면 한다”고 했다.전용근 전북약사회장도 “올해 3도 약사회 친선교류회를 준비하신 이효선 회장님 노고에 감사하다는 말씀드린다”면서 “즐거운 시간이었고, 내년에도 여기 모인 모든 분들 꼭 뵐 수 있길 바란다”고 말했다.한편 경북, 전북, 강원 3개 지부의 친선교류회는 지난 2008년부터 현재까지 이어지고 있다.2025-11-03 10:41:13김지은 -
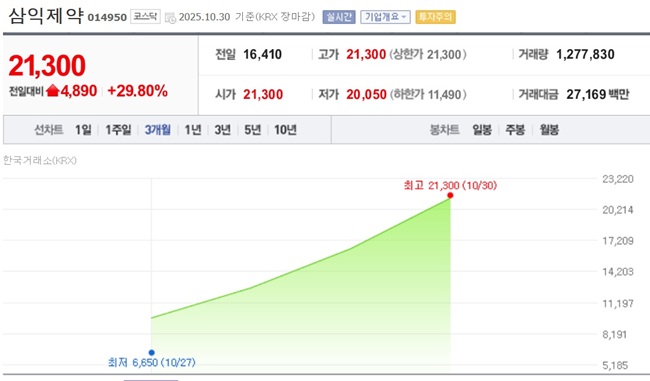 삼익제약, 상한가 행진...오너가 지분 가치 급등[데일리팜=이석준 기자] 삼익제약이 코스닥 데뷔 후 4연상이다. 시가총액은 2000억원까지 치솟았다. 삼익제약은 이충환 외 14인이 63.39%를 보유하고 있다. 주가 급등으로 오너일가 평가액도 1200억원을 돌파했다. 최대주주 이충환 대표 지분 가치도 400억원을 넘어섰다.차별화된 경쟁력이 부각되고 있다는 평가다. 특히 삼익제약 독자적 플랫폼을 적용한 신사업 장기지속형 주사제 개발이 주목받고 있다. 여기에 최대주주측이 보유한 지분율 63% 가량이 사실상 묶인 주식이어서 이른바 품귀 현상이 발생하고 있다는 분석이다.삼익제약은 27일 코스닥 데뷔 후 4거래일 연속 상한가를 기록했다. 삼익제약은 27일 코스닥에 입성했다. 이후 27일, 28일, 29일, 30일 4거래일 연속 상한가를 쳤다. 이에 30일 종가는 2만1300원까지 치솟았다. 시총은 1954억원이다.삼익제약은 최대주주 측근 지분율이 높은 곳이다. 최대주주 이충환 대표(21.81%), 이세영 회장(11.63%), 이용석 부사장(10.16%) 등 15인이 63.39%를 쥐고 있다.주가가 급등하면서 이들의 지분 가치도 치솟았다. 주식 평가액은 이충환 대표 426억원, 이세영 회장 227억원, 이용석 부사장 213억원이 됐다. 이충환 대표와 이용석 부사장은 창업주 이세영 회장의 장차남이다. 이대로 주가 상승세가 이어지면 삼부자의 주식 평가액은 1000억원을 넘게 된다.업계는 최대주주측이 보유한 지분율 63% 가량이 사실상 묶인 주식이어서 이른바 품귀 현상이 발생하고 있다고 분석했다. 실제 이들의 보호예수 기간은 상장 후 2년이다.삼익제약 최대주주 외 14인은 전체의 63.39%를 쥐고 있다.(기타주주 14.56% 제외) 다양한 경쟁력이 부각되면서 주가를 밀어올리고 있다는 분석도 나온다.장기지속형 주사제 개발이 대표적이다. 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에 도전한다.장기지속형 주사제 개발의 경우 자체 상표등록(UniSphero)까지 출원했다. 퍼스트인 클래스가 아닌 베스트인 클래스의 제품을 만들기 위해 중장기 목표로 개발중이다.UniSpheroTM는 미세 입자 멤브레인을 이용한 마이크로스피어 제조 플랫폼이다. 마이크로스피어 입자의 크기와 분포를 정밀하게 제어할 수 있는 삼익제약의 고유 기술이다. 높은 재현성과 균일한 입도 분포도가 특징이다. 장기지속형 주사제 기술 및 장비 관련 특허등록 1건, 특허출헌 2건 등 지속적인 특허 출원 예정이다.생산 능력도 늘리고 있다.인천 제1공장 증축(2026년), 원주 제2공장 착공(2027년) 등이다. 어떤 의약품을 생산하느냐에 따라 다르지만 현 제품군으로 케파를 따져봤을 때 인천 1공장은 600억원 정도다. 이후 증축을 통해 1000억원 수준으로 확대할 계획이다. 원주 2공장까지 합쳐지면 최대 2500억원 생산 능력을 갖추게 된다. 삼익제약은 30일 인천공장 별관 신축을 위해 73억원을 투자하겠다고 공시했다.2025-10-31 06:14:34이석준
삼익제약, 상한가 행진...오너가 지분 가치 급등[데일리팜=이석준 기자] 삼익제약이 코스닥 데뷔 후 4연상이다. 시가총액은 2000억원까지 치솟았다. 삼익제약은 이충환 외 14인이 63.39%를 보유하고 있다. 주가 급등으로 오너일가 평가액도 1200억원을 돌파했다. 최대주주 이충환 대표 지분 가치도 400억원을 넘어섰다.차별화된 경쟁력이 부각되고 있다는 평가다. 특히 삼익제약 독자적 플랫폼을 적용한 신사업 장기지속형 주사제 개발이 주목받고 있다. 여기에 최대주주측이 보유한 지분율 63% 가량이 사실상 묶인 주식이어서 이른바 품귀 현상이 발생하고 있다는 분석이다.삼익제약은 27일 코스닥 데뷔 후 4거래일 연속 상한가를 기록했다. 삼익제약은 27일 코스닥에 입성했다. 이후 27일, 28일, 29일, 30일 4거래일 연속 상한가를 쳤다. 이에 30일 종가는 2만1300원까지 치솟았다. 시총은 1954억원이다.삼익제약은 최대주주 측근 지분율이 높은 곳이다. 최대주주 이충환 대표(21.81%), 이세영 회장(11.63%), 이용석 부사장(10.16%) 등 15인이 63.39%를 쥐고 있다.주가가 급등하면서 이들의 지분 가치도 치솟았다. 주식 평가액은 이충환 대표 426억원, 이세영 회장 227억원, 이용석 부사장 213억원이 됐다. 이충환 대표와 이용석 부사장은 창업주 이세영 회장의 장차남이다. 이대로 주가 상승세가 이어지면 삼부자의 주식 평가액은 1000억원을 넘게 된다.업계는 최대주주측이 보유한 지분율 63% 가량이 사실상 묶인 주식이어서 이른바 품귀 현상이 발생하고 있다고 분석했다. 실제 이들의 보호예수 기간은 상장 후 2년이다.삼익제약 최대주주 외 14인은 전체의 63.39%를 쥐고 있다.(기타주주 14.56% 제외) 다양한 경쟁력이 부각되면서 주가를 밀어올리고 있다는 분석도 나온다.장기지속형 주사제 개발이 대표적이다. 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에 도전한다.장기지속형 주사제 개발의 경우 자체 상표등록(UniSphero)까지 출원했다. 퍼스트인 클래스가 아닌 베스트인 클래스의 제품을 만들기 위해 중장기 목표로 개발중이다.UniSpheroTM는 미세 입자 멤브레인을 이용한 마이크로스피어 제조 플랫폼이다. 마이크로스피어 입자의 크기와 분포를 정밀하게 제어할 수 있는 삼익제약의 고유 기술이다. 높은 재현성과 균일한 입도 분포도가 특징이다. 장기지속형 주사제 기술 및 장비 관련 특허등록 1건, 특허출헌 2건 등 지속적인 특허 출원 예정이다.생산 능력도 늘리고 있다.인천 제1공장 증축(2026년), 원주 제2공장 착공(2027년) 등이다. 어떤 의약품을 생산하느냐에 따라 다르지만 현 제품군으로 케파를 따져봤을 때 인천 1공장은 600억원 정도다. 이후 증축을 통해 1000억원 수준으로 확대할 계획이다. 원주 2공장까지 합쳐지면 최대 2500억원 생산 능력을 갖추게 된다. 삼익제약은 30일 인천공장 별관 신축을 위해 73억원을 투자하겠다고 공시했다.2025-10-31 06:14:34이석준 -
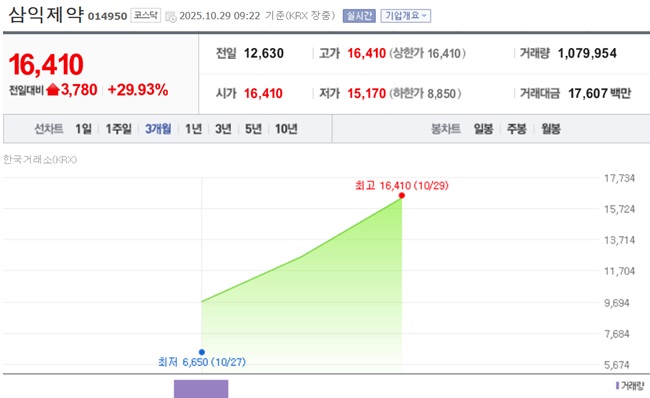 삼익제약 3일 연속 상한가…차별화된 경쟁력 부각[데일리팜=이석준 기자] 삼익제약이 코스닥 입성 후 3거래일 연속 상한가다. 시가총액은 1500억원을 넘어섰다.차별화된 경쟁력이 부각되고 있다는 평가다. 26년 연속 흑자(실적), 세계 최초 당뇨병 치료제 복합제 개발(R&D), CMO 경쟁력(시설) 등이다. '실적-R&D-시설' 3박자다.특히 신사업 장기지속형 주사제 개발이 주목받고 있다. 삼익제약은 독자적 플랫폼을 적용해 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에 도전하고 있다. 플랫폼 기술은 기업 가치(시총) 상승으로 연동되는 경우가 많다. 삼익제약은 29일 오전 9시 14분 기준 전 거래일 대비 29.93% 오른 1만 6410원에 거래 중이다. 이대로 장을 마치면 27일 코스닥 데뷔 후 3거래일 연속 상한가를 기록한다.다양한 경쟁력이 부각되고 있다.먼저 실적이다. 삼익제약의 2029년 매출 목표(연결 기준)는 1114억원이다. 2024년 매출(545억원)의 2배가 넘는 수치다. 상장 5년 후 100% 성장하겠다는 자신감이다.자신감의 원천은 CMO 사업이다. 레드오션이지만 틈새 CMO 시장을 공략한다. 염산메트포르민 대량 생산, 이층정 기술 적용 등 차별화 전략으로 CMO 수주를 늘린다. 이를 통해 외형과 수익성을 동시에 잡는다는 계획이다. 현재 CMO 거래처는 42곳이며 대표적으로 대웅바이오, 동국제약, 한미약품 등이 있다.주력 제품도 성장하고 있다. 대표적으로 '피오시타정'이다. 이 제품은 시타글립틴+피오글리타존 최초 당뇨병 복합제다. 2023년 11월 급여를 받고 시장에 진입하고 있다. 현재 종합병원 10여 군데 랜딩한 상태다. 연내 서울대병원에도 도전하고 있다. 생산 능력도 늘리고 있다.인천 제1공장 증축(2026년), 원주 제2공장 착공(2027년) 등이다. 이를 통해 ▲효율적 생산 및 비용 관리(원가 절감) ▲신규 제형 생산(이층정) ▲생산 케파 및 가동율 확대 ▲경쟁력 있는 특화 제품군 영업에 나선다. 시설 확충은 자체 현금과 상장 조달 자금으로 투입할 계획이다.기존 인천공장은 글로벌 GMP 수준의 생산 및 품질관리 시스템을 갖추고 있다. 제품 164개, CMO 30개(49개 업체) 품목을 다루고 있다. 정제(연 5억7000만정), 경질캡슐제(연 4896만 캡슐), 과립제(연 1176만포), 내용액제(연 1440만포) 등의 다양한 제형의 생산능력을 보유하고 있다.어떤 의약품을 생산하느냐에 따라 다르지만 현 제품군으로 케파를 따져봤을 때 인천 1공장은 600억원 정도다. 이후 증축을 통해 1000억원 수준으로 확대할 계획이다. 원주 2공장까지 합쳐지면 최대 2500억원 생산 능력을 갖추게 된다. 이는 매출 확대로 연결된다.제약사 본질 중 하나인 R&D 역량도 강화한다.장기지속형 주사제 개발이 대표적이다. 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에 도전한다.장기지속형 주사제 개발의 경우 자체 상표등록(UniSphero)까지 출원했다. 퍼스트인 클래스가 아닌 베스트인 클래스의 제품을 만들기 위해 중장기 목표로 개발중이다.UniSpheroTM는 미세 입자 멤브레인을 이용한 마이크로스피어 제조 플랫폼이다. 마이크로스피어 입자의 크기와 분포를 정밀하게 제어할 수 있는 삼익제약의 고유 기술이다. 높은 재현성과 균일한 입도 분포도가 특징이다. 장기지속형 주사제 기술 및 장비 관련 특허등록 1건, 특허출헌 2건 등 지속적인 특허 출원 예정이다.R&D 인적 파이프라인도 확보된 상태다.이충환 대표와 권영이 대표(CTO 겸직)를 필두로 학술개발팀, 중앙연구소, DI팀이 유기적으로 협력하며 신제품 개발, 업무 전문성 및 역량을 강화하고 있다.업계 관계자는 "삼익제약의 차별화된 경쟁력이 부각되면서 시총을 끌어올리고 있다. 특히 장기지속형 주사제는 최근 제약산업 R&D 트렌드인 만큼 큰 경쟁력으로 작용하고 있다"고 분석했다.한편 삼익제약 최대주주는 오너 2세 이충환(21.81%) 대표다. 창업주 이세영 회장은 11.63% 지분을 보유중이다. 이충환 대표 동생 이용석 부사장은 10.90%다. 이용석 부사장은 삼익제약 자회사 팜베이를 맡고 있다.2025-10-29 09:19:20이석준
삼익제약 3일 연속 상한가…차별화된 경쟁력 부각[데일리팜=이석준 기자] 삼익제약이 코스닥 입성 후 3거래일 연속 상한가다. 시가총액은 1500억원을 넘어섰다.차별화된 경쟁력이 부각되고 있다는 평가다. 26년 연속 흑자(실적), 세계 최초 당뇨병 치료제 복합제 개발(R&D), CMO 경쟁력(시설) 등이다. '실적-R&D-시설' 3박자다.특히 신사업 장기지속형 주사제 개발이 주목받고 있다. 삼익제약은 독자적 플랫폼을 적용해 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에 도전하고 있다. 플랫폼 기술은 기업 가치(시총) 상승으로 연동되는 경우가 많다. 삼익제약은 29일 오전 9시 14분 기준 전 거래일 대비 29.93% 오른 1만 6410원에 거래 중이다. 이대로 장을 마치면 27일 코스닥 데뷔 후 3거래일 연속 상한가를 기록한다.다양한 경쟁력이 부각되고 있다.먼저 실적이다. 삼익제약의 2029년 매출 목표(연결 기준)는 1114억원이다. 2024년 매출(545억원)의 2배가 넘는 수치다. 상장 5년 후 100% 성장하겠다는 자신감이다.자신감의 원천은 CMO 사업이다. 레드오션이지만 틈새 CMO 시장을 공략한다. 염산메트포르민 대량 생산, 이층정 기술 적용 등 차별화 전략으로 CMO 수주를 늘린다. 이를 통해 외형과 수익성을 동시에 잡는다는 계획이다. 현재 CMO 거래처는 42곳이며 대표적으로 대웅바이오, 동국제약, 한미약품 등이 있다.주력 제품도 성장하고 있다. 대표적으로 '피오시타정'이다. 이 제품은 시타글립틴+피오글리타존 최초 당뇨병 복합제다. 2023년 11월 급여를 받고 시장에 진입하고 있다. 현재 종합병원 10여 군데 랜딩한 상태다. 연내 서울대병원에도 도전하고 있다. 생산 능력도 늘리고 있다.인천 제1공장 증축(2026년), 원주 제2공장 착공(2027년) 등이다. 이를 통해 ▲효율적 생산 및 비용 관리(원가 절감) ▲신규 제형 생산(이층정) ▲생산 케파 및 가동율 확대 ▲경쟁력 있는 특화 제품군 영업에 나선다. 시설 확충은 자체 현금과 상장 조달 자금으로 투입할 계획이다.기존 인천공장은 글로벌 GMP 수준의 생산 및 품질관리 시스템을 갖추고 있다. 제품 164개, CMO 30개(49개 업체) 품목을 다루고 있다. 정제(연 5억7000만정), 경질캡슐제(연 4896만 캡슐), 과립제(연 1176만포), 내용액제(연 1440만포) 등의 다양한 제형의 생산능력을 보유하고 있다.어떤 의약품을 생산하느냐에 따라 다르지만 현 제품군으로 케파를 따져봤을 때 인천 1공장은 600억원 정도다. 이후 증축을 통해 1000억원 수준으로 확대할 계획이다. 원주 2공장까지 합쳐지면 최대 2500억원 생산 능력을 갖추게 된다. 이는 매출 확대로 연결된다.제약사 본질 중 하나인 R&D 역량도 강화한다.장기지속형 주사제 개발이 대표적이다. 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에 도전한다.장기지속형 주사제 개발의 경우 자체 상표등록(UniSphero)까지 출원했다. 퍼스트인 클래스가 아닌 베스트인 클래스의 제품을 만들기 위해 중장기 목표로 개발중이다.UniSpheroTM는 미세 입자 멤브레인을 이용한 마이크로스피어 제조 플랫폼이다. 마이크로스피어 입자의 크기와 분포를 정밀하게 제어할 수 있는 삼익제약의 고유 기술이다. 높은 재현성과 균일한 입도 분포도가 특징이다. 장기지속형 주사제 기술 및 장비 관련 특허등록 1건, 특허출헌 2건 등 지속적인 특허 출원 예정이다.R&D 인적 파이프라인도 확보된 상태다.이충환 대표와 권영이 대표(CTO 겸직)를 필두로 학술개발팀, 중앙연구소, DI팀이 유기적으로 협력하며 신제품 개발, 업무 전문성 및 역량을 강화하고 있다.업계 관계자는 "삼익제약의 차별화된 경쟁력이 부각되면서 시총을 끌어올리고 있다. 특히 장기지속형 주사제는 최근 제약산업 R&D 트렌드인 만큼 큰 경쟁력으로 작용하고 있다"고 분석했다.한편 삼익제약 최대주주는 오너 2세 이충환(21.81%) 대표다. 창업주 이세영 회장은 11.63% 지분을 보유중이다. 이충환 대표 동생 이용석 부사장은 10.90%다. 이용석 부사장은 삼익제약 자회사 팜베이를 맡고 있다.2025-10-29 09:19:20이석준 -
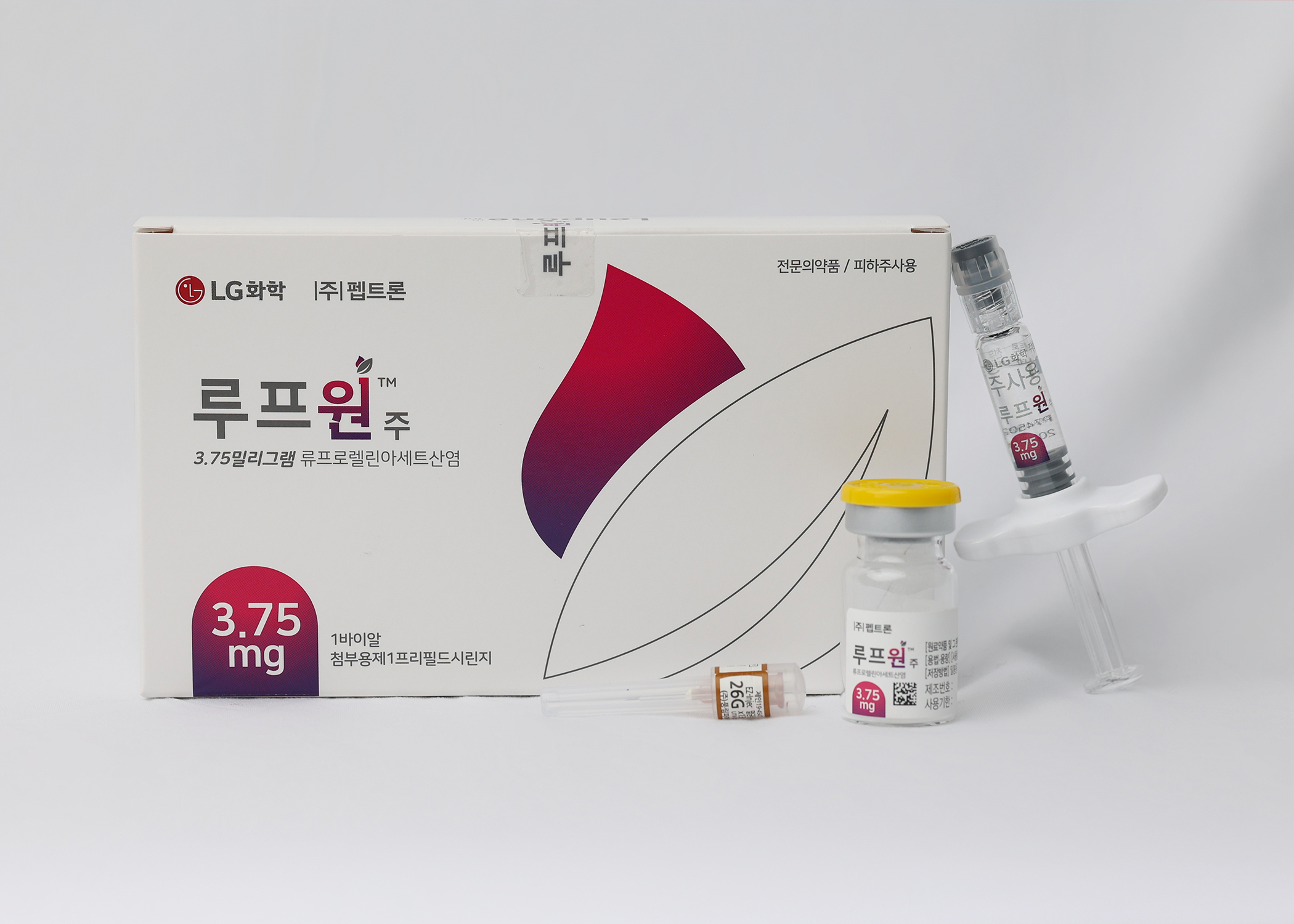 LG화학, 성조숙증 치료제 '루프원' 출시LG화학의 성조숙증 치료제 '루프원' (자료: LG화학) [데일리팜=차지현 기자] LG화학이 소아 친화형 성조숙증 치료제를 새롭게 선보인다.LG화학은 중추성 사춘기 조발증(이하 성조숙증) 치료제 '루프원주'(성분명 류프로렐린) 국내 판매를 본격화한다고 24일 밝혔다.루프원은 생식샘 자극 방출 호르몬(GnRH) 유사체로, 뇌하수체의 GnRH 수용체에 작용해 성호르몬 분비 억제 효과를 내며 이를 통해 사춘기를 지연시키는 역할을 한다.LG화학은 2023년 성조숙증 아이들이 안심하고 사용할 수 있는 치료제를 안정적으로 제공하기 위해 펩타이드 기반 의약품 개발 및 제조 기업 펩트론과 루프원 국내 판매 계약을 체결했다.이 계약에 따라 루프원 개발사인 펩트론이 약효지속형 주사제 전용 시설인 오송공장에서 제품을 생산하고, LG화학이 국내 마케팅, 영업 등 유통 전반을 담당한다.LG화학은 아이들과 보호자 관점에서의 루프원 주요 이점으로 ▲소아 친화적인 투약 환경 구현, ▲예측 가능한 치료 효과 및 안전성을 꼽았다.루프원에는 펩트론 고유의 스마트 데포(Smart Depot) 기술을 기반으로 약물 입자 크기 미세화 공정이 적용됐고, 이를 통해 기존 제품들보다 얇은 주사 바늘이 채택됐다. LG화학은 장기간 반복적인 주사 치료를 경험할 아이들의 심리적 안정감에 기여하고, 이를 바탕으로 투약 순응도가 높아질 것이라는 기대다.김성호 LG화학 스페셜티-케어 사업부장은 "LG화학은 90년대 성장호르몬 최초 국산화를 통해 저신장증 아이들의 치료 환경을 획기적으로 변화시킨 경험이 있다"며 "성조숙증 아이들 및 보호자, 의료진의 목소리에 귀 기울이고, 이에 대한 솔루션을 사업에 적재적소 반영해 실질적인 고객가치를 실현해 나가겠다"고 말했다.성조숙증은 시상하부-뇌하수체-생식샘 축의 조기 성숙으로 인해 여아에서 만 8세 이전, 남아에서 만 9세 이전에 이차 성징이 나타나는 질환이다. 건강보험심사평가원 통계에 따르면 성조숙증 환자 수는 2019년 약 10만명에서 2024년 약 17만명으로 매해 10% 이상 증가했다.성조숙증 치료제는 성조숙증의 진행으로 사춘기가 빨라져서 유전적 목표보다 훨씬 작은 성인 키가 예상될 때 예측 키만큼 자라도록 도와주는 치료제다. 전문 의료진의 판단에 따라 치료 여부를 결정해야 한다.2025-10-24 14:23:36차지현
LG화학, 성조숙증 치료제 '루프원' 출시LG화학의 성조숙증 치료제 '루프원' (자료: LG화학) [데일리팜=차지현 기자] LG화학이 소아 친화형 성조숙증 치료제를 새롭게 선보인다.LG화학은 중추성 사춘기 조발증(이하 성조숙증) 치료제 '루프원주'(성분명 류프로렐린) 국내 판매를 본격화한다고 24일 밝혔다.루프원은 생식샘 자극 방출 호르몬(GnRH) 유사체로, 뇌하수체의 GnRH 수용체에 작용해 성호르몬 분비 억제 효과를 내며 이를 통해 사춘기를 지연시키는 역할을 한다.LG화학은 2023년 성조숙증 아이들이 안심하고 사용할 수 있는 치료제를 안정적으로 제공하기 위해 펩타이드 기반 의약품 개발 및 제조 기업 펩트론과 루프원 국내 판매 계약을 체결했다.이 계약에 따라 루프원 개발사인 펩트론이 약효지속형 주사제 전용 시설인 오송공장에서 제품을 생산하고, LG화학이 국내 마케팅, 영업 등 유통 전반을 담당한다.LG화학은 아이들과 보호자 관점에서의 루프원 주요 이점으로 ▲소아 친화적인 투약 환경 구현, ▲예측 가능한 치료 효과 및 안전성을 꼽았다.루프원에는 펩트론 고유의 스마트 데포(Smart Depot) 기술을 기반으로 약물 입자 크기 미세화 공정이 적용됐고, 이를 통해 기존 제품들보다 얇은 주사 바늘이 채택됐다. LG화학은 장기간 반복적인 주사 치료를 경험할 아이들의 심리적 안정감에 기여하고, 이를 바탕으로 투약 순응도가 높아질 것이라는 기대다.김성호 LG화학 스페셜티-케어 사업부장은 "LG화학은 90년대 성장호르몬 최초 국산화를 통해 저신장증 아이들의 치료 환경을 획기적으로 변화시킨 경험이 있다"며 "성조숙증 아이들 및 보호자, 의료진의 목소리에 귀 기울이고, 이에 대한 솔루션을 사업에 적재적소 반영해 실질적인 고객가치를 실현해 나가겠다"고 말했다.성조숙증은 시상하부-뇌하수체-생식샘 축의 조기 성숙으로 인해 여아에서 만 8세 이전, 남아에서 만 9세 이전에 이차 성징이 나타나는 질환이다. 건강보험심사평가원 통계에 따르면 성조숙증 환자 수는 2019년 약 10만명에서 2024년 약 17만명으로 매해 10% 이상 증가했다.성조숙증 치료제는 성조숙증의 진행으로 사춘기가 빨라져서 유전적 목표보다 훨씬 작은 성인 키가 예상될 때 예측 키만큼 자라도록 도와주는 치료제다. 전문 의료진의 판단에 따라 치료 여부를 결정해야 한다.2025-10-24 14:23:36차지현 -
 "5년 후 100% 성장" 삼익제약의 CMO 사업 자신감[데일리팜=이석준 기자] 삼익제약의 2029년 매출 목표(연결 기준)는 1114억원이다. 2024년 매출(545억원)의 2배가 넘는 수치다. 상장 5년 후 100% 성장하겠다는 자신감이다. 삼익제약은 10월 27일 코스닥에 입성한다.자신감의 원천은 CMO 사업이다. 레드오션이지만 틈새 CMO 시장을 공략한다. 염산메트포르민 대량 생산, 이층정 기술 적용 등으로 CMO 수주를 늘린다. 이를 통해 외형과 수익성을 동시에 잡는다.CMO 시설 능력(CAPA)은 현재 600억원 정도다. 향후 최대 2500억원까지 늘릴 계획이다. 시설 확충에는 퍼스트제네릭과 복합제 신약으로 벌어들인 자체 현금과 상장 자금을 적극 활용한다.제약사 본질 중 하나인 R&D 역량도 강화한다. 장기지속형 주사제 개발이 대표적이다. 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에 도전한다. 독자적 플랫폼 기술(특허 출원)을 적용해 기존 제품과 차별화를 둔다. 플랫폼 기술은 향후 기업 가치(시가총액) 상승으로 연동될 가능성이 높다.R&D 인적 파이프라인도 확보된 상태다. 이충환 대표와 권영이 대표(CTO 겸직)를 필두로 학술개발팀, 중앙연구소, DI팀이 유기적으로 협력하며 신제품 개발, 업무 전문성 및 역량을 강화하고 있다.데일리팜은 2세 이충환 삼익제약 대표를 만나 향후 경영 전략 및 비전을 들어봤다. 아래는 일문일답.상장 배경은스팩 상장을 택했다. 밸류 문제라기 보다는 '돌다리도 두드려보고 건너자'는 경영 기조가 반영됐다. CMO 시설 등에 투자금이 필요한 상황에서 어떻게 하면 안정적이게 자금을 조달할 수 있을까 생각했다. 여기서 빚을 내지 않는 상장을 택하게 됐다. 상장을 통해 삼익제약에서 기존에 볼 수 없었던 과감한 선제 투자를 할 계획이다.회사만의 경쟁력은주력 품목 양대 축으로 퍼스트 제네릭과 복합제 신약이 있다. 대표적으로 '피오시타정'은 시타글립틴+피오글리타존 최초 당뇨병 복합제다. 2023년 11월 급여를 받고 시장에 진입하고 있다. 현재 종합병원 10여 군데 랜딩한 상태다. 연내 서울대병원에도 도전하고 있다.레드오션인 CMO 시장에서는 틈새 전략을 펼치고 있다. 예를 들어 염산메트포르민은 당뇨병 치료제의 가장 기본적인 성분으로 오랜 기간 안전성과 유효성이 확보됐다. 다만 원가 측면에서 수익성이 나쁘다보니 외주 수요가 발생하고 있다. 삼익제약은 이를 기회로 보고 타 제약사들의 염산메트포르민 수요를 끌어 모았다. 단일 성분으로 생산량을 늘리고 공정 개선 및 원부자재 가격을 낮춰 CMO 경쟁력을 확보했다.삼익제약의 복합제 제형 기술 중 하나인 ‘이층정’ 기술도 경쟁력이 있다. 이를 통한 CMO 수주를 늘리는 노력도 진행중이다. 현재 이층정 제형 기술을 내세워 CMO를 진행하고자하는 플레이어는 없는 것으로 안다. 복합제는 각 성분을 별개의 레이어로 구분하는 다층정 기술이 필수적이다. 이를 통해 용출패턴, 각 성분간 간섭을 조절할 수 있다.시설 투자 계획은CMO 사업 확대로 시설도 확충하고 있다.인천 제1공장 증축(2026년), 원주 제2공장 착공(2027년) 등이다. 이를 통해 ▲효율적 생산 및 비용 관리(원가 절감) ▲신규 제형 생산(이층정) ▲생산 케파 및 가동율 확대 ▲경쟁력 있는 특화 제품군 영업에 나선다. 시설 확충은 자체 현금과 상장 조달 자금으로 투입할 계획이다.기존 인천공장은 글로벌 GMP 수준의 생산 및 품질관리 시스템을 갖추고 있다. 제품 164개, CMO 30개(49개 업체) 품목을 다루고 있다. 정제(연 5억7000만정), 경질캡슐제(연 4896만 캡슐), 과립제(연 1176만포), 내용액제(연 1440만포) 등의 다양한 제형의 생산능력을 보유하고 있다.어떤 의약품을 생산하느냐에 따라 다르지만 현 제품군으로 케파를 따져봤을 때 인천 1공장은 600억원 정도다. 이후 증축을 통해 1000억원 수준으로 확대할 계획이다. 원주 2공장까지 합쳐지면 최대 2500억원 생산 능력을 갖추게 된다. 이는 매출 확대로 연결된다. 타 제약사 공장 인수는 현재까지는 생각하고 있지 않다.장기지속형 주사제 개발도 주목받고 있다장기지속형 주사제 개발의 경우 자체 상표등록(UniSphero)까지 출원했다. 퍼스트인 클래스가 아닌 베스트인 클래스의 제품을 만들기 위해 중장기 목표로 개발중이다.UniSpheroTM는 미세 입자 멤브레인을 이용한 마이크로스피어 제조 플랫폼이다. 마이크로스피어 입자의 크기와 분포를 정밀하게 제어할 수 있는 삼익제약의 고유 기술이다. 높은 재현성과 균일한 입도 분포도가 특징이다. 장기지속형 주사제 기술 및 장비 관련 특허등록 1건, 특허출헌 2건 등 지속적인 특허 출원 예정이다.해당 플랫폼 기술을 통해 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 다양한 파프라인을 구축하고 있다. 회사는 임상 단계에 따라 해외 제약사와 라이선스 아웃 기회도 노리고 있다.R&D 인력도 경쟁력 중 하나다삼익제약 CTO 역할 담당하고 있는 권영이 대표이사가 공장의 생산과 품질경영 부분을 관장하고 R&D 총괄도 담당하고 있다. CTO 아래 조직도상으로 중앙연구소, 학술개발팀, DI(Data Integrity)팀이 구성돼 있다. 현재 기준 구성인원은 총 16명(CTO포함)이며 추가적으로 연구인력 충원은 지속하고 있다.R&D 또는 CMO 파트너는R&D 부문은 일부 약학 대학교 연구소와 협업하는 사례가 있지만 외부적으로 공개할 수준까지는 아니다. 현재 CMO 거래처는 42곳이며 대표적으로 대웅바이오, 동국제약, 한미약품 등이 있다.향후 실적 및 주주 가치 제고 계획은회사는 큰 틀에서 매출과 영업이익을 늘리며 우상향 지속 성장에 방점을 두며 경영을 할 생각이다. 세부적으로는 지금까지 견지해 온 영업이익 대비 배당률을 그 이상으로 유지할 생각이다. 투자자들과 원활한 소통을 위해 커뮤니케이션 채널 다양화도 진행할 계획이다. 자회사 팜베이를 통해 경영 다각화 노력(의약품 물류유통, 온오프라인 광고대행, 정수기 유통판매)도 하고 있다. 팜베이는 이용석 부사장(2세)이 담당한다.2025-09-30 06:15:47이석준
"5년 후 100% 성장" 삼익제약의 CMO 사업 자신감[데일리팜=이석준 기자] 삼익제약의 2029년 매출 목표(연결 기준)는 1114억원이다. 2024년 매출(545억원)의 2배가 넘는 수치다. 상장 5년 후 100% 성장하겠다는 자신감이다. 삼익제약은 10월 27일 코스닥에 입성한다.자신감의 원천은 CMO 사업이다. 레드오션이지만 틈새 CMO 시장을 공략한다. 염산메트포르민 대량 생산, 이층정 기술 적용 등으로 CMO 수주를 늘린다. 이를 통해 외형과 수익성을 동시에 잡는다.CMO 시설 능력(CAPA)은 현재 600억원 정도다. 향후 최대 2500억원까지 늘릴 계획이다. 시설 확충에는 퍼스트제네릭과 복합제 신약으로 벌어들인 자체 현금과 상장 자금을 적극 활용한다.제약사 본질 중 하나인 R&D 역량도 강화한다. 장기지속형 주사제 개발이 대표적이다. 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에 도전한다. 독자적 플랫폼 기술(특허 출원)을 적용해 기존 제품과 차별화를 둔다. 플랫폼 기술은 향후 기업 가치(시가총액) 상승으로 연동될 가능성이 높다.R&D 인적 파이프라인도 확보된 상태다. 이충환 대표와 권영이 대표(CTO 겸직)를 필두로 학술개발팀, 중앙연구소, DI팀이 유기적으로 협력하며 신제품 개발, 업무 전문성 및 역량을 강화하고 있다.데일리팜은 2세 이충환 삼익제약 대표를 만나 향후 경영 전략 및 비전을 들어봤다. 아래는 일문일답.상장 배경은스팩 상장을 택했다. 밸류 문제라기 보다는 '돌다리도 두드려보고 건너자'는 경영 기조가 반영됐다. CMO 시설 등에 투자금이 필요한 상황에서 어떻게 하면 안정적이게 자금을 조달할 수 있을까 생각했다. 여기서 빚을 내지 않는 상장을 택하게 됐다. 상장을 통해 삼익제약에서 기존에 볼 수 없었던 과감한 선제 투자를 할 계획이다.회사만의 경쟁력은주력 품목 양대 축으로 퍼스트 제네릭과 복합제 신약이 있다. 대표적으로 '피오시타정'은 시타글립틴+피오글리타존 최초 당뇨병 복합제다. 2023년 11월 급여를 받고 시장에 진입하고 있다. 현재 종합병원 10여 군데 랜딩한 상태다. 연내 서울대병원에도 도전하고 있다.레드오션인 CMO 시장에서는 틈새 전략을 펼치고 있다. 예를 들어 염산메트포르민은 당뇨병 치료제의 가장 기본적인 성분으로 오랜 기간 안전성과 유효성이 확보됐다. 다만 원가 측면에서 수익성이 나쁘다보니 외주 수요가 발생하고 있다. 삼익제약은 이를 기회로 보고 타 제약사들의 염산메트포르민 수요를 끌어 모았다. 단일 성분으로 생산량을 늘리고 공정 개선 및 원부자재 가격을 낮춰 CMO 경쟁력을 확보했다.삼익제약의 복합제 제형 기술 중 하나인 ‘이층정’ 기술도 경쟁력이 있다. 이를 통한 CMO 수주를 늘리는 노력도 진행중이다. 현재 이층정 제형 기술을 내세워 CMO를 진행하고자하는 플레이어는 없는 것으로 안다. 복합제는 각 성분을 별개의 레이어로 구분하는 다층정 기술이 필수적이다. 이를 통해 용출패턴, 각 성분간 간섭을 조절할 수 있다.시설 투자 계획은CMO 사업 확대로 시설도 확충하고 있다.인천 제1공장 증축(2026년), 원주 제2공장 착공(2027년) 등이다. 이를 통해 ▲효율적 생산 및 비용 관리(원가 절감) ▲신규 제형 생산(이층정) ▲생산 케파 및 가동율 확대 ▲경쟁력 있는 특화 제품군 영업에 나선다. 시설 확충은 자체 현금과 상장 조달 자금으로 투입할 계획이다.기존 인천공장은 글로벌 GMP 수준의 생산 및 품질관리 시스템을 갖추고 있다. 제품 164개, CMO 30개(49개 업체) 품목을 다루고 있다. 정제(연 5억7000만정), 경질캡슐제(연 4896만 캡슐), 과립제(연 1176만포), 내용액제(연 1440만포) 등의 다양한 제형의 생산능력을 보유하고 있다.어떤 의약품을 생산하느냐에 따라 다르지만 현 제품군으로 케파를 따져봤을 때 인천 1공장은 600억원 정도다. 이후 증축을 통해 1000억원 수준으로 확대할 계획이다. 원주 2공장까지 합쳐지면 최대 2500억원 생산 능력을 갖추게 된다. 이는 매출 확대로 연결된다. 타 제약사 공장 인수는 현재까지는 생각하고 있지 않다.장기지속형 주사제 개발도 주목받고 있다장기지속형 주사제 개발의 경우 자체 상표등록(UniSphero)까지 출원했다. 퍼스트인 클래스가 아닌 베스트인 클래스의 제품을 만들기 위해 중장기 목표로 개발중이다.UniSpheroTM는 미세 입자 멤브레인을 이용한 마이크로스피어 제조 플랫폼이다. 마이크로스피어 입자의 크기와 분포를 정밀하게 제어할 수 있는 삼익제약의 고유 기술이다. 높은 재현성과 균일한 입도 분포도가 특징이다. 장기지속형 주사제 기술 및 장비 관련 특허등록 1건, 특허출헌 2건 등 지속적인 특허 출원 예정이다.해당 플랫폼 기술을 통해 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 다양한 파프라인을 구축하고 있다. 회사는 임상 단계에 따라 해외 제약사와 라이선스 아웃 기회도 노리고 있다.R&D 인력도 경쟁력 중 하나다삼익제약 CTO 역할 담당하고 있는 권영이 대표이사가 공장의 생산과 품질경영 부분을 관장하고 R&D 총괄도 담당하고 있다. CTO 아래 조직도상으로 중앙연구소, 학술개발팀, DI(Data Integrity)팀이 구성돼 있다. 현재 기준 구성인원은 총 16명(CTO포함)이며 추가적으로 연구인력 충원은 지속하고 있다.R&D 또는 CMO 파트너는R&D 부문은 일부 약학 대학교 연구소와 협업하는 사례가 있지만 외부적으로 공개할 수준까지는 아니다. 현재 CMO 거래처는 42곳이며 대표적으로 대웅바이오, 동국제약, 한미약품 등이 있다.향후 실적 및 주주 가치 제고 계획은회사는 큰 틀에서 매출과 영업이익을 늘리며 우상향 지속 성장에 방점을 두며 경영을 할 생각이다. 세부적으로는 지금까지 견지해 온 영업이익 대비 배당률을 그 이상으로 유지할 생각이다. 투자자들과 원활한 소통을 위해 커뮤니케이션 채널 다양화도 진행할 계획이다. 자회사 팜베이를 통해 경영 다각화 노력(의약품 물류유통, 온오프라인 광고대행, 정수기 유통판매)도 하고 있다. 팜베이는 이용석 부사장(2세)이 담당한다.2025-09-30 06:15:47이석준 -
 한미약품 "아모프렐 심혈관질환 연구 성과 공개"한미약품이 유럽심장학회(ESC)에서 고혈압과 이상지질혈증 동반 치료 복합제 임상 결과와 한국인 초고위험군 대상 심혈관질환 관리 지표를 발표했다. (자료: 한미약품) [데일리팜=차지현 기자] 한미약품이 유럽심장학회(ESC)에서 고혈압과 이상지질혈증 동반 치료 복합제 임상 결과와 한국인 초고위험군 대상 심혈관질환 관리 지표를 발표했다고 25일 밝혔다.ESC는 유럽심장학회가 주관하는 세계 최대 규모의 심혈관 분야 학술대회다. 올해 ESC는 지난 29일부터 9월 1일까지 스페인 마드리드에서 열렸다. 한미약품은 '아모프렐'과 '아모잘탄엑스큐'의 임상연구 결과와 한국인 초고위험군 잔여 콜레스테롤 연구 성과를 공유했다.한미약품에 따르면 올해 학회에는 동국대학교 의과대학 심장내과 이무용 교수, 양산부산대병원 순환기내과 천민구 교수, 원주세브란스기독병원 심장내과 이중희 교수가 참여해 ▲세계 최초 1/3 용량 3제 항고혈압제 아모프렐의 임상 3상 연구 결과 ▲고혈압·이상지질혈증 4제 복합제 아모잘탄엑스큐의 임상 4상 연구 결과 ▲국내 대규모 환자 데이터를 기반으로 한 잔여 콜레스테롤 임상 기준점 제시 연구 등 주요 심혈관질환 관련 연구 성과를 발표했다.아모프렐, 초기 고혈압 치료 패러다임 전환 가능성 제시첫 발표는 ESC 공식 포스터 세션에서 아모프렐 임상 책임 연구자인 동국대학교 의과대학 심장내과 이무용 교수가 맡았다. 이 교수는 한미약품이 지난 8월 출시한 저용량 3제 항고혈압제 아모프렐의 임상연구 결과를 통해 초기 고혈압 치료 패러다임 전환 가능성 제시했다.ESC에서 공개된 HM-APOLLO-301(이하 301 연구)과 HM-APOLLO-302(이하 302 연구) 연구는 국내 본태성 고혈압 환자를 대상으로 아모프렐(암로디핀 1.67mg+로사르탄 16.67mg+클로르탈리돈 4.17mg)과 표준 단일제(암로디핀 5mg 또는 로사르탄 50mg)의 8주간 혈압 강하 효과를 비교한 임상 3상 연구다.연구 결과 아모프렐은 수축기 및 이완기 혈압 강하 측면에서 단일제 대비 비열등성 또는 우월성을 입증했다. 목표 혈압 도달률도 유의하게 높았다. 또한 중대한 약물 이상반응은 보고되지 않아 우수한 내약성도 확인됐다.이무용 교수는 "이번 연구 결과는 최근 국내외에서 주목하고 있는 저용량 항고혈압 복합제의 유효성과 안전성을 다시 한번 확인한 의미 있는 결과"라며 "연구 결과를 바탕으로 출시된 아모프렐정은 세계 최초의 1/3 용량 3제 항고혈압제로 고혈압 환자의 초기 치료에서 보다 효과적으로 혈압을 조절하며 우리나라 고혈압 환자의 지속 치료율과 혈압 조절률 개선에 큰 역할을 할 것으로 기대된다"고 했다.아모잘탄엑스큐, 복약순응도 낮은 환자 치료 옵션 입증양산부산대병원 순환기내과 천민구 교수는 아모잘탄엑스큐의 임상 4상 연구 결과 발표를 통해 복약순응도가 낮은 죽상경화성 심혈관질환(ASCVD) 환자에서 혈압과 지질 조절을 동시에 개선함으로써 치료 편의성과 환자 만족도까지 높이는 치료 옵션임을 발표했다.이번 연구는 AMOREMIO이라는 명칭으로 진행된 국내 다기관 관찰연구다. 복약순응도가 낮은 ASCVD 환자를 대상으로 4제 고정용량복합제 아모잘탄엑스큐(암로디핀+로사르탄+로수바스타틴+에제티미브)의 효과를 평가했다.연구 결과 아모잘탄엑스큐로 전환한 환자들의 혈압과 지질 수치가 모두 유의한 차이로 개선됐으며, 치료 만족도 또한 크게 향상됐다. 또 치료 만족도 조사에서 최고 만족도(5점)를 선택한 환자 비율은 기존 치료 1.82%에서 전환 후 41.94%로 크게 증가했다. 이로써 복약 편의성과 환자 수용성 측면에서도 긍정적인 결과를 보여주며 환자 중심 복합제로서의 가치를 입증했다는 게 회사 측 설명이다.천 교수는 "이번 연구는 복약순응도가 낮은 고위험 심혈관질환 환자에서 아모잘탄엑스큐가 치료 효과뿐 아니라 복약편의성과 만족도까지 동시에 개선할 수 있음을 보여준 의미 있는 결과"라며 "복잡한 약물요법으로 인한 복약순응도 저하 문제를 해결할 수 있는 현실적 대안으로서 아모잘탄엑스큐의 임상적 가치를 입증했다"고 했다.한미-연세원주의대, 한국인 초고위험군 잔여 콜레스테롤 기준 인사이트 제시한미약품은 이번 학회에서 원주세브란스기독병원 심장내과 이중희 교수팀과 공동 연구를 통해 밝힌 최신 연구결과도 함께 발표했다.이번 연구는 국민건강보험공단 데이터베이스를 기반으로 2011년부터 2020년까지 관상동맥 중재술(PCI) 또는 우회술(CABG)을 받은 국내 관상동맥(CAD) 환자 52만 5646명을 대상으로 진행됐다.연구팀은 잔여 콜레스테롤(RC) 수치가 높을수록 복합 심뇌혈관 사건 발생 위험이 선형적으로 증가하는 경향을 확인했다. 특히 18mg/dL 이상일 경우 18mg/dL 미만일 때에 비해 복합 심혈관 사건 위험이 유의하게 증가하는 것으로 나타났다.이 교수는 "이번 연구는 관상동맥 시술을 받은 국내 대규모 환자 데이터를 기반으로 잔여 콜레스테롤의 임상적 기준점을 제시한 최초의 연구로, 특히 초고위험군 환자에서 잔여 콜레스테롤 관리의 중요성을 강조할 수 있는 근거를 마련했다"며 "향후 심혈관질환 예방 및 치료 전략에 있어 잔여 콜레스테롤이 주요한 지표로 활용되기를 기대한다"고 말했다.한미약품 국내사업본부장 박명희 전무는 "이번 ESC 발표를 통해 아모프렐은 고혈압 환자의 초기 치료 전략에서 유효성과 안전성을 동시에 확보한 새로운 치료 옵션으로서의 가능성을 제시했다"면서 "아모잘탄엑스큐는 고혈압과 이상지질혈증을 동반한 환자에서 우수한 유효성과 치료 만족도를 통해 복합제의 임상적 가치를 입증했다"고 했다.2025-09-25 09:12:47차지현
한미약품 "아모프렐 심혈관질환 연구 성과 공개"한미약품이 유럽심장학회(ESC)에서 고혈압과 이상지질혈증 동반 치료 복합제 임상 결과와 한국인 초고위험군 대상 심혈관질환 관리 지표를 발표했다. (자료: 한미약품) [데일리팜=차지현 기자] 한미약품이 유럽심장학회(ESC)에서 고혈압과 이상지질혈증 동반 치료 복합제 임상 결과와 한국인 초고위험군 대상 심혈관질환 관리 지표를 발표했다고 25일 밝혔다.ESC는 유럽심장학회가 주관하는 세계 최대 규모의 심혈관 분야 학술대회다. 올해 ESC는 지난 29일부터 9월 1일까지 스페인 마드리드에서 열렸다. 한미약품은 '아모프렐'과 '아모잘탄엑스큐'의 임상연구 결과와 한국인 초고위험군 잔여 콜레스테롤 연구 성과를 공유했다.한미약품에 따르면 올해 학회에는 동국대학교 의과대학 심장내과 이무용 교수, 양산부산대병원 순환기내과 천민구 교수, 원주세브란스기독병원 심장내과 이중희 교수가 참여해 ▲세계 최초 1/3 용량 3제 항고혈압제 아모프렐의 임상 3상 연구 결과 ▲고혈압·이상지질혈증 4제 복합제 아모잘탄엑스큐의 임상 4상 연구 결과 ▲국내 대규모 환자 데이터를 기반으로 한 잔여 콜레스테롤 임상 기준점 제시 연구 등 주요 심혈관질환 관련 연구 성과를 발표했다.아모프렐, 초기 고혈압 치료 패러다임 전환 가능성 제시첫 발표는 ESC 공식 포스터 세션에서 아모프렐 임상 책임 연구자인 동국대학교 의과대학 심장내과 이무용 교수가 맡았다. 이 교수는 한미약품이 지난 8월 출시한 저용량 3제 항고혈압제 아모프렐의 임상연구 결과를 통해 초기 고혈압 치료 패러다임 전환 가능성 제시했다.ESC에서 공개된 HM-APOLLO-301(이하 301 연구)과 HM-APOLLO-302(이하 302 연구) 연구는 국내 본태성 고혈압 환자를 대상으로 아모프렐(암로디핀 1.67mg+로사르탄 16.67mg+클로르탈리돈 4.17mg)과 표준 단일제(암로디핀 5mg 또는 로사르탄 50mg)의 8주간 혈압 강하 효과를 비교한 임상 3상 연구다.연구 결과 아모프렐은 수축기 및 이완기 혈압 강하 측면에서 단일제 대비 비열등성 또는 우월성을 입증했다. 목표 혈압 도달률도 유의하게 높았다. 또한 중대한 약물 이상반응은 보고되지 않아 우수한 내약성도 확인됐다.이무용 교수는 "이번 연구 결과는 최근 국내외에서 주목하고 있는 저용량 항고혈압 복합제의 유효성과 안전성을 다시 한번 확인한 의미 있는 결과"라며 "연구 결과를 바탕으로 출시된 아모프렐정은 세계 최초의 1/3 용량 3제 항고혈압제로 고혈압 환자의 초기 치료에서 보다 효과적으로 혈압을 조절하며 우리나라 고혈압 환자의 지속 치료율과 혈압 조절률 개선에 큰 역할을 할 것으로 기대된다"고 했다.아모잘탄엑스큐, 복약순응도 낮은 환자 치료 옵션 입증양산부산대병원 순환기내과 천민구 교수는 아모잘탄엑스큐의 임상 4상 연구 결과 발표를 통해 복약순응도가 낮은 죽상경화성 심혈관질환(ASCVD) 환자에서 혈압과 지질 조절을 동시에 개선함으로써 치료 편의성과 환자 만족도까지 높이는 치료 옵션임을 발표했다.이번 연구는 AMOREMIO이라는 명칭으로 진행된 국내 다기관 관찰연구다. 복약순응도가 낮은 ASCVD 환자를 대상으로 4제 고정용량복합제 아모잘탄엑스큐(암로디핀+로사르탄+로수바스타틴+에제티미브)의 효과를 평가했다.연구 결과 아모잘탄엑스큐로 전환한 환자들의 혈압과 지질 수치가 모두 유의한 차이로 개선됐으며, 치료 만족도 또한 크게 향상됐다. 또 치료 만족도 조사에서 최고 만족도(5점)를 선택한 환자 비율은 기존 치료 1.82%에서 전환 후 41.94%로 크게 증가했다. 이로써 복약 편의성과 환자 수용성 측면에서도 긍정적인 결과를 보여주며 환자 중심 복합제로서의 가치를 입증했다는 게 회사 측 설명이다.천 교수는 "이번 연구는 복약순응도가 낮은 고위험 심혈관질환 환자에서 아모잘탄엑스큐가 치료 효과뿐 아니라 복약편의성과 만족도까지 동시에 개선할 수 있음을 보여준 의미 있는 결과"라며 "복잡한 약물요법으로 인한 복약순응도 저하 문제를 해결할 수 있는 현실적 대안으로서 아모잘탄엑스큐의 임상적 가치를 입증했다"고 했다.한미-연세원주의대, 한국인 초고위험군 잔여 콜레스테롤 기준 인사이트 제시한미약품은 이번 학회에서 원주세브란스기독병원 심장내과 이중희 교수팀과 공동 연구를 통해 밝힌 최신 연구결과도 함께 발표했다.이번 연구는 국민건강보험공단 데이터베이스를 기반으로 2011년부터 2020년까지 관상동맥 중재술(PCI) 또는 우회술(CABG)을 받은 국내 관상동맥(CAD) 환자 52만 5646명을 대상으로 진행됐다.연구팀은 잔여 콜레스테롤(RC) 수치가 높을수록 복합 심뇌혈관 사건 발생 위험이 선형적으로 증가하는 경향을 확인했다. 특히 18mg/dL 이상일 경우 18mg/dL 미만일 때에 비해 복합 심혈관 사건 위험이 유의하게 증가하는 것으로 나타났다.이 교수는 "이번 연구는 관상동맥 시술을 받은 국내 대규모 환자 데이터를 기반으로 잔여 콜레스테롤의 임상적 기준점을 제시한 최초의 연구로, 특히 초고위험군 환자에서 잔여 콜레스테롤 관리의 중요성을 강조할 수 있는 근거를 마련했다"며 "향후 심혈관질환 예방 및 치료 전략에 있어 잔여 콜레스테롤이 주요한 지표로 활용되기를 기대한다"고 말했다.한미약품 국내사업본부장 박명희 전무는 "이번 ESC 발표를 통해 아모프렐은 고혈압 환자의 초기 치료 전략에서 유효성과 안전성을 동시에 확보한 새로운 치료 옵션으로서의 가능성을 제시했다"면서 "아모잘탄엑스큐는 고혈압과 이상지질혈증을 동반한 환자에서 우수한 유효성과 치료 만족도를 통해 복합제의 임상적 가치를 입증했다"고 했다.2025-09-25 09:12:47차지현 -
 10월 국감, 14·15일 복지부…17일 공단…21일 식약처[데일리팜=이정환 기자] 국회 보건복지위원회가 내달(10월) 14일 보건복지부와 질병관리청을 시작으로 정기국회 국정감사 일정을 시작한다.19일 박주민 복지위원장과 여야 간사단은 국감 일정안을 협의 중이다. 간사단은 오는 23일까지 최종 일정에 합의할 계획이다.현재까지 논의 중인 안은 내달 14일 화요일과 15일 수요일 이틀 간 복지부·질병청 국감 후 하루 쉰 다음 날인 내달 17일 금요일 국민건강보험공단과 건강보험심사평가원 국감을 진행하는 일정이다.복지부·질병청은 여의도 국회에서, 건보공단·심평원은 강원도 원주 현장 국감 실시를 검토 중이다.내달 21일 화요일에는 식품의약품안전처 국감을 국회에서 진행하고 22일 수요일엔 보건산업진흥원 등 보건 분야 산하기관을 일제히 감사할 계획이다.24일 금요일엔 국민연금공단, 28일 화요일엔 복지 분야 산하기관 감사에 나선다.30일 목요일 종합국감을 끝으로 복지위 국감은 막을 내릴 전망이다.2025-09-19 16:46:12이정환
10월 국감, 14·15일 복지부…17일 공단…21일 식약처[데일리팜=이정환 기자] 국회 보건복지위원회가 내달(10월) 14일 보건복지부와 질병관리청을 시작으로 정기국회 국정감사 일정을 시작한다.19일 박주민 복지위원장과 여야 간사단은 국감 일정안을 협의 중이다. 간사단은 오는 23일까지 최종 일정에 합의할 계획이다.현재까지 논의 중인 안은 내달 14일 화요일과 15일 수요일 이틀 간 복지부·질병청 국감 후 하루 쉰 다음 날인 내달 17일 금요일 국민건강보험공단과 건강보험심사평가원 국감을 진행하는 일정이다.복지부·질병청은 여의도 국회에서, 건보공단·심평원은 강원도 원주 현장 국감 실시를 검토 중이다.내달 21일 화요일에는 식품의약품안전처 국감을 국회에서 진행하고 22일 수요일엔 보건산업진흥원 등 보건 분야 산하기관을 일제히 감사할 계획이다.24일 금요일엔 국민연금공단, 28일 화요일엔 복지 분야 산하기관 감사에 나선다.30일 목요일 종합국감을 끝으로 복지위 국감은 막을 내릴 전망이다.2025-09-19 16:46:12이정환 -
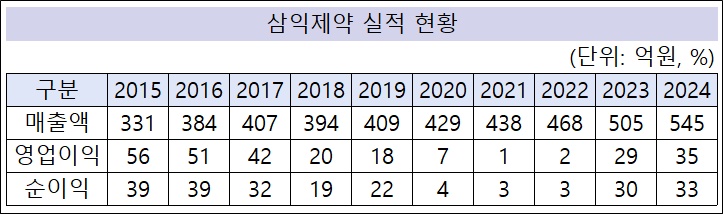 '실적·R&D·시설' 경쟁력…삼익제약의 IPO 성공 방정식[데일리팜 이석준 기자] 삼익제약이 실적, R&D, 시설 경쟁력을 바탕으로 코스닥 입성에 도전한다. 26년 연속 흑자(실적), 세계 최초 당뇨병 치료제 복합제 개발(R&D), CMO 경쟁력(시설) 등이 IPO 성공 방정식으로 자리잡고 있다.신사업 장기지속형 주사제 개발도 나서고 있다. 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에서다. 독자적 플랫폼 기술을 적용해 기존 제품과 차별화를 둔다. 플랫폼 기술은 향후 기업 가치(시가총액) 상승으로 연동될 가능성이 높다. 업계에 따르면 삼익제약은 10월 코스닥 입성을 위해 관련 절차를 밟고 있다. 지난 5월 한국거래소에 코스닥 스팩합병 상장을 위한 예비심사 청구서를 제출했다. 하나금융제28호스팩과 흡수합병을 통해 상장한다. 합병비율은 1대 0.2809383, 합병기일은 10월 13일, 신주 상장 예정일은 10월 27일이다.삼익제약 경쟁력 3대 키워드는 실적, R&D, 시설이 꼽힌다.먼저 실적이다. 삼익제약은 3대 만성질환(고혈압, 당뇨병, 고지혈증) 치료제 중심으로 견고한 실적을 내고 있다.실제 삼익제약의 지난해 매출액은 545억원으로 전년(505억원) 대비 7.9% 증가했다. 역대 최고 수치다. 같은기간 영업이익(29억→35억원)과 순이익(30억→33억원)도 20.7%, 10% 늘었다. 회사는 2029년 즈음 외형 1000억원 돌파가 가능하다고 보고 있다.범위를 넓혀도 2021~2024년 CAGR(연평균성장률)은 매출 7.6%, 이중 CMO 사업은 27.7%다. 영업이익과 순이익은 26년(1999~2024년) 연속 흑자를 달성중이다. 2024년 기준 부채비율 23.5% 등 재무구조도 탄탄하다는 평가다. 자기자본(516억원)도 매년 확충되고 있다. R&D 경쟁력도 쌓고 있다. 권영이 대표이사(CTO 겸직)를 필두로 학술개발팀, 중앙연구소, DI팀이 유기적으로 협력하며 신제품 개발, 업무 전문성 및 역량을 강화하고 있다.대표적으로 피오시타정은 시타글립틴+피오글리타존 최초 복합제다. 2023년 11월 급여를 받고 시장에 진입하고 있다.세브란스병원(강남/용인)과 성심병원(강남/동탄), 서울의료원, 상계백병원 포함 주요 병원 8곳에서 처방이 시작됐으며 서울아산병원, 서울대학교병원, 한양대학교병원 등 20여개 병원에서 연내 DC 상정을 준비 중이다. 삼익제약은 이를 통해 전국 50여 병원에서 피오시타정의 처방이 이뤄질 것으로 예상하고 있다.이외도 삼익제약은 SGLT-2i와 DPP-4i 복합제 '포르자듀오정(다파글리플로진/시타글립틴)', DPP-4i와 Met XR 복합제 '자누맥스엠엑스알서방정(시타글립틴/메트포르민)', DDP-4i와 TZD 복합제 '피오시타정(시타글립틴/피오글리타존) 등 당뇨병치료제 라인업을 갖추고 있다.독자적인 플랫폼 기술(UniSpheroTM)을 활용한 장기지속형 주사제 개발도 나서고 있다. UniSpheroTM는 미세 입자 멤브레인을 이용한 마이크로스피어 제조 플랫폼이다. 마이크로스피어 입자의 크기와 분포를 정밀하게 제어할 수 있는 삼익제약의 고유 기술이다. 높은 재현성과 균일한 입도 분포도가 특징이다. 장기지속형 주사제 기술 및 장비 관련 특허등록 1건, 특허출헌 2건 등 지속적인 특허출원 예정이다.해당 플랫폼 기술을 통해 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 다양한 파프라인을 구축하고 있다. 회사는 임상 단계에 따라 해외 제약사와 라이선스 아웃 기회도 노리고 있다. CMO 사업 확대로 시설도 확충하고 있다.인천 제1공장 증축(2026년), 원주 제2공장 착공(2027년) 등이다. 이를 통해 ▲효율적 생산 및 비용 관리(원가 절감) ▲신규 제형 생산(이층정) ▲생산 케파 및 가동율 확대 ▲경쟁력 있는 특화 제품군 영업에 나선다. 시설 확충은 영업이익과 상장 조달 자금으로 투입할 계획이다.기존 인천공장은 글로벌 GMP 수준의 생산 및 품질관리 시스템을 갖추고 있다. 제품 164개, CMO 30개(49개 업체) 품목을 다루고 있다. 정제(연 5억7000만정), 경질캡슐제(연 4896만 캡슐), 과립제(연 1176만포), 내용액제(연 1440만포) 등의 다양한 제형의 생산능력을 보유하고 있다.회사 관계자는 “수년간 축적된 전문성과 시장 경쟁력을 바탕으로 안정적인 재무 성장을 이뤄왔다. 이번 코스닥 상장은 경영 투명성을 높이고, 주주 및 투자자들과의 신뢰를 더욱 공고히 하기 위한 것”이라고 말했다.이어 “상장을 통해 확보될 자금은 만성질환 치료제 포트폴리오 강화 및 생산설비 확충, 연구개발(R&D) 투자 확대에 투입할 예정이다. 전문의약품 분야 선도기업으로서의 지위를 더욱 확고히 하고, 'Total Healthcare Company'로 비전 실현을 가속화하겠다”고 강조했다.한편 삼익제약 최대주주는 오너 2세 이충환(28.47%) 대표다. 창업주 이세영 회장은 15.19% 지분을 보유중이다.2025-09-19 12:00:23이석준
'실적·R&D·시설' 경쟁력…삼익제약의 IPO 성공 방정식[데일리팜 이석준 기자] 삼익제약이 실적, R&D, 시설 경쟁력을 바탕으로 코스닥 입성에 도전한다. 26년 연속 흑자(실적), 세계 최초 당뇨병 치료제 복합제 개발(R&D), CMO 경쟁력(시설) 등이 IPO 성공 방정식으로 자리잡고 있다.신사업 장기지속형 주사제 개발도 나서고 있다. 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 미래 수요가 높은 질환에서다. 독자적 플랫폼 기술을 적용해 기존 제품과 차별화를 둔다. 플랫폼 기술은 향후 기업 가치(시가총액) 상승으로 연동될 가능성이 높다. 업계에 따르면 삼익제약은 10월 코스닥 입성을 위해 관련 절차를 밟고 있다. 지난 5월 한국거래소에 코스닥 스팩합병 상장을 위한 예비심사 청구서를 제출했다. 하나금융제28호스팩과 흡수합병을 통해 상장한다. 합병비율은 1대 0.2809383, 합병기일은 10월 13일, 신주 상장 예정일은 10월 27일이다.삼익제약 경쟁력 3대 키워드는 실적, R&D, 시설이 꼽힌다.먼저 실적이다. 삼익제약은 3대 만성질환(고혈압, 당뇨병, 고지혈증) 치료제 중심으로 견고한 실적을 내고 있다.실제 삼익제약의 지난해 매출액은 545억원으로 전년(505억원) 대비 7.9% 증가했다. 역대 최고 수치다. 같은기간 영업이익(29억→35억원)과 순이익(30억→33억원)도 20.7%, 10% 늘었다. 회사는 2029년 즈음 외형 1000억원 돌파가 가능하다고 보고 있다.범위를 넓혀도 2021~2024년 CAGR(연평균성장률)은 매출 7.6%, 이중 CMO 사업은 27.7%다. 영업이익과 순이익은 26년(1999~2024년) 연속 흑자를 달성중이다. 2024년 기준 부채비율 23.5% 등 재무구조도 탄탄하다는 평가다. 자기자본(516억원)도 매년 확충되고 있다. R&D 경쟁력도 쌓고 있다. 권영이 대표이사(CTO 겸직)를 필두로 학술개발팀, 중앙연구소, DI팀이 유기적으로 협력하며 신제품 개발, 업무 전문성 및 역량을 강화하고 있다.대표적으로 피오시타정은 시타글립틴+피오글리타존 최초 복합제다. 2023년 11월 급여를 받고 시장에 진입하고 있다.세브란스병원(강남/용인)과 성심병원(강남/동탄), 서울의료원, 상계백병원 포함 주요 병원 8곳에서 처방이 시작됐으며 서울아산병원, 서울대학교병원, 한양대학교병원 등 20여개 병원에서 연내 DC 상정을 준비 중이다. 삼익제약은 이를 통해 전국 50여 병원에서 피오시타정의 처방이 이뤄질 것으로 예상하고 있다.이외도 삼익제약은 SGLT-2i와 DPP-4i 복합제 '포르자듀오정(다파글리플로진/시타글립틴)', DPP-4i와 Met XR 복합제 '자누맥스엠엑스알서방정(시타글립틴/메트포르민)', DDP-4i와 TZD 복합제 '피오시타정(시타글립틴/피오글리타존) 등 당뇨병치료제 라인업을 갖추고 있다.독자적인 플랫폼 기술(UniSpheroTM)을 활용한 장기지속형 주사제 개발도 나서고 있다. UniSpheroTM는 미세 입자 멤브레인을 이용한 마이크로스피어 제조 플랫폼이다. 마이크로스피어 입자의 크기와 분포를 정밀하게 제어할 수 있는 삼익제약의 고유 기술이다. 높은 재현성과 균일한 입도 분포도가 특징이다. 장기지속형 주사제 기술 및 장비 관련 특허등록 1건, 특허출헌 2건 등 지속적인 특허출원 예정이다.해당 플랫폼 기술을 통해 류마티스관절염치료제, 면역보조치료제, 비만치료제 등 다양한 파프라인을 구축하고 있다. 회사는 임상 단계에 따라 해외 제약사와 라이선스 아웃 기회도 노리고 있다. CMO 사업 확대로 시설도 확충하고 있다.인천 제1공장 증축(2026년), 원주 제2공장 착공(2027년) 등이다. 이를 통해 ▲효율적 생산 및 비용 관리(원가 절감) ▲신규 제형 생산(이층정) ▲생산 케파 및 가동율 확대 ▲경쟁력 있는 특화 제품군 영업에 나선다. 시설 확충은 영업이익과 상장 조달 자금으로 투입할 계획이다.기존 인천공장은 글로벌 GMP 수준의 생산 및 품질관리 시스템을 갖추고 있다. 제품 164개, CMO 30개(49개 업체) 품목을 다루고 있다. 정제(연 5억7000만정), 경질캡슐제(연 4896만 캡슐), 과립제(연 1176만포), 내용액제(연 1440만포) 등의 다양한 제형의 생산능력을 보유하고 있다.회사 관계자는 “수년간 축적된 전문성과 시장 경쟁력을 바탕으로 안정적인 재무 성장을 이뤄왔다. 이번 코스닥 상장은 경영 투명성을 높이고, 주주 및 투자자들과의 신뢰를 더욱 공고히 하기 위한 것”이라고 말했다.이어 “상장을 통해 확보될 자금은 만성질환 치료제 포트폴리오 강화 및 생산설비 확충, 연구개발(R&D) 투자 확대에 투입할 예정이다. 전문의약품 분야 선도기업으로서의 지위를 더욱 확고히 하고, 'Total Healthcare Company'로 비전 실현을 가속화하겠다”고 강조했다.한편 삼익제약 최대주주는 오너 2세 이충환(28.47%) 대표다. 창업주 이세영 회장은 15.19% 지분을 보유중이다.2025-09-19 12:00:23이석준 -
 2년 임상 종료...애엽 급여삭제 위기에 개량신약 불똥[데일리팜=천승현 기자] 애엽 추출물 성분 위염치료제의 급여 삭제 위기가 차세대 스티렌 개발에도 영향을 미칠 수 있다는 우려가 확산된다. 동아에스티가 2년 동안 수백명의 피험자를 대상으로 복용 횟수를 줄인 개량신약의 임상시험을 마쳤지만 상업화 여부가 불투명해졌다. 환자의 복용 편의성을 높이기 위해 적잖은 비용과 시간을 들인 연구개발 노력이 급여재평가 결과 수포로 돌아갈 수 있다는 불만이 나오는 실정이다.17일 식품의약품안전처에 따르면 동아에스티가 진행 중인 DA-5219 임상3상시험이 지난 7월 15일 최종 시험대상자 관찰이 종료됐다. 지난 2023년 10월 DA-5219의 급만성 위염에 대한 임상3상시험 계획을 승인 받은 이후 2년 만에 임상시험이 마무리됐다. 급성 또는 만성 위염 환자에서 DA-5219을 스티렌과 비교해 유효성 및 안전성을 평가하기 위한 임상시험이다.DA-5219은 애엽 추출물 성분 스티렌을 복용 횟수를 1일 3회에서 1회로 줄인 서방형 제제다. 애엽 추출물의 용량이 스티렌 60mg보다 3배 많은 180mg 함유한 것으로 추정된다.임상시험에서 시험군은 DA-5219를 1일 1회 1정씩 가급적 일정한 시간에 식후 경구 투여하고 비교군은 대조약인 스티렌은 1일 3회 1정씩 투여하는 방식으로 진행됐다. 약물 복용 후 상부 위장관 내시경 검사상 위점막 미란의 유효율을 비교하는 방식으로 유효성과 안전성을 비교 평가한다.임상시험은 현대병원, 인하대의과대학부속병원, 건국대병원, 강동경희대의대병원, 아산사회복지재단서울아산병원, 가톨릭대여의도성모병원, 가톨릭대인천성모병원, 고신대 복음병원, 부산대병원, 분당서울대병원, 삼성서울병원, 서울대병원, 원주세브란스기독병원, 연세대의과대학세브란스병원, 영남대병원, 이화여자대의과대학부속서울병원, 예수병원유지재단 예수병원, 전북대병원, 중앙대병원, 충남대병원, 칠곡경북대병원, 가톨릭대서울성모병원, 건양대병원, 춘천성심병원, 한림대성심병원 등 26곳에서 진행됐다.임상시험 기간은 2023년 12월부터 올해 12월로 설계됐다. 목표 시험 대상자 452명에 대한 최종 시험대상자 관찰이 종료되면서 사실상 임상시험이 마무리됐다. 임상시험에는 수십억원이 투입된 것으로 전해졌다.애엽 추출물 의약품은 쑥을 기반으로 만드는 천연물의약품이다. 동아에스티의 ‘스티렌’이 오리지널 제품으로 급성위염과 만성위염의 위점막 병변, 출혈, 발적, 부종 등의 개선에 사용된다. ‘비스테로이드소염진통제(NSAID) 투여로 인한 위염 예방’ 적응증도 보유 중이다.동아에스티는 지난 2015년 10월 스티렌 주 성분의 용량을 60mg에서 90mg으로 늘려 1일 2회 복용하는 스티렌투엑스를 허가받은 바 있다. DA-5219가 식약처 허가를 받으면 스티렌투엑스에 이어 10년 만에 복용 편의성을 개선한 개량신약이 등장하는 셈이다.동아에스티가 2년 동안 전국 임상시험 기관에서 DA-5219의 임상시험을 진행했지만 임상시험에 성공하더라도 상업화 여부를 장담할 수 없는 상황이다. 임상시험 대조약 스티렌이 급여 탈락 위기에 처했기 때문이다.건강보험심사평가원은 지난달 7일 약제급여평가위원회에서 심의한 결과 애엽 추출물에 대해 임상적 유용성 근거가 없다는 이유로 급여 적정성이 없다는 결론을 내렸다. 보건복지부는 지난해 2월 2025년 약제 급여적정성 재평가 대상으로 올로파타딘염산염, 위령선·괄루근·하고초, 베포타스틴, 구형흡착탄, 애엽추출물, 엘오르니틴엘아스프르트산, 케노데속시콜산-우르소데속시콜산삼수화물마그네슘염 등 8개 성분을 확정했다.제약사들은 지난 3월 재평가에 필요한 임상적 유용성, 비용효과성, 사회적 요구도 등의 자료를 급여 적정성 재평가 자료를 제출했다. 하지만 급여재평가 공고 1년 6개월 만에 애엽추출물에 대해 급여 삭제 판단을 내렸다. 제약사들의 이의신청이 받아들여지지 않으면 애엽 추출물은 급여 시장에서 퇴출된다.애엽 추출물의 급여 퇴출이 확정되면 DA-5219가 식약처 허가를 통과하더라도 급여 등재를 장담하기 쉽지 않은 상황이다. 1일 복용 횟수를 줄여 복용 편의성을 높였지만 애엽 추출물의 급여 적정성이 인정받지 못했다는 이유로 급여 등재를 낙관할 수 없다. 보건당국의 급여재평가 결과 제약사들의 연구개발 노력이 수포로 돌아갈 수 있다는 우려가 나오는 실정이다.애엽 추출물의 급여 재평가는 제네릭 의약품을 대상으로 진행하는 동등성 재평가에도 영향을 미칠 전망이다.제약사 50여곳은 지난 6월 말 식품의약품안전처에 애엽 성분 위염치료제의 임상시험 계획서를 제출했다. 오리지널 의약품 스티렌과 스티렌투엑스를 각각 대조약으로 위염치료제 효능을 비교하는 내용의 임상시험이다.식약처의 동등성 재평가 지시에 따른 임상시험 수행 계획이다. 식약처는 지난해 12월 한약·생약제제 전문의약품 212개 품목에 대해 동등성 재평가를 지시했다. 오리지널 의약품과의 동등성을 입증하면 허가를 인정해주겠다는 의미다. 애엽 성분 의약품 135개 품목이 동등성 재평가 대상에 포함됐다.식약처는 6월 30일까지 재평가 신청서 및 시험계획서를 제출하도록 제약사들에 지시했다. 재평가 결과보고서 제출기한은 계획서 검토 결과 통보시 결정·안내할 예정이다. 업계에서는 이르면 이달 중 임상계획서 승인 여부가 결정날 것으로 기대하고 있다.스티렌과 스티렌투엑스와 같은 제조방식으로 에탄올을 사용해 유효 성분을 추출한 제네릭 제품이 이번 동등성 재평가 대상 의약품이다.지엘파마, 종근당, 대원제약, 안국약품, 제일약품 등이 이소프로판올을 용매로 사용해 유효 성분을 추출한 애엽 성분 의약품은 임상시험을 통해 허가를 받았다는 이유로 재평가 대상에서 제외됐다. 의약품 조사기관 유비스트에 따르면 지난 상반기 애엽 성분 위염치료제 외래 처방시장은 616억원으로 집계됐다. 처방 시장에서는 애엽에탄올연조엑스의 점유율이 에엽이소프로판올연조엑스를 압도했다. 지난 상반기 애엽에탄올연조엑스의 처방금액은 471억원으로 애엽 전체 시장의 76.3%를 차지했다.하지만 애엽 추출물의 급여재평가 탈락 변수가 발생하면서 애엽에탄올연조엑스 성분 제네릭의 동등성 재평가 수행 여부가 불투명해졌다애엽추출물의 급여 탈락이 결정되면 제약사들이 추진 중인 동등성 재평가 임상시험도 동력이 꺾이게 된다. 급여 삭제는 사실상 시장 퇴출을 의미하기 때문에 제약사들이 제네릭 제품의 허가 유지를 목표로 거액을 들여 임상시험을 진행하는 의미가 상실된다.제약사들은 동등성 재평가 대상 애엽 추출물 의약품을 스티렌과 스티렌투엑스와 각각 비교 임상시험하는 방식으로 동등성을 입증할 계획이다. 생약제제 특성상 유효 성분의 혈중농도를 비교하는 생물학적동등성시험으로 동등성을 입증하기 어렵다는 이유에서다. 스티렌과 스티렌투엑스 제네릭 제품들은 비교 용출과 비교 붕해 방식으로 허가받았다.동등성 평가 임상시험은 애엽 성분 의약품을 생산하는 수탁사를 중심으로 진행된다. 풍림무약이 애엽 성분 60mg와 90mg 2건의 임상시험을 별도로 진행하고, 마더스제약이 애엽 성분 60mg의 임상시험을 수행하는 방식이다. 임상시험 1건당 모집 피험자는 400명 이상 설정한 것으로 전해졌다. 3건의 임상시험 비용은 총 150억원으로 책정된 것으로 알려졌다.제약사들은 스티렌 제네릭의 동등성 평가 임상시험 계획을 설계하는 과정에서 CRO 업체들과 계약도 마친 것으로 전해졌다. 계약금을 비롯해 임상시험 사전 준비를 위해 일정 규모의 비용도 지출한 상태다.애엽 추출물의 급여 삭제가 확정되더라도 제네릭 업체들이 모두 동등성 재평가 임상시험을 포기하지 않을 것이란 견해도 제기된다. 제약사들이 애엽 추출물의 급여 삭제에 반발해 행정소송과 함께 집행정지를 청구하면서 급여 잔류를 모색하는 전략이 가능하다. 만약 스티렌 제네릭의 동등성 재평가를 포기할 경우 허가가 취소되기 때문에 급여 삭제를 저지하기 위한 법정 투쟁도 불가능해진다.임상 마치고도 상업화 불투명2025-09-17 06:20:00천승현
2년 임상 종료...애엽 급여삭제 위기에 개량신약 불똥[데일리팜=천승현 기자] 애엽 추출물 성분 위염치료제의 급여 삭제 위기가 차세대 스티렌 개발에도 영향을 미칠 수 있다는 우려가 확산된다. 동아에스티가 2년 동안 수백명의 피험자를 대상으로 복용 횟수를 줄인 개량신약의 임상시험을 마쳤지만 상업화 여부가 불투명해졌다. 환자의 복용 편의성을 높이기 위해 적잖은 비용과 시간을 들인 연구개발 노력이 급여재평가 결과 수포로 돌아갈 수 있다는 불만이 나오는 실정이다.17일 식품의약품안전처에 따르면 동아에스티가 진행 중인 DA-5219 임상3상시험이 지난 7월 15일 최종 시험대상자 관찰이 종료됐다. 지난 2023년 10월 DA-5219의 급만성 위염에 대한 임상3상시험 계획을 승인 받은 이후 2년 만에 임상시험이 마무리됐다. 급성 또는 만성 위염 환자에서 DA-5219을 스티렌과 비교해 유효성 및 안전성을 평가하기 위한 임상시험이다.DA-5219은 애엽 추출물 성분 스티렌을 복용 횟수를 1일 3회에서 1회로 줄인 서방형 제제다. 애엽 추출물의 용량이 스티렌 60mg보다 3배 많은 180mg 함유한 것으로 추정된다.임상시험에서 시험군은 DA-5219를 1일 1회 1정씩 가급적 일정한 시간에 식후 경구 투여하고 비교군은 대조약인 스티렌은 1일 3회 1정씩 투여하는 방식으로 진행됐다. 약물 복용 후 상부 위장관 내시경 검사상 위점막 미란의 유효율을 비교하는 방식으로 유효성과 안전성을 비교 평가한다.임상시험은 현대병원, 인하대의과대학부속병원, 건국대병원, 강동경희대의대병원, 아산사회복지재단서울아산병원, 가톨릭대여의도성모병원, 가톨릭대인천성모병원, 고신대 복음병원, 부산대병원, 분당서울대병원, 삼성서울병원, 서울대병원, 원주세브란스기독병원, 연세대의과대학세브란스병원, 영남대병원, 이화여자대의과대학부속서울병원, 예수병원유지재단 예수병원, 전북대병원, 중앙대병원, 충남대병원, 칠곡경북대병원, 가톨릭대서울성모병원, 건양대병원, 춘천성심병원, 한림대성심병원 등 26곳에서 진행됐다.임상시험 기간은 2023년 12월부터 올해 12월로 설계됐다. 목표 시험 대상자 452명에 대한 최종 시험대상자 관찰이 종료되면서 사실상 임상시험이 마무리됐다. 임상시험에는 수십억원이 투입된 것으로 전해졌다.애엽 추출물 의약품은 쑥을 기반으로 만드는 천연물의약품이다. 동아에스티의 ‘스티렌’이 오리지널 제품으로 급성위염과 만성위염의 위점막 병변, 출혈, 발적, 부종 등의 개선에 사용된다. ‘비스테로이드소염진통제(NSAID) 투여로 인한 위염 예방’ 적응증도 보유 중이다.동아에스티는 지난 2015년 10월 스티렌 주 성분의 용량을 60mg에서 90mg으로 늘려 1일 2회 복용하는 스티렌투엑스를 허가받은 바 있다. DA-5219가 식약처 허가를 받으면 스티렌투엑스에 이어 10년 만에 복용 편의성을 개선한 개량신약이 등장하는 셈이다.동아에스티가 2년 동안 전국 임상시험 기관에서 DA-5219의 임상시험을 진행했지만 임상시험에 성공하더라도 상업화 여부를 장담할 수 없는 상황이다. 임상시험 대조약 스티렌이 급여 탈락 위기에 처했기 때문이다.건강보험심사평가원은 지난달 7일 약제급여평가위원회에서 심의한 결과 애엽 추출물에 대해 임상적 유용성 근거가 없다는 이유로 급여 적정성이 없다는 결론을 내렸다. 보건복지부는 지난해 2월 2025년 약제 급여적정성 재평가 대상으로 올로파타딘염산염, 위령선·괄루근·하고초, 베포타스틴, 구형흡착탄, 애엽추출물, 엘오르니틴엘아스프르트산, 케노데속시콜산-우르소데속시콜산삼수화물마그네슘염 등 8개 성분을 확정했다.제약사들은 지난 3월 재평가에 필요한 임상적 유용성, 비용효과성, 사회적 요구도 등의 자료를 급여 적정성 재평가 자료를 제출했다. 하지만 급여재평가 공고 1년 6개월 만에 애엽추출물에 대해 급여 삭제 판단을 내렸다. 제약사들의 이의신청이 받아들여지지 않으면 애엽 추출물은 급여 시장에서 퇴출된다.애엽 추출물의 급여 퇴출이 확정되면 DA-5219가 식약처 허가를 통과하더라도 급여 등재를 장담하기 쉽지 않은 상황이다. 1일 복용 횟수를 줄여 복용 편의성을 높였지만 애엽 추출물의 급여 적정성이 인정받지 못했다는 이유로 급여 등재를 낙관할 수 없다. 보건당국의 급여재평가 결과 제약사들의 연구개발 노력이 수포로 돌아갈 수 있다는 우려가 나오는 실정이다.애엽 추출물의 급여 재평가는 제네릭 의약품을 대상으로 진행하는 동등성 재평가에도 영향을 미칠 전망이다.제약사 50여곳은 지난 6월 말 식품의약품안전처에 애엽 성분 위염치료제의 임상시험 계획서를 제출했다. 오리지널 의약품 스티렌과 스티렌투엑스를 각각 대조약으로 위염치료제 효능을 비교하는 내용의 임상시험이다.식약처의 동등성 재평가 지시에 따른 임상시험 수행 계획이다. 식약처는 지난해 12월 한약·생약제제 전문의약품 212개 품목에 대해 동등성 재평가를 지시했다. 오리지널 의약품과의 동등성을 입증하면 허가를 인정해주겠다는 의미다. 애엽 성분 의약품 135개 품목이 동등성 재평가 대상에 포함됐다.식약처는 6월 30일까지 재평가 신청서 및 시험계획서를 제출하도록 제약사들에 지시했다. 재평가 결과보고서 제출기한은 계획서 검토 결과 통보시 결정·안내할 예정이다. 업계에서는 이르면 이달 중 임상계획서 승인 여부가 결정날 것으로 기대하고 있다.스티렌과 스티렌투엑스와 같은 제조방식으로 에탄올을 사용해 유효 성분을 추출한 제네릭 제품이 이번 동등성 재평가 대상 의약품이다.지엘파마, 종근당, 대원제약, 안국약품, 제일약품 등이 이소프로판올을 용매로 사용해 유효 성분을 추출한 애엽 성분 의약품은 임상시험을 통해 허가를 받았다는 이유로 재평가 대상에서 제외됐다. 의약품 조사기관 유비스트에 따르면 지난 상반기 애엽 성분 위염치료제 외래 처방시장은 616억원으로 집계됐다. 처방 시장에서는 애엽에탄올연조엑스의 점유율이 에엽이소프로판올연조엑스를 압도했다. 지난 상반기 애엽에탄올연조엑스의 처방금액은 471억원으로 애엽 전체 시장의 76.3%를 차지했다.하지만 애엽 추출물의 급여재평가 탈락 변수가 발생하면서 애엽에탄올연조엑스 성분 제네릭의 동등성 재평가 수행 여부가 불투명해졌다애엽추출물의 급여 탈락이 결정되면 제약사들이 추진 중인 동등성 재평가 임상시험도 동력이 꺾이게 된다. 급여 삭제는 사실상 시장 퇴출을 의미하기 때문에 제약사들이 제네릭 제품의 허가 유지를 목표로 거액을 들여 임상시험을 진행하는 의미가 상실된다.제약사들은 동등성 재평가 대상 애엽 추출물 의약품을 스티렌과 스티렌투엑스와 각각 비교 임상시험하는 방식으로 동등성을 입증할 계획이다. 생약제제 특성상 유효 성분의 혈중농도를 비교하는 생물학적동등성시험으로 동등성을 입증하기 어렵다는 이유에서다. 스티렌과 스티렌투엑스 제네릭 제품들은 비교 용출과 비교 붕해 방식으로 허가받았다.동등성 평가 임상시험은 애엽 성분 의약품을 생산하는 수탁사를 중심으로 진행된다. 풍림무약이 애엽 성분 60mg와 90mg 2건의 임상시험을 별도로 진행하고, 마더스제약이 애엽 성분 60mg의 임상시험을 수행하는 방식이다. 임상시험 1건당 모집 피험자는 400명 이상 설정한 것으로 전해졌다. 3건의 임상시험 비용은 총 150억원으로 책정된 것으로 알려졌다.제약사들은 스티렌 제네릭의 동등성 평가 임상시험 계획을 설계하는 과정에서 CRO 업체들과 계약도 마친 것으로 전해졌다. 계약금을 비롯해 임상시험 사전 준비를 위해 일정 규모의 비용도 지출한 상태다.애엽 추출물의 급여 삭제가 확정되더라도 제네릭 업체들이 모두 동등성 재평가 임상시험을 포기하지 않을 것이란 견해도 제기된다. 제약사들이 애엽 추출물의 급여 삭제에 반발해 행정소송과 함께 집행정지를 청구하면서 급여 잔류를 모색하는 전략이 가능하다. 만약 스티렌 제네릭의 동등성 재평가를 포기할 경우 허가가 취소되기 때문에 급여 삭제를 저지하기 위한 법정 투쟁도 불가능해진다.임상 마치고도 상업화 불투명2025-09-17 06:20:00천승현 -
 인보사 미국 진출 자신감?...코오롱티슈진, 1225억 조달[데일리팜=차지현 기자] 코오롱그룹의 바이오 자회사 코오롱티슈진이 대규모 자금 조달에 나섰다. 골관절염 유전자치료제 미국 품목허가와 상업화를 위해서다. 회사는 잇단 투자 유치와 인재 확보 등을 병행하며 재도약에 사활을 건 분위기다.1225억 규모 CB 발행 결정…"인보사 FDA 허가와 상업화 준비"12일 금융감독원에 따르면 코오롱티슈진은 이날 이사회를 열고 4회차 전환사채(CB) 발행을 의결했다. CB는 주식과 채권의 성격을 모두 지닌 주식연계채권이다. 채권자가 회사에 돈을 빌려주고 이자를 받다가, 주가가 오르면 주식으로 전환할 수 있다.이번에 코오롱티슈진이 발행하는 CB는 1225억원 규모다. 파나세아, 스틱호라이즌, IBKC-카스피안 T 8호 신기술투자조합 등 기관 투자자가 참여, 물량을 인수하는 형태다. 해당 CB는 표면이자율과 만기이자율이 모두 0%인 '빵빵채권'이다.CB 전환가액은 21만8090원이다. 코오롱티슈진은 2017년 코스닥 입성 당시 보통주가 아닌 증권예탁증권(KDR)로 상장했다. DR은 기업이 해외에서 주식을 발행할 경우 외국의 예탁기관이 현지에서 증권을 발행·유통해 원주와 상호 전환이 가능하도록 한 주식대체증서다.코오롱티슈진은 이번 CB 발행에서 신주 발행가액을 1 KDR 당 4만3618원으로 산출했다. 코오롱티슈진의 보통주 1주가 5KDR이라는 점을 고려하면 발행일 종가 대비 약 12.1% 할인한 수준이다. CB 발행을 결정한 12일 종가 기준 코오롱티슈진 주가는 4만9650원이었다.CB를 주식으로 전환할 수 있는 전환청구 기간은 오는 2026년 9월 26일부터 2030년 8월 26일까지다. 전환이 이뤄질 경우 발행 가능한 주식 수는 56만1694주로 전체 주식의 약 3.3%에 해당한다. 이번 CB에는 투자자가 만기 전 조기상환을 청구할 수 있는 풋옵션(매도청구권) 조항도 달렸다.코오롱티슈진은 이번 CB를 통해 조달한 자금을 인보사 미국 식품의약국(FDA) 품목허가와 상업화를 위한 준비에 사용할 계획이다. 세부적으로 올해 225억원, 내년 1000억원의 운영 자금을 배정했다.국내 허가 불발됐지만 미국서 기사회생 불씨, 미국 3상 총력인보사는 코오롱그룹 또다른 계열사 코오롱생명과학이 지난 2017년 7월 식품의약품안전처 허가를 받은 세계 최초 골관절염 유전자치료제다. 코오롱생명과학이 인보사 아시아 판권을, 코오롱티슈진은 미국과 유럽을 포함한 글로벌 전역 판권을 갖고 있다.인보사는 2019년 3월 미국 3상 진행 과정에서 핵심 성분 중 하나인 연골유래세포가 종양 유발 가능성이 높은 신장유래세포로 변경됐다는 사실이 드러나면서 논란을 빚었다. 이 여파로 식품의약품안전처는 인보사 품목허가를 취소했다. 이어 2019년 5월 미국 식품의약국(FDA)으로부터 임상중지 통보를 받았다.코오롱생명과학은 서울행정법원에 인보사 품목허가 처분 취소 소송을 제기했다. 그러나 서울행정법원은 2021년 식약처의 처분이 정당하다며 원고 패소 판결을 내렸다. 이어 지난해 초 2심 재판부까지 식약처의 손을 들어주는 판결을 내리면서 국내 재출시 가능성은 사라졌다.다만 미국의 경우 희망의 불씨가 남아 있다. 2020년 4월 FDA가 임상재개를 수용하면서다. 인보사의 국내 재기는 불발됐지만 세계 최대 의약품 시장인 미국 출시에 성공한다면 더 큰 반전의 계기를 마련할 수 있다. 코오롱티슈진은 2020년 12월부터 코오롱생명과학은 환자 투약을 재개했다. 미국 전역 80개 병원에서 환자 1000명을 대상으로 임상을 진행했고, 지난해 7월 환자 투약을 마무리했다. 코오롱티슈진은 향후 2년간 인보사 투약 환자를 대상으로 추적 관찰을 진행한다. 이 기간 인보사의 FDA 품목허가를 위한 준비를 병행해 FDA 승인 시기를 최대한 앞당기겠다는 게 회사 측 입장이다.특히 코오롱티슈진은 올 초 사법 리스크 해소 이후 인보사 회생 작업에 한층 속도를 내는 모습이다. 지난해 11월 서울중앙지방법원은 1심 판결에서 이웅열 코오롱 명예회장과 전직 임원 등에 무죄를 선고했다. 앞서 이웅열 명예회장 등은 2020년 인보사 성분 조작 등에 관여, 자본시장과 금융투자업에 관한 법률을 위반한 혐의로 기소된 바 있다.인보사에 대한 코오롱티슈진의 의지는 잇단 투자 유치 행보에서도 엿볼 수 있다. 코오롱티슈진은 지난 2월에도 565억원 규모 CB를 발행했다. 해당 CB 역시 표면 이자율과 만기 이자율이 모두 0%로, 유진투자증권, 한양증권, 키움증권, 한국투자증권 등이 인수했다. 코오롱티슈진은 2022년과 2024년에도 각각 330억원과 245억원 규모 CB를 발행, 외부에서 자금을 끌어왔다.코오롱티슈진은 모회사 코오롱으로부터도 지속해서 자금 수혈을 받아왔다. 코오롱은 지난 2021년부터 다섯 차례에 걸쳐 코오롱티슈진 제3자배정 유증에 참여했다. 코오롱은 코오롱티슈진에 ▲2021년 355억원 ▲2022년 388억원 ▲2023년 400억원 ▲2024년 478억원을 출자했다. 여기에 지난 1월 441억원 규모 코오롱티슈진 유상증자에 단독으로 참여, 자금을 추가로 투입했다.인재 확보에도 공을 들이고 있다. 코오롱그룹은 올 초 전승호 전 종근당 고문을 영입하고 코오롱티슈진 각자대표로 선임했다. 전 고문은 대웅제약을 1조 클럽 반열에 올려놓은 주역으로 꼽힌다. 전 고문은 서울대 약학대학 출신으로 2003년부터 작년 상반기까지 대웅제약에 21년간 몸 담았다. 대웅제약에서 전 대표는 라이선싱 팀장, 글로벌전략 팀장, 글로벌사업본부장 등을 거쳤다. 2018년 대웅제약 대표이사 사장으로 선임됐고 한 차례 연임을 통해 작년 초까지 대웅제약의 사령탑을 맡았다.전 고문은 지난해 초 대웅제약 사내이사 임기 만료 이후 대웅인베스트먼트, 아피셀테라퓨틱스 등 계열사 대표이사와 사내이사를 역임했다. 이후 대웅제약을 관두고 작년 5월부터 종근당에서 고문으로 경영 자문을 담당했다. 전 고문은 종근당에서 3개월간의 짧은 고문직 역할을 마치고 코오롱그룹으로 적을 옮겼다.2025-09-13 06:17:18차지현
인보사 미국 진출 자신감?...코오롱티슈진, 1225억 조달[데일리팜=차지현 기자] 코오롱그룹의 바이오 자회사 코오롱티슈진이 대규모 자금 조달에 나섰다. 골관절염 유전자치료제 미국 품목허가와 상업화를 위해서다. 회사는 잇단 투자 유치와 인재 확보 등을 병행하며 재도약에 사활을 건 분위기다.1225억 규모 CB 발행 결정…"인보사 FDA 허가와 상업화 준비"12일 금융감독원에 따르면 코오롱티슈진은 이날 이사회를 열고 4회차 전환사채(CB) 발행을 의결했다. CB는 주식과 채권의 성격을 모두 지닌 주식연계채권이다. 채권자가 회사에 돈을 빌려주고 이자를 받다가, 주가가 오르면 주식으로 전환할 수 있다.이번에 코오롱티슈진이 발행하는 CB는 1225억원 규모다. 파나세아, 스틱호라이즌, IBKC-카스피안 T 8호 신기술투자조합 등 기관 투자자가 참여, 물량을 인수하는 형태다. 해당 CB는 표면이자율과 만기이자율이 모두 0%인 '빵빵채권'이다.CB 전환가액은 21만8090원이다. 코오롱티슈진은 2017년 코스닥 입성 당시 보통주가 아닌 증권예탁증권(KDR)로 상장했다. DR은 기업이 해외에서 주식을 발행할 경우 외국의 예탁기관이 현지에서 증권을 발행·유통해 원주와 상호 전환이 가능하도록 한 주식대체증서다.코오롱티슈진은 이번 CB 발행에서 신주 발행가액을 1 KDR 당 4만3618원으로 산출했다. 코오롱티슈진의 보통주 1주가 5KDR이라는 점을 고려하면 발행일 종가 대비 약 12.1% 할인한 수준이다. CB 발행을 결정한 12일 종가 기준 코오롱티슈진 주가는 4만9650원이었다.CB를 주식으로 전환할 수 있는 전환청구 기간은 오는 2026년 9월 26일부터 2030년 8월 26일까지다. 전환이 이뤄질 경우 발행 가능한 주식 수는 56만1694주로 전체 주식의 약 3.3%에 해당한다. 이번 CB에는 투자자가 만기 전 조기상환을 청구할 수 있는 풋옵션(매도청구권) 조항도 달렸다.코오롱티슈진은 이번 CB를 통해 조달한 자금을 인보사 미국 식품의약국(FDA) 품목허가와 상업화를 위한 준비에 사용할 계획이다. 세부적으로 올해 225억원, 내년 1000억원의 운영 자금을 배정했다.국내 허가 불발됐지만 미국서 기사회생 불씨, 미국 3상 총력인보사는 코오롱그룹 또다른 계열사 코오롱생명과학이 지난 2017년 7월 식품의약품안전처 허가를 받은 세계 최초 골관절염 유전자치료제다. 코오롱생명과학이 인보사 아시아 판권을, 코오롱티슈진은 미국과 유럽을 포함한 글로벌 전역 판권을 갖고 있다.인보사는 2019년 3월 미국 3상 진행 과정에서 핵심 성분 중 하나인 연골유래세포가 종양 유발 가능성이 높은 신장유래세포로 변경됐다는 사실이 드러나면서 논란을 빚었다. 이 여파로 식품의약품안전처는 인보사 품목허가를 취소했다. 이어 2019년 5월 미국 식품의약국(FDA)으로부터 임상중지 통보를 받았다.코오롱생명과학은 서울행정법원에 인보사 품목허가 처분 취소 소송을 제기했다. 그러나 서울행정법원은 2021년 식약처의 처분이 정당하다며 원고 패소 판결을 내렸다. 이어 지난해 초 2심 재판부까지 식약처의 손을 들어주는 판결을 내리면서 국내 재출시 가능성은 사라졌다.다만 미국의 경우 희망의 불씨가 남아 있다. 2020년 4월 FDA가 임상재개를 수용하면서다. 인보사의 국내 재기는 불발됐지만 세계 최대 의약품 시장인 미국 출시에 성공한다면 더 큰 반전의 계기를 마련할 수 있다. 코오롱티슈진은 2020년 12월부터 코오롱생명과학은 환자 투약을 재개했다. 미국 전역 80개 병원에서 환자 1000명을 대상으로 임상을 진행했고, 지난해 7월 환자 투약을 마무리했다. 코오롱티슈진은 향후 2년간 인보사 투약 환자를 대상으로 추적 관찰을 진행한다. 이 기간 인보사의 FDA 품목허가를 위한 준비를 병행해 FDA 승인 시기를 최대한 앞당기겠다는 게 회사 측 입장이다.특히 코오롱티슈진은 올 초 사법 리스크 해소 이후 인보사 회생 작업에 한층 속도를 내는 모습이다. 지난해 11월 서울중앙지방법원은 1심 판결에서 이웅열 코오롱 명예회장과 전직 임원 등에 무죄를 선고했다. 앞서 이웅열 명예회장 등은 2020년 인보사 성분 조작 등에 관여, 자본시장과 금융투자업에 관한 법률을 위반한 혐의로 기소된 바 있다.인보사에 대한 코오롱티슈진의 의지는 잇단 투자 유치 행보에서도 엿볼 수 있다. 코오롱티슈진은 지난 2월에도 565억원 규모 CB를 발행했다. 해당 CB 역시 표면 이자율과 만기 이자율이 모두 0%로, 유진투자증권, 한양증권, 키움증권, 한국투자증권 등이 인수했다. 코오롱티슈진은 2022년과 2024년에도 각각 330억원과 245억원 규모 CB를 발행, 외부에서 자금을 끌어왔다.코오롱티슈진은 모회사 코오롱으로부터도 지속해서 자금 수혈을 받아왔다. 코오롱은 지난 2021년부터 다섯 차례에 걸쳐 코오롱티슈진 제3자배정 유증에 참여했다. 코오롱은 코오롱티슈진에 ▲2021년 355억원 ▲2022년 388억원 ▲2023년 400억원 ▲2024년 478억원을 출자했다. 여기에 지난 1월 441억원 규모 코오롱티슈진 유상증자에 단독으로 참여, 자금을 추가로 투입했다.인재 확보에도 공을 들이고 있다. 코오롱그룹은 올 초 전승호 전 종근당 고문을 영입하고 코오롱티슈진 각자대표로 선임했다. 전 고문은 대웅제약을 1조 클럽 반열에 올려놓은 주역으로 꼽힌다. 전 고문은 서울대 약학대학 출신으로 2003년부터 작년 상반기까지 대웅제약에 21년간 몸 담았다. 대웅제약에서 전 대표는 라이선싱 팀장, 글로벌전략 팀장, 글로벌사업본부장 등을 거쳤다. 2018년 대웅제약 대표이사 사장으로 선임됐고 한 차례 연임을 통해 작년 초까지 대웅제약의 사령탑을 맡았다.전 고문은 지난해 초 대웅제약 사내이사 임기 만료 이후 대웅인베스트먼트, 아피셀테라퓨틱스 등 계열사 대표이사와 사내이사를 역임했다. 이후 대웅제약을 관두고 작년 5월부터 종근당에서 고문으로 경영 자문을 담당했다. 전 고문은 종근당에서 3개월간의 짧은 고문직 역할을 마치고 코오롱그룹으로 적을 옮겼다.2025-09-13 06:17:18차지현
오늘의 TOP 10
- 14천여 품목, 1월 무더기 인하…품목·인하율 아직도 '깜깜이'
- 2믿을건 임상 성공 뿐?...콜린알포 사수 벼랑 끝 총력전
- 3창고형약국, 조제용 슈도에페드린 무차별 판매 논란
- 4상장사 줄었지만 체급↑…바이오 IPO 시장 '옥석 가리기'
- 5[2025 결산] GMP 취소 법적 공방…생약 재평가 시동
- 6오늘부터 의사가 마약류 '식욕억제제' 처방시 투약내역 확인
- 7이 대통령 "탈모약·비만약 건보급여 가능성 검토하라"
- 8'키트루다' 약가협상 마무리...내달 적응증 급여 확대
- 91차 급여 두드리는 골형성촉진제...복지부 "적정성 검토"
- 10의약외품이 손발톱약으로 둔갑…약사회, 국민신문고 민원
-
순위상품명횟수
-
1타이레놀정500mg(10정)30,426
-
2판콜에스내복액16,732
-
3텐텐츄정(10정)13,671
-
4까스활명수큐액12,867
-
5판피린큐액12,851














![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
