총 21건
-
 지씨지놈, 상장 6개월...주주들 투자회수에 오버행 부담↑[데일리팜=차지현 기자] GC그룹 유전체 분석 계열사 지씨지놈 투자자가 상장 반 년 만에 대규모 지분 매각을 통해 투자금 회수(엑시트)에 나섰다. 지씨지놈 입장에서는 잔여 재무적 투자자(FI) 지분에 따른 오버행 부담과 주가 관리가 향후 핵심 과제로 떠올랐다.16일 금융감독원에 따르면 지노베이션1호사모투자 합자회사는 지난 9일부터 15일까지 다섯 차례에 걸쳐 지씨지놈 주식 98만9094주를 장내 매도했다. 1주당 평균 처분 단가는 7707원이다.세부적으로 지노베이션1호는 9일 25만9444주를 1주당 7165원에 매도했고 이튿날 10만주를 주당 7249원에 처분했다. 이어 12월 11일 53만1000주를 주당 7980원에 매도했고 다음날인 12일에는 9만5000주를 주당 8128원에 팔았다. 또 15일 3650주 주당 8053원에 추가 매도했다. 이번 매도를 통해 지노베이션1호가 확보한 금액은 76억원이다.지씨지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 이 회사는 올해 6월 10일 기술특례 제도를 통해 코스닥 시장에 상장했다. 상장 당시 공모가는 1만500원으로 책정됐다.지노베이션1호는 지씨지놈 FI이자 주요 주주다. 앞서 지노베이션1호는 2020년 12월 지씨지놈이 발행한 200억원 규모 전환사채(CB)를 인수하며 첫 투자를 단행했다. CB 전환가액은 주당 5625원으로 전액 보통주로 전환될 경우 355만5555주를 취득할 수 있는 구조다.지노베이션1호는 2022년 11월과 2024년 11월 두 차례에 걸쳐 해당 CB를 전량 보통주로 전환했다. 지씨지놈 상장 전 지노베이션1호 지분율은 18%로 녹십자에 이은 2대주주였다. 이후 공모 절차를 거치며 상장 직후 지분율은 15%로 낮아졌다.지노베이션1호의 대규모 지분 매각은 이번이 처음이 아니다. 이 펀드는 지씨지놈 상장 직후인 6월 11일 51만1111주를 주당 1만3817원에 매도했다. 이는 공모가 대비 32% 높은 수치로 전환가액 기준 취득 원가와 비교하면 2.5배에 달하는 가격이다. 이어 같은 달 12일 10만주를 주당 1만867원, 13일 5만5000주를 주당 1만8원, 18일 4만5000주를 주당 9252원에 각각 처분했다. 이들 매도 단가는 모두 전환가액 기준으로 1.6배 이상에 해당한다.이로써 상장 이후 지금까지 지노베이션1호는 170만205주를 처분해 167억원의 자금을 회수했다. 전환가액 기준으로 이번까지 매각한 물량의 취득 원가가 약 96억원인 점을 감안하면 지노베이션1호는 누적 약 72억원의 차익을 실현한 것으로 추산된다. 초기 취득 원가 대비 약 1.7배의 회수 성과를 거둔 셈이다.잔여 지분을 통한 추가 회수 여지도 남아 있다. 현재까지 처분한 물량은 전체 취득 주식의 48% 수준으로 12월 15일 기준 지노베이션1호 펀드는 185만5350주를 보유 중으로 처분 후 지분율은 약 8%다. 이는 15일 종가 7850원 기준 약 146억원 규모다. 현재 주가가 공모가에는 못 미치지만 초기 취득 단가를 웃돌고 있어 언제든 시장에 출회될 가능성이 남은 상태다.지씨지놈 입장에서는 FI의 지속적인 매도 물량을 소화하고 주가를 공모가 수준으로 회복시키는 게 남은 과제로 꼽힌다. 지씨지놈은 연구개발(R&D) 고도화와 검사 포트폴리오 확장을 통해 기업가치 제고를 꾀한다는 구상이다.회사는 기업공개(IPO) 당시 공모 자금을 다중암 조기 선별검사 제품의 암종 확대와 차세대염기서열분석(NGS) 플랫폼 추가, 검사 설비 증설과 검사실 확장 등에 투입해 중장기 성장 기반을 강화하겠다는 계획을 내놓은 바 있다. 특히 고부가가치 정밀진단 영역에서 제품 경쟁력을 높이고 국내 병원 네트워크를 넘어 글로벌 시장 매출 비중을 확대해 수익성 개선과 실적 가시성을 동시에 높이겠다는 전략이다.이 같은 성장 전략은 실적으로 가시화하는 모습이다. 지씨지놈은 올 3분기 누적 영업이익 10억원을 기록, 전년 동기 대비 흑자전환에 성공했다. 같은 기간 매출은 전년 동기 대비 26% 성장한 235억원으로 집계됐다. 검진 검사와 산과 검사의 매출 증가세가 전체 실적 성장을 견인했다는 평가다.2025-12-16 12:05:46차지현 기자
지씨지놈, 상장 6개월...주주들 투자회수에 오버행 부담↑[데일리팜=차지현 기자] GC그룹 유전체 분석 계열사 지씨지놈 투자자가 상장 반 년 만에 대규모 지분 매각을 통해 투자금 회수(엑시트)에 나섰다. 지씨지놈 입장에서는 잔여 재무적 투자자(FI) 지분에 따른 오버행 부담과 주가 관리가 향후 핵심 과제로 떠올랐다.16일 금융감독원에 따르면 지노베이션1호사모투자 합자회사는 지난 9일부터 15일까지 다섯 차례에 걸쳐 지씨지놈 주식 98만9094주를 장내 매도했다. 1주당 평균 처분 단가는 7707원이다.세부적으로 지노베이션1호는 9일 25만9444주를 1주당 7165원에 매도했고 이튿날 10만주를 주당 7249원에 처분했다. 이어 12월 11일 53만1000주를 주당 7980원에 매도했고 다음날인 12일에는 9만5000주를 주당 8128원에 팔았다. 또 15일 3650주 주당 8053원에 추가 매도했다. 이번 매도를 통해 지노베이션1호가 확보한 금액은 76억원이다.지씨지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 이 회사는 올해 6월 10일 기술특례 제도를 통해 코스닥 시장에 상장했다. 상장 당시 공모가는 1만500원으로 책정됐다.지노베이션1호는 지씨지놈 FI이자 주요 주주다. 앞서 지노베이션1호는 2020년 12월 지씨지놈이 발행한 200억원 규모 전환사채(CB)를 인수하며 첫 투자를 단행했다. CB 전환가액은 주당 5625원으로 전액 보통주로 전환될 경우 355만5555주를 취득할 수 있는 구조다.지노베이션1호는 2022년 11월과 2024년 11월 두 차례에 걸쳐 해당 CB를 전량 보통주로 전환했다. 지씨지놈 상장 전 지노베이션1호 지분율은 18%로 녹십자에 이은 2대주주였다. 이후 공모 절차를 거치며 상장 직후 지분율은 15%로 낮아졌다.지노베이션1호의 대규모 지분 매각은 이번이 처음이 아니다. 이 펀드는 지씨지놈 상장 직후인 6월 11일 51만1111주를 주당 1만3817원에 매도했다. 이는 공모가 대비 32% 높은 수치로 전환가액 기준 취득 원가와 비교하면 2.5배에 달하는 가격이다. 이어 같은 달 12일 10만주를 주당 1만867원, 13일 5만5000주를 주당 1만8원, 18일 4만5000주를 주당 9252원에 각각 처분했다. 이들 매도 단가는 모두 전환가액 기준으로 1.6배 이상에 해당한다.이로써 상장 이후 지금까지 지노베이션1호는 170만205주를 처분해 167억원의 자금을 회수했다. 전환가액 기준으로 이번까지 매각한 물량의 취득 원가가 약 96억원인 점을 감안하면 지노베이션1호는 누적 약 72억원의 차익을 실현한 것으로 추산된다. 초기 취득 원가 대비 약 1.7배의 회수 성과를 거둔 셈이다.잔여 지분을 통한 추가 회수 여지도 남아 있다. 현재까지 처분한 물량은 전체 취득 주식의 48% 수준으로 12월 15일 기준 지노베이션1호 펀드는 185만5350주를 보유 중으로 처분 후 지분율은 약 8%다. 이는 15일 종가 7850원 기준 약 146억원 규모다. 현재 주가가 공모가에는 못 미치지만 초기 취득 단가를 웃돌고 있어 언제든 시장에 출회될 가능성이 남은 상태다.지씨지놈 입장에서는 FI의 지속적인 매도 물량을 소화하고 주가를 공모가 수준으로 회복시키는 게 남은 과제로 꼽힌다. 지씨지놈은 연구개발(R&D) 고도화와 검사 포트폴리오 확장을 통해 기업가치 제고를 꾀한다는 구상이다.회사는 기업공개(IPO) 당시 공모 자금을 다중암 조기 선별검사 제품의 암종 확대와 차세대염기서열분석(NGS) 플랫폼 추가, 검사 설비 증설과 검사실 확장 등에 투입해 중장기 성장 기반을 강화하겠다는 계획을 내놓은 바 있다. 특히 고부가가치 정밀진단 영역에서 제품 경쟁력을 높이고 국내 병원 네트워크를 넘어 글로벌 시장 매출 비중을 확대해 수익성 개선과 실적 가시성을 동시에 높이겠다는 전략이다.이 같은 성장 전략은 실적으로 가시화하는 모습이다. 지씨지놈은 올 3분기 누적 영업이익 10억원을 기록, 전년 동기 대비 흑자전환에 성공했다. 같은 기간 매출은 전년 동기 대비 26% 성장한 235억원으로 집계됐다. 검진 검사와 산과 검사의 매출 증가세가 전체 실적 성장을 견인했다는 평가다.2025-12-16 12:05:46차지현 기자 -
 동아ST·그래디언트, 신약개발 공동연구 업무협약[데일리팜=노병철 기자] 동아에스티(대표이사 사장 정재훈)는 지난 21일 동아에스티 용인 연구단지에서 그래디언트 바이오컨버전스(대표이사 이진근)와 AI기반 오가노이드 및 유전체 분석을 활용한 신약개발 초기 단계 공동연구 업무협약을 체결했다고 22일 밝혔다.이번 협약은 양사의 기술력과 연구 역량을 결합해 예측 한계, 높은 비용, 장기 개발 기간 등 기존 신약개발의 구조적 문제를 극복하고 난치성 질환 치료제 개발을 앞당기기 위해 마련됐다.협약에 따라 양사는 ▲AI 기반 오가노이드 및 유전체 빅데이터 분석을 통한 신규 타깃 발굴 및 신약개발 ▲PDO(Patient-Derived Organoid,환자 유래 오가노이드)를 활용한 다양한 암종의 약물 반응 분석 및 정밀의료 기반 약물 스크리닝 ▲hiPSC(human induced Pluripotent Stem Cell, 역분화 줄기세포) 기반 뇌 오가노이드를 활용한 알츠하이머병, 타우병증 등 난치성 뇌질환 후보물질 유효성 검증을 위해 협력한다.그래디언트 바이오컨버전스는 임직원의 약 80% 이상이 연구진으로 구성된 기업으로 약1,000 종의 PDO와 유전체 정보(NGS) 데이터 기반의 오가노이드 뱅킹 시스템을 보유하고 있다. 독자적인 AI 플랫폼과 오가노이드 및 크리스퍼 유전자 가위(CRISPR-Cas9) 기술을 통해 신규 항암 타깃을 발굴하며, iPSC(induced Pluripotent Stem Cell, 유도만능줄기세포) 유래 오가노이드 구축 및 약물 스크리닝 서비스 등의 핵심 플랫폼을 보유한 오가노이드 기반 타깃 발굴 전문 기업이다.그래디언트 바이오컨버전스 이진근 대표는 “그래디언트 바이오컨버전스의 오가노이드 플랫폼과 동아에스티의 신약개발 역량이 만나, 신약개발 초기 단계의 정밀성과 효율성을 크게 높일 수 있을 것“이라며 “양사의 기술력과 자원을 결합해 신약개발을 더욱 신속하고 효과적으로 이끌어가겠다”고 말했다.동아에스티 김미경 연구본부장은 “양사가 보유한 기술력과 연구 역량이 결합되면 독자적인 약물 타깃 발굴과 효과적인 후보물질 선정이 가능해질 것이다”며 “그래디언트 바이오컨버전스와 긴밀히 협력해 혁신적인 연구 성과를 창출하고 글로벌 신약개발 경쟁력을 강화해 나가겠다”고 말했다.2025-08-22 09:44:08노병철
동아ST·그래디언트, 신약개발 공동연구 업무협약[데일리팜=노병철 기자] 동아에스티(대표이사 사장 정재훈)는 지난 21일 동아에스티 용인 연구단지에서 그래디언트 바이오컨버전스(대표이사 이진근)와 AI기반 오가노이드 및 유전체 분석을 활용한 신약개발 초기 단계 공동연구 업무협약을 체결했다고 22일 밝혔다.이번 협약은 양사의 기술력과 연구 역량을 결합해 예측 한계, 높은 비용, 장기 개발 기간 등 기존 신약개발의 구조적 문제를 극복하고 난치성 질환 치료제 개발을 앞당기기 위해 마련됐다.협약에 따라 양사는 ▲AI 기반 오가노이드 및 유전체 빅데이터 분석을 통한 신규 타깃 발굴 및 신약개발 ▲PDO(Patient-Derived Organoid,환자 유래 오가노이드)를 활용한 다양한 암종의 약물 반응 분석 및 정밀의료 기반 약물 스크리닝 ▲hiPSC(human induced Pluripotent Stem Cell, 역분화 줄기세포) 기반 뇌 오가노이드를 활용한 알츠하이머병, 타우병증 등 난치성 뇌질환 후보물질 유효성 검증을 위해 협력한다.그래디언트 바이오컨버전스는 임직원의 약 80% 이상이 연구진으로 구성된 기업으로 약1,000 종의 PDO와 유전체 정보(NGS) 데이터 기반의 오가노이드 뱅킹 시스템을 보유하고 있다. 독자적인 AI 플랫폼과 오가노이드 및 크리스퍼 유전자 가위(CRISPR-Cas9) 기술을 통해 신규 항암 타깃을 발굴하며, iPSC(induced Pluripotent Stem Cell, 유도만능줄기세포) 유래 오가노이드 구축 및 약물 스크리닝 서비스 등의 핵심 플랫폼을 보유한 오가노이드 기반 타깃 발굴 전문 기업이다.그래디언트 바이오컨버전스 이진근 대표는 “그래디언트 바이오컨버전스의 오가노이드 플랫폼과 동아에스티의 신약개발 역량이 만나, 신약개발 초기 단계의 정밀성과 효율성을 크게 높일 수 있을 것“이라며 “양사의 기술력과 자원을 결합해 신약개발을 더욱 신속하고 효과적으로 이끌어가겠다”고 말했다.동아에스티 김미경 연구본부장은 “양사가 보유한 기술력과 연구 역량이 결합되면 독자적인 약물 타깃 발굴과 효과적인 후보물질 선정이 가능해질 것이다”며 “그래디언트 바이오컨버전스와 긴밀히 협력해 혁신적인 연구 성과를 창출하고 글로벌 신약개발 경쟁력을 강화해 나가겠다”고 말했다.2025-08-22 09:44:08노병철 -
 차세대 유전자 침묵 치료, 'RNAi' 치료제 플랫폼에 대해핵산 치료제는 구성 성분에 따라 DNA 기반 약제와 RNA 기반 약제로 구분되며, RNA 기반 약제는 안티센스 올리고뉴클레오티드(antisense oligonucleotide, ASO), 유전자 발현을 억제하는 소형 간섭 RNA(small interfering RNA, siRNA), 마이크로RNA(miRNA), 메신저 RNA(mRNA), 그리고 아프타머(aptamer) 등이 있다.이 중 siRNA는 합성된 이중가닥 RNA(double-stranded RNA, dsRNA)로서, 센스 가닥(sense strand)과 안티센스 가닥(antisense strand)으로 구성되며, 일반적으로 19~25 염기쌍의 길이를 가지고 있다. 이 중 안티센스 가닥은 RNA 유도 침묵 복합체(RNA-induced silencing complex, RISC) 내에서 특정 mRNA를 인식하고 절단하는 가이드 역할을 한다.이러한 siRNA를 기반으로 하는 RNA 간섭(RNAi) 치료제의 개발은 2000년대 초반부터 본격적으로 시작되었으며, 약 20년에 걸친 기술 축적과 전달 플랫폼의 발전을 통해 상용화 단계에 도달하였다. 2018년, 트랜스사이레틴(transthyretin, TTR) 매개 가족성 아밀로이드 다발신경병증(hATTR) 치료제 파티시란(Patisiran)이 미국 FDA로부터 최초로 승인을 받으며 siRNA 기반 치료제의 상업화가 본격화되었다.이후 다양한 GalNAc conjugate(갈낙 접합체) 기반의 siRNA 치료제들이 연이어 FDA 승인을 획득하였다. 주요 승인 약제로는 2019년 급성 간성 포르피린증(acute hepatic porphyria, AHP) 치료제 기보시란(Givosiran), 2020년 원발성 옥살산뇨증 1형(primary hyperoxaluria type 1, PH1) 치료제 루마시란(Lumasiran), 2021년 고지혈증 치료제 인클리시란(Inclisiran), 2022년 hATTR 치료제 브루시란(Vutrisiran)이 있다.또한 2023년에는 PH1 치료제로 네도시란(Nedosiran), 2025년에는 A형 및 B형 혈우병 환자(항응고 인자 억제제 보유 여부와 무관)의 예방 치료제로 피투시란(Fitusiran)이 승인되었다.이러한 siRNA 기반 RNA 간섭(RNAi) 치료제 플랫폼은 암, 바이러스 감염, 유전성 대사질환 등 다양한 질환의 병태생리를 직접 조절할 수 있는 차세대 정밀의학 전략으로 주목받고 있으며, 이는 단순한 유전자 발현 억제를 넘어, 특정 병인 단백질의 발현을 선택적으로 차단함으로써 질병의 근원을 표적하는 질병 수정형(disease-modifying) 치료제로서의 가능성을 제시하고 있다. RNA(Ribonucleic acid, 리보핵산)는 무엇인가? 핵산은 생명체의 유전 정보를 저장하고 전달하는 데 핵심적인 역할을 하며, 그중 RNA는 진핵세포와 원핵세포 모두에서 유전자 발현 및 세포 내 조절 과정에 필수적인 고분자 생체분자로서, DNA와 함께 분자생물학의 센트랄 도그마(central dogma)를 구성하는 주요 요소이다.RNA는 주로 DNA의 유전 정보를 단백질로 전달하는 전령(messenger)의 역할로 인식되어 왔으나, 다양한 연구 결과에 따라 RNA는 단순한 정보 매개체를 넘어 효소적 기능, 유전자 발현 조절, 구조적 지지, 면역 조절 인자 등 폭넓은 생물학적 기능을 수행하는 분자로 밝혀졌다. 이에 따라 RNA는 단백질과 동등하거나 그 이상으로 기능적 다양성을 지닌 핵심 생체분자로 평가되고 있다.RNA는 리보오스를 포함한 단일가닥 핵산으로 구성되며, DNA와 달리 염기로 우라실(uracil)을 포함하고, 2′-탄소 위치에 하이드록시기(2′-OH group)를 갖는 리보오스를 지닌다. 이러한 구조적 특성은 RNA에 높은 구조적 유연성과 화학적 반응성을 부여하여, 다양한 입체 구조를 형성하고 특정 단백질이나 다른 핵산과 선택적으로 결합하며, 심지어 효소적 반응을 촉매할 수 있는 생화학적 기반이 된다.실제로 RNA는 염기 서열에 의한 상보적 결합 외에도 루프(loop), 헤어핀(hairpin), 스템(stem), 벌지(bulge), 가상매듭(pseudoknot) 등 복잡한 이차 및 삼차 구조를 형성하며, 이를 통해 단백질-리간드 상호작용, 효소 활성, 핵-세포질 간 수송, 세포 내 위치 특이적 기능 수행 등에 관여한다.RNA는 유전자 발현 조절, 세포분화, 세포주기, 세포사멸, 스트레스 반응, 면역 조절 등 거의 모든 생리적·병리적 현상에 직·간접적으로 관여하며, DNA로부터 유래된 정보를 전달하는 역할외에도 전사(transcription)와 번역(translation) 간의 연결을 매개하고 유전자 발현의 정밀한 조절자로 작용한다.특히 진핵세포에서는 RNA가 전사 후 변형(post-transcriptional modification), 스플라이싱(splicing), RNA 편집(RNA editing), 핵-세포질 수송(nuclear export), 안정성 조절, 국소화(localization) 등 유전자 발현을 다양한 수준에서 정교하게 조절한다하지먼 RNA의 기능 이상은 다양한 질환의 발병과 밀접하게 연관되어 있다. 즉 RNA의 안정성 혹은 조절 기전이 교란되면 특정 단백질의 비정상적 발현이 초래되며, 이는 암, 신경퇴행성 질환, 심혈관 질환, 자가면역 질환 등 다양한 병태생리적 상태를 유발하거나 악화시킬 수 있다.최근 연구에 따르면 RNA의 구조적 변이, 염기서열 돌연변이, 또는 RNA-단백질 상호작용의 이상은 질환의 새로운 병인으로 부상하고 있으며, RNA 수준에서의 진단 및 치료 접근은 생명과학의 주요 연구 영역으로 부각되고 있다.RNA에는 어떤 종류가 있는가? RNA는 그 기능에 따라 여러 유형으로 분류된다(Figure 1). 가장 기본인 형태는 전령 RNA(messenger RNA, mRNA)로, DNA의 유전 정보를 복사하여 리보솜으로 전달하며 단백질 합성에 직접 관여한다. 전이 RNA(transfer RNA, tRNA)는 아미노산을 리보솜으로 운반하는 역할을 하며, 리보솜 RNA(ribosomal RNA, rRNA)는 리보솜의 구조적 및 촉매적 핵심 요소로 기능한다.이 외에도 최근에는 유전자 발현을 정밀하게 조절하는 비번역 RNA(non-coding RNA)들이 주목받고 있다. 예를 들어, 소간섭 RNA(small interfering RNA, siRNA), 마이크로 RNA(microRNA, miRNA), 긴 비암호화 RNA(long non-coding RNA, lncRNA) 등은 세포 내 유전자 조절 네트워크의 핵심 조절자로 작용한다. 1. mRNA(messenger RNA, 전령 RNA) mRNA가 전달하는 유전 정보는 염기의 종류, 배열, 그리고 길이에 의해 결정된다. DNA는 아데닌(A), 구아닌(G), 시토신(C), 티민(T)의 네 가지 염기로 구성되어 있는 반면, RNA는 티민 대신 우라실(U)을 포함한다. 유전 정보는 이러한 염기의 조합으로 구성되며, RNA 중 mRNA는 전사(transcription) 후 모든 처리가 완료된 형태로, 5′-cap 구조와 poly(A) tail(폴리 A 꼬리)을 갖추고 있으며, 스플라이싱(splicing)도 완료된 상태이다.mRNA는 DNA의 유전 정보를 기반으로 리보솜에서 단백질을 합성할 때 번역 서열(translation sequence)로 작용하므로, 세포 내에서 mRNA의 발현 수준을 조절하는 것은 생명 현상을 통제하는 데 매우 중요하다.성숙한 mRNA는 긴 poly(A) tail을 가지며, 이 아데닌 꼬리는 mRNA의 분해를 방지하고 안정적인 기능 수행을 돕는다. 그러나 시간이 지나면 탈아데닐화(deadenylation) 효소에 의해 이 꼬리는 점차 짧아지게 되고, 이는 mRNA 분해의 신호로 작용한다. 반면, mRNA의 말단에 혼합 꼬리(mixed tail)가 형성될 경우, 이는 아데닌 꼬리의 제거 과정을 방해하여 mRNA의 분해를 억제하고 안정성을 높이는 것으로 알려져 있다. 따라서 혼합 꼬리는 mRNA의 생존을 유지하는 데 중요한 조절 요소로 작용한다.2. ncRNA(non-coding RNA, 비암호화 RNA) 센트럴 도그마에 따르면, 단백질을 암호화하지 않는 RNA는 비암호화 RNA(non-coding RNA, ncRNA)로 분류된다. 비록 ncRNA는 단백질을 직접 생성하지는 않지만, 전사 후 조절(post-transcriptional regulation) 및 후성유전학(epigenetic) 기전에 관여하는 중요한 조절자로 밝혀지고 있다.ncRNA는 기능적 역할에 따라 크게 하우스키핑 비암호화 RNA(housekeeping ncRNA)와 조절 비암호화 RNA(regulatory ncRNA)로 나뉘며, 그 길이에 따라 다시 분류된다. 일반적으로 200개 이하의 뉴클레오타이드(nucleotide)로 구성된 경우를 작은 ncRNA(small ncRNA 또는 short/medium ncRNA)라 하고, 200개 이상의 뉴클레오타이드를 포함할 경우 긴 ncRNA(long non-coding RNA, lncRNA)로 분류된다. 이들은 기능, 전사 후 가공, 상호작용 양상 등에 따라 더욱 세분화된다.1) Housekeeping ncRNA(하우스키핑 비암호화 RNA) ① tRNA(transfer RNA, 운반 RNA) tRNA는 단백질 합성 과정에서 mRNA의 코돈(codon)에 상보적으로 결합하는 안티코돈(anticodon)을 가지고 있으며, 해당 코돈에 대응하는 아미노산을 리보솜으로 운반하는 역할을 한다. 즉, mRNA의 코돈을 해독하여 해당 아미노산을 정확히 리보솜에 전달하고, 폴리펩타이드 사슬의 신장(elongation) 과정에 기여함으로써 단백질 합성의 핵심 요소로 작용한다.tRNA는 전사된 직후 바로 기능하는 것이 아니라 pre-tRNA라는 전구체 형태로 먼저 생성된다. 이 pre-tRNA는 5′ 말단과 3′ 말단에 불필요한 염기 서열을 포함하며, 일부는 안티코돈 고리(anticodon loop)에 인트론(intron)을 포함하기도 한다. 성숙한 tRNA는 이러한 전사 후 가공 과정을 통해 구조적으로 안정화되고 생물학적 활성을 갖춘다.② rRNA(ribosomal RNA, 리보솜 RNA) rRNA는 리보솜의 핵심 구성 요소로, 다양한 리보솜 단백질과 결합하여 기능적 리보솜 복합체를 형성한다. 리보솜은 세포 내 단백질 생합성의 중심 기구이며, rRNA는 전체 세포 내 RNA의 약 80%를 차지할 정도로 풍부하게 존재한다.rRNA는 단순한 구조적 지지체에 그치지 않고, 촉매적 기능까지 수행한다. 특히, 리보솜의 대단위 서브유닛(large subunit)에 존재하는 rRNA는 펩티딜전이효소(peptidyl transferase)로 작용하여 아미노산 사이의 펩타이드 결합 형성을 촉진한다. 이는 RNA 자체가 효소 활성을 수행하는 대표적 예로, rRNA가 리보자임(ribozyme)으로 기능함을 보여준다.2) Regulatory ncRNA(조절 비암호화 RNA) 인간 유전체는 약 30억 개의 염기쌍(base pairs)으로 구성되어 있으나, 이 중 약 1% 정도만이 단백질을 암호화하는 유전자로 기능하는 것으로 오랫동안 여겨져 왔다. 이러한 전통적인 관점을 검증하고 유전체의 기능적 요소를 체계적으로 규명하기 위해 시작된 국제적 연구가 바로 ENCODE(Encyclopedia of DNA Elements) 프로젝트이다.ENCODE 프로젝트를 통해 밝혀진 핵심 사실은, 과거에 ‘쓰레기 DNA(junk DNA)’ 혹은 ‘암흑 물질(dark matter)’로 간주되었던 비암호화 영역이 실제로 생화학적 활성 및 생물학적 기능을 수행한다는 점이다. 이는 ncRNA가 단순한 유전 정보의 부산물이 아니라, 유전자 발현을 정밀하게 조절하는 중요한 조절자(regulator)로 기능할 수 있음을 의미한다.특히, 차세대 염기서열 분석기법(NGS) 등 기술의 발전으로 유전체 전체의 전사(transcription) 양상을 정밀하게 분석할 수 있게 되었고, 그 결과 유전체의 실제 전사 비율이 단 1%가 아니라 약 80%에 이른다는 사실이 밝혀졌다. 이는 유전체의 대부분이 기능적 목적을 가지고 의도적으로 전사된다는 점을 시사한다.이러한 발견은 ncRNA, 특히 조절 비암호화 RNA(regulatory ncRNA)의 중요성을 부각시켰으며, 이들은 전사 후 조절, 염색질 구조 변형, 유전자 발현 억제 및 활성화, 세포 분화, 그리고 항상성 유지 등 다양한 생명 현상에 핵심적인 역할을 수행하는 것으로 밝혀졌다.① Small ncRNA(sncRNA, 작은 비암호화 RNA) a. miRNA(microRNA, 마이크로 RNA) miRNA는 RNA 간섭(RNA interference, RNAi)과 유사한 기전을 따르는, 자연적으로 존재하는 유전자 발현 조절 메커니즘이다. 현재까지 인간에서 수백 종의 miRNA가 확인되었으며, 전체적으로는 50,000종 이상이 존재할 것으로 추정된다.miRNA는 일반적으로 약 22개의 염기로 구성된 짧은 단일가닥 RNA이며, 표적 mRNA와 부분적으로 상보적인 염기서열을 인식하여 결합한다. 이를 통해 mRNA의 번역을 억제하거나 분해를 유도함으로써 유전자 발현을 음성 조절(negative regulation)한다.miRNA는 특히 개체 발생, 세포 분화, 세포 주기 조절, 세포사멸, 암 억제 또는 촉진 등 다양한 생명현상의 조절자로 기능하며, 이의 이상 발현은 암, 심혈관 질환, 신경계 질환 등 여러 병태생리학적 상태와 밀접한 관련이 있는 것으로 알려져 있다.b. siRNA(small interfering RNA, 소간섭 RNA) siRNA는 보통 인위적으로 합성된 긴 이중가닥 RNA(dsRNA)를 세포 외부에서 도입한 후, 세포 내에서 ATP-의존성 RNase인 Dicer에 의해 절단되어 생성되는 길이 21~23 염기쌍의 짧은 dsRNA이다.siRNA는 성숙한 miRNA(mature miRNA)와 구조적으로 유사하나, 기원과 기능적 특성에서 차이를 보인다. 특히 표적 mRNA와의 염기서열 상보성에 있어서 뚜렷한 차이가 있다. siRNA는 표적 mRNA와 완전한 상보성을 이루어 정확한 표적 유전자만을 선택적으로 억제하는 반면, miRNA는 일반적으로 불완전한 상보성을 바탕으로 여러 유전자의 번역을 동시에 조절할 수 있다.이러한 차이로 인해 siRNA는 고특이적 유전자 침묵(specific gene silencing)에 적합하며, miRNA는 보다 광범위한 유전자 조절(global regulation)에 기여하는 특성을 가진다.c. snRNA(small nuclear RNA, 작은 핵 RNA) snRNA는 주로 핵 내에서 pre-mRNA의 스플라이싱(splicing)에 관여하는 짧은 RNA 분자이다. 대표적으로 U1, U2, U4, U5, U6 등의 snRNA가 스플라이스좀(spliceosome)이라는 RNA-단백질 복합체(RNP complex)를 형성하여, 인트론(intron)의 제거 및 엑손(exon)의 연결에 필수적인 역할을 수행한다.snRNA는 mRNA 성숙 과정에서 엑손-인트론 경계의 인식과 절단을 통해 유전자 발현의 정밀한 조절을 수행하는 핵심 인자로 기능한다.d. snoRNA(small nucleolar RNA, 작은 인 RNA) snoRNA는 주로 세포핵 내 핵소체(nucleolus)에 존재하는 RNA로, rRNA의 성숙 및 가공에 핵심적인 역할을 한다. snoRNA는 pre-rRNA(전구체 리보솜 RNA)와 상보적인 염기서열을 바탕으로 결합하여, 특정 위치의 염기를 화학적으로 변형하거나 절단 위치를 안내한다.snoRNA의 주요 기능은 rRNA 염기에 대해 2′-O-메틸화(2′-O-methylation) 또는 위우리딘(pseudouridine)으로의 전환을 유도한다. 이러한 변형은 rRNA의 구조적 안정성과 리보솜 기능에 매우 중요하다. 또한 snoRNA는 pre-rRNA가 정확한 위치에서 절단되도록 도와줌으로써, 최종적으로 기능을 갖춘 성숙한 rRNA의 형성에 기여한다.② long ncRNA(lncRNA, 긴 비암호화 RNA) lncRNA는 단백질을 직접 암호화하지 않지만, 포유류 전사체(transcriptome) 내에서 비교적 풍부하게 존재하며 세포 기능에 다양한 방식으로 기여한다. 특히, lncRNA는 염색질 구조 조절 효소(chromatin-modifying enzyme)를 모집하거나 그 활성을 조절함으로써, 표적 유전자의 전사 활성 조절에 관여하는 것으로 잘 알려져 있다.lncRNA의 생물학적 기능은 크게 세 가지 기전으로 요약될 수 있다. 첫째, 시스(cis) 또는 트랜스(trans) 위치에서 전사 조절자(transcriptional regulator)로 작용하여, 인접 유전자의 발현을 직접 조절하거나, 떨어진 위치에 존재하는 유전자에 영향을 미친다.둘째, RNA 가공(splicing 등) 과정이나 전사 후(post-transcriptional) 조절, 또는 단백질 활성을 조절하는 기능을 수행한다. 이 경우 lncRNA는 특정 단백질 또는 RNA와 상호작용함으로써 기능적 복합체를 형성하거나, 조절자의 기능을 매개하는 플랫폼으로 작용한다.셋째, 일부 lncRNA는 핵 내 도메인(nuclear domain)의 구조적 구성에 기여하여, 세포핵 내 공간적 조직화와 기능적 구획화를 조절하는 역할을 수행한다. 이는 핵 내 RNA-단백질 복합체 형성과 같은 고차원적인 구조적 조절과 연관된다.lncRNA는 일반적으로 조직 또는 세포 유형 특이적인 발현 양상을 보이며, 단일 세포당 평균적으로 1개 미만의 사본만 검출되는 경우가 많다. 그러나 특정 조직이나 핵의 특정 구획에서는 높은 수준으로 발현되어, 기능적 다양성과 세포 간 복잡성을 더욱 증가시키는 요인으로 작용한다.특히, lncRNA는 개체 발생, 세포 분화, 노화, 스트레스 반응 등 다양한 생리적 과정뿐 아니라, 암의 발생 및 진행과 같은 병리적 현상에서도 중요한 조절 인자로 기능함이 밝혀지면서, 분자생물학 및 암 연구 분야에서 활발한 주목을 받고 있다.RNA 침묵(RNA silencing)은 어떤 현상인가? 생명체 내에서 유전자 발현은 정교한 조절 기전에 의해 통제되며, 이러한 조절은 개체의 발생, 항상성 유지, 외부 자극에 대한 반응, 병리적 상태에서의 적응 등 다양한 생물학적 과정에 핵심적인 역할을 한다. 이 가운데 유전자 침묵(gene silencing)은 특정 유전자의 발현을 억제하거나 완전히 차단하는 생물학적 현상이다.유전자 침묵(Gene silencing)에는 전사 시 유전자 침묵(transcriptional gene silencing, TGS)와, 전사 후 유전자 침묵(post-transcriptional gene silencing, PTGS)이 존재한다. 이 중 TGS는 일반적으로 DNA 메틸화(DNA methylation), 히스톤 변형(histone modification), 이질 염색질 형성(heterochromatinization) 등의 후성유전학적 메커니즘에 의해 매개되며, 유전자 접근성을 구조적으로 차단함으로써 발현을 억제한다.RNA 침묵(RNA silencing)은 유전자 침묵의 하위 개념으로, 주로 RNA 분자에 의해 매개되는 전사 후 유전자 침묵(PTGS) 기전을 지칭한다. RNA 침묵은 1990년대 후반, 식물과 동물, 곰팡이 등 다양한 진핵생물에서 확인되었으며, 진화적으로 보존된 염기서열 특이적 유전자 조절 기전으로 기능한다.RNA 침묵의 중심에는 짧은 비암호화 RNA 분자들, 즉 siRNA, miRNA, piRNA가 있으며, 이들은 각각 고유한 기원과 작용 기전을 통해 표적 mRNA의 발현을 억제한다.miRNA는 내인성 전사체로부터 유래하며, 개체의 발달, 세포 분화, 세포 주기, 세포사멸 등 생리적 과정뿐만 아니라 암, 심혈관 질환, 신경계 질환 등의 병태생리적 상태에서 정밀한 유전자 조절자로 기능한다.siRNA는 외부에서 유래된 dsRNA에 의해 형성되며, 실험적 유전자 침묵 기법이나 RNA 간섭 기반 치료제에 직접적인 유전자 억제 도구로 활용되고 있다.piRNA는 주로 생식세포에서 발현되며, 트랜스포존 억제, 유전체 안정성 유지, 세포 계통 유지 등 특수한 기능을 수행한다.RNA 침묵은 다양한 진핵생물에서 보편적으로 나타나며, 바이러스 감염에 대한 방어 기전, 전이 요소 억제, 비정상적 전사체 제거 등 세포 수준의 품질관리 및 유전체 보호 시스템으로 작용한다. 이러한 점에서 RNA 침묵은 단순한 유전자 억제를 넘어 생물학적 균형과 유전체 기능 유지의 핵심 축으로 간주된다.최근 RNA 침묵 기전은 치료 표적 및 플랫폼 기술로도 활발히 연구되고 있으며, siRNA 기반 치료제, antisense oligonucleotide(ASO) 기술 등은 RNA 침묵 원리를 기반으로 개발된 RNA 기반 정밀 의약품으로 발전하여 다양한 질환에서 임상적으로 응용되고 있다.RNA 간섭(RNA interference, RNAi)은 어떤 현상인가? RNAi는 1998년 Andrew Fire와 Craig Mello가 예쁜꼬마선충(Caenorhabditis elegans)을 대상으로 한 실험에서 처음 보고한 현상으로, 외부에서 도입된 이중가닥 RNA(dsRNA)가 세포 내 특정 mRNA를 인식하고 이를 선택적으로 분해함으로써 유전자 발현을 억제하는 고유의 생물학적 기전이다. 이 발견은 유전자 발현 조절에 대한 이해를 근본적으로 전환시켰으며, 두 연구자는 해당 업적으로 2006년 노벨 생리의학상을 수상하였다.RNA 침묵은 유전자 발현 억제를 유도하는 상위 개념이고, 그 중 RNAi는 기전이 명확히 규명되고 약물화 가능성이 높은 대표적인 하위 경로에 해당한다. RNAi는 염기서열 특이적 방식으로 작용하여, 표적 유전자의 발현을 정밀하게 제어할 수 있는 장점을 지니며, 바이러스 방어, 전이인자 억제, 후성유전 조절, 발생 및 분화 조절 등 다양한 생물학적 과정에 기여한다.특히 RNAi는 유전자 기능 연구, 질병 모델링, 표적 유전자 억제를 통한 치료제 개발 등 기초연구 및 임상분야 모두에서 응용 가능성이 높은 기술로 주목받고 있으며, siRNA 기반 치료제는 이러한 RNAi 원리를 임상에 성공적으로 도입한 대표적인 예로 평가되고 있다.소간섭 RNA(small interefering RNA, siRNA)는 무엇인가? siRNA는 RNAi 현상을 매개하는 대표적인 dsRNA로, 특정 mRNA의 발현을 염기서열 특이적으로 억제하는 기능을 수행한다. siRNA는 miRNA와 달리 전사산물의 절단(cleavage)을 직접 유도하는 강력한 침묵 효과를 나타낸다.이는 특히 바이러스 유전체, 종양 특이 유전자, 병리적 유전자 돌연변이 등을 표적으로 하는 데 적합하다. 이러한 특이성과 효능을 바탕으로 siRNA는 유전자 기능 연구뿐 아니라 질병 치료를 위한 유전자 기반 약물 플랫폼으로 빠르게 발전하고 있다.하지만, siRNA는 그 자체의 불안정성, 세포막 투과성 부족, 면역 자극 가능성 등의 한계도 지니고 있어, 이를 극복하기 위한 다양한 전달 시스템(delivery system) 개발이 병행되고 있다. 특히, 갈낵(GalNAc) 기반 간세포 표적 전달 시스템은 siRNA 치료제의 성공적 상용화에 핵심적인 기술로 평가된다.RNAi는 외부 또는 내부에서 유래된 dsRNA에 의해 유도되며, siRNA는 RNAi 경로의 핵심 매개체로 작용한다. siRNA는 RNAi이라 불리는 다단계 과정을 통해 유전자 발현을 억제하는 데 핵심적인 역할을 한다(Figure 1). 첫 번째 단계, dsRNA의 세포 내 유입과 Dicer에 의한 절단 siRNA는 주로 외인성 또는 인공적으로 도입된 dsRNA의 절단에 의해 생성된다. 일단 dsRNA가 세포 내로 유입되면 세포질(cytoplasm)에서 작용을 시작한다. 자연 상태에서는 긴 dsRNA 또는 전구체(pre-siRNA)가 Dicer라는 RNase III 계열의 효소에 의해 절단되어 siRNA가 생성된다. 그러나 합성 siRNA는 21~23개 염기쌍의 짧은 이중가닥 RNA로 구성되며, 이미 Dicer 가공 단계를 생략한 형태로 설계되어 있다.두번째 단계, RNA 유도 침묵 복합체(RNA-induced silencing complex, RISC) 형성과 가이드 스트랜드 선택 세포질 내에서 siRNA는 RISC와 결합하게 된다. RISC는 Argonaute(AGO) 단백질을 핵심으로 하는 다단백 복합체이며, siRNA는 이 복합체에 의해 가이드 가닥(guide strand)와 패신저 가닥(passenger strand)로 분리된다. 이 과정에서 AGO2는 패신저 가닥을 제거하거나 분해하며, 가이드 가닥만이 RISC에 안정적으로 결합된다. 가이드 가닥은 이후 표적 mRNA의 염기서열을 인식한다.세 번째 단계, mRNA 인식 및 절단(유전자 침묵 유도) 가이드 가닥이 결합된 활성화된 RISC는 세포질 내에 존재하는 상보적 염기서열을 가진 mRNA를 탐색한다. siRNA와 표적 mRNA가 완전한 상보성을 이루는 경우, AGO2의 엔도뉴클레아제 활성이 유도되어 표적 mRNA를 특정 위치에서 절단(cleavage)하게 된다. 절단된 mRNA는 이후 세포 내 핵산 분해효소에 의해 빠르게 분해되며, 이는 궁극적으로 해당 유전자의 단백질 발현 억제로 이어진다.이러한 유전자 침묵은 염기서열 특이적이며, 시간적으로 수 일에서 수 주 이상 지속될 수 있으며, 반복 투여 시 누적 효과를 기대할 수 있다. 또한, siRNA는 번역 후 단계에 작용하기 때문에, 단백질 발현을 정밀하게 조절할 수 있는 장점이 있다.RNA 기반 치료제(RNA-based therapeutics)란 무엇인가? RNA 기반 치료제는 특정 유전자 또는 병리적 단백질의 발현을 직접적으로 조절하거나, 필요한 단백질을 체내에서 직접 합성하도록 유도함으로써 질병의 원인 자체를 정밀하게 조절할 수 있는 치료 전략이다. 이러한 치료제는 RNA의 구조적 및 기능적 다양성에 따라 여러 유형으로 분류된다.대표적인 RNA 기반 치료제에는 단백질 생성을 직접 유도하는 mRNA 치료제, 특정 mRNA를 분해하거나 스플라이싱을 조절하는 ASO, RNAi 기전을 통해 유전자 발현을 억제하는 siRNA 및 miRNA 유사체, 특정 단백질에 선택적으로 결합하여 기능을 저해하는 RNA 압타머(aptamer) 등이 있다.이들 치료제는 유전자 수준의 정밀한 조절이 필요한 질환에서 특히 유효성이 크며, 암, 유전질환, 감염병, 대사질환 등 다양한 분야에서 치료 효과가 확인되고 있다.RNA 기반 치료제의 가장 큰 강점은 염기서열 상보성에 기반한 높은 표적 특이성과 설계의 유연성이다. 환자의 유전 정보나 발현 프로파일에 따라 맞춤형으로 표적을 설계할 수 있으며, 기존의 항체나 저분자 화합물로는 접근이 어려운 내재적 유전자 조절 단계에 직접 개입할 수 있다는 이점이 있다.그러나 RNA 분자의 구조적 불안정성, 면역 자극 가능성, 세포 내 전달의 어려움은 여전히 극복해야 할 중요한 과제로 남아 있다. 이를 해결하기 위해 지질 나노입자(lipid nanoparticle, LNP), 갈낙(GalNAc) 접합체, 엑소좀(exosome), 바이러스 벡터 등 다양한 전달 기술이 병행 개발되고 있으며, RNA 분자 자체에 대한 화학적 변형 연구 또한 활발히 진행 중이다.RNAi 기반 치료제(RNA interference-based therapeutics)란 무엇인가? RNAi는 짧은 dsRNA 조각이 세포 내 RNA 유도 침묵 복합체(RISC)에 의해 가이드되어, 상보적인 서열을 갖는 표적 mRNA를 절단함으로써 유전자 발현을 억제한다. 이 과정은 고도로 염기서열 특이적인 방식으로 이루어지며, 세포 내에서 자연스럽게 일어나는 중요한 방어 및 조절 기전이다.RNAi 기반 치료제는 병리적 유전자의 발현을 직접적으로 차단함으로써, 단백질 생성 자체를 근본적으로 억제할 수 있는 전략이다. 이는 기존의 단백질 표적 저해제들이 개입하기 어려운 전사 후(post-transcriptional) 단계에 개입할 수 있다는 점에서 근본적으로 다른 치료 접근법을 제공한다. 특히 유전자 과발현 또는 독성 단백질의 생성이 질병의 주요 병태기전인 경우에 매우 적합하며, 유전질환, 암, 간질환, 감염병 등 다양한 질환에서 임상적 적용이 활발히 진행되고 있다.RNAi 기반 치료제는 작용 기전에 따라 크게 세 가지로 구분된다. 첫째, siRNA는 화학적으로 합성된 짧은 dsRNA로, 표적 mRNA에 대해 높은 서열 특이성을 갖는다. GalNAc(갈낙) 기반 간 표적화 기술, 리포솜 또는 지질나노입자(LNP) 기반 세포 내 전달 기술을 활용하여 체내 적용이 가능하며, 현재 대부분의 RNAi 치료제가 이 플랫폼을 기반으로 한다.둘째, shRNA(short hairpin RNA)는 플라스미드나 바이러스 벡터를 통해 세포 내에서 안정적으로 발현되며, 지속적인 유전자 억제를 유도하는 구조이다. 주로 세포를 체외에서 조작하는 ex vivo 유전자 치료 전략에 활용된다.셋째, miRNA 유도체는 내인성 microRNA의 기능을 모방하거나 경쟁적으로 억제하여, 보다 광범위한 유전자 네트워크를 조절하는 방식으로 개발 중이다. 이는 특정 유전자뿐 아니라 관련된 다수의 유전자를 동시에 조절할 수 있는 장점이 있다.따라서 RNAi 기반 치료제는 유전자 수준에서의 정밀 제어, 고특이성, 그리고 효율적인 발현 억제라는 특성을 지니며, 기존의 저분자 화합물이나 단백질 기반 치료제와는 차별화되는 생물학적 전략을 제공한다.실제로 Givosiran, Lumasiran, Inclisiran 등은 각각 급성 간성 포르피린증(AHP), 원발성 옥살산뇨증 1형(PH1), 고지혈증 등의 적응증으로 다수 국가에서 시판 승인을 획득하였으며, 이는 RNAi 기술이 실용적인 치료 플랫폼으로 진입했음을 보여주는 중요한 이정표가 되었다.GalNAc-siRNA란 무엇인가? siRNA는 분자량이 작고 음전하를 띠는 친수성 분자로서 세포막을 자발적으로 통과하기 어려우며, 혈중에서 RNase에 의해 쉽게 분해되는 한계를 지닌다. 이러한 점에서 siRNA의 안정적이고 표적 특이적인 전달은 치료 효과를 극대화하기 위해 반드시 극복되어야 할 과제이다.이에 따라 다양한 siRNA 전달 시스템(delivery vector)이 개발되어 왔으며, GalNAc conjugate, 지질 나노입자(lipid nanoparticle, LNP), 고분자 기반 전달체 등 다양한 전달 플랫폼이 개발되고 있으며, 이들은 siRNA의 생체 내 안정성 및 조직 특이적 투과성을 개선하는 데 중요한 역할을 하고 있다.이 중 약물을 세포 표면 수용체 리간드와 결합시키는 방식(GalNAc conjugate)은 표적 약물 전달을 위한 유망한 경로로 보고되고 있다. 이러한 수용체는 특정 세포 유형에만 발현되며, 일부 질환에서는 특정 장기나 조직에서 과발현된다.3방향 GalNAc(triantennary GalNAc)은 siRNA의 안티센스(antisense) 사슬 3′ 말단과 결합하여 GalNAc-siRNA conjugate를 형성한다. siRNA는 화학적으로 직접 합성할 수 있으며, 또는 효소 전사로 얻어진 긴 이중가닥 RNA를 세포질 RNase III 엔도뉴클레아제인 Dicer의 작용으로 절단하여 21~23 nt 길이의 siRNA를 생성할 수 있다. 이 siRNA는 3′ 말단에 두 개의 돌출된 뉴클레오타이드, 5′ 말단에 인산기, 그리고 가운데에 19 nt의 상보적인 이중가닥 영역을 가진다.따라서 siRNA와 GalNAc을 결합시켜 피하 주사로 투여하면, GalNAc-siRNA conjugate가 ASGPR(Asialoglycoprotein receptor)에 결합되고, 이어 ASGPR 매개 세포 내 유입(endocytosis)을 통해 세포 내로 들어가게 된다(Figure 2).GalNAc은 간세포 이외의 조직에서는 거의 발현되지 않는 수용체에 대한 높은 결합 친화성을 가지므로, siRNA 분자의 간 특이적(targeted delivery to hepatocytes) 전달을 가능하게 한다. GalNAc-siRNA의 작용 기전은? GalNAc-siRNA의 작용 기전의 핵심은, GalNAc-siRNA conjugate가 간세포 표면의 수용체(asialoglycoprotein receptor, ASGPR)에 선택적으로 인식되고 전달된다는 점에 있다. siRNA는 본래 음전하를 띠고 분자량이 큰 친수성 분자로서, 세포막을 자발적으로 통과하기 어렵다. 하지만 GalNAc으로 변형된 siRNA는 간세포에 특이적으로 발현되는 ASGPR를 통해 표적 조직으로 선택적 전달될 수 있으며, 효율적인 세포 내 유입도 가능하게 된다.ASGPR은 간소엽(liver lobule) 내 간 실질세포(hepatocyte)의 혈관사이 공간(hepatic sinusoid space) 표면에 주로 발현되는 수용체로, GalNAc-siRNA conjugate가 체내에 주입되면 GalNAc-siRNA-ASGPR 복합체는 세포 내로 유입되어 엔도솜(endosome) 내에서 분리된다. 이후 siRNA는 엔도솜으로부터 방출되고, GalNAc은 분해되어 제거된다. ASGPR을 포함한 소포는 다시 세포막과 융합되어 간세포 표면으로 되돌아가 수용체 순환(recycling)을 마친다.엔도솜에서 방출된 siRNA는 헬리케이스(helicase)에 의해 이중가닥 구조가 풀리고, 안티센스 가닥(antisense strand)은 Ago2 단백질을 포함한 다양한 효소들과 함께 RISC를 형성한다. RISC는 표적 mRNA와 상보적인 염기서열에 결합하며, Ago2는 안티센스 가닥의 5′ 말단에서 10번째와 11번째 염기 사이의 인산다이에스터 결합(phosphodiester bond)을 절단하여 mRNA를 분해하고 유전자 발현을 억제한다(Figure 3). siRNA 기반 RNAi 치료제 플랫폼의 특장점은? RNAi은 dsRNA의 존재에 의해 유도되는 유전자 침묵 현상으로, 세포 내에서 특정 mRNA를 선택적으로 분해함으로써 유전자 발현을 전사 후 수준에서 억제하는 고도로 보존된 생물학적 기전이다. RNAi 기전의 핵심 실행 인자인 siRNA는 염기서열 상보성에 기반하여 표적 mRNA를 인식하고 절단함으로써, 병리 단백질의 발현을 효과적으로 차단할 수 있다.이러한 기전을 치료 전략에 응용한 siRNA 기반 RNAi 플랫폼은 기존의 단백질 중심 치료제와는 차별화된 분자적 기전을 바탕으로 정밀하고 지속적인 유전자 억제를 가능하게 하며, 새로운 치료 패러다임으로 주목받고 있다.siRNA 기반 플랫폼의 가장 큰 장점 중 하나는 높은 표적 특이성(target specificity)이다. siRNA는 21~23개의 염기쌍으로 구성된 짧은 dsRNA 분자로, 염기서열 상보성에 따라 특정 mRNA만을 선택적으로 인식하여 작용하므로, 오프타깃(off-target) 효과를 최소화할 수 있다. 여기에 2'-O-methyl, 2'-fluoro 등의 화학적 변형을 적용하면 분해 저항성과 면역자극 회피 능력이 향상되어, 약물의 안전성과 유효성을 동시에 확보할 수 있다.또한 siRNA는 단백질 구조 정보에 의존하지 않고 유전자 염기서열 정보만으로 설계가 가능하기 때문에, 기존 저분자 화합물이나 단백질 기반 치료제들이 접근하기 어려운 ‘undruggable’ 표적(예: 비구조 단백질, 비효소 단백질 등)에 대해서도 유효하게 작용할 수 있다. 특히 단백질 생성 이전 단계인 mRNA 수준에서 병리 유전자의 발현을 차단하기 때문에, 병리 단백질의 생성 자체를 원천적으로 억제할 수 있다는 점에서 치료의 근본적 접근이 가능하다.siRNA 치료제는 일반적으로 한 번의 투여로 수 주에서 수개월간 지속적인 유전자 억제 효과를 유도할 수 있어, 만성질환 치료에서 약물 순응도 향상과 투여 횟수 감소라는 측면에서도 큰 장점을 제공한다.특히 GalNAc-siRNA 전달 플랫폼은 간세포 표면에 특이적으로 발현되는 ASGPR에 선택적으로 결합함으로써 고도의 간 특이성을 확보하면서도 피하주사가 가능하다는 점에서, 임상적 실용성과 접근성이 뛰어나다.siRNA 기반 RNAi 치료제 플랫폼의 문제점과 해결책은 무엇인가? siRNA 기반 RNAi 치료제는 유전자 발현을 정밀하게 조절할 수 있는 혁신적 플랫폼이지만 그 임상적 활용과 적용 범위를 넓히는 데에는 여전히 해결해야 할 중대한 제약이 존재한다. 이러한 한계는 약물의 물리화학적 특성, 전달 효율, 표적 조직 선택성, 면역 반응, 그리고 장기 안전성 측면에서 다양하게 나타난다.첫째, siRNA는 상대적으로 불안정한 고분자 음전하 물질로서, 체내에서 효소적 분해에 매우 취약하다. 자연 상태의 siRNA는 혈중에서 수 분 이내에 빠르게 분해되며, 조직으로 도달하기 전에 대부분 소실된다. 이러한 문제는 여러 화학적 변형을 통해 일부 개선되고 있으나, 여전히 체내 안정성과 전달 효율 간의 균형 조절은 중요한 과제로 남아 있다.둘째, siRNA는 세포막을 통과하기 어려운 물리적 특성을 가지고 있어, 전달 시스템에 대한 의존성이 매우 크다. GalNAc-siRNA 및 LNP-siRNA와 같은 플랫폼은 간세포 표적화에는 성공하였지만, 중추신경계, 심장, 폐, 근육 등 간 이외 조직으로의 선택적 전달은 여전히 기술적으로 제한적이다. 특히 혈관뇌장벽(BBB)과 같은 생리학적 장벽은 siRNA의 중추신경계 질환 치료 적용을 어렵게 하는 근본적 한계로 작용한다.셋째, siRNA는 본질적으로 면역 자극 가능성을 내포한다. siRNA 분자는 Toll-like receptor 3, 7, 8 등에 의해 인식되어 인터페론 반응 및 선천면역 경로를 활성화할 수 있으며, 이는 약물의 안전성과 내약성에 문제를 유발할 수 있다. 특히 반복 투여 시 면역 반응의 축적 또는 과민반응 발생 가능성은 장기 치료에 대한 제한 요소로 작용할 수 있다. 이러한 면역학적 문제는 화학적 안정화 및 설계 최적화를 통해 일부 완화되고 있으나, 특정 환자군에서는 여전히 우려 요소로 간주된다.넷째, siRNA 기반 RNAi는 유전자 발현을 일방적으로 억제(silencing)하는 방식이므로, 표적 유전자의 기능이 완전히 제거되는 것이 항상 바람직하지 않을 수 있다. 일부 유전자는 생리적 항상성 유지에 부분적으로 기여하므로, 과도한 억제가 예기치 않은 부작용이나 대체 경로 활성화를 유발할 수 있다. 특히 하나의 유전자가 다양한 기능을 수행하는 경우(pleiotropy), 정밀한 용량 조절과 억제 수준의 모니터링이 필수적이다.마지막으로, siRNA 기반 치료제는 아직까지 국소 투여나 ex vivo 적용이 제한적이며, 전신 투여를 기본으로 하기 때문에 조직 특이성, 투여 용량, 약물 반감기, 약물 상호작용 등에 대한 정밀한 약물동력학적 이해가 요구된다. 또한 생산 비용이 상대적으로 높고, 대규모 상업화 과정에서의 제조 일관성 및 품질 관리도 반드시 고려해야 할 요소이다.결론적으로, siRNA 기반 RNAi 치료제 플랫폼은 고유의 치료적 강점에도 불구하고, 약물 전달, 조직 선택성, 면역 자극성, 장기 안전성, 비용 구조 등 다양한 기술적 제약에 직면해 있다. 이러한 한계는 siRNA 분자 설계 기술과 전달 플랫폼, 임상 개발 전략의 지속적인 고도화를 통해 극복 가능할 것으로 보인다.다음 편부터 ① 기보시란(Givosiran) ② 루마시란(Lumasiran) ③ 인클리시란(Inclisiran) ④ 브루시란(Vutrisiran) ⑤ 네도시란(Nedosiran) ⑥ 피투시란(Fitusiran) 등의 순으로 게재될 예정이다.참고문헌 1. Giuseppe Cammarata, et al. “Emerging noncoding RNAs contained in extracellular vesicles” Ther Adv Med Oncol 2022, Vol. 14: 1–20 2. Synthesis of GalNAc-siRNA Conjugates(출처: Front. Pharmacol., 14 December 2022). 3. Lei Zhang et al. “The therapeutic prospects of N-acetylgalactosamine-siRNA conjugates“ Front. Pharmacol., 14 December 2022. 3. Vinod Khatri et al. ”Design Synthesis and Biomedical Applications of Glycotripods for Targeting Trimeric Lectins“ Eur J Org Chem Volume 26, Issue 9 March 1, 2023. 4. Katyayani Tatiparti et al. “Review siRNA Delivery Strategies: A Comprehensive Review of Recent Developments” Nanomaterials 2017, 7, 77, 5. Ogochukwu Amaeze et al. “The absorption, distribution, metabolism and elimination characteristics of small interfering RNA therapeutics and the opportunity to predict disposition in pregnant women” Drug Metabolism and Disposition 53 (2025) 100018. 6. 기타 인터넷 자료2025-07-25 06:33:37최병철 박사
차세대 유전자 침묵 치료, 'RNAi' 치료제 플랫폼에 대해핵산 치료제는 구성 성분에 따라 DNA 기반 약제와 RNA 기반 약제로 구분되며, RNA 기반 약제는 안티센스 올리고뉴클레오티드(antisense oligonucleotide, ASO), 유전자 발현을 억제하는 소형 간섭 RNA(small interfering RNA, siRNA), 마이크로RNA(miRNA), 메신저 RNA(mRNA), 그리고 아프타머(aptamer) 등이 있다.이 중 siRNA는 합성된 이중가닥 RNA(double-stranded RNA, dsRNA)로서, 센스 가닥(sense strand)과 안티센스 가닥(antisense strand)으로 구성되며, 일반적으로 19~25 염기쌍의 길이를 가지고 있다. 이 중 안티센스 가닥은 RNA 유도 침묵 복합체(RNA-induced silencing complex, RISC) 내에서 특정 mRNA를 인식하고 절단하는 가이드 역할을 한다.이러한 siRNA를 기반으로 하는 RNA 간섭(RNAi) 치료제의 개발은 2000년대 초반부터 본격적으로 시작되었으며, 약 20년에 걸친 기술 축적과 전달 플랫폼의 발전을 통해 상용화 단계에 도달하였다. 2018년, 트랜스사이레틴(transthyretin, TTR) 매개 가족성 아밀로이드 다발신경병증(hATTR) 치료제 파티시란(Patisiran)이 미국 FDA로부터 최초로 승인을 받으며 siRNA 기반 치료제의 상업화가 본격화되었다.이후 다양한 GalNAc conjugate(갈낙 접합체) 기반의 siRNA 치료제들이 연이어 FDA 승인을 획득하였다. 주요 승인 약제로는 2019년 급성 간성 포르피린증(acute hepatic porphyria, AHP) 치료제 기보시란(Givosiran), 2020년 원발성 옥살산뇨증 1형(primary hyperoxaluria type 1, PH1) 치료제 루마시란(Lumasiran), 2021년 고지혈증 치료제 인클리시란(Inclisiran), 2022년 hATTR 치료제 브루시란(Vutrisiran)이 있다.또한 2023년에는 PH1 치료제로 네도시란(Nedosiran), 2025년에는 A형 및 B형 혈우병 환자(항응고 인자 억제제 보유 여부와 무관)의 예방 치료제로 피투시란(Fitusiran)이 승인되었다.이러한 siRNA 기반 RNA 간섭(RNAi) 치료제 플랫폼은 암, 바이러스 감염, 유전성 대사질환 등 다양한 질환의 병태생리를 직접 조절할 수 있는 차세대 정밀의학 전략으로 주목받고 있으며, 이는 단순한 유전자 발현 억제를 넘어, 특정 병인 단백질의 발현을 선택적으로 차단함으로써 질병의 근원을 표적하는 질병 수정형(disease-modifying) 치료제로서의 가능성을 제시하고 있다. RNA(Ribonucleic acid, 리보핵산)는 무엇인가? 핵산은 생명체의 유전 정보를 저장하고 전달하는 데 핵심적인 역할을 하며, 그중 RNA는 진핵세포와 원핵세포 모두에서 유전자 발현 및 세포 내 조절 과정에 필수적인 고분자 생체분자로서, DNA와 함께 분자생물학의 센트랄 도그마(central dogma)를 구성하는 주요 요소이다.RNA는 주로 DNA의 유전 정보를 단백질로 전달하는 전령(messenger)의 역할로 인식되어 왔으나, 다양한 연구 결과에 따라 RNA는 단순한 정보 매개체를 넘어 효소적 기능, 유전자 발현 조절, 구조적 지지, 면역 조절 인자 등 폭넓은 생물학적 기능을 수행하는 분자로 밝혀졌다. 이에 따라 RNA는 단백질과 동등하거나 그 이상으로 기능적 다양성을 지닌 핵심 생체분자로 평가되고 있다.RNA는 리보오스를 포함한 단일가닥 핵산으로 구성되며, DNA와 달리 염기로 우라실(uracil)을 포함하고, 2′-탄소 위치에 하이드록시기(2′-OH group)를 갖는 리보오스를 지닌다. 이러한 구조적 특성은 RNA에 높은 구조적 유연성과 화학적 반응성을 부여하여, 다양한 입체 구조를 형성하고 특정 단백질이나 다른 핵산과 선택적으로 결합하며, 심지어 효소적 반응을 촉매할 수 있는 생화학적 기반이 된다.실제로 RNA는 염기 서열에 의한 상보적 결합 외에도 루프(loop), 헤어핀(hairpin), 스템(stem), 벌지(bulge), 가상매듭(pseudoknot) 등 복잡한 이차 및 삼차 구조를 형성하며, 이를 통해 단백질-리간드 상호작용, 효소 활성, 핵-세포질 간 수송, 세포 내 위치 특이적 기능 수행 등에 관여한다.RNA는 유전자 발현 조절, 세포분화, 세포주기, 세포사멸, 스트레스 반응, 면역 조절 등 거의 모든 생리적·병리적 현상에 직·간접적으로 관여하며, DNA로부터 유래된 정보를 전달하는 역할외에도 전사(transcription)와 번역(translation) 간의 연결을 매개하고 유전자 발현의 정밀한 조절자로 작용한다.특히 진핵세포에서는 RNA가 전사 후 변형(post-transcriptional modification), 스플라이싱(splicing), RNA 편집(RNA editing), 핵-세포질 수송(nuclear export), 안정성 조절, 국소화(localization) 등 유전자 발현을 다양한 수준에서 정교하게 조절한다하지먼 RNA의 기능 이상은 다양한 질환의 발병과 밀접하게 연관되어 있다. 즉 RNA의 안정성 혹은 조절 기전이 교란되면 특정 단백질의 비정상적 발현이 초래되며, 이는 암, 신경퇴행성 질환, 심혈관 질환, 자가면역 질환 등 다양한 병태생리적 상태를 유발하거나 악화시킬 수 있다.최근 연구에 따르면 RNA의 구조적 변이, 염기서열 돌연변이, 또는 RNA-단백질 상호작용의 이상은 질환의 새로운 병인으로 부상하고 있으며, RNA 수준에서의 진단 및 치료 접근은 생명과학의 주요 연구 영역으로 부각되고 있다.RNA에는 어떤 종류가 있는가? RNA는 그 기능에 따라 여러 유형으로 분류된다(Figure 1). 가장 기본인 형태는 전령 RNA(messenger RNA, mRNA)로, DNA의 유전 정보를 복사하여 리보솜으로 전달하며 단백질 합성에 직접 관여한다. 전이 RNA(transfer RNA, tRNA)는 아미노산을 리보솜으로 운반하는 역할을 하며, 리보솜 RNA(ribosomal RNA, rRNA)는 리보솜의 구조적 및 촉매적 핵심 요소로 기능한다.이 외에도 최근에는 유전자 발현을 정밀하게 조절하는 비번역 RNA(non-coding RNA)들이 주목받고 있다. 예를 들어, 소간섭 RNA(small interfering RNA, siRNA), 마이크로 RNA(microRNA, miRNA), 긴 비암호화 RNA(long non-coding RNA, lncRNA) 등은 세포 내 유전자 조절 네트워크의 핵심 조절자로 작용한다. 1. mRNA(messenger RNA, 전령 RNA) mRNA가 전달하는 유전 정보는 염기의 종류, 배열, 그리고 길이에 의해 결정된다. DNA는 아데닌(A), 구아닌(G), 시토신(C), 티민(T)의 네 가지 염기로 구성되어 있는 반면, RNA는 티민 대신 우라실(U)을 포함한다. 유전 정보는 이러한 염기의 조합으로 구성되며, RNA 중 mRNA는 전사(transcription) 후 모든 처리가 완료된 형태로, 5′-cap 구조와 poly(A) tail(폴리 A 꼬리)을 갖추고 있으며, 스플라이싱(splicing)도 완료된 상태이다.mRNA는 DNA의 유전 정보를 기반으로 리보솜에서 단백질을 합성할 때 번역 서열(translation sequence)로 작용하므로, 세포 내에서 mRNA의 발현 수준을 조절하는 것은 생명 현상을 통제하는 데 매우 중요하다.성숙한 mRNA는 긴 poly(A) tail을 가지며, 이 아데닌 꼬리는 mRNA의 분해를 방지하고 안정적인 기능 수행을 돕는다. 그러나 시간이 지나면 탈아데닐화(deadenylation) 효소에 의해 이 꼬리는 점차 짧아지게 되고, 이는 mRNA 분해의 신호로 작용한다. 반면, mRNA의 말단에 혼합 꼬리(mixed tail)가 형성될 경우, 이는 아데닌 꼬리의 제거 과정을 방해하여 mRNA의 분해를 억제하고 안정성을 높이는 것으로 알려져 있다. 따라서 혼합 꼬리는 mRNA의 생존을 유지하는 데 중요한 조절 요소로 작용한다.2. ncRNA(non-coding RNA, 비암호화 RNA) 센트럴 도그마에 따르면, 단백질을 암호화하지 않는 RNA는 비암호화 RNA(non-coding RNA, ncRNA)로 분류된다. 비록 ncRNA는 단백질을 직접 생성하지는 않지만, 전사 후 조절(post-transcriptional regulation) 및 후성유전학(epigenetic) 기전에 관여하는 중요한 조절자로 밝혀지고 있다.ncRNA는 기능적 역할에 따라 크게 하우스키핑 비암호화 RNA(housekeeping ncRNA)와 조절 비암호화 RNA(regulatory ncRNA)로 나뉘며, 그 길이에 따라 다시 분류된다. 일반적으로 200개 이하의 뉴클레오타이드(nucleotide)로 구성된 경우를 작은 ncRNA(small ncRNA 또는 short/medium ncRNA)라 하고, 200개 이상의 뉴클레오타이드를 포함할 경우 긴 ncRNA(long non-coding RNA, lncRNA)로 분류된다. 이들은 기능, 전사 후 가공, 상호작용 양상 등에 따라 더욱 세분화된다.1) Housekeeping ncRNA(하우스키핑 비암호화 RNA) ① tRNA(transfer RNA, 운반 RNA) tRNA는 단백질 합성 과정에서 mRNA의 코돈(codon)에 상보적으로 결합하는 안티코돈(anticodon)을 가지고 있으며, 해당 코돈에 대응하는 아미노산을 리보솜으로 운반하는 역할을 한다. 즉, mRNA의 코돈을 해독하여 해당 아미노산을 정확히 리보솜에 전달하고, 폴리펩타이드 사슬의 신장(elongation) 과정에 기여함으로써 단백질 합성의 핵심 요소로 작용한다.tRNA는 전사된 직후 바로 기능하는 것이 아니라 pre-tRNA라는 전구체 형태로 먼저 생성된다. 이 pre-tRNA는 5′ 말단과 3′ 말단에 불필요한 염기 서열을 포함하며, 일부는 안티코돈 고리(anticodon loop)에 인트론(intron)을 포함하기도 한다. 성숙한 tRNA는 이러한 전사 후 가공 과정을 통해 구조적으로 안정화되고 생물학적 활성을 갖춘다.② rRNA(ribosomal RNA, 리보솜 RNA) rRNA는 리보솜의 핵심 구성 요소로, 다양한 리보솜 단백질과 결합하여 기능적 리보솜 복합체를 형성한다. 리보솜은 세포 내 단백질 생합성의 중심 기구이며, rRNA는 전체 세포 내 RNA의 약 80%를 차지할 정도로 풍부하게 존재한다.rRNA는 단순한 구조적 지지체에 그치지 않고, 촉매적 기능까지 수행한다. 특히, 리보솜의 대단위 서브유닛(large subunit)에 존재하는 rRNA는 펩티딜전이효소(peptidyl transferase)로 작용하여 아미노산 사이의 펩타이드 결합 형성을 촉진한다. 이는 RNA 자체가 효소 활성을 수행하는 대표적 예로, rRNA가 리보자임(ribozyme)으로 기능함을 보여준다.2) Regulatory ncRNA(조절 비암호화 RNA) 인간 유전체는 약 30억 개의 염기쌍(base pairs)으로 구성되어 있으나, 이 중 약 1% 정도만이 단백질을 암호화하는 유전자로 기능하는 것으로 오랫동안 여겨져 왔다. 이러한 전통적인 관점을 검증하고 유전체의 기능적 요소를 체계적으로 규명하기 위해 시작된 국제적 연구가 바로 ENCODE(Encyclopedia of DNA Elements) 프로젝트이다.ENCODE 프로젝트를 통해 밝혀진 핵심 사실은, 과거에 ‘쓰레기 DNA(junk DNA)’ 혹은 ‘암흑 물질(dark matter)’로 간주되었던 비암호화 영역이 실제로 생화학적 활성 및 생물학적 기능을 수행한다는 점이다. 이는 ncRNA가 단순한 유전 정보의 부산물이 아니라, 유전자 발현을 정밀하게 조절하는 중요한 조절자(regulator)로 기능할 수 있음을 의미한다.특히, 차세대 염기서열 분석기법(NGS) 등 기술의 발전으로 유전체 전체의 전사(transcription) 양상을 정밀하게 분석할 수 있게 되었고, 그 결과 유전체의 실제 전사 비율이 단 1%가 아니라 약 80%에 이른다는 사실이 밝혀졌다. 이는 유전체의 대부분이 기능적 목적을 가지고 의도적으로 전사된다는 점을 시사한다.이러한 발견은 ncRNA, 특히 조절 비암호화 RNA(regulatory ncRNA)의 중요성을 부각시켰으며, 이들은 전사 후 조절, 염색질 구조 변형, 유전자 발현 억제 및 활성화, 세포 분화, 그리고 항상성 유지 등 다양한 생명 현상에 핵심적인 역할을 수행하는 것으로 밝혀졌다.① Small ncRNA(sncRNA, 작은 비암호화 RNA) a. miRNA(microRNA, 마이크로 RNA) miRNA는 RNA 간섭(RNA interference, RNAi)과 유사한 기전을 따르는, 자연적으로 존재하는 유전자 발현 조절 메커니즘이다. 현재까지 인간에서 수백 종의 miRNA가 확인되었으며, 전체적으로는 50,000종 이상이 존재할 것으로 추정된다.miRNA는 일반적으로 약 22개의 염기로 구성된 짧은 단일가닥 RNA이며, 표적 mRNA와 부분적으로 상보적인 염기서열을 인식하여 결합한다. 이를 통해 mRNA의 번역을 억제하거나 분해를 유도함으로써 유전자 발현을 음성 조절(negative regulation)한다.miRNA는 특히 개체 발생, 세포 분화, 세포 주기 조절, 세포사멸, 암 억제 또는 촉진 등 다양한 생명현상의 조절자로 기능하며, 이의 이상 발현은 암, 심혈관 질환, 신경계 질환 등 여러 병태생리학적 상태와 밀접한 관련이 있는 것으로 알려져 있다.b. siRNA(small interfering RNA, 소간섭 RNA) siRNA는 보통 인위적으로 합성된 긴 이중가닥 RNA(dsRNA)를 세포 외부에서 도입한 후, 세포 내에서 ATP-의존성 RNase인 Dicer에 의해 절단되어 생성되는 길이 21~23 염기쌍의 짧은 dsRNA이다.siRNA는 성숙한 miRNA(mature miRNA)와 구조적으로 유사하나, 기원과 기능적 특성에서 차이를 보인다. 특히 표적 mRNA와의 염기서열 상보성에 있어서 뚜렷한 차이가 있다. siRNA는 표적 mRNA와 완전한 상보성을 이루어 정확한 표적 유전자만을 선택적으로 억제하는 반면, miRNA는 일반적으로 불완전한 상보성을 바탕으로 여러 유전자의 번역을 동시에 조절할 수 있다.이러한 차이로 인해 siRNA는 고특이적 유전자 침묵(specific gene silencing)에 적합하며, miRNA는 보다 광범위한 유전자 조절(global regulation)에 기여하는 특성을 가진다.c. snRNA(small nuclear RNA, 작은 핵 RNA) snRNA는 주로 핵 내에서 pre-mRNA의 스플라이싱(splicing)에 관여하는 짧은 RNA 분자이다. 대표적으로 U1, U2, U4, U5, U6 등의 snRNA가 스플라이스좀(spliceosome)이라는 RNA-단백질 복합체(RNP complex)를 형성하여, 인트론(intron)의 제거 및 엑손(exon)의 연결에 필수적인 역할을 수행한다.snRNA는 mRNA 성숙 과정에서 엑손-인트론 경계의 인식과 절단을 통해 유전자 발현의 정밀한 조절을 수행하는 핵심 인자로 기능한다.d. snoRNA(small nucleolar RNA, 작은 인 RNA) snoRNA는 주로 세포핵 내 핵소체(nucleolus)에 존재하는 RNA로, rRNA의 성숙 및 가공에 핵심적인 역할을 한다. snoRNA는 pre-rRNA(전구체 리보솜 RNA)와 상보적인 염기서열을 바탕으로 결합하여, 특정 위치의 염기를 화학적으로 변형하거나 절단 위치를 안내한다.snoRNA의 주요 기능은 rRNA 염기에 대해 2′-O-메틸화(2′-O-methylation) 또는 위우리딘(pseudouridine)으로의 전환을 유도한다. 이러한 변형은 rRNA의 구조적 안정성과 리보솜 기능에 매우 중요하다. 또한 snoRNA는 pre-rRNA가 정확한 위치에서 절단되도록 도와줌으로써, 최종적으로 기능을 갖춘 성숙한 rRNA의 형성에 기여한다.② long ncRNA(lncRNA, 긴 비암호화 RNA) lncRNA는 단백질을 직접 암호화하지 않지만, 포유류 전사체(transcriptome) 내에서 비교적 풍부하게 존재하며 세포 기능에 다양한 방식으로 기여한다. 특히, lncRNA는 염색질 구조 조절 효소(chromatin-modifying enzyme)를 모집하거나 그 활성을 조절함으로써, 표적 유전자의 전사 활성 조절에 관여하는 것으로 잘 알려져 있다.lncRNA의 생물학적 기능은 크게 세 가지 기전으로 요약될 수 있다. 첫째, 시스(cis) 또는 트랜스(trans) 위치에서 전사 조절자(transcriptional regulator)로 작용하여, 인접 유전자의 발현을 직접 조절하거나, 떨어진 위치에 존재하는 유전자에 영향을 미친다.둘째, RNA 가공(splicing 등) 과정이나 전사 후(post-transcriptional) 조절, 또는 단백질 활성을 조절하는 기능을 수행한다. 이 경우 lncRNA는 특정 단백질 또는 RNA와 상호작용함으로써 기능적 복합체를 형성하거나, 조절자의 기능을 매개하는 플랫폼으로 작용한다.셋째, 일부 lncRNA는 핵 내 도메인(nuclear domain)의 구조적 구성에 기여하여, 세포핵 내 공간적 조직화와 기능적 구획화를 조절하는 역할을 수행한다. 이는 핵 내 RNA-단백질 복합체 형성과 같은 고차원적인 구조적 조절과 연관된다.lncRNA는 일반적으로 조직 또는 세포 유형 특이적인 발현 양상을 보이며, 단일 세포당 평균적으로 1개 미만의 사본만 검출되는 경우가 많다. 그러나 특정 조직이나 핵의 특정 구획에서는 높은 수준으로 발현되어, 기능적 다양성과 세포 간 복잡성을 더욱 증가시키는 요인으로 작용한다.특히, lncRNA는 개체 발생, 세포 분화, 노화, 스트레스 반응 등 다양한 생리적 과정뿐 아니라, 암의 발생 및 진행과 같은 병리적 현상에서도 중요한 조절 인자로 기능함이 밝혀지면서, 분자생물학 및 암 연구 분야에서 활발한 주목을 받고 있다.RNA 침묵(RNA silencing)은 어떤 현상인가? 생명체 내에서 유전자 발현은 정교한 조절 기전에 의해 통제되며, 이러한 조절은 개체의 발생, 항상성 유지, 외부 자극에 대한 반응, 병리적 상태에서의 적응 등 다양한 생물학적 과정에 핵심적인 역할을 한다. 이 가운데 유전자 침묵(gene silencing)은 특정 유전자의 발현을 억제하거나 완전히 차단하는 생물학적 현상이다.유전자 침묵(Gene silencing)에는 전사 시 유전자 침묵(transcriptional gene silencing, TGS)와, 전사 후 유전자 침묵(post-transcriptional gene silencing, PTGS)이 존재한다. 이 중 TGS는 일반적으로 DNA 메틸화(DNA methylation), 히스톤 변형(histone modification), 이질 염색질 형성(heterochromatinization) 등의 후성유전학적 메커니즘에 의해 매개되며, 유전자 접근성을 구조적으로 차단함으로써 발현을 억제한다.RNA 침묵(RNA silencing)은 유전자 침묵의 하위 개념으로, 주로 RNA 분자에 의해 매개되는 전사 후 유전자 침묵(PTGS) 기전을 지칭한다. RNA 침묵은 1990년대 후반, 식물과 동물, 곰팡이 등 다양한 진핵생물에서 확인되었으며, 진화적으로 보존된 염기서열 특이적 유전자 조절 기전으로 기능한다.RNA 침묵의 중심에는 짧은 비암호화 RNA 분자들, 즉 siRNA, miRNA, piRNA가 있으며, 이들은 각각 고유한 기원과 작용 기전을 통해 표적 mRNA의 발현을 억제한다.miRNA는 내인성 전사체로부터 유래하며, 개체의 발달, 세포 분화, 세포 주기, 세포사멸 등 생리적 과정뿐만 아니라 암, 심혈관 질환, 신경계 질환 등의 병태생리적 상태에서 정밀한 유전자 조절자로 기능한다.siRNA는 외부에서 유래된 dsRNA에 의해 형성되며, 실험적 유전자 침묵 기법이나 RNA 간섭 기반 치료제에 직접적인 유전자 억제 도구로 활용되고 있다.piRNA는 주로 생식세포에서 발현되며, 트랜스포존 억제, 유전체 안정성 유지, 세포 계통 유지 등 특수한 기능을 수행한다.RNA 침묵은 다양한 진핵생물에서 보편적으로 나타나며, 바이러스 감염에 대한 방어 기전, 전이 요소 억제, 비정상적 전사체 제거 등 세포 수준의 품질관리 및 유전체 보호 시스템으로 작용한다. 이러한 점에서 RNA 침묵은 단순한 유전자 억제를 넘어 생물학적 균형과 유전체 기능 유지의 핵심 축으로 간주된다.최근 RNA 침묵 기전은 치료 표적 및 플랫폼 기술로도 활발히 연구되고 있으며, siRNA 기반 치료제, antisense oligonucleotide(ASO) 기술 등은 RNA 침묵 원리를 기반으로 개발된 RNA 기반 정밀 의약품으로 발전하여 다양한 질환에서 임상적으로 응용되고 있다.RNA 간섭(RNA interference, RNAi)은 어떤 현상인가? RNAi는 1998년 Andrew Fire와 Craig Mello가 예쁜꼬마선충(Caenorhabditis elegans)을 대상으로 한 실험에서 처음 보고한 현상으로, 외부에서 도입된 이중가닥 RNA(dsRNA)가 세포 내 특정 mRNA를 인식하고 이를 선택적으로 분해함으로써 유전자 발현을 억제하는 고유의 생물학적 기전이다. 이 발견은 유전자 발현 조절에 대한 이해를 근본적으로 전환시켰으며, 두 연구자는 해당 업적으로 2006년 노벨 생리의학상을 수상하였다.RNA 침묵은 유전자 발현 억제를 유도하는 상위 개념이고, 그 중 RNAi는 기전이 명확히 규명되고 약물화 가능성이 높은 대표적인 하위 경로에 해당한다. RNAi는 염기서열 특이적 방식으로 작용하여, 표적 유전자의 발현을 정밀하게 제어할 수 있는 장점을 지니며, 바이러스 방어, 전이인자 억제, 후성유전 조절, 발생 및 분화 조절 등 다양한 생물학적 과정에 기여한다.특히 RNAi는 유전자 기능 연구, 질병 모델링, 표적 유전자 억제를 통한 치료제 개발 등 기초연구 및 임상분야 모두에서 응용 가능성이 높은 기술로 주목받고 있으며, siRNA 기반 치료제는 이러한 RNAi 원리를 임상에 성공적으로 도입한 대표적인 예로 평가되고 있다.소간섭 RNA(small interefering RNA, siRNA)는 무엇인가? siRNA는 RNAi 현상을 매개하는 대표적인 dsRNA로, 특정 mRNA의 발현을 염기서열 특이적으로 억제하는 기능을 수행한다. siRNA는 miRNA와 달리 전사산물의 절단(cleavage)을 직접 유도하는 강력한 침묵 효과를 나타낸다.이는 특히 바이러스 유전체, 종양 특이 유전자, 병리적 유전자 돌연변이 등을 표적으로 하는 데 적합하다. 이러한 특이성과 효능을 바탕으로 siRNA는 유전자 기능 연구뿐 아니라 질병 치료를 위한 유전자 기반 약물 플랫폼으로 빠르게 발전하고 있다.하지만, siRNA는 그 자체의 불안정성, 세포막 투과성 부족, 면역 자극 가능성 등의 한계도 지니고 있어, 이를 극복하기 위한 다양한 전달 시스템(delivery system) 개발이 병행되고 있다. 특히, 갈낵(GalNAc) 기반 간세포 표적 전달 시스템은 siRNA 치료제의 성공적 상용화에 핵심적인 기술로 평가된다.RNAi는 외부 또는 내부에서 유래된 dsRNA에 의해 유도되며, siRNA는 RNAi 경로의 핵심 매개체로 작용한다. siRNA는 RNAi이라 불리는 다단계 과정을 통해 유전자 발현을 억제하는 데 핵심적인 역할을 한다(Figure 1). 첫 번째 단계, dsRNA의 세포 내 유입과 Dicer에 의한 절단 siRNA는 주로 외인성 또는 인공적으로 도입된 dsRNA의 절단에 의해 생성된다. 일단 dsRNA가 세포 내로 유입되면 세포질(cytoplasm)에서 작용을 시작한다. 자연 상태에서는 긴 dsRNA 또는 전구체(pre-siRNA)가 Dicer라는 RNase III 계열의 효소에 의해 절단되어 siRNA가 생성된다. 그러나 합성 siRNA는 21~23개 염기쌍의 짧은 이중가닥 RNA로 구성되며, 이미 Dicer 가공 단계를 생략한 형태로 설계되어 있다.두번째 단계, RNA 유도 침묵 복합체(RNA-induced silencing complex, RISC) 형성과 가이드 스트랜드 선택 세포질 내에서 siRNA는 RISC와 결합하게 된다. RISC는 Argonaute(AGO) 단백질을 핵심으로 하는 다단백 복합체이며, siRNA는 이 복합체에 의해 가이드 가닥(guide strand)와 패신저 가닥(passenger strand)로 분리된다. 이 과정에서 AGO2는 패신저 가닥을 제거하거나 분해하며, 가이드 가닥만이 RISC에 안정적으로 결합된다. 가이드 가닥은 이후 표적 mRNA의 염기서열을 인식한다.세 번째 단계, mRNA 인식 및 절단(유전자 침묵 유도) 가이드 가닥이 결합된 활성화된 RISC는 세포질 내에 존재하는 상보적 염기서열을 가진 mRNA를 탐색한다. siRNA와 표적 mRNA가 완전한 상보성을 이루는 경우, AGO2의 엔도뉴클레아제 활성이 유도되어 표적 mRNA를 특정 위치에서 절단(cleavage)하게 된다. 절단된 mRNA는 이후 세포 내 핵산 분해효소에 의해 빠르게 분해되며, 이는 궁극적으로 해당 유전자의 단백질 발현 억제로 이어진다.이러한 유전자 침묵은 염기서열 특이적이며, 시간적으로 수 일에서 수 주 이상 지속될 수 있으며, 반복 투여 시 누적 효과를 기대할 수 있다. 또한, siRNA는 번역 후 단계에 작용하기 때문에, 단백질 발현을 정밀하게 조절할 수 있는 장점이 있다.RNA 기반 치료제(RNA-based therapeutics)란 무엇인가? RNA 기반 치료제는 특정 유전자 또는 병리적 단백질의 발현을 직접적으로 조절하거나, 필요한 단백질을 체내에서 직접 합성하도록 유도함으로써 질병의 원인 자체를 정밀하게 조절할 수 있는 치료 전략이다. 이러한 치료제는 RNA의 구조적 및 기능적 다양성에 따라 여러 유형으로 분류된다.대표적인 RNA 기반 치료제에는 단백질 생성을 직접 유도하는 mRNA 치료제, 특정 mRNA를 분해하거나 스플라이싱을 조절하는 ASO, RNAi 기전을 통해 유전자 발현을 억제하는 siRNA 및 miRNA 유사체, 특정 단백질에 선택적으로 결합하여 기능을 저해하는 RNA 압타머(aptamer) 등이 있다.이들 치료제는 유전자 수준의 정밀한 조절이 필요한 질환에서 특히 유효성이 크며, 암, 유전질환, 감염병, 대사질환 등 다양한 분야에서 치료 효과가 확인되고 있다.RNA 기반 치료제의 가장 큰 강점은 염기서열 상보성에 기반한 높은 표적 특이성과 설계의 유연성이다. 환자의 유전 정보나 발현 프로파일에 따라 맞춤형으로 표적을 설계할 수 있으며, 기존의 항체나 저분자 화합물로는 접근이 어려운 내재적 유전자 조절 단계에 직접 개입할 수 있다는 이점이 있다.그러나 RNA 분자의 구조적 불안정성, 면역 자극 가능성, 세포 내 전달의 어려움은 여전히 극복해야 할 중요한 과제로 남아 있다. 이를 해결하기 위해 지질 나노입자(lipid nanoparticle, LNP), 갈낙(GalNAc) 접합체, 엑소좀(exosome), 바이러스 벡터 등 다양한 전달 기술이 병행 개발되고 있으며, RNA 분자 자체에 대한 화학적 변형 연구 또한 활발히 진행 중이다.RNAi 기반 치료제(RNA interference-based therapeutics)란 무엇인가? RNAi는 짧은 dsRNA 조각이 세포 내 RNA 유도 침묵 복합체(RISC)에 의해 가이드되어, 상보적인 서열을 갖는 표적 mRNA를 절단함으로써 유전자 발현을 억제한다. 이 과정은 고도로 염기서열 특이적인 방식으로 이루어지며, 세포 내에서 자연스럽게 일어나는 중요한 방어 및 조절 기전이다.RNAi 기반 치료제는 병리적 유전자의 발현을 직접적으로 차단함으로써, 단백질 생성 자체를 근본적으로 억제할 수 있는 전략이다. 이는 기존의 단백질 표적 저해제들이 개입하기 어려운 전사 후(post-transcriptional) 단계에 개입할 수 있다는 점에서 근본적으로 다른 치료 접근법을 제공한다. 특히 유전자 과발현 또는 독성 단백질의 생성이 질병의 주요 병태기전인 경우에 매우 적합하며, 유전질환, 암, 간질환, 감염병 등 다양한 질환에서 임상적 적용이 활발히 진행되고 있다.RNAi 기반 치료제는 작용 기전에 따라 크게 세 가지로 구분된다. 첫째, siRNA는 화학적으로 합성된 짧은 dsRNA로, 표적 mRNA에 대해 높은 서열 특이성을 갖는다. GalNAc(갈낙) 기반 간 표적화 기술, 리포솜 또는 지질나노입자(LNP) 기반 세포 내 전달 기술을 활용하여 체내 적용이 가능하며, 현재 대부분의 RNAi 치료제가 이 플랫폼을 기반으로 한다.둘째, shRNA(short hairpin RNA)는 플라스미드나 바이러스 벡터를 통해 세포 내에서 안정적으로 발현되며, 지속적인 유전자 억제를 유도하는 구조이다. 주로 세포를 체외에서 조작하는 ex vivo 유전자 치료 전략에 활용된다.셋째, miRNA 유도체는 내인성 microRNA의 기능을 모방하거나 경쟁적으로 억제하여, 보다 광범위한 유전자 네트워크를 조절하는 방식으로 개발 중이다. 이는 특정 유전자뿐 아니라 관련된 다수의 유전자를 동시에 조절할 수 있는 장점이 있다.따라서 RNAi 기반 치료제는 유전자 수준에서의 정밀 제어, 고특이성, 그리고 효율적인 발현 억제라는 특성을 지니며, 기존의 저분자 화합물이나 단백질 기반 치료제와는 차별화되는 생물학적 전략을 제공한다.실제로 Givosiran, Lumasiran, Inclisiran 등은 각각 급성 간성 포르피린증(AHP), 원발성 옥살산뇨증 1형(PH1), 고지혈증 등의 적응증으로 다수 국가에서 시판 승인을 획득하였으며, 이는 RNAi 기술이 실용적인 치료 플랫폼으로 진입했음을 보여주는 중요한 이정표가 되었다.GalNAc-siRNA란 무엇인가? siRNA는 분자량이 작고 음전하를 띠는 친수성 분자로서 세포막을 자발적으로 통과하기 어려우며, 혈중에서 RNase에 의해 쉽게 분해되는 한계를 지닌다. 이러한 점에서 siRNA의 안정적이고 표적 특이적인 전달은 치료 효과를 극대화하기 위해 반드시 극복되어야 할 과제이다.이에 따라 다양한 siRNA 전달 시스템(delivery vector)이 개발되어 왔으며, GalNAc conjugate, 지질 나노입자(lipid nanoparticle, LNP), 고분자 기반 전달체 등 다양한 전달 플랫폼이 개발되고 있으며, 이들은 siRNA의 생체 내 안정성 및 조직 특이적 투과성을 개선하는 데 중요한 역할을 하고 있다.이 중 약물을 세포 표면 수용체 리간드와 결합시키는 방식(GalNAc conjugate)은 표적 약물 전달을 위한 유망한 경로로 보고되고 있다. 이러한 수용체는 특정 세포 유형에만 발현되며, 일부 질환에서는 특정 장기나 조직에서 과발현된다.3방향 GalNAc(triantennary GalNAc)은 siRNA의 안티센스(antisense) 사슬 3′ 말단과 결합하여 GalNAc-siRNA conjugate를 형성한다. siRNA는 화학적으로 직접 합성할 수 있으며, 또는 효소 전사로 얻어진 긴 이중가닥 RNA를 세포질 RNase III 엔도뉴클레아제인 Dicer의 작용으로 절단하여 21~23 nt 길이의 siRNA를 생성할 수 있다. 이 siRNA는 3′ 말단에 두 개의 돌출된 뉴클레오타이드, 5′ 말단에 인산기, 그리고 가운데에 19 nt의 상보적인 이중가닥 영역을 가진다.따라서 siRNA와 GalNAc을 결합시켜 피하 주사로 투여하면, GalNAc-siRNA conjugate가 ASGPR(Asialoglycoprotein receptor)에 결합되고, 이어 ASGPR 매개 세포 내 유입(endocytosis)을 통해 세포 내로 들어가게 된다(Figure 2).GalNAc은 간세포 이외의 조직에서는 거의 발현되지 않는 수용체에 대한 높은 결합 친화성을 가지므로, siRNA 분자의 간 특이적(targeted delivery to hepatocytes) 전달을 가능하게 한다. GalNAc-siRNA의 작용 기전은? GalNAc-siRNA의 작용 기전의 핵심은, GalNAc-siRNA conjugate가 간세포 표면의 수용체(asialoglycoprotein receptor, ASGPR)에 선택적으로 인식되고 전달된다는 점에 있다. siRNA는 본래 음전하를 띠고 분자량이 큰 친수성 분자로서, 세포막을 자발적으로 통과하기 어렵다. 하지만 GalNAc으로 변형된 siRNA는 간세포에 특이적으로 발현되는 ASGPR를 통해 표적 조직으로 선택적 전달될 수 있으며, 효율적인 세포 내 유입도 가능하게 된다.ASGPR은 간소엽(liver lobule) 내 간 실질세포(hepatocyte)의 혈관사이 공간(hepatic sinusoid space) 표면에 주로 발현되는 수용체로, GalNAc-siRNA conjugate가 체내에 주입되면 GalNAc-siRNA-ASGPR 복합체는 세포 내로 유입되어 엔도솜(endosome) 내에서 분리된다. 이후 siRNA는 엔도솜으로부터 방출되고, GalNAc은 분해되어 제거된다. ASGPR을 포함한 소포는 다시 세포막과 융합되어 간세포 표면으로 되돌아가 수용체 순환(recycling)을 마친다.엔도솜에서 방출된 siRNA는 헬리케이스(helicase)에 의해 이중가닥 구조가 풀리고, 안티센스 가닥(antisense strand)은 Ago2 단백질을 포함한 다양한 효소들과 함께 RISC를 형성한다. RISC는 표적 mRNA와 상보적인 염기서열에 결합하며, Ago2는 안티센스 가닥의 5′ 말단에서 10번째와 11번째 염기 사이의 인산다이에스터 결합(phosphodiester bond)을 절단하여 mRNA를 분해하고 유전자 발현을 억제한다(Figure 3). siRNA 기반 RNAi 치료제 플랫폼의 특장점은? RNAi은 dsRNA의 존재에 의해 유도되는 유전자 침묵 현상으로, 세포 내에서 특정 mRNA를 선택적으로 분해함으로써 유전자 발현을 전사 후 수준에서 억제하는 고도로 보존된 생물학적 기전이다. RNAi 기전의 핵심 실행 인자인 siRNA는 염기서열 상보성에 기반하여 표적 mRNA를 인식하고 절단함으로써, 병리 단백질의 발현을 효과적으로 차단할 수 있다.이러한 기전을 치료 전략에 응용한 siRNA 기반 RNAi 플랫폼은 기존의 단백질 중심 치료제와는 차별화된 분자적 기전을 바탕으로 정밀하고 지속적인 유전자 억제를 가능하게 하며, 새로운 치료 패러다임으로 주목받고 있다.siRNA 기반 플랫폼의 가장 큰 장점 중 하나는 높은 표적 특이성(target specificity)이다. siRNA는 21~23개의 염기쌍으로 구성된 짧은 dsRNA 분자로, 염기서열 상보성에 따라 특정 mRNA만을 선택적으로 인식하여 작용하므로, 오프타깃(off-target) 효과를 최소화할 수 있다. 여기에 2'-O-methyl, 2'-fluoro 등의 화학적 변형을 적용하면 분해 저항성과 면역자극 회피 능력이 향상되어, 약물의 안전성과 유효성을 동시에 확보할 수 있다.또한 siRNA는 단백질 구조 정보에 의존하지 않고 유전자 염기서열 정보만으로 설계가 가능하기 때문에, 기존 저분자 화합물이나 단백질 기반 치료제들이 접근하기 어려운 ‘undruggable’ 표적(예: 비구조 단백질, 비효소 단백질 등)에 대해서도 유효하게 작용할 수 있다. 특히 단백질 생성 이전 단계인 mRNA 수준에서 병리 유전자의 발현을 차단하기 때문에, 병리 단백질의 생성 자체를 원천적으로 억제할 수 있다는 점에서 치료의 근본적 접근이 가능하다.siRNA 치료제는 일반적으로 한 번의 투여로 수 주에서 수개월간 지속적인 유전자 억제 효과를 유도할 수 있어, 만성질환 치료에서 약물 순응도 향상과 투여 횟수 감소라는 측면에서도 큰 장점을 제공한다.특히 GalNAc-siRNA 전달 플랫폼은 간세포 표면에 특이적으로 발현되는 ASGPR에 선택적으로 결합함으로써 고도의 간 특이성을 확보하면서도 피하주사가 가능하다는 점에서, 임상적 실용성과 접근성이 뛰어나다.siRNA 기반 RNAi 치료제 플랫폼의 문제점과 해결책은 무엇인가? siRNA 기반 RNAi 치료제는 유전자 발현을 정밀하게 조절할 수 있는 혁신적 플랫폼이지만 그 임상적 활용과 적용 범위를 넓히는 데에는 여전히 해결해야 할 중대한 제약이 존재한다. 이러한 한계는 약물의 물리화학적 특성, 전달 효율, 표적 조직 선택성, 면역 반응, 그리고 장기 안전성 측면에서 다양하게 나타난다.첫째, siRNA는 상대적으로 불안정한 고분자 음전하 물질로서, 체내에서 효소적 분해에 매우 취약하다. 자연 상태의 siRNA는 혈중에서 수 분 이내에 빠르게 분해되며, 조직으로 도달하기 전에 대부분 소실된다. 이러한 문제는 여러 화학적 변형을 통해 일부 개선되고 있으나, 여전히 체내 안정성과 전달 효율 간의 균형 조절은 중요한 과제로 남아 있다.둘째, siRNA는 세포막을 통과하기 어려운 물리적 특성을 가지고 있어, 전달 시스템에 대한 의존성이 매우 크다. GalNAc-siRNA 및 LNP-siRNA와 같은 플랫폼은 간세포 표적화에는 성공하였지만, 중추신경계, 심장, 폐, 근육 등 간 이외 조직으로의 선택적 전달은 여전히 기술적으로 제한적이다. 특히 혈관뇌장벽(BBB)과 같은 생리학적 장벽은 siRNA의 중추신경계 질환 치료 적용을 어렵게 하는 근본적 한계로 작용한다.셋째, siRNA는 본질적으로 면역 자극 가능성을 내포한다. siRNA 분자는 Toll-like receptor 3, 7, 8 등에 의해 인식되어 인터페론 반응 및 선천면역 경로를 활성화할 수 있으며, 이는 약물의 안전성과 내약성에 문제를 유발할 수 있다. 특히 반복 투여 시 면역 반응의 축적 또는 과민반응 발생 가능성은 장기 치료에 대한 제한 요소로 작용할 수 있다. 이러한 면역학적 문제는 화학적 안정화 및 설계 최적화를 통해 일부 완화되고 있으나, 특정 환자군에서는 여전히 우려 요소로 간주된다.넷째, siRNA 기반 RNAi는 유전자 발현을 일방적으로 억제(silencing)하는 방식이므로, 표적 유전자의 기능이 완전히 제거되는 것이 항상 바람직하지 않을 수 있다. 일부 유전자는 생리적 항상성 유지에 부분적으로 기여하므로, 과도한 억제가 예기치 않은 부작용이나 대체 경로 활성화를 유발할 수 있다. 특히 하나의 유전자가 다양한 기능을 수행하는 경우(pleiotropy), 정밀한 용량 조절과 억제 수준의 모니터링이 필수적이다.마지막으로, siRNA 기반 치료제는 아직까지 국소 투여나 ex vivo 적용이 제한적이며, 전신 투여를 기본으로 하기 때문에 조직 특이성, 투여 용량, 약물 반감기, 약물 상호작용 등에 대한 정밀한 약물동력학적 이해가 요구된다. 또한 생산 비용이 상대적으로 높고, 대규모 상업화 과정에서의 제조 일관성 및 품질 관리도 반드시 고려해야 할 요소이다.결론적으로, siRNA 기반 RNAi 치료제 플랫폼은 고유의 치료적 강점에도 불구하고, 약물 전달, 조직 선택성, 면역 자극성, 장기 안전성, 비용 구조 등 다양한 기술적 제약에 직면해 있다. 이러한 한계는 siRNA 분자 설계 기술과 전달 플랫폼, 임상 개발 전략의 지속적인 고도화를 통해 극복 가능할 것으로 보인다.다음 편부터 ① 기보시란(Givosiran) ② 루마시란(Lumasiran) ③ 인클리시란(Inclisiran) ④ 브루시란(Vutrisiran) ⑤ 네도시란(Nedosiran) ⑥ 피투시란(Fitusiran) 등의 순으로 게재될 예정이다.참고문헌 1. Giuseppe Cammarata, et al. “Emerging noncoding RNAs contained in extracellular vesicles” Ther Adv Med Oncol 2022, Vol. 14: 1–20 2. Synthesis of GalNAc-siRNA Conjugates(출처: Front. Pharmacol., 14 December 2022). 3. Lei Zhang et al. “The therapeutic prospects of N-acetylgalactosamine-siRNA conjugates“ Front. Pharmacol., 14 December 2022. 3. Vinod Khatri et al. ”Design Synthesis and Biomedical Applications of Glycotripods for Targeting Trimeric Lectins“ Eur J Org Chem Volume 26, Issue 9 March 1, 2023. 4. Katyayani Tatiparti et al. “Review siRNA Delivery Strategies: A Comprehensive Review of Recent Developments” Nanomaterials 2017, 7, 77, 5. Ogochukwu Amaeze et al. “The absorption, distribution, metabolism and elimination characteristics of small interfering RNA therapeutics and the opportunity to predict disposition in pregnant women” Drug Metabolism and Disposition 53 (2025) 100018. 6. 기타 인터넷 자료2025-07-25 06:33:37최병철 박사 -
 정밀의료 협력 늘리는 일루미나…바이오 빅데이터 구축[데일리팜=황병우 기자] DNA 시퀀싱 및 마이크로어레이 기술 분야 선두주자인 일루미나(Illumina)가 국내 파트너링 협력을 늘리며 정밀의료 생태계 확장을 노린다.유전체 분석 기업 마크로젠과 함께 한국 정부의 국가 통합 바이오 빅데이터 구축 사업하는 등 회사가 가진 차세대 시퀀싱(NGS) 기술과의 시너지를 목표로 하고 있다.일루미나는 이달 18일 간담회를 개최하고 회사의 NGS 기술의 임상 도입과 정부가 추진 중인 '국가 바이오 빅데이터 구축 시범사업'을 통한 정밀의료 발전 의지를 밝혔다.현재 일루미나는 유전체 분석 기업 마크로젠과 함께 한국 정부의 국가 통합 바이오 빅데이터 구축 사업에 참여하고 있다.해당 사업은 한국인 14만5952건의 인간 전장 유전체(WGS) 데이터를 2026년 말까지 생산 및 분석할 예정이며, 일루미나는 마크로젠 컨소시엄의 기술 파트너로서 포함돼 있다.국가 통합 바이오 빅데이터 구축 사업은 2020년 시범사업을 시작으로 지금까지 약 2만 건의 유전체 분석을 완료했으며, 이 중 1만 건은 희귀질환 환자의 유전체였다. 또 2028년까지 약 77만 명, 2032년까지 총 100만 명의 한국인 바이오 빅데이터를 구축해 정밀의료를 실현하는 것을 목표로 하고 있다.맥브라이드 일루미나 코리아 제너럴 매니저로버트 맥브라이드 일루미나 코리아 제너럴 매니저(GM)는 "한국은 임상 현장에 NGS 기술을 빠르게 도입함으로써 유전체 연구를 실제 적용할 수 있는 솔루션으로 전환하는 선도국가로 자리매김하고 있다"며 "국가의 중요한 바이오 빅데이터 구축 사업체 참여해 업계를 선도하는 시퀀싱 기술을 제공해, 국내 과학 리더십과 환자 치료 발전에 기여하게 되어 뜻깊게 생각한다"고 밝혔다.또 이승빈 마크로젠 최고과학책임자(CSO)는 "국가 바이오 빅데이터 구축 사업은 단순한 자료수집을 넘어, 개인 맞춤형 의료 시대를 위한 기반을 마련하는 데 목적이 있다. 이번 사업은 개인 맞춤형 의료가 실현되는 미래를 위한 기반을 구축하는 것"이라고 설명했다.실제 국가 바이오 빅데이터 사업은 한국인의 유전적 특성을 반영하면서 글로벌 유전체 연구에서의 격차를 해소하는 것이 핵심이다.정밀의료가 미래 비전을 넘어 현 의료의 핵심으로 리잡고 있는 상황에서 유전질환에 대한 통찰 제시를 통해 혁신을 제공하겠다는 것이다. 이는 국내에 정밀의료 생태계 조성을 노리고 있는 일루미나의 목표와도 맞물린다.최근 일루미나는 MiSeq i100 시리즈를 출시하는 등 NGS 시장 확장을 시도하고 있다.해당 제품은 NGS에 대한 전문 지식이 많지 않은 기관에서도 정밀의료를 위한 유전체 분석을 더 쉽게 수행할 수 있도록 간편하고, 경제적인 소형 데스크탑형 시퀀싱 시스템으로 설계된 것이 특징이다.엘리스 일루미나 아시아 태평양·중동·아프리카 지역 메디컬 어페어 매니저케이티 엘리스 일루미나 아시아 태평양·중동·아프리카 지역 메디컬 어페어 매니저는 "유전체학은 정밀의학의 진화를 가속화 중으로, 특히 종양학 분야에서 표적 치료가 기존 항암 치료에 비해 우수한 임상결과를 입증한 연구들이 발표되고 있다"며 "일루미나는 향후 멀티오믹스 접근법을 통합해 더 깊이 있는 생물학적 통찰을 제공해 전장 유전체 분석 활용이 더 확대되기를 기대하고 있다"고 전했다.다만 NGS가 적용되던 선별급여가 축소되는 등 시장 확대를 위해 정부의 제도적 지원의 허들도 존재한다.NGS 검사는 2017년부터 선별급여 항목에 편입돼 본인부담률 50%가 적용됐지만 복지부가 적합성 평가에 따른 본인부담률 변경을 결정하면서 폐암을 제외한 대부분 암종의 본인부담률이 80%로 상향된 바 있다.이에 대해 맥브라이드 제너럴 매니저는 "임상 유전체 시장이 빠르게 성장하고 있고 회사는 의료계와 협업하고 기술을 조언하는 역할을 하고 있다"며 "기술을 적용하는 데 있어 정부의 신중함은 이해하고 있으며, 향후 기술의 확대 적용이 적절하게 될 수 있도록 회사도 노력하겠다"고 말했다.이어 엘리스 매니저는 "회사는 의사 등 연구자의 연구 프로그램의 지원을 진행하는 등 지역별 요구도를 이해하고 근거를 만들기 위해 협업을 진행하고 있다"며 "나라별 규제 등이 존재할 수 있지만 의사결정에 도움이 될 수 있도록 필요한 협업에 대해 할 수 있는 최대의 지원을 하고 있다"고 덧붙였다.2025-06-18 11:35:30황병우
정밀의료 협력 늘리는 일루미나…바이오 빅데이터 구축[데일리팜=황병우 기자] DNA 시퀀싱 및 마이크로어레이 기술 분야 선두주자인 일루미나(Illumina)가 국내 파트너링 협력을 늘리며 정밀의료 생태계 확장을 노린다.유전체 분석 기업 마크로젠과 함께 한국 정부의 국가 통합 바이오 빅데이터 구축 사업하는 등 회사가 가진 차세대 시퀀싱(NGS) 기술과의 시너지를 목표로 하고 있다.일루미나는 이달 18일 간담회를 개최하고 회사의 NGS 기술의 임상 도입과 정부가 추진 중인 '국가 바이오 빅데이터 구축 시범사업'을 통한 정밀의료 발전 의지를 밝혔다.현재 일루미나는 유전체 분석 기업 마크로젠과 함께 한국 정부의 국가 통합 바이오 빅데이터 구축 사업에 참여하고 있다.해당 사업은 한국인 14만5952건의 인간 전장 유전체(WGS) 데이터를 2026년 말까지 생산 및 분석할 예정이며, 일루미나는 마크로젠 컨소시엄의 기술 파트너로서 포함돼 있다.국가 통합 바이오 빅데이터 구축 사업은 2020년 시범사업을 시작으로 지금까지 약 2만 건의 유전체 분석을 완료했으며, 이 중 1만 건은 희귀질환 환자의 유전체였다. 또 2028년까지 약 77만 명, 2032년까지 총 100만 명의 한국인 바이오 빅데이터를 구축해 정밀의료를 실현하는 것을 목표로 하고 있다.맥브라이드 일루미나 코리아 제너럴 매니저로버트 맥브라이드 일루미나 코리아 제너럴 매니저(GM)는 "한국은 임상 현장에 NGS 기술을 빠르게 도입함으로써 유전체 연구를 실제 적용할 수 있는 솔루션으로 전환하는 선도국가로 자리매김하고 있다"며 "국가의 중요한 바이오 빅데이터 구축 사업체 참여해 업계를 선도하는 시퀀싱 기술을 제공해, 국내 과학 리더십과 환자 치료 발전에 기여하게 되어 뜻깊게 생각한다"고 밝혔다.또 이승빈 마크로젠 최고과학책임자(CSO)는 "국가 바이오 빅데이터 구축 사업은 단순한 자료수집을 넘어, 개인 맞춤형 의료 시대를 위한 기반을 마련하는 데 목적이 있다. 이번 사업은 개인 맞춤형 의료가 실현되는 미래를 위한 기반을 구축하는 것"이라고 설명했다.실제 국가 바이오 빅데이터 사업은 한국인의 유전적 특성을 반영하면서 글로벌 유전체 연구에서의 격차를 해소하는 것이 핵심이다.정밀의료가 미래 비전을 넘어 현 의료의 핵심으로 리잡고 있는 상황에서 유전질환에 대한 통찰 제시를 통해 혁신을 제공하겠다는 것이다. 이는 국내에 정밀의료 생태계 조성을 노리고 있는 일루미나의 목표와도 맞물린다.최근 일루미나는 MiSeq i100 시리즈를 출시하는 등 NGS 시장 확장을 시도하고 있다.해당 제품은 NGS에 대한 전문 지식이 많지 않은 기관에서도 정밀의료를 위한 유전체 분석을 더 쉽게 수행할 수 있도록 간편하고, 경제적인 소형 데스크탑형 시퀀싱 시스템으로 설계된 것이 특징이다.엘리스 일루미나 아시아 태평양·중동·아프리카 지역 메디컬 어페어 매니저케이티 엘리스 일루미나 아시아 태평양·중동·아프리카 지역 메디컬 어페어 매니저는 "유전체학은 정밀의학의 진화를 가속화 중으로, 특히 종양학 분야에서 표적 치료가 기존 항암 치료에 비해 우수한 임상결과를 입증한 연구들이 발표되고 있다"며 "일루미나는 향후 멀티오믹스 접근법을 통합해 더 깊이 있는 생물학적 통찰을 제공해 전장 유전체 분석 활용이 더 확대되기를 기대하고 있다"고 전했다.다만 NGS가 적용되던 선별급여가 축소되는 등 시장 확대를 위해 정부의 제도적 지원의 허들도 존재한다.NGS 검사는 2017년부터 선별급여 항목에 편입돼 본인부담률 50%가 적용됐지만 복지부가 적합성 평가에 따른 본인부담률 변경을 결정하면서 폐암을 제외한 대부분 암종의 본인부담률이 80%로 상향된 바 있다.이에 대해 맥브라이드 제너럴 매니저는 "임상 유전체 시장이 빠르게 성장하고 있고 회사는 의료계와 협업하고 기술을 조언하는 역할을 하고 있다"며 "기술을 적용하는 데 있어 정부의 신중함은 이해하고 있으며, 향후 기술의 확대 적용이 적절하게 될 수 있도록 회사도 노력하겠다"고 말했다.이어 엘리스 매니저는 "회사는 의사 등 연구자의 연구 프로그램의 지원을 진행하는 등 지역별 요구도를 이해하고 근거를 만들기 위해 협업을 진행하고 있다"며 "나라별 규제 등이 존재할 수 있지만 의사결정에 도움이 될 수 있도록 필요한 협업에 대해 할 수 있는 최대의 지원을 하고 있다"고 덧붙였다.2025-06-18 11:35:30황병우 -
 진캐스트, 인비트로큐사와 전략적 파트너십 체결인비트로큐 스티븐 회장(왼쪽)과 진캐스트 이병철 대표가 계약체결 후 기념사진을 촬영하고 있다. [데일리팜=노병철 기자] 암진단 회사 진캐스트(Genecast)는 싱가포르에 기반을 둔 글로벌 바이오기업 인비트로큐(Invitrocue)사와 암진단에 대한 전략적 파트너십과 제품 공급에 대한 마스터서비스 계약을 체결했다고 16일 밝혔다.인비트로큐와 진캐스트가 협력해 개발한 암 치료 프로그램(Real-Time Patient Adaptive Cancer Care Program)이 첫 선을 보인다. 이 시스템은 암 치료의 새로운 패러다임을 열 것으로 기대된다.이번 계약으로 인비트로큐는 진캐스트의 암진단 중합효소, 진단키트, 암패널 제품을 싱가포르 및 독일을 포함한 유럽과 미국에 우선적으로 공급하게 된다.이 치료 시스템은 인비트로큐의 'Onco-PDO' 플랫폼 기술과 진캐스트의 초고감도 혈액 내 암진단 'ADPS' 기술을 결합했다.인비트로큐는 싱가포르에 본사, 독일/호주/태국에 지사를 두고 말기 암 치료에도 유효한 진단 서비스 ‘Onco-PDO’를 제공하고 있으며, 미국, 한국에 진출을 앞두고 있는 글로벌 회사이다. 현재 독일에서는 이미 ‘Onco-PDO’에 대한 보험 적용이 시작된 상태다.인비트로큐의 ‘Onco-PDO’ 플랫폼 기술은 환자 유래 오가노이드(Organoid)를 이용하여 환자의 개인별 최적의 치료약물과 사용량을 선별하고, 진캐스트의 ‘ADPS’는 치료 약물이 환자에게 적용했을 때 주간단위의 혈액검사를 통해 치료 반응과 재발 신호를 실시간으로 추적한다.진캐스트의 ‘ADPS(Allele-Discriminating Priming System)’ 원천기술은 극미량으로 존재하는 혈액 내 ctDNA도 검출하는 초고민감도 플랫폼 기술이다.특히 ‘ADPS’ 기술은 하버드 의과대학, 삼성서울병원과 같은 기관의 연구로 검증된 기술로서 기존 검사보다 100배 높은 민감도(0.001~0.01% MAF)로 암 바이오마커를 탐지할 수 있어, 재발이나 약물 내성을 조기에 발견할 수 있는 것이 강점이다. 검사 결과는 1~2일 내에 제공되며, 진단 비용도 기존 NGS 대비 크게 절감될 전망이다.이 프로그램은 올해 3분기에 독일, 태국에서 먼저 도입되며, 미국, 기타 유럽, 싱가포르와 한국 등으로 점진적으로 확대될 예정이다.인비트로큐사 스티븐 팡 회장은 "이 시스템은 적기에 최적의 암 치료 정보를 제공 함으로써 시행착오를 줄이고 치료 결과를 근본적으로 개선할 것"이라고 말했다.진캐스트 이병철 대표는 "주간 단위 모니터링으로 암 변화에 선제적으로 대응할 수 있게 됐다"고 설명했다.이 프로그램을 기획한 자일로닉스(Xylonix) 정진혁 대표는 "폐암, 3중음성유방암 등 치료 반응이 빠르게 변하는 암종에서 특히 효과적일 것"이라며 "말기에도 최적 치료 선택 후 빠르고 지속적인 조정이 가능해져 치료 효과 제고에 기여할 것"이라고 평가했다.2025-06-16 14:45:12노병철
진캐스트, 인비트로큐사와 전략적 파트너십 체결인비트로큐 스티븐 회장(왼쪽)과 진캐스트 이병철 대표가 계약체결 후 기념사진을 촬영하고 있다. [데일리팜=노병철 기자] 암진단 회사 진캐스트(Genecast)는 싱가포르에 기반을 둔 글로벌 바이오기업 인비트로큐(Invitrocue)사와 암진단에 대한 전략적 파트너십과 제품 공급에 대한 마스터서비스 계약을 체결했다고 16일 밝혔다.인비트로큐와 진캐스트가 협력해 개발한 암 치료 프로그램(Real-Time Patient Adaptive Cancer Care Program)이 첫 선을 보인다. 이 시스템은 암 치료의 새로운 패러다임을 열 것으로 기대된다.이번 계약으로 인비트로큐는 진캐스트의 암진단 중합효소, 진단키트, 암패널 제품을 싱가포르 및 독일을 포함한 유럽과 미국에 우선적으로 공급하게 된다.이 치료 시스템은 인비트로큐의 'Onco-PDO' 플랫폼 기술과 진캐스트의 초고감도 혈액 내 암진단 'ADPS' 기술을 결합했다.인비트로큐는 싱가포르에 본사, 독일/호주/태국에 지사를 두고 말기 암 치료에도 유효한 진단 서비스 ‘Onco-PDO’를 제공하고 있으며, 미국, 한국에 진출을 앞두고 있는 글로벌 회사이다. 현재 독일에서는 이미 ‘Onco-PDO’에 대한 보험 적용이 시작된 상태다.인비트로큐의 ‘Onco-PDO’ 플랫폼 기술은 환자 유래 오가노이드(Organoid)를 이용하여 환자의 개인별 최적의 치료약물과 사용량을 선별하고, 진캐스트의 ‘ADPS’는 치료 약물이 환자에게 적용했을 때 주간단위의 혈액검사를 통해 치료 반응과 재발 신호를 실시간으로 추적한다.진캐스트의 ‘ADPS(Allele-Discriminating Priming System)’ 원천기술은 극미량으로 존재하는 혈액 내 ctDNA도 검출하는 초고민감도 플랫폼 기술이다.특히 ‘ADPS’ 기술은 하버드 의과대학, 삼성서울병원과 같은 기관의 연구로 검증된 기술로서 기존 검사보다 100배 높은 민감도(0.001~0.01% MAF)로 암 바이오마커를 탐지할 수 있어, 재발이나 약물 내성을 조기에 발견할 수 있는 것이 강점이다. 검사 결과는 1~2일 내에 제공되며, 진단 비용도 기존 NGS 대비 크게 절감될 전망이다.이 프로그램은 올해 3분기에 독일, 태국에서 먼저 도입되며, 미국, 기타 유럽, 싱가포르와 한국 등으로 점진적으로 확대될 예정이다.인비트로큐사 스티븐 팡 회장은 "이 시스템은 적기에 최적의 암 치료 정보를 제공 함으로써 시행착오를 줄이고 치료 결과를 근본적으로 개선할 것"이라고 말했다.진캐스트 이병철 대표는 "주간 단위 모니터링으로 암 변화에 선제적으로 대응할 수 있게 됐다"고 설명했다.이 프로그램을 기획한 자일로닉스(Xylonix) 정진혁 대표는 "폐암, 3중음성유방암 등 치료 반응이 빠르게 변하는 암종에서 특히 효과적일 것"이라며 "말기에도 최적 치료 선택 후 빠르고 지속적인 조정이 가능해져 치료 효과 제고에 기여할 것"이라고 평가했다.2025-06-16 14:45:12노병철 -
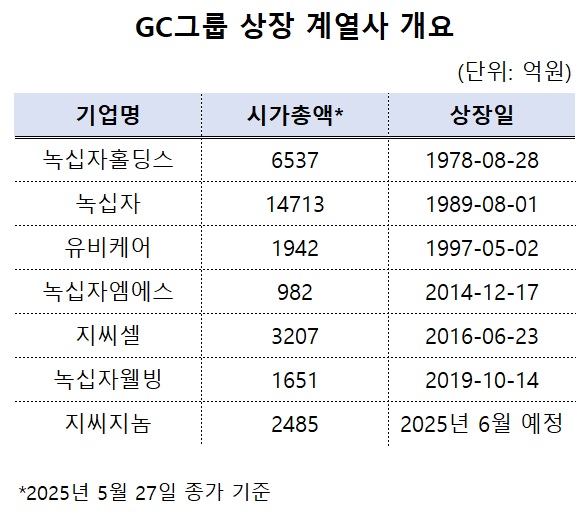 GC그룹, 제약업계 최다 상장사 7개 확보...총 시총 3조↑[데일리팜=차지현 기자] GC그룹 유전체 분석 계열사 GC지놈이 기업공개(IPO)에 나선다. GC지놈이 성공적으로 코스닥에 입성하면 GC그룹 상장 계열사는 총 7개로 확대된다. 이들 기업의 총 시가총액은 3조원을 넘어설 전망이다.GC지놈 희망 밴드 상단서 공모가 확정, 내달 코스닥 입성 추진28일 금융감독원에 따르면 GC지놈은 27일 최종 공모가를 1만500원으로 확정했다. 1주당 희망 공모가 밴드 상단에서 최종 가격이 결정됐다.GC지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 질병 진단과 예측은 물론 이를 통해 맞춤형 치료까지 지원하겠다는 목표다. 삼성서울병원 교수 출신 기창석 대표가 2018년부터 회사를 이끌고 있다.유전자 분석과 인공지능(AI) 기반 정밀진단 솔루션이 GC지놈의 핵심 기술이다. 국내 약 900여개 병·의원과 검진 기관에 300종 이상 산과, 건강검진, 암 정밀진단, 유전 희귀질환 분야 맞춤형 분자진단 서비스를 제공 중이다. 현재 미국, 유럽, 중동, 아시아태평양 등 19개국에 진출한 상태다.앞서 GC지놈은 지난 19일부터 23일까지 5영업일 동안 수요예측을 진행했다. 수요예측에는 총 1692개 기관이 참여해 547.47대 1의 경쟁률을 기록했다. 참여 기관의 95.1%가 밴드 상단 이상의 가격을 제시했다.희망 공모 밴드 상단에서 최종 공모가가 결정되면서 GC지놈은 이번 IPO를 통해 420억원의 자금을 조달하게 됐다. 최종 공모가 기준 예상 시가총액은 2485억원이다.GC지놈은 IPO로 확보한 공모 자금을 연구개발(R&D)과 시설 투자에 활용할 예정이다. 공모가 하단 기준 공모액에서 상장주선인의 인수 금액과 발행제비용을 제외한 순수입금 353억원을 R&D와 검사설비 증설, 검사실 확장, 서버구축 등에 사용한다. 세부적으로 R&D 측면에서는 다중암 조기 선별검사 제품의 암종 확대, NGS 플랫폼 추가 등에 투입하겠다는 계획을 제시했다.국내 제약사 중 상장 계열사 수 1위…상장 계열사 총 시총 2조9032억GC그룹은 국내 제약사 중 가장 많은 상장사를 보유한 기업으로 손꼽힌다. 현재 GC그룹의 상장 계열사는 녹십자홀딩스, 녹십자, 녹십자웰빙, 녹십자엠에스, 지씨셀, 유비케어 등 총 6곳이다. 국내 상위 제약사로 거론되는 종근당그룹과 JW그룹, 동아쏘시오그룹은 각각 4곳씩, 한미약품그룹은 3곳의 상장 계열사를 거느리고 있다.녹십자는 1세대 개성상인으로 불리는 고(故) 허채경 한일시멘트 창업자의 차남인 고(故) 허영섭 회장이 1967년 부친의 지원을 받아 만든 수도미생물약품판매로 출발했다. 1969년 '극동제약', 1971년 '녹십자'로 사명을 변경했고 1978년 8월 녹십자홀딩스가 유가증권시장에 상장했다. 이어 1989년 8월 녹십자홀딩스 핵심 자회사 녹십자가 코스피에 입성했다.CG그룹은 2001년 국내 제약업계 최초로 지주사 체제로 전환했다. 녹십자홀딩스가 지주사로서 그룹 전체의 경영전략 수립과 신사업 진출, 출자 자산의 포트폴리오 관리 등을 맡고, 실제 사업은 각 자회사가 수행하는 구조다.2014년 CG그룹 계열 녹십자엠에스가 코스닥 시장에 상장했다. 2003년 설립된 녹십자엠에스는 체외진단용의약품, 의료기기의약품과 의약외품 제조판매를 주 사업으로 영위 중이다. 3월 말 기준 녹십자가 녹십자엠에스 지분 40.3%로 최대주주에 올라 있고 허일섭 GC 회장도 녹십자엠에스 지분 10.1%를 보유 중이다.GC그룹의 제대혈과 세포치료제 사업 계열사 녹십자랩셀은 2016년 코스닥에 진입했다. 앞서 녹십자는 지난 2012년 150억원을 투자해 녹십자셀의 전신인 이노셀을 사들인 바 있다. 이후 2021년 녹십자셀이 녹십자랩셀에 흡수합병되면서 사명이 지씨셀로 변경됐다. 3월 말 기준 지씨셀에 대한 녹십자와 녹십자홀딩스 지분율은 각각 33.3%와 8.5%다.(자료: 한국거래소, 금융감독원) 영양 주사제, 건강기능식품 제조와 판매 등을 영위하는 녹십자웰빙은 2019년 10월 코스닥에 상장했다. 녹십자웰빙은 녹십자홀딩스와 일본 바이오프로덕츠의 한국법인 제이비피코리아의 합작투자 회사 '지씨재팬바이오'로 2004년 설립됐다. 이후 2015년 천연물 의약품과 소재 전문회사인 녹십자HS와 녹십자의 WB사업부를 합병·인수하면서 녹십자웰빙으로 사명이 바뀌었다.GC그룹은 대형 인수합병(M&A)을 통해서도 보유 상장사를 확대했다. 지씨케어(옛 녹십자헬스케어)는 지난 2021년 월 2088억원을 들여 IT 기업 유비케어를 인수했다. 지씨케어는 녹십자그룹의 헬스케어 부문 자회사로 IT 기반의 차별화된 개인 맞춤형 건강관리 서비스를 제공하는 헬스케어 전문 기업이다.녹십자홀딩스는 지씨케어와 함께 재무적투자자 시냅틱인베스트먼트와 공동으로 유비케어의 지분 52.65%를 취득했다. 유비케어 인수대금 2088억원 중 녹십자홀딩스가 녹십자헬스케어의 유상증자에 참여하는 방식으로 789억원을 투자하고 녹십자헬스케어가 500억원 가량을 외부 차입을 통해 조달했다. 녹십자그룹 차원에서 유비케어 인수에 1289억원을 투입했다.GC지놈이 성공적으로 코스닥에 입성하면 GC그룹 입장에선 상장 계열사가 총 7개로 확대된다. 이들 기업의 총 시총은 3조1517억원에 달할 것으로 추산된다. 27일 종가 기준 GC그룹이 보유한 상장 계열사 6곳의 시총은 총 2조9032억원 수준이다.2025-05-28 12:00:33차지현
GC그룹, 제약업계 최다 상장사 7개 확보...총 시총 3조↑[데일리팜=차지현 기자] GC그룹 유전체 분석 계열사 GC지놈이 기업공개(IPO)에 나선다. GC지놈이 성공적으로 코스닥에 입성하면 GC그룹 상장 계열사는 총 7개로 확대된다. 이들 기업의 총 시가총액은 3조원을 넘어설 전망이다.GC지놈 희망 밴드 상단서 공모가 확정, 내달 코스닥 입성 추진28일 금융감독원에 따르면 GC지놈은 27일 최종 공모가를 1만500원으로 확정했다. 1주당 희망 공모가 밴드 상단에서 최종 가격이 결정됐다.GC지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 질병 진단과 예측은 물론 이를 통해 맞춤형 치료까지 지원하겠다는 목표다. 삼성서울병원 교수 출신 기창석 대표가 2018년부터 회사를 이끌고 있다.유전자 분석과 인공지능(AI) 기반 정밀진단 솔루션이 GC지놈의 핵심 기술이다. 국내 약 900여개 병·의원과 검진 기관에 300종 이상 산과, 건강검진, 암 정밀진단, 유전 희귀질환 분야 맞춤형 분자진단 서비스를 제공 중이다. 현재 미국, 유럽, 중동, 아시아태평양 등 19개국에 진출한 상태다.앞서 GC지놈은 지난 19일부터 23일까지 5영업일 동안 수요예측을 진행했다. 수요예측에는 총 1692개 기관이 참여해 547.47대 1의 경쟁률을 기록했다. 참여 기관의 95.1%가 밴드 상단 이상의 가격을 제시했다.희망 공모 밴드 상단에서 최종 공모가가 결정되면서 GC지놈은 이번 IPO를 통해 420억원의 자금을 조달하게 됐다. 최종 공모가 기준 예상 시가총액은 2485억원이다.GC지놈은 IPO로 확보한 공모 자금을 연구개발(R&D)과 시설 투자에 활용할 예정이다. 공모가 하단 기준 공모액에서 상장주선인의 인수 금액과 발행제비용을 제외한 순수입금 353억원을 R&D와 검사설비 증설, 검사실 확장, 서버구축 등에 사용한다. 세부적으로 R&D 측면에서는 다중암 조기 선별검사 제품의 암종 확대, NGS 플랫폼 추가 등에 투입하겠다는 계획을 제시했다.국내 제약사 중 상장 계열사 수 1위…상장 계열사 총 시총 2조9032억GC그룹은 국내 제약사 중 가장 많은 상장사를 보유한 기업으로 손꼽힌다. 현재 GC그룹의 상장 계열사는 녹십자홀딩스, 녹십자, 녹십자웰빙, 녹십자엠에스, 지씨셀, 유비케어 등 총 6곳이다. 국내 상위 제약사로 거론되는 종근당그룹과 JW그룹, 동아쏘시오그룹은 각각 4곳씩, 한미약품그룹은 3곳의 상장 계열사를 거느리고 있다.녹십자는 1세대 개성상인으로 불리는 고(故) 허채경 한일시멘트 창업자의 차남인 고(故) 허영섭 회장이 1967년 부친의 지원을 받아 만든 수도미생물약품판매로 출발했다. 1969년 '극동제약', 1971년 '녹십자'로 사명을 변경했고 1978년 8월 녹십자홀딩스가 유가증권시장에 상장했다. 이어 1989년 8월 녹십자홀딩스 핵심 자회사 녹십자가 코스피에 입성했다.CG그룹은 2001년 국내 제약업계 최초로 지주사 체제로 전환했다. 녹십자홀딩스가 지주사로서 그룹 전체의 경영전략 수립과 신사업 진출, 출자 자산의 포트폴리오 관리 등을 맡고, 실제 사업은 각 자회사가 수행하는 구조다.2014년 CG그룹 계열 녹십자엠에스가 코스닥 시장에 상장했다. 2003년 설립된 녹십자엠에스는 체외진단용의약품, 의료기기의약품과 의약외품 제조판매를 주 사업으로 영위 중이다. 3월 말 기준 녹십자가 녹십자엠에스 지분 40.3%로 최대주주에 올라 있고 허일섭 GC 회장도 녹십자엠에스 지분 10.1%를 보유 중이다.GC그룹의 제대혈과 세포치료제 사업 계열사 녹십자랩셀은 2016년 코스닥에 진입했다. 앞서 녹십자는 지난 2012년 150억원을 투자해 녹십자셀의 전신인 이노셀을 사들인 바 있다. 이후 2021년 녹십자셀이 녹십자랩셀에 흡수합병되면서 사명이 지씨셀로 변경됐다. 3월 말 기준 지씨셀에 대한 녹십자와 녹십자홀딩스 지분율은 각각 33.3%와 8.5%다.(자료: 한국거래소, 금융감독원) 영양 주사제, 건강기능식품 제조와 판매 등을 영위하는 녹십자웰빙은 2019년 10월 코스닥에 상장했다. 녹십자웰빙은 녹십자홀딩스와 일본 바이오프로덕츠의 한국법인 제이비피코리아의 합작투자 회사 '지씨재팬바이오'로 2004년 설립됐다. 이후 2015년 천연물 의약품과 소재 전문회사인 녹십자HS와 녹십자의 WB사업부를 합병·인수하면서 녹십자웰빙으로 사명이 바뀌었다.GC그룹은 대형 인수합병(M&A)을 통해서도 보유 상장사를 확대했다. 지씨케어(옛 녹십자헬스케어)는 지난 2021년 월 2088억원을 들여 IT 기업 유비케어를 인수했다. 지씨케어는 녹십자그룹의 헬스케어 부문 자회사로 IT 기반의 차별화된 개인 맞춤형 건강관리 서비스를 제공하는 헬스케어 전문 기업이다.녹십자홀딩스는 지씨케어와 함께 재무적투자자 시냅틱인베스트먼트와 공동으로 유비케어의 지분 52.65%를 취득했다. 유비케어 인수대금 2088억원 중 녹십자홀딩스가 녹십자헬스케어의 유상증자에 참여하는 방식으로 789억원을 투자하고 녹십자헬스케어가 500억원 가량을 외부 차입을 통해 조달했다. 녹십자그룹 차원에서 유비케어 인수에 1289억원을 투입했다.GC지놈이 성공적으로 코스닥에 입성하면 GC그룹 입장에선 상장 계열사가 총 7개로 확대된다. 이들 기업의 총 시총은 3조1517억원에 달할 것으로 추산된다. 27일 종가 기준 GC그룹이 보유한 상장 계열사 6곳의 시총은 총 2조9032억원 수준이다.2025-05-28 12:00:33차지현 -
 GC지놈, 공모가 1만500원…공모가 상단[데일리팜=차지현 기자] 녹십자그룹 유전체 분석 계열사 GC지놈(대표이사 기창석)이 최종 공모가를 1만500원으로 확정했다. 1주당 희망 공모가 밴드 상단에서 최종 가격이 결정됐다.GC지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 질병 진단과 예측은 물론 이를 통해 맞춤형 치료까지 지원하겠다는 목표다. 삼성서울병원 교수 출신 기창석 대표가 2018년부터 회사를 이끌고 있다.유전자 분석과 인공지능(AI) 기반 정밀진단 솔루션이 GC지놈 의 핵심 기술이다. 국내 약 900여개 병·의원과 검진 기관에 300종 이상 산과, 건강검진, 암 정밀진단, 유전 희귀질환 분야 맞춤형 분자진단 서비스를 제공 중이다. 현재 미국, 유럽, 중동, 아시아태평양 등 19개국에 진출한 상태다.앞서 GC지놈은 지난 19일부터 23일까지 5영업일 동안 수요예측을 진행했다. 수요예측에는 총 1692개 기관이 참여해 547.47대 1의 경쟁률을 기록했다. 참여 기관의 95.1%가 밴드 상단 이상의 가격을 제시했다.희망 공모 밴드 상단에서 최종 공모가가 결정되면서 GC지놈은 이번 기업공개(IPO)를 통해 420억원의 자금을 조달하게 됐다. 최종 공모가 기준 예상 시가총액은 2485억원이다.GC지놈은 IPO로 확보한 공모 자금을 연구개발(R&D)과 시설 투자에 활용할 예정이다. 공모가 하단 기준 공모액에서 상장주선인의 인수 금액과 발행제비용을 제외한 순수입금 353억원을 R&D와 검사설비 증설, 검사실 확장, 서버구축 등에 사용한다. 세부적으로 R&D 측면에서는 다중암 조기 선별검사 제품의 암종 확대, NGS 플랫폼 추가 등에 투입하겠다는 계획을 제시했다.GC지놈은 오는 29일~30일 이틀간 기관투자자와 일반투자자를 대상으로 청약을 실시, 내달 초 코스닥 시장에 상장할 계획이다. 상장 주관사는 삼성증권이다.기창석 GC지놈 대표이사는 "당사의 기업가치를 긍정적으로 평가해 많은 성원을 보내준 모든 투자자에께 진심으로 감사한다"면서 "GC지놈은 300종 이상의 다양한 유전자 검사 서비스를 900개 이상의 병∙의원에 제공하며, 안정적인 매출 성장을 지속하고 있다"고 했다. 이어 그는 "글로벌 시장에서의 실적과 입지를 더욱 강화하면서 글로벌 탑 티어 액체생검·임상유전체 분석 선도 기업으로 도약할 것"이라고 덧붙였다.2025-05-27 15:11:11차지현
GC지놈, 공모가 1만500원…공모가 상단[데일리팜=차지현 기자] 녹십자그룹 유전체 분석 계열사 GC지놈(대표이사 기창석)이 최종 공모가를 1만500원으로 확정했다. 1주당 희망 공모가 밴드 상단에서 최종 가격이 결정됐다.GC지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 질병 진단과 예측은 물론 이를 통해 맞춤형 치료까지 지원하겠다는 목표다. 삼성서울병원 교수 출신 기창석 대표가 2018년부터 회사를 이끌고 있다.유전자 분석과 인공지능(AI) 기반 정밀진단 솔루션이 GC지놈 의 핵심 기술이다. 국내 약 900여개 병·의원과 검진 기관에 300종 이상 산과, 건강검진, 암 정밀진단, 유전 희귀질환 분야 맞춤형 분자진단 서비스를 제공 중이다. 현재 미국, 유럽, 중동, 아시아태평양 등 19개국에 진출한 상태다.앞서 GC지놈은 지난 19일부터 23일까지 5영업일 동안 수요예측을 진행했다. 수요예측에는 총 1692개 기관이 참여해 547.47대 1의 경쟁률을 기록했다. 참여 기관의 95.1%가 밴드 상단 이상의 가격을 제시했다.희망 공모 밴드 상단에서 최종 공모가가 결정되면서 GC지놈은 이번 기업공개(IPO)를 통해 420억원의 자금을 조달하게 됐다. 최종 공모가 기준 예상 시가총액은 2485억원이다.GC지놈은 IPO로 확보한 공모 자금을 연구개발(R&D)과 시설 투자에 활용할 예정이다. 공모가 하단 기준 공모액에서 상장주선인의 인수 금액과 발행제비용을 제외한 순수입금 353억원을 R&D와 검사설비 증설, 검사실 확장, 서버구축 등에 사용한다. 세부적으로 R&D 측면에서는 다중암 조기 선별검사 제품의 암종 확대, NGS 플랫폼 추가 등에 투입하겠다는 계획을 제시했다.GC지놈은 오는 29일~30일 이틀간 기관투자자와 일반투자자를 대상으로 청약을 실시, 내달 초 코스닥 시장에 상장할 계획이다. 상장 주관사는 삼성증권이다.기창석 GC지놈 대표이사는 "당사의 기업가치를 긍정적으로 평가해 많은 성원을 보내준 모든 투자자에께 진심으로 감사한다"면서 "GC지놈은 300종 이상의 다양한 유전자 검사 서비스를 900개 이상의 병∙의원에 제공하며, 안정적인 매출 성장을 지속하고 있다"고 했다. 이어 그는 "글로벌 시장에서의 실적과 입지를 더욱 강화하면서 글로벌 탑 티어 액체생검·임상유전체 분석 선도 기업으로 도약할 것"이라고 덧붙였다.2025-05-27 15:11:11차지현 -
 GC지놈, 아랍에미리트 신규 공급계약 체결[데일리팜=차지현 기자] 녹십자그룹 유전체 분석 계열사 GC지놈(대표이사 기창석)이 중동 시장 진출에 속도를 내고 있다.GC지놈은 아랍에미리트에 본사를 둔 의료기기와 헬스케어 솔루션 전문 유통업체 폴베르트 메디컬 유한책임회사(Vollwert Medical LLC)와 비침습산전검사 '지니프트'(G-NIPT) 공급 계약을 체결했다고 27일 밝혔다.지니프트는 GC지놈의 차세대 염기서열분석기법(NGS)을 이용해 산모의 혈액 내 존재하는 태아 DNA를 검출, 염색체 이상 여부를 확인하는 검사다. 인공지능(AI) 기술과 DNA 단편거리(FD) 개념을 최초로 도입해 기존 방식보다 검출 정확도와 신뢰도를 대폭 향상했다는 게 회사 측 설명이다.이번 공급계약을 통해 GC지놈은 아랍에미리트 내 브랜드 인지도를 제고하고, 중장기적으로 시장 점유율을 확대해 나갈 예정이다. 아랍에미리트는 출산 전 유전 질환 조기 진단 수요가 꾸준히 증가하고 있고, 비침습산전검사 시장도 연평균 19% 이상의 높은 성장세를 보이고 있다.GC지놈 파트너사인 폴베르트는 의료 장비와 병원 시스템 분야에서 오랜 경험을 바탕으로 아랍에미리트 내 폭넓은 병∙의원 네트워크를 구축하고 있다. 사우디아라비아, 카타르, 오만, 쿠웨이트, 바레인 등 중동 주요 국가에 대한 유통 채널도 보유 중이다. 이를 통해 GC지놈은 추후 중동 전역으로 서비스 확대가 가능할 것으로 전망했다.기창석 GC지놈 대표는 "폴베르트와 협력을 통해 희귀 유전 질환 검사 등으로 서비스 포트폴리오를 확대할 수 있는 기반을 마련해 나갈 예정"이라며 "자사의 우수한 제품력을 바탕으로 해외 시장 진출에 속도를 낼 것"이라고 했다.2025-05-27 10:40:56차지현
GC지놈, 아랍에미리트 신규 공급계약 체결[데일리팜=차지현 기자] 녹십자그룹 유전체 분석 계열사 GC지놈(대표이사 기창석)이 중동 시장 진출에 속도를 내고 있다.GC지놈은 아랍에미리트에 본사를 둔 의료기기와 헬스케어 솔루션 전문 유통업체 폴베르트 메디컬 유한책임회사(Vollwert Medical LLC)와 비침습산전검사 '지니프트'(G-NIPT) 공급 계약을 체결했다고 27일 밝혔다.지니프트는 GC지놈의 차세대 염기서열분석기법(NGS)을 이용해 산모의 혈액 내 존재하는 태아 DNA를 검출, 염색체 이상 여부를 확인하는 검사다. 인공지능(AI) 기술과 DNA 단편거리(FD) 개념을 최초로 도입해 기존 방식보다 검출 정확도와 신뢰도를 대폭 향상했다는 게 회사 측 설명이다.이번 공급계약을 통해 GC지놈은 아랍에미리트 내 브랜드 인지도를 제고하고, 중장기적으로 시장 점유율을 확대해 나갈 예정이다. 아랍에미리트는 출산 전 유전 질환 조기 진단 수요가 꾸준히 증가하고 있고, 비침습산전검사 시장도 연평균 19% 이상의 높은 성장세를 보이고 있다.GC지놈 파트너사인 폴베르트는 의료 장비와 병원 시스템 분야에서 오랜 경험을 바탕으로 아랍에미리트 내 폭넓은 병∙의원 네트워크를 구축하고 있다. 사우디아라비아, 카타르, 오만, 쿠웨이트, 바레인 등 중동 주요 국가에 대한 유통 채널도 보유 중이다. 이를 통해 GC지놈은 추후 중동 전역으로 서비스 확대가 가능할 것으로 전망했다.기창석 GC지놈 대표는 "폴베르트와 협력을 통해 희귀 유전 질환 검사 등으로 서비스 포트폴리오를 확대할 수 있는 기반을 마련해 나갈 예정"이라며 "자사의 우수한 제품력을 바탕으로 해외 시장 진출에 속도를 낼 것"이라고 했다.2025-05-27 10:40:56차지현 -
 CG인바이츠 "NGS 검사 미국 병리학회 인증 획득"[데일리팜=이석준 기자] CG인바이츠(대표 이호영, 오수연)는 현재 서비스 중인 차세대 염기서열 분석검사(NGS) 및 마이크로어레이(Microarray) 임상 검사 부문에서 미국 병리학회(CAP) 인증을 받았다고 20일 밝혔다.회사에 따르면 CAP는 1961년에 설립됐으며 병리학계에서 세계 최대 규모의 학회이자 가장 권위있는 임상검사실 인증기관이다. CAP인증 획득은 임상검사실 정도관리의 국제 기준 및 표준으로 여겨진다.해당 인증은 임상 검사를 제공하는 검사 실적, 관리, 기록뿐 아니라 임직원들의 업무 처리수준, 시설 상태, 장비, 안전 및 운영 등 모든 부분에서 최고 수준으로 관리가 되고 있는지에 대해 심사위원단의 철저한 현장 실사를 거쳐야 최종 인증을 획득할 수 있다.CG인바이츠는 이번 인증으로 국내에서 비의료기관으로는 유일하게 CAP 인증을 획득한 기관이 됐다.오수연 대표이사는 "CAP 인증 획득을 통해 글로벌 최고 수준의 유전체 분석서비스가 가능해졌으며 국내는 물론 해외 시장에서 유전체 분석 서비스의 대외 경쟁력을 강화해 더 많은 검사 서비스를 활발하게 제공할 수 있는 기반을 확보했다”고 밝혔다.한편, CG인바이츠가 포함된 인바이츠생태계는 데이터 기반 개인 맞춤형 건강관리, 질환관리 및 AI기반 질환예측 구현을 목표로 구성된 헬스케어 기업군이다. 서로가 보유한 핵심 역량을 유기적으로 연계시켜 데이터의 측정 및 수집, 분석과 융합에서 상용화에 이르는 맞춤형 정밀 헬스케어의 전 주기 가치사슬을 구축하고 있다.2025-05-20 14:01:55이석준
CG인바이츠 "NGS 검사 미국 병리학회 인증 획득"[데일리팜=이석준 기자] CG인바이츠(대표 이호영, 오수연)는 현재 서비스 중인 차세대 염기서열 분석검사(NGS) 및 마이크로어레이(Microarray) 임상 검사 부문에서 미국 병리학회(CAP) 인증을 받았다고 20일 밝혔다.회사에 따르면 CAP는 1961년에 설립됐으며 병리학계에서 세계 최대 규모의 학회이자 가장 권위있는 임상검사실 인증기관이다. CAP인증 획득은 임상검사실 정도관리의 국제 기준 및 표준으로 여겨진다.해당 인증은 임상 검사를 제공하는 검사 실적, 관리, 기록뿐 아니라 임직원들의 업무 처리수준, 시설 상태, 장비, 안전 및 운영 등 모든 부분에서 최고 수준으로 관리가 되고 있는지에 대해 심사위원단의 철저한 현장 실사를 거쳐야 최종 인증을 획득할 수 있다.CG인바이츠는 이번 인증으로 국내에서 비의료기관으로는 유일하게 CAP 인증을 획득한 기관이 됐다.오수연 대표이사는 "CAP 인증 획득을 통해 글로벌 최고 수준의 유전체 분석서비스가 가능해졌으며 국내는 물론 해외 시장에서 유전체 분석 서비스의 대외 경쟁력을 강화해 더 많은 검사 서비스를 활발하게 제공할 수 있는 기반을 확보했다”고 밝혔다.한편, CG인바이츠가 포함된 인바이츠생태계는 데이터 기반 개인 맞춤형 건강관리, 질환관리 및 AI기반 질환예측 구현을 목표로 구성된 헬스케어 기업군이다. 서로가 보유한 핵심 역량을 유기적으로 연계시켜 데이터의 측정 및 수집, 분석과 융합에서 상용화에 이르는 맞춤형 정밀 헬스케어의 전 주기 가치사슬을 구축하고 있다.2025-05-20 14:01:55이석준 -
 난소암 엇박자 급여체계, 환자 부담...개선 여론 고조[데일리팜=황병우 기자] 상동재조합결핍(HRd) 양성 난소암에 대한 급여 확대에도 불구하고, 관련 검사가 비급여인 상황을 해결하고자 학회가 발 벗고 나섰다.업계에 따르면 대한부인종양학회는 최근 보건복지부에 HRd 검사의 급여 적용을 제안하기 위해 관련 근거를 수집 중이다.HRd는 DNA 손상 메커니즘 중 하나인 상동 재조합 경로의 결핍을 의미한다. HRd가 양성이면 암세포가 DNA 손상을 효율적으로 복구하지 못한다.특히 유방암, 난소암 등에서 주로 발현되는 BRCA1/2 유전자 변이로 HRd가 나타나며, 난소암에서 HRd 발현 빈도는 임상적으로 50%가량으로 알려졌다.대한부인종양학회가 HRd 검사에 주목하는 이유는 난소암 치료제인 제줄라의 급여 확대와 관련이 있다.제줄라는 지난해 10월부터 건강보험 급여 기준이 상동재조합결핍(HRd) 양성 난소암 치료로 확대됐다. 그간 제줄라는 난소암 1차 요법에서 백금기반요법에 반응한 BRCA 변이 난소암 환자 대상 유지요법에 급여가 인정되고 있었다.해당 급여 확대로 제줄라는 HRd 양성 난소암 환자의 1차 단독 유지요법에 유일하게 보험급여 적용되는 PARP(Poly ADP-ribose Polymerase) 억제제로 자리매김했다.제줄라 제품사진실제 제줄라는 급여 확대 이후 약 7개월이 지난 시점에서 처방을 지속적으로 늘리고 있는 상태다. 난소암 환자들은 100mg 정제 2개를 1일 1회만 복용하게 되는데, 기존 난소암 치료제 가운데 1일 1회 복용은 제줄라가 유일하다.특히 허가 임상인 PRIMA 연구뿐만 아니라 추적 관찰 연구를 통해 장기간의 PFS 연장 혜택을 확인한 만큼 급여 확대 이후 처방이 증가하는 것은 자연스러운 흐름이다.문제는 급여 확대의 핵심인 HRd 양성에 있다. 급여 기준이 HRd 양성 난소암 치료인 만큼 HRd 양성 여부를 필수적으로 확인해야 한다.하지만 현재 제줄라가 급여가 적용되는 것과 달리 HRd 검사는 비급여로 남아 있는 상태다.HRd 검사는 차세대염기서열분석(NGS)에 기반한 유전자 패널 검사가 필요한 데 이를 위해 약 250만원을 환자가 부담해야 하는 상황이다.반면, BRCA1/2 변이 검사는 국가사업과 일부 건강보험 적용을 통해 상대적으로 접근성이 높아, 두 검사 간의 격차가 발생하고 있다.즉, 급여가 확대된 제줄라를 처방받기 위해서는 고가의 비급여 검사를 환자가 부담해야 하는 간극이 발생하는 것이다.대한부인종양학회 역시 이 같은 문제점을 인지하고 해결책을 마련하기 위해 정책을 제안한다는 계획이다.학회 관계자는 "환자로서는 급여 약제를 처방하기 위해서 비급여 검사를 해야한다는 점은 이해하기 어려울 수밖에 없는 부분"이라며 "한국의 검사체계와 외국 사례 등의 검토 및 회의를 통해 보건복지부에 관련 의견을 전달하려고 구상하고 있다"고 밝혔다.HRd 검사에 대한 학회의 의견은 이르면 상반기 중으로 보건복지부와 건강보험심사평가원 등에 전달할 예정이지만 제도권 편입을 위한 실질적 논의로 이어질지는 좀 더 지켜봐야 한다.난소암에서 HRd 발현 빈도가 약 50%에 달하고, 치료 전 대부분의 환자가 검사를 받아야 한다는 점을 고려하면, 재정적 부담이라는 현실적인 문제도 남아 있기 때문이다.학회 관계자는 "국내 난소암 환자의 치료 성과 향상을 위해서는 HRd 검사의 원활한 도입과 활용이 필수적인 만큼 제도적 뒷받침이 필요할 것으로 본다"고 덧붙였다.2025-05-02 06:00:16황병우
난소암 엇박자 급여체계, 환자 부담...개선 여론 고조[데일리팜=황병우 기자] 상동재조합결핍(HRd) 양성 난소암에 대한 급여 확대에도 불구하고, 관련 검사가 비급여인 상황을 해결하고자 학회가 발 벗고 나섰다.업계에 따르면 대한부인종양학회는 최근 보건복지부에 HRd 검사의 급여 적용을 제안하기 위해 관련 근거를 수집 중이다.HRd는 DNA 손상 메커니즘 중 하나인 상동 재조합 경로의 결핍을 의미한다. HRd가 양성이면 암세포가 DNA 손상을 효율적으로 복구하지 못한다.특히 유방암, 난소암 등에서 주로 발현되는 BRCA1/2 유전자 변이로 HRd가 나타나며, 난소암에서 HRd 발현 빈도는 임상적으로 50%가량으로 알려졌다.대한부인종양학회가 HRd 검사에 주목하는 이유는 난소암 치료제인 제줄라의 급여 확대와 관련이 있다.제줄라는 지난해 10월부터 건강보험 급여 기준이 상동재조합결핍(HRd) 양성 난소암 치료로 확대됐다. 그간 제줄라는 난소암 1차 요법에서 백금기반요법에 반응한 BRCA 변이 난소암 환자 대상 유지요법에 급여가 인정되고 있었다.해당 급여 확대로 제줄라는 HRd 양성 난소암 환자의 1차 단독 유지요법에 유일하게 보험급여 적용되는 PARP(Poly ADP-ribose Polymerase) 억제제로 자리매김했다.제줄라 제품사진실제 제줄라는 급여 확대 이후 약 7개월이 지난 시점에서 처방을 지속적으로 늘리고 있는 상태다. 난소암 환자들은 100mg 정제 2개를 1일 1회만 복용하게 되는데, 기존 난소암 치료제 가운데 1일 1회 복용은 제줄라가 유일하다.특히 허가 임상인 PRIMA 연구뿐만 아니라 추적 관찰 연구를 통해 장기간의 PFS 연장 혜택을 확인한 만큼 급여 확대 이후 처방이 증가하는 것은 자연스러운 흐름이다.문제는 급여 확대의 핵심인 HRd 양성에 있다. 급여 기준이 HRd 양성 난소암 치료인 만큼 HRd 양성 여부를 필수적으로 확인해야 한다.하지만 현재 제줄라가 급여가 적용되는 것과 달리 HRd 검사는 비급여로 남아 있는 상태다.HRd 검사는 차세대염기서열분석(NGS)에 기반한 유전자 패널 검사가 필요한 데 이를 위해 약 250만원을 환자가 부담해야 하는 상황이다.반면, BRCA1/2 변이 검사는 국가사업과 일부 건강보험 적용을 통해 상대적으로 접근성이 높아, 두 검사 간의 격차가 발생하고 있다.즉, 급여가 확대된 제줄라를 처방받기 위해서는 고가의 비급여 검사를 환자가 부담해야 하는 간극이 발생하는 것이다.대한부인종양학회 역시 이 같은 문제점을 인지하고 해결책을 마련하기 위해 정책을 제안한다는 계획이다.학회 관계자는 "환자로서는 급여 약제를 처방하기 위해서 비급여 검사를 해야한다는 점은 이해하기 어려울 수밖에 없는 부분"이라며 "한국의 검사체계와 외국 사례 등의 검토 및 회의를 통해 보건복지부에 관련 의견을 전달하려고 구상하고 있다"고 밝혔다.HRd 검사에 대한 학회의 의견은 이르면 상반기 중으로 보건복지부와 건강보험심사평가원 등에 전달할 예정이지만 제도권 편입을 위한 실질적 논의로 이어질지는 좀 더 지켜봐야 한다.난소암에서 HRd 발현 빈도가 약 50%에 달하고, 치료 전 대부분의 환자가 검사를 받아야 한다는 점을 고려하면, 재정적 부담이라는 현실적인 문제도 남아 있기 때문이다.학회 관계자는 "국내 난소암 환자의 치료 성과 향상을 위해서는 HRd 검사의 원활한 도입과 활용이 필수적인 만큼 제도적 뒷받침이 필요할 것으로 본다"고 덧붙였다.2025-05-02 06:00:16황병우 -
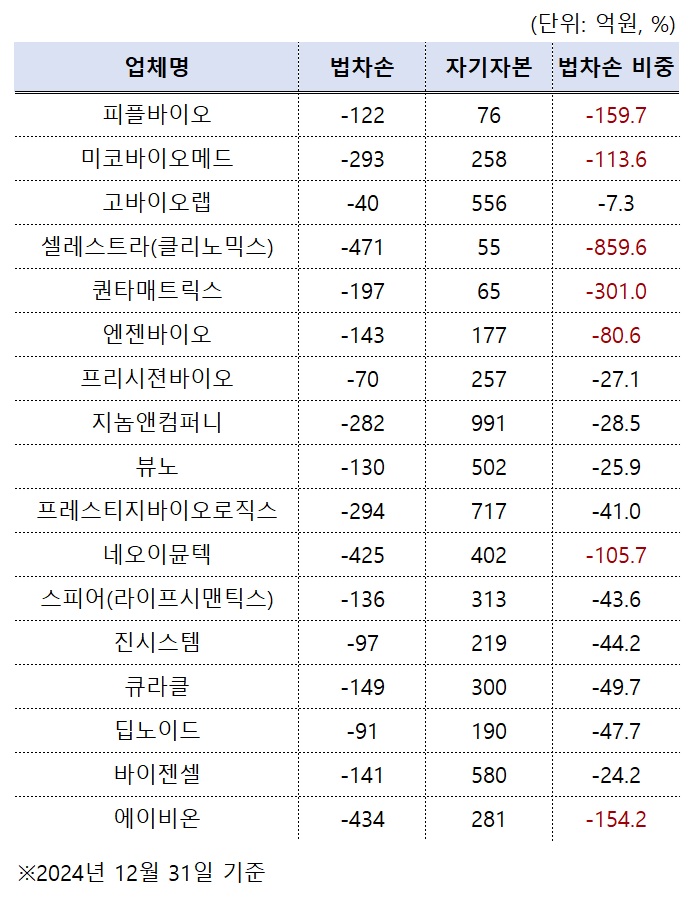 '법차손의 덫'...관리종목 유예 만료 바이오 7곳 경고등[데일리팜=차지현 기자] 특례상장 제도로 코스닥에 입성한 바이오 기업 가운데 관리종목 지정 위기에 놓인 기업이 속속 나오고 있다. 한국거래소 관리종목 지정 유예 기간이 끝나면서다. 일부 기업은 대규모 유상증자를 통해 자본금을 확충하는 등 관리종목 지정 요건에서 벗어나기 위해 안간힘을 쓰는 분위기다.18일 금융감독원에 따르면 2023년부로 법인세비용차감전계속사업손실(법차손) 관련 특례상장 관리종목 유예 기간이 만료된 바이오텍은 총 17곳이다. 2020년 10월부터 2021년 9월까지 특례제도로 코스닥 시장에 입성한 기업들이 여기에 해당한다.피플바이오, 미코바이오메드, 고바이오랩, 셀레스트라(전 클리노믹스), 퀀타매트릭스, 엔젠바이오, 프리시젼바이오, 지놈앤컴퍼니, 뷰노, 프레스티지바이오로직스, 네오이뮨텍, 스피어(전 라이프시맨틱스), 진시스템, 큐라클, 딥노이드, 바이젠셀, 에이비온 등이다.법차손은 사업에서 발생한 지속적인 손실 규모에서 법인세를 차감하기 전 수치를 말한다. 회사가 실제로 본업으로 얼마나 손실을 냈는지를 잘 보여주는 지표다.최근 3년간 2회 이상 법차손이 자본의 50% 초과하면 거래소 관리종목 지정 사유에 포함된다. 다만 기술 특례나 성장성 특례 제도로 상장한 기업은 상장 연도 포함 3년 동안 적용이 유예된다.법차손 유예 기간이 끝난 기업 중 지난해 기준 자기자본 대비 법차손 비율이 50%를 초과한 업체는 7곳이다. 2023년 특례상장 관리종목 유예 기간이 만료된 바이오텍 중 41%에 달하는 업체가 이듬해 법차손 비중 50%를 넘긴 것이다.셀레스트라는 지난해 자기자본 대비 법차손 비율이 860%까지 치솟았다. 작년 셀레스트라의 법차손은 471억원, 자본총계는 55억원이었다. 셀레스트라는 유전체 진단 검사, 진단용 시약 제조와 판매 등을 주사업으로 영위한다. 셀레스트라는 2020년 12월 상장해 2023년부로 법차손 요건 유예 기간이 끝났다.퀀타매트릭스의 경우 지난해 법차손 비중 301%를 기록했다. 지난해 퀀타매트릭스는 법차손 197억원을 냈는데 자본총계는 65억원에 불과했다. 2010년 설립한 퀀타매트릭스는 2020년 말 기술특례 방식으로 코스닥에 상장했다. 퀀타매트릭스는 혈액 기반 알츠하이머병 진단 기술을 보유 중이다.(자료: 금융감독원) 피플바이오와 에이비온은 지난해 자기자본 대비 법차손 비율이 160%와 154%로 관리종목 지정 기준인 50%를 훨씬 초과했다. 작년 기준 법차손 규모를 보면 피플바이오는 122억원, 에이비온은 434억원 수준이었다. 같은 기간 자본총계는 피플바이오 76억원, 에이비온 281억원이었다.미코바이오메드와 네오이뮨텍은 작년 법차손 비중 100%를 넘겼다. 미코바이오메드의 지난해 법차손은 293억원, 자본총계는 258억원으로 자기자본 대비 법차손 비율이 114%였다. 네오이뮨텍의 법차손 비중은 106%로 나타났다. 네오이뮨텍의 지난해 말 자본총계는 402억원이었다. 네오이뮨텍은 작년 한 해 법차손 425억원을 내면서 법차손 비중이 높아졌다.엔젠바이오의 지난해 법차손 비중은 81%였다. 작년 엔젠바이오의 법차손은 143억원, 자본총계는 177억원이다. 엔젠바이오는 국내 최초로 차세대염기서열(NGS) 기반 DNA·RNA 암 정밀진단과 분석 기술을 상용화한 업체로, 2020년 12월 상장했다. 이에 따라 엔젠바이오는 2023년 법차손 요건 유예가 만료됐다.이외 자기자본 대비 법차손 비중 40%를 넘긴 곳도 5곳으로 집계됐다. 스피어, 진시스템, 큐라클, 딥노이드 등이 여기에 속한다. 특히 특히 큐라클은 작년 법차손 비율이 49%로 관리종목 지정 요건을 겨우 맞췄다. 같은 기간 딥노이드도 법차손 비중 48%를 기록했다.최근 3년간 직전 사업연도 중 자기자본 대비 법차손 비율이 50%를 넘는 사업연도가 2번 이상이면 관리종목으로 지정된다. 이후 같은 상황이 이어지면 상장폐지 사유에 해당한다. 작년 법차손 비중 50%를 넘긴 기업이 올해에도 법차손 문제를 해소하지 못하면 관리종목으로 지정되는 수순이다.지난해 법차손 관련 관리종목 요건을 충족한 업체도 마냥 안심할 수는 없는 상황이다. 수익성 개선 없이 유상증자나 전환사채(CB) 발행 등 일회성 자본 확충으로 기준선을 넘긴 경우 향후 다시 법차손 비중이 50%를 초과할 가능성이 크기 때문이다.실제 2023년 법차손 관련 관리종목 요건을 충족한 업체 대부분이 최근 유상증자 또는 CB로 자본을 확충한 이력이 있다. 지놈앤컴퍼니는 작년 7월 45억원 규모 CB를, 뷰노는 지난해 말 237억원 규모 영구 CB를 발행했다.또 라이프시맨틱스는 작년 말 휴웍스어드바이저를 대상으로 150억원 규모 CB를 발행했다. 프레스티지바이오로직스는 모회사인 프레스티지바이오파마를 대상으로 한 제 3자배정 유상증자를 통해 900억원의 자금을 조달했다.법차손 요건을 만족하지 못해 관리종목으로 편입되는 바이오 업체가 증가하면서 업계에서는 관련 요건을 완화해달라는 요구가 이어지고 있다. 오랜 기간 막대한 연구개발(R&D) 자금을 투입하는 신약개발 업종 특성상 적자 구조는 불가피하다. 연구에 집중할수록 관리종목에 오를 가능성이 큰 구조인 만큼, 법차손에서 R&D 비용을 상쇄하는 등 유연화가 필요하다는 게 업체들의 입장이다.올해 들어서만 애니젠, DXVX, 브릿지바이오, 에스씨엠생명과학, 카이노스메드 등 5곳 이상 바이오 업체가 법차손 요건으로 인해 관리종목으로 지정됐다.2025-04-18 12:00:39차지현
'법차손의 덫'...관리종목 유예 만료 바이오 7곳 경고등[데일리팜=차지현 기자] 특례상장 제도로 코스닥에 입성한 바이오 기업 가운데 관리종목 지정 위기에 놓인 기업이 속속 나오고 있다. 한국거래소 관리종목 지정 유예 기간이 끝나면서다. 일부 기업은 대규모 유상증자를 통해 자본금을 확충하는 등 관리종목 지정 요건에서 벗어나기 위해 안간힘을 쓰는 분위기다.18일 금융감독원에 따르면 2023년부로 법인세비용차감전계속사업손실(법차손) 관련 특례상장 관리종목 유예 기간이 만료된 바이오텍은 총 17곳이다. 2020년 10월부터 2021년 9월까지 특례제도로 코스닥 시장에 입성한 기업들이 여기에 해당한다.피플바이오, 미코바이오메드, 고바이오랩, 셀레스트라(전 클리노믹스), 퀀타매트릭스, 엔젠바이오, 프리시젼바이오, 지놈앤컴퍼니, 뷰노, 프레스티지바이오로직스, 네오이뮨텍, 스피어(전 라이프시맨틱스), 진시스템, 큐라클, 딥노이드, 바이젠셀, 에이비온 등이다.법차손은 사업에서 발생한 지속적인 손실 규모에서 법인세를 차감하기 전 수치를 말한다. 회사가 실제로 본업으로 얼마나 손실을 냈는지를 잘 보여주는 지표다.최근 3년간 2회 이상 법차손이 자본의 50% 초과하면 거래소 관리종목 지정 사유에 포함된다. 다만 기술 특례나 성장성 특례 제도로 상장한 기업은 상장 연도 포함 3년 동안 적용이 유예된다.법차손 유예 기간이 끝난 기업 중 지난해 기준 자기자본 대비 법차손 비율이 50%를 초과한 업체는 7곳이다. 2023년 특례상장 관리종목 유예 기간이 만료된 바이오텍 중 41%에 달하는 업체가 이듬해 법차손 비중 50%를 넘긴 것이다.셀레스트라는 지난해 자기자본 대비 법차손 비율이 860%까지 치솟았다. 작년 셀레스트라의 법차손은 471억원, 자본총계는 55억원이었다. 셀레스트라는 유전체 진단 검사, 진단용 시약 제조와 판매 등을 주사업으로 영위한다. 셀레스트라는 2020년 12월 상장해 2023년부로 법차손 요건 유예 기간이 끝났다.퀀타매트릭스의 경우 지난해 법차손 비중 301%를 기록했다. 지난해 퀀타매트릭스는 법차손 197억원을 냈는데 자본총계는 65억원에 불과했다. 2010년 설립한 퀀타매트릭스는 2020년 말 기술특례 방식으로 코스닥에 상장했다. 퀀타매트릭스는 혈액 기반 알츠하이머병 진단 기술을 보유 중이다.(자료: 금융감독원) 피플바이오와 에이비온은 지난해 자기자본 대비 법차손 비율이 160%와 154%로 관리종목 지정 기준인 50%를 훨씬 초과했다. 작년 기준 법차손 규모를 보면 피플바이오는 122억원, 에이비온은 434억원 수준이었다. 같은 기간 자본총계는 피플바이오 76억원, 에이비온 281억원이었다.미코바이오메드와 네오이뮨텍은 작년 법차손 비중 100%를 넘겼다. 미코바이오메드의 지난해 법차손은 293억원, 자본총계는 258억원으로 자기자본 대비 법차손 비율이 114%였다. 네오이뮨텍의 법차손 비중은 106%로 나타났다. 네오이뮨텍의 지난해 말 자본총계는 402억원이었다. 네오이뮨텍은 작년 한 해 법차손 425억원을 내면서 법차손 비중이 높아졌다.엔젠바이오의 지난해 법차손 비중은 81%였다. 작년 엔젠바이오의 법차손은 143억원, 자본총계는 177억원이다. 엔젠바이오는 국내 최초로 차세대염기서열(NGS) 기반 DNA·RNA 암 정밀진단과 분석 기술을 상용화한 업체로, 2020년 12월 상장했다. 이에 따라 엔젠바이오는 2023년 법차손 요건 유예가 만료됐다.이외 자기자본 대비 법차손 비중 40%를 넘긴 곳도 5곳으로 집계됐다. 스피어, 진시스템, 큐라클, 딥노이드 등이 여기에 속한다. 특히 특히 큐라클은 작년 법차손 비율이 49%로 관리종목 지정 요건을 겨우 맞췄다. 같은 기간 딥노이드도 법차손 비중 48%를 기록했다.최근 3년간 직전 사업연도 중 자기자본 대비 법차손 비율이 50%를 넘는 사업연도가 2번 이상이면 관리종목으로 지정된다. 이후 같은 상황이 이어지면 상장폐지 사유에 해당한다. 작년 법차손 비중 50%를 넘긴 기업이 올해에도 법차손 문제를 해소하지 못하면 관리종목으로 지정되는 수순이다.지난해 법차손 관련 관리종목 요건을 충족한 업체도 마냥 안심할 수는 없는 상황이다. 수익성 개선 없이 유상증자나 전환사채(CB) 발행 등 일회성 자본 확충으로 기준선을 넘긴 경우 향후 다시 법차손 비중이 50%를 초과할 가능성이 크기 때문이다.실제 2023년 법차손 관련 관리종목 요건을 충족한 업체 대부분이 최근 유상증자 또는 CB로 자본을 확충한 이력이 있다. 지놈앤컴퍼니는 작년 7월 45억원 규모 CB를, 뷰노는 지난해 말 237억원 규모 영구 CB를 발행했다.또 라이프시맨틱스는 작년 말 휴웍스어드바이저를 대상으로 150억원 규모 CB를 발행했다. 프레스티지바이오로직스는 모회사인 프레스티지바이오파마를 대상으로 한 제 3자배정 유상증자를 통해 900억원의 자금을 조달했다.법차손 요건을 만족하지 못해 관리종목으로 편입되는 바이오 업체가 증가하면서 업계에서는 관련 요건을 완화해달라는 요구가 이어지고 있다. 오랜 기간 막대한 연구개발(R&D) 자금을 투입하는 신약개발 업종 특성상 적자 구조는 불가피하다. 연구에 집중할수록 관리종목에 오를 가능성이 큰 구조인 만큼, 법차손에서 R&D 비용을 상쇄하는 등 유연화가 필요하다는 게 업체들의 입장이다.올해 들어서만 애니젠, DXVX, 브릿지바이오, 에스씨엠생명과학, 카이노스메드 등 5곳 이상 바이오 업체가 법차손 요건으로 인해 관리종목으로 지정됐다.2025-04-18 12:00:39차지현 -
 AI부터 유전자가위까지…제약, 액체생검 플랫폼 확보 분주[데일리팜=손형민 기자] 국내 제약바이오업계가 암을 조기진단할 수 있는 액체생검 기술 확보에 분주하다. 액체생검은 혈액이나 체액, 소변 등으로 암 진단이 가능해 직접 종양을 떼어내는 조직검사 대비 빠르고 간편하며, 환자의 생체 조직이 없는 경우에도 활용될 수 있다. GC지놈, 랩지노믹스 등이 인공지능(AI)과 유전자편집 기술을 통해 이 시장에 도전장을 내밀었다.12일 관련 업계에 따르면 GC지놈은 최근 AI 기반 액체생검 데이터를 활용한 폐암 검출 알고리즘에 관한 연구 결과를 국제학술지 ‘캔써리서치’에 게재했다.GC지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 질병 진단과 예측은 물론 이를 통해 맞춤형 치료까지 지원하겠다는 목표다. 삼성서울병원 교수 출신 기창석 대표가 2018년부터 회사를 이끌고 있다.GC지놈은 혈액에서 세포유리 DNA를 분석해 폐암을 검출하는 알고리즘을 개발했다. '유전자 단편 말단 및 크기(FEMS)’ 기술과 딥러닝 알고리즘을 활용해 폐암 조기 검출의 정확도를 높인 게 특징이다. FEMS 기술은 폐암 조기 발견에서 민감도 91.0%를 기록하며 기존 유전체 분석 기술보다 성과를 나타냈다.연구진은 한국인 2777명의 데이터를 사용해 모델을 구축한 후 한국인 검증 코호트(1247명)와 백인 검증 코호트(100명)에서 성능을 평가했다.연구 결과, 한국인 검증 집단에서 95.5%의 민감도와 83.8%의 특이도를, 백인 검증 집단에서는 94.0%의 민감도와 84.0%의 특이도를 기록했다. 1~2기 초기 폐암 환자에서도 91.1%의 민감도를 보여 조기 암 진단 성과를 나타냈다.GC지놈은 지난 2023년 9월 아이캔서치를 출시했다. 아이캔서치는 GC지놈이 개발한 AI 기반 액체생검 진단 플랫폼이다.아이캔서치는 AI 알고리즘을 활용해 혈관 속을 떠다니는 세포유리 DNA(cfDNA) 중 순환 종양 DNA(ctDNA)를 추출해 차세대 염기서열 분석법(NGS)으로 암 존재 가능성을 조기에 확인할 수 있다. 암세포에서 유래된 cfDNA는 세포에서 혈액으로 방출된 DNA로 자가유래 세포의 특징을 고스란히 지니고 있다.아이캔서치는 총 5000여 명(암 환자 1300여 명, 일반인 3700여 명)의 샘플 분석을 통해 검사 정확도를 입증했다. 아이캔서치가 진단할 수 있는 암종은 폐암, 간암, 대장암, 담도암, 식도암, 난소암 등 총 6가지 암종이다. 허가 연구에서 1기암 진단 민감도는 81.1%를 기록하고 있는 것으로 알려진다.유전자가위로 암 조기진단 시대 열리나진씨커의 '크리스핀셋'진씨커는 액체생검에 크리스퍼(CRISPR) 유전자 가위 기술을 적용한 액체생검 제품 '크리스핀셋 하모니'를 보유하고 있다. 유전자 가위는 유전자를 편집하기 위해 DNA 특정 부위를 인식해 절단하는 분자생물학적 도구다.유전체 교정 도구에는 CRISPR/Cas-9, 징크핑거뉴클라아제, 탈렌 등이 있다. 그중 CRISPR/Cas-9은 3세대 유전자 가위 기술로 분류된다. CRISPR/Cas-9의 작용 원리는 상보적 염기서열을 지닌 RNA와 Cas-9 복합체를 핵 내로 넣어 상보적 DNA에 결합한 후 Cas-9이 DNA를 두 가닥으로 자르는 방식이다.진씨커에 따르면 이 회사의 유전자 가위 기술을 이용하면 정상 유전자에서 유래된 cfDNA만 겨냥해 절단한다. 종양 크기가 1㎤인 극초기 암환자는 ctDNA 비율이 0.022%에 불과하지만 기존 액체생검은 ctDNA가 0.1% 미만일 때는 검진이 불가능하다.진씨커의 유전자 가위 기술은 정상 유전자에서 유래된 cfDNA만 겨냥해 절단하고 이후 증폭과정을 거치면 절단된 유전자는 증폭하지 못한다. 대신 혈액 속 유전자 가운데 ctDNA 비율이 최대 100배까지 증가하는 것으로 나타났다.진씨커는 고대안암병원과 손잡고 건강검진 시장에 진출했다. 고대안암병원 건강검진센터를 통해 대표적인 암종 11가지(간암, 갑상선암, 난소암, 담도암, 대장암, 방광암, 유방암, 위암, 자궁경부암, 췌장암, 폐암)의 위험도를 예측해 안내하고, 각 진료과 전문의를 통해 추가 정밀검사를 안내하는 형태다.액체생검 상용화는 성공…한계도 여전암환자의 조직 추출은 항암제 내성이 생긴 이후에는 점차 어려워진다. 첫 조직검사 시 대개 90% 이상의 확률로 조직 추출이 가능하지만 항암제 내성 환자에서 재조직검사를 시행할 때 점차 그 확률이 떨어진다. 액체생검의 가장 큰 강점은 기존 조직검사와 달리 비침습성 검사 요법이라는 것이다.이에 액체생검이 조직검사를 대체할 수 있는 후보로 거론되고 있지만 아직까지는 일부 암에만 적용 가능하고 100%에 근접하는 정확도를 보여주지는 못해 추가 검사가 필요한 상황이다. 다만 암의 조기 진단과 예측 측면에서는 유용한 도구로 활용될 수 있다. 이에 주요 액체생검 진단 바이오기업들은 조기 암 진단 시장을 노리고 있다.싸이토젠과 아이엠비디엑스는 액체생검 분야에서 활발한 활동을 전개하고 있다.싸이토젠은 혈액 내 순환종양세포(CTC)를 기반으로 한 액체생검 플랫폼을 개발했다. 이 회사는 2023년 11월 미국 국립보건원(NIH) 산하 로젠버그 연구소에 해당 플랫폼을 추가로 공급했다. 이는 작년 미국국립암연구소(NCI)에 이어 두 번째 공급이다.싸이토젠은 일본 시장 진출에도 박차를 가하고 있다. 2023년 내에 일본 현지법인을 설립하고 도쿄에 액체생검 분석센터를 구축할 계획이다. 이는 미국에 이은 두 번째 해외 거점으로, 일본 내 제약사 및 연구기관과의 협력을 강화해 현지 고객들의 요구에 신속하게 대응할 수 있을 것으로 싸이토젠은 기대하고 있다.아이엠비디엑스는 지난해 11월 다중 암 조기진단 플랫폼인 '캔서파인드'를 출시하며 액체생검 시장에 본격적으로 진입했다. 캔서파인드는 한 번의 혈액 검사로 대장암, 위암, 간암 등 8가지 암종을 동시에 검사할 수 있는 제품이다. 현재 국내 10개 상급종합병원에서 상용화됐다.아이엠비디엑스는 향후 캔서파인드 적용 암종을 20종으로 확대하고 검사 비용을 기존 100만원에서 30만원으로 낮추겠다는 계획이다.2025-04-12 06:20:49손형민
AI부터 유전자가위까지…제약, 액체생검 플랫폼 확보 분주[데일리팜=손형민 기자] 국내 제약바이오업계가 암을 조기진단할 수 있는 액체생검 기술 확보에 분주하다. 액체생검은 혈액이나 체액, 소변 등으로 암 진단이 가능해 직접 종양을 떼어내는 조직검사 대비 빠르고 간편하며, 환자의 생체 조직이 없는 경우에도 활용될 수 있다. GC지놈, 랩지노믹스 등이 인공지능(AI)과 유전자편집 기술을 통해 이 시장에 도전장을 내밀었다.12일 관련 업계에 따르면 GC지놈은 최근 AI 기반 액체생검 데이터를 활용한 폐암 검출 알고리즘에 관한 연구 결과를 국제학술지 ‘캔써리서치’에 게재했다.GC지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 질병 진단과 예측은 물론 이를 통해 맞춤형 치료까지 지원하겠다는 목표다. 삼성서울병원 교수 출신 기창석 대표가 2018년부터 회사를 이끌고 있다.GC지놈은 혈액에서 세포유리 DNA를 분석해 폐암을 검출하는 알고리즘을 개발했다. '유전자 단편 말단 및 크기(FEMS)’ 기술과 딥러닝 알고리즘을 활용해 폐암 조기 검출의 정확도를 높인 게 특징이다. FEMS 기술은 폐암 조기 발견에서 민감도 91.0%를 기록하며 기존 유전체 분석 기술보다 성과를 나타냈다.연구진은 한국인 2777명의 데이터를 사용해 모델을 구축한 후 한국인 검증 코호트(1247명)와 백인 검증 코호트(100명)에서 성능을 평가했다.연구 결과, 한국인 검증 집단에서 95.5%의 민감도와 83.8%의 특이도를, 백인 검증 집단에서는 94.0%의 민감도와 84.0%의 특이도를 기록했다. 1~2기 초기 폐암 환자에서도 91.1%의 민감도를 보여 조기 암 진단 성과를 나타냈다.GC지놈은 지난 2023년 9월 아이캔서치를 출시했다. 아이캔서치는 GC지놈이 개발한 AI 기반 액체생검 진단 플랫폼이다.아이캔서치는 AI 알고리즘을 활용해 혈관 속을 떠다니는 세포유리 DNA(cfDNA) 중 순환 종양 DNA(ctDNA)를 추출해 차세대 염기서열 분석법(NGS)으로 암 존재 가능성을 조기에 확인할 수 있다. 암세포에서 유래된 cfDNA는 세포에서 혈액으로 방출된 DNA로 자가유래 세포의 특징을 고스란히 지니고 있다.아이캔서치는 총 5000여 명(암 환자 1300여 명, 일반인 3700여 명)의 샘플 분석을 통해 검사 정확도를 입증했다. 아이캔서치가 진단할 수 있는 암종은 폐암, 간암, 대장암, 담도암, 식도암, 난소암 등 총 6가지 암종이다. 허가 연구에서 1기암 진단 민감도는 81.1%를 기록하고 있는 것으로 알려진다.유전자가위로 암 조기진단 시대 열리나진씨커의 '크리스핀셋'진씨커는 액체생검에 크리스퍼(CRISPR) 유전자 가위 기술을 적용한 액체생검 제품 '크리스핀셋 하모니'를 보유하고 있다. 유전자 가위는 유전자를 편집하기 위해 DNA 특정 부위를 인식해 절단하는 분자생물학적 도구다.유전체 교정 도구에는 CRISPR/Cas-9, 징크핑거뉴클라아제, 탈렌 등이 있다. 그중 CRISPR/Cas-9은 3세대 유전자 가위 기술로 분류된다. CRISPR/Cas-9의 작용 원리는 상보적 염기서열을 지닌 RNA와 Cas-9 복합체를 핵 내로 넣어 상보적 DNA에 결합한 후 Cas-9이 DNA를 두 가닥으로 자르는 방식이다.진씨커에 따르면 이 회사의 유전자 가위 기술을 이용하면 정상 유전자에서 유래된 cfDNA만 겨냥해 절단한다. 종양 크기가 1㎤인 극초기 암환자는 ctDNA 비율이 0.022%에 불과하지만 기존 액체생검은 ctDNA가 0.1% 미만일 때는 검진이 불가능하다.진씨커의 유전자 가위 기술은 정상 유전자에서 유래된 cfDNA만 겨냥해 절단하고 이후 증폭과정을 거치면 절단된 유전자는 증폭하지 못한다. 대신 혈액 속 유전자 가운데 ctDNA 비율이 최대 100배까지 증가하는 것으로 나타났다.진씨커는 고대안암병원과 손잡고 건강검진 시장에 진출했다. 고대안암병원 건강검진센터를 통해 대표적인 암종 11가지(간암, 갑상선암, 난소암, 담도암, 대장암, 방광암, 유방암, 위암, 자궁경부암, 췌장암, 폐암)의 위험도를 예측해 안내하고, 각 진료과 전문의를 통해 추가 정밀검사를 안내하는 형태다.액체생검 상용화는 성공…한계도 여전암환자의 조직 추출은 항암제 내성이 생긴 이후에는 점차 어려워진다. 첫 조직검사 시 대개 90% 이상의 확률로 조직 추출이 가능하지만 항암제 내성 환자에서 재조직검사를 시행할 때 점차 그 확률이 떨어진다. 액체생검의 가장 큰 강점은 기존 조직검사와 달리 비침습성 검사 요법이라는 것이다.이에 액체생검이 조직검사를 대체할 수 있는 후보로 거론되고 있지만 아직까지는 일부 암에만 적용 가능하고 100%에 근접하는 정확도를 보여주지는 못해 추가 검사가 필요한 상황이다. 다만 암의 조기 진단과 예측 측면에서는 유용한 도구로 활용될 수 있다. 이에 주요 액체생검 진단 바이오기업들은 조기 암 진단 시장을 노리고 있다.싸이토젠과 아이엠비디엑스는 액체생검 분야에서 활발한 활동을 전개하고 있다.싸이토젠은 혈액 내 순환종양세포(CTC)를 기반으로 한 액체생검 플랫폼을 개발했다. 이 회사는 2023년 11월 미국 국립보건원(NIH) 산하 로젠버그 연구소에 해당 플랫폼을 추가로 공급했다. 이는 작년 미국국립암연구소(NCI)에 이어 두 번째 공급이다.싸이토젠은 일본 시장 진출에도 박차를 가하고 있다. 2023년 내에 일본 현지법인을 설립하고 도쿄에 액체생검 분석센터를 구축할 계획이다. 이는 미국에 이은 두 번째 해외 거점으로, 일본 내 제약사 및 연구기관과의 협력을 강화해 현지 고객들의 요구에 신속하게 대응할 수 있을 것으로 싸이토젠은 기대하고 있다.아이엠비디엑스는 지난해 11월 다중 암 조기진단 플랫폼인 '캔서파인드'를 출시하며 액체생검 시장에 본격적으로 진입했다. 캔서파인드는 한 번의 혈액 검사로 대장암, 위암, 간암 등 8가지 암종을 동시에 검사할 수 있는 제품이다. 현재 국내 10개 상급종합병원에서 상용화됐다.아이엠비디엑스는 향후 캔서파인드 적용 암종을 20종으로 확대하고 검사 비용을 기존 100만원에서 30만원으로 낮추겠다는 계획이다.2025-04-12 06:20:49손형민 -
 녹십자 계열 GC지놈 IPO 속도…"2028년 순익 220억 전망"[데일리팜=차지현 기자] 기업공개(IPO)를 추진 중인 녹십자그룹 유전체 분석 계열사 지씨지놈이 기업가치 산정을 위한 비교 기업에 해외 상장사 3곳을 포함했다. 오는 2028년까지 약 221억원의 순이익을 달성하겠다는 목표도 내놨다. 이를 기반으로 추산한 예상 시가총액은 2130억~2485억원이다.9일 금융감독원에 따르면 지씨지놈(대표이사 기창석)은 8일 증권신고서를 제출하고 코스닥 상장을 위한 공모 절차에 돌입했다. 한국거래소 상장 예비심사를 통과한 지 2주도 채 지나지 않아 신고서를 제출하면서 발 빠르게 움직이는 모습이다.앞서 지씨지놈은 지난달 26일 코스닥 기술특례상장을 위한 예심 승인을 획득한 바 있다. 기술특례상장의 첫 관문인 기술성평가는 지난해 11월 거래소 지정 전문 평가기관으로부터 각각 A등급을 획득하면서 무난하게 통과했다.지씨지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 질병 진단과 예측은 물론 이를 통해 맞춤형 치료까지 지원하겠다는 포부다. 삼성서울병원 교수 출신 기창석 대표가 2018년부터 회사를 이끌고 있다.지씨지놈의 사업은 크게 ▲산과 검사 ▲암 정밀진단 ▲검진검사 ▲유전희귀 정밀진단 등 4가지다. 현재 국내 상급종합병원 45개 기관을 포함해 병·의원 900여곳에 300종 이상 산과, 건강검진, 암 정밀진단, 유전 희귀질환 분야 맞춤형 분자진단 서비스를 제공 중이다. 현재 미국, 유럽, 중동, 아시아태평양 등 19개국에도 진출한 상태다. 이들 제품을 앞세워 지씨지놈은 지난해 매출 259억원, 순손실 13억원을 올렸다.(자료: 금융감독원) 지씨지놈은 공모 예정 주식 400만주를 포함해 총 2366만6666주를 상장할 계획이다. 공모 구조는 100% 신주모집이다. 공모가 희망 범위는 9000원에서 1만500원이다. 이를 기반으로 한 공모 금액은 360억~420억원, 예상 시가총액은 2130억~2485억원이다.지씨지놈은 희망 공모가액을 계산하기 위해 상대가치법 중 주가수익비율(PER) 계산 방법을 활용했다. PER은 주가를 한 주당 얻을 수 있는 이익(주당순이익)으로 나눈 값으로 기업 영업활동의 수익성과 위험성, 시장 평가 등을 종합 반영한 지표다. 유사한 사업을 영위하는 기업들의 순이익, 발행주식총수, 기준주가 등을 고려해 기업가치를 산출했다.먼저 지씨지놈은 2028년 220억6700만원의 순이익을 낼 수 있을 것으로 전망했다. 올해 순이익 47억원을 기록해 흑자전환하고 이후 3년간 순이익이 5배가량 성장할 것으로 내다봤다. 여기에 할인율 15%를 적용해 추정 순이익을 현재 가치로 환산한 뒤 비교 기업 4곳의 PER 26.04배를 곱해 희망 공모 범위를 결정했다.눈에 띄는 점은 지씨지놈이 비교 기업으로 선정한 4곳 중 3곳이 모두 해외 기업이라는 점이다. 지씨지놈이 비교 기업으로 선정한 곳은 바디텍메드, 레비티(Revvity), 홀로직(Hologic), 디아소린(DiaSorin) 등이다. 코스닥에 상장한 바디텍메드를 제외하고 나머지 3개사 모두 해외 상장사다.2023년 퍼킨엘머에서 분할하며 출범한 레비티는 연간 3조원 이상 매출을 내는 생명과학·진단 업체다. 뉴욕증권거래소에 'RVTY'라는 종목코드(티커)로 상장돼 있다. 8일 종가 기준 시가총액은 110억달러(약 16조원)다.홀로직은 유방촬영기기, 자궁경부암 진단기기 등 여성 건강과 조기 진단에 특화된 의료기기 제품을 보유 중이다. 1985년 설립해 1990년 나스닥에 상장했다. 'HOLX'라는 티커로 거래 중으로, 8일 종가 기준 시총은 131억달러(약 19조원)이다. 홀로직의 2023년 매출은 5조1867억원, 영업이익은 1조1816억원이다.디아소린은 이탈리아 소재 면역화학과 분자진단 전문 체외진단 업체다. 골대사, 심혈관 질환, 자가면역 질환 등 다양한 분야 진단 솔루션을 제공한다. 2023년 디아소린 매출과 영업이익은 각각 1조6221억원, 3331억원이다. 2007년 이탈리아 증권거래소에 상장했다. 8일 종가 기준 디아소린 시총은 51억3200만유로(약 8조원)이다.지씨지놈은 IPO로 확보한 공모 자금을 연구개발(R&D)과 시설 투자에 활용할 예정이다. 공모가 하단 기준 공모액에서 상장주선인의 인수 금액과 발행제비용을 제외한 순수입금 353억원을 R&D와 검사설비 증설, 검사실 확장, 서버구축 등에 사용한다. 세부적으로 R&D 측면에서는 다중암 조기 선별검사 제품의 암종 확대, NGS 플랫폼 추가 등에 투입하겠다는 계획을 제시했다.지씨지놈은 내달 12일부터 16일까지 5영업일 동안 수요예측을 진행한다. 이후 같은 달 22일부터 23일 이틀간 기관투자자와 일반투자자를 대상으로 청약을 실시, 상반기 내 코스닥에 입성하는 걸 목표로 한다. 상장 주관사는 삼성증권이다.지씨지놈이 성공적으로 코스닥에 입성하면 GC그룹 입장에선 상장 계열사가 총 7개로 확대된다. 그룹의 상장 계열사는 녹십자홀딩스, 녹십자, 녹십자웰빙, 녹십자엠에스, 지씨셀, 유비케어 등이 있다.2025-04-09 12:00:47차지현
녹십자 계열 GC지놈 IPO 속도…"2028년 순익 220억 전망"[데일리팜=차지현 기자] 기업공개(IPO)를 추진 중인 녹십자그룹 유전체 분석 계열사 지씨지놈이 기업가치 산정을 위한 비교 기업에 해외 상장사 3곳을 포함했다. 오는 2028년까지 약 221억원의 순이익을 달성하겠다는 목표도 내놨다. 이를 기반으로 추산한 예상 시가총액은 2130억~2485억원이다.9일 금융감독원에 따르면 지씨지놈(대표이사 기창석)은 8일 증권신고서를 제출하고 코스닥 상장을 위한 공모 절차에 돌입했다. 한국거래소 상장 예비심사를 통과한 지 2주도 채 지나지 않아 신고서를 제출하면서 발 빠르게 움직이는 모습이다.앞서 지씨지놈은 지난달 26일 코스닥 기술특례상장을 위한 예심 승인을 획득한 바 있다. 기술특례상장의 첫 관문인 기술성평가는 지난해 11월 거래소 지정 전문 평가기관으로부터 각각 A등급을 획득하면서 무난하게 통과했다.지씨지놈은 2013년 출범한 임상유전체 분석 전문 업체다. 녹십자가 유전자 분석과 질병유전자 발굴 사업을 위해 약 20억원을 출자해 설립했다. 환자의 유전자 정보를 분석해 질병 정보를 제공하는 사업을 영위한다. 질병 진단과 예측은 물론 이를 통해 맞춤형 치료까지 지원하겠다는 포부다. 삼성서울병원 교수 출신 기창석 대표가 2018년부터 회사를 이끌고 있다.지씨지놈의 사업은 크게 ▲산과 검사 ▲암 정밀진단 ▲검진검사 ▲유전희귀 정밀진단 등 4가지다. 현재 국내 상급종합병원 45개 기관을 포함해 병·의원 900여곳에 300종 이상 산과, 건강검진, 암 정밀진단, 유전 희귀질환 분야 맞춤형 분자진단 서비스를 제공 중이다. 현재 미국, 유럽, 중동, 아시아태평양 등 19개국에도 진출한 상태다. 이들 제품을 앞세워 지씨지놈은 지난해 매출 259억원, 순손실 13억원을 올렸다.(자료: 금융감독원) 지씨지놈은 공모 예정 주식 400만주를 포함해 총 2366만6666주를 상장할 계획이다. 공모 구조는 100% 신주모집이다. 공모가 희망 범위는 9000원에서 1만500원이다. 이를 기반으로 한 공모 금액은 360억~420억원, 예상 시가총액은 2130억~2485억원이다.지씨지놈은 희망 공모가액을 계산하기 위해 상대가치법 중 주가수익비율(PER) 계산 방법을 활용했다. PER은 주가를 한 주당 얻을 수 있는 이익(주당순이익)으로 나눈 값으로 기업 영업활동의 수익성과 위험성, 시장 평가 등을 종합 반영한 지표다. 유사한 사업을 영위하는 기업들의 순이익, 발행주식총수, 기준주가 등을 고려해 기업가치를 산출했다.먼저 지씨지놈은 2028년 220억6700만원의 순이익을 낼 수 있을 것으로 전망했다. 올해 순이익 47억원을 기록해 흑자전환하고 이후 3년간 순이익이 5배가량 성장할 것으로 내다봤다. 여기에 할인율 15%를 적용해 추정 순이익을 현재 가치로 환산한 뒤 비교 기업 4곳의 PER 26.04배를 곱해 희망 공모 범위를 결정했다.눈에 띄는 점은 지씨지놈이 비교 기업으로 선정한 4곳 중 3곳이 모두 해외 기업이라는 점이다. 지씨지놈이 비교 기업으로 선정한 곳은 바디텍메드, 레비티(Revvity), 홀로직(Hologic), 디아소린(DiaSorin) 등이다. 코스닥에 상장한 바디텍메드를 제외하고 나머지 3개사 모두 해외 상장사다.2023년 퍼킨엘머에서 분할하며 출범한 레비티는 연간 3조원 이상 매출을 내는 생명과학·진단 업체다. 뉴욕증권거래소에 'RVTY'라는 종목코드(티커)로 상장돼 있다. 8일 종가 기준 시가총액은 110억달러(약 16조원)다.홀로직은 유방촬영기기, 자궁경부암 진단기기 등 여성 건강과 조기 진단에 특화된 의료기기 제품을 보유 중이다. 1985년 설립해 1990년 나스닥에 상장했다. 'HOLX'라는 티커로 거래 중으로, 8일 종가 기준 시총은 131억달러(약 19조원)이다. 홀로직의 2023년 매출은 5조1867억원, 영업이익은 1조1816억원이다.디아소린은 이탈리아 소재 면역화학과 분자진단 전문 체외진단 업체다. 골대사, 심혈관 질환, 자가면역 질환 등 다양한 분야 진단 솔루션을 제공한다. 2023년 디아소린 매출과 영업이익은 각각 1조6221억원, 3331억원이다. 2007년 이탈리아 증권거래소에 상장했다. 8일 종가 기준 디아소린 시총은 51억3200만유로(약 8조원)이다.지씨지놈은 IPO로 확보한 공모 자금을 연구개발(R&D)과 시설 투자에 활용할 예정이다. 공모가 하단 기준 공모액에서 상장주선인의 인수 금액과 발행제비용을 제외한 순수입금 353억원을 R&D와 검사설비 증설, 검사실 확장, 서버구축 등에 사용한다. 세부적으로 R&D 측면에서는 다중암 조기 선별검사 제품의 암종 확대, NGS 플랫폼 추가 등에 투입하겠다는 계획을 제시했다.지씨지놈은 내달 12일부터 16일까지 5영업일 동안 수요예측을 진행한다. 이후 같은 달 22일부터 23일 이틀간 기관투자자와 일반투자자를 대상으로 청약을 실시, 상반기 내 코스닥에 입성하는 걸 목표로 한다. 상장 주관사는 삼성증권이다.지씨지놈이 성공적으로 코스닥에 입성하면 GC그룹 입장에선 상장 계열사가 총 7개로 확대된다. 그룹의 상장 계열사는 녹십자홀딩스, 녹십자, 녹십자웰빙, 녹십자엠에스, 지씨셀, 유비케어 등이 있다.2025-04-09 12:00:47차지현 -
 혁신형 제약 인증 취소, 리베이트 처분 규정 완화최상목 부총리 겸 기획재정부 장관 [데일리팜=강신국 기자] 리베이트 처분을 받은 제약사의 '혁신형 제약기업 인증' 취소 기준이 완화될 것으로 보인다.불법 리베이트 관련 인증 요건이 너무 엄격하다는 것인데, 리베이트 척결을 내건 기존 정부 방침과는 동떨어지는 것 아니냐는 비판도 나올 것으로 전망된다.정부는 4일 경제관계장관회의에서 '기업 역동성 제고 및 신산업 촉진을 위한 경제규제 혁신 방안'을 확정했다. 이번 대책은 우리 기업의 역동성 제고를 위해 경제단체, 기업 건의 등을 적극·신속히 반영해 기획재정부와 국무조정실을 중심으로 범 부처가 마련했다.◆혁신형 제약기업 인증 취소기준 개선 = 먼저 혁신형 제약기업 인증제의 불법 리베이트 관련 인증 요건이 엄격해 제약사의 신약개발 의지 저해할 우려가 있다는 게 정부 판단이다.즉 ▲3년 간 불법 리베이트로 약사법을 위반해 2회 이상 과징금 처분을 받거나 ▲리베이트 총 합계액이 500만원 이상인 경우 인증 취소 가능하다는 규정을 개정하겠다는 것이다.정부는 산업계·학계 등 전문가 의견 수렴을 거쳐 혁신형 제약기업 인증취소 기준 개선방안(복지부 고시)을 내년에 마련하기로 했다.한편 혁신형 제약기업 인증을 받으면 ▲신약개발 관련 정부 R&D 과제 참여시 가점 부여 ▲연구인력개발 비용 법인세액 공제 ▲연구시설 건축시 입지규제 완화 ▲정책자금 융자 특례 등의 혜택이 있다.◆의약품 품목허가에 첨단재생임상연구결과 활용 = 첨단재생임상연구는 약사법상 임상시험과 다른 기준이 적용돼 첨단바이오의약품 개발시 허가근거로 활용이 어려웠다.이를 개선해 첨단재생임상연구의 결과를 첨단바이오의약품의 품목허가 허가심사 자료로 활용할 수 있도록 이달 중 가이드라인을 마련한다.가칭 첨단재생의료 임상연구 품목허가 연계 가이드라인을 제정해 일정 수준 이상의 연구 결과에 대해서는 품목허가 허가심사 자료로 활용 가능하도록 하겠다는 것이다.◆비타민B군 건강기능식품 동시분석방법 도입 = 현재 비타민B군(B1, B2, B6, 나이아신, 엽산)을 동시에 분석하는 시험법이 '건강기능식품의 기준 및 규격'에 없어 제품개발 과정이 지연됐다.이에 정부는 내년 1월 연구용역을 통해 건강기능식품에 대해서도 다양한 제형에서 성질을 분석할 수 있는 시험법을 개발·도입하기로 했다.◆소아·청소년과 대상 건강관리 시스템 개발 및 시범서비스 추진 = 긴 진료 대기 등 국민 불편 해소를 위해 AI 등 디지털 기술을 활용한 국민 체감 건강관리 서비스가 도입된다.특히, 저출산으로 인해 소아 의료수요와 의료 자원 감소세가 더욱 심화됨에 따라 소아 의료 이용 접근성 저하되고 있는 만큼 소아청소년과 건강관리 시스템을 개발하겠다는 것이다.즉 진단치료 방향제시, 진료기록 작성지원 등 의료진 업무지원과 소아질환 관리에 필요한 건강상담, 소아희귀질환에 대한 보호자 정보제공 등을 AI기반으로 하자는 게 주요 골자다. 정부는 해당 사업에 4년간 총 320억원을 투입할 예정이다.아울러 정부는 ▲디지털 의료제품 규제 지원센터 신설·운영 ▲미성년자 대상 소비자 직접 의뢰 유전자 검사(DTC) 규제 개선 ▲동물대체시험법 활성화 법안 제정 ▲NGS(차세대 염기서열 분석) 패널데이터 기반 암 정밀의료 기술개발 지원 ▲혁신의료기술 실시 신고 구비서류 간소화 등도 혁신 방안으로 제시했다.2024-12-05 11:57:06강신국
혁신형 제약 인증 취소, 리베이트 처분 규정 완화최상목 부총리 겸 기획재정부 장관 [데일리팜=강신국 기자] 리베이트 처분을 받은 제약사의 '혁신형 제약기업 인증' 취소 기준이 완화될 것으로 보인다.불법 리베이트 관련 인증 요건이 너무 엄격하다는 것인데, 리베이트 척결을 내건 기존 정부 방침과는 동떨어지는 것 아니냐는 비판도 나올 것으로 전망된다.정부는 4일 경제관계장관회의에서 '기업 역동성 제고 및 신산업 촉진을 위한 경제규제 혁신 방안'을 확정했다. 이번 대책은 우리 기업의 역동성 제고를 위해 경제단체, 기업 건의 등을 적극·신속히 반영해 기획재정부와 국무조정실을 중심으로 범 부처가 마련했다.◆혁신형 제약기업 인증 취소기준 개선 = 먼저 혁신형 제약기업 인증제의 불법 리베이트 관련 인증 요건이 엄격해 제약사의 신약개발 의지 저해할 우려가 있다는 게 정부 판단이다.즉 ▲3년 간 불법 리베이트로 약사법을 위반해 2회 이상 과징금 처분을 받거나 ▲리베이트 총 합계액이 500만원 이상인 경우 인증 취소 가능하다는 규정을 개정하겠다는 것이다.정부는 산업계·학계 등 전문가 의견 수렴을 거쳐 혁신형 제약기업 인증취소 기준 개선방안(복지부 고시)을 내년에 마련하기로 했다.한편 혁신형 제약기업 인증을 받으면 ▲신약개발 관련 정부 R&D 과제 참여시 가점 부여 ▲연구인력개발 비용 법인세액 공제 ▲연구시설 건축시 입지규제 완화 ▲정책자금 융자 특례 등의 혜택이 있다.◆의약품 품목허가에 첨단재생임상연구결과 활용 = 첨단재생임상연구는 약사법상 임상시험과 다른 기준이 적용돼 첨단바이오의약품 개발시 허가근거로 활용이 어려웠다.이를 개선해 첨단재생임상연구의 결과를 첨단바이오의약품의 품목허가 허가심사 자료로 활용할 수 있도록 이달 중 가이드라인을 마련한다.가칭 첨단재생의료 임상연구 품목허가 연계 가이드라인을 제정해 일정 수준 이상의 연구 결과에 대해서는 품목허가 허가심사 자료로 활용 가능하도록 하겠다는 것이다.◆비타민B군 건강기능식품 동시분석방법 도입 = 현재 비타민B군(B1, B2, B6, 나이아신, 엽산)을 동시에 분석하는 시험법이 '건강기능식품의 기준 및 규격'에 없어 제품개발 과정이 지연됐다.이에 정부는 내년 1월 연구용역을 통해 건강기능식품에 대해서도 다양한 제형에서 성질을 분석할 수 있는 시험법을 개발·도입하기로 했다.◆소아·청소년과 대상 건강관리 시스템 개발 및 시범서비스 추진 = 긴 진료 대기 등 국민 불편 해소를 위해 AI 등 디지털 기술을 활용한 국민 체감 건강관리 서비스가 도입된다.특히, 저출산으로 인해 소아 의료수요와 의료 자원 감소세가 더욱 심화됨에 따라 소아 의료 이용 접근성 저하되고 있는 만큼 소아청소년과 건강관리 시스템을 개발하겠다는 것이다.즉 진단치료 방향제시, 진료기록 작성지원 등 의료진 업무지원과 소아질환 관리에 필요한 건강상담, 소아희귀질환에 대한 보호자 정보제공 등을 AI기반으로 하자는 게 주요 골자다. 정부는 해당 사업에 4년간 총 320억원을 투입할 예정이다.아울러 정부는 ▲디지털 의료제품 규제 지원센터 신설·운영 ▲미성년자 대상 소비자 직접 의뢰 유전자 검사(DTC) 규제 개선 ▲동물대체시험법 활성화 법안 제정 ▲NGS(차세대 염기서열 분석) 패널데이터 기반 암 정밀의료 기술개발 지원 ▲혁신의료기술 실시 신고 구비서류 간소화 등도 혁신 방안으로 제시했다.2024-12-05 11:57:06강신국 -
 R&D 혁신 이끄는 '오가노이드', 캐시카우 원동력 부상[데일리팜=노병철 기자] 국내외적으로 대체동물시험을 촉진하기 위한 법안들이 속속 등장하면서 오가노이드 기반 R&D산업이 주목받고 있다.오가노이드(organoid)는 인간의 줄기세포나 전구세포를 사용해 특정 장기의 구조와 기능을 3차원적으로 모사한 미니어처 형태의 인공 장기다.오가노이드는 실제 장기와 유사한 시험 환경을 연구원에게 제공하며, 세포 간 상호작용과 조직 특유의 구조를 재현할 수도 있다.이는 2차원 세포 배양 방식에 비해 훨씬 더 정교한 연구 모델로서 활용되고 있으며, 질병 연구나 신약 개발, 독성 평가 등에서 새로운 시험 방법으로 평가받고 있는 기술이다.대표적으로 글로벌 제약사인 로슈는 간암과 같은 특정 질병 연구에서 오가노이드를 활용해 약물의 효과와 독성을 평가하고 있으며, 머크(Merck)는 종양 오가노이드 모델을 활용해 새로운 항암제를 테스트하고 있는 것으로 알려져 있다.이외에도 아스트라제네카와 글락소스미스클라인(GSK)은 각각 폐 오가노이드 모델과 뇌 오가노이드 모델을 활용해 호흡기 질환 치료제와 신경질환 치료제 개발을 이어가고 있다.오가노이드 기술관련 국내 대표주자로는 JW중외제약, 차바이오텍, 그래디언트바이오컨버전스, 오가노이드사이언스 등 10개 안팎의 기업을 들 수 있다.먼저 JW중외제약은 신약 개발 과정에서 오가노이드를 선도적으로 도입해 활용하고 있는 제약사다.대표적으로 최근 미국 텍사스주에서 열린 미국 피부연구학회(Society of Investigative Dermatology)에서 JW중외제약은 탈모치료제 혁신 신약후보물질 ‘JW0061’에 대한 전임상 연구 결과를 발표해 참가자들의 많은 관심을 받았다.JW중외제약이 공개한 연구결과에 따르면 인간의 두피에서 JW0061이 모낭을 생성하는지 예측하기 위해 피부 오가노이드 모델을 활용해 전임상 시험을 진행, 표준치료제에 비해 약물 처리 5일째, 10일째 기준 모낭 수가 각각 7.2배, 4.0배 많다는 모낭생성 효능 시험 데이터를 확인했다.2023년에는 JW중외제약 연구법인 C&C신약연구소가 정밀의료 혁신기업 ‘엠비디’와 3D 암 오가노이드 진단 플랫폼 기반의 혁신 항암제 개발을 위한 연구 협력을 체결, 오가노이드 플랫폼을 활용해 다양한 종양 적응증을 탐색해 나가는 과제를 수행하고 있다. 차바이오텍도 오픈이노베이션과 CDMO를 통해 오가노이드 재생치료제 사업에 공을 들이고 있다.차바이오텍은 지난 3월, 재생의료용 세포치료제 개발기업 셀인셀즈와 연골질환 오가노이드치료제 위탁생산(CDMO) 계약을 했다.이번 계약으로 차바이오텍은 자회사인 차바이오랩 의약품 제조시설에서 고품질 오가노이드 재생치료제 개발용 줄기세포의 세포은행을 구축해 셀인셀즈에 제공할 예정이다.이에 따라 셀인셀즈는 줄기세포 유래 오가노이드 재생치료제 개발에 속도를 올릴 수 있게 됐고, 차바이오텍은 세포은행 구축 후 임상용 의약품 생산도 기대할 수 있게 됐다.셀인셀즈는 피부재생, 연골재생, 혈관생성 등 다양한 질환의 오가노이드 재생치료제 파이프라인을 보유, 95% 이상 확률로 균일한 오가노이드를 대량 생산할 수 있는 기술을 갖고 있다.기술 확장과 고도화를 위해 오가노이드와 인공지능(AI) 기술을 융합해 생산공정 자동화, 기준 및 시험방법 마련, 대량 생산 최적화 솔루션 개발 등을 추진 중이다.오가노이드 기반 차세대 재생치료제 개발 전문기업 오가노이드사이언스는 전략적 파트너십을 활용해 오가노이드 기반 사업을 확장하고 있다.오가노이드사이언스는 이달 중순 신약개발기업 그라스메디와 MOU를 맺고, 동물실험없는 반려동물 헬스케어시대를 앞당길 계획이다.오가노이드사이언스는 이번 전략적 파트너십을 계기로 공동 연구 프로젝트를 추진, 기술 교류 및 인재 양성 등 구체적인 협력 방안을 지속 논의할 방침이다.또, 차세대 의약외품 및 반려동물 관련 상품 개발을 가속화하고 글로벌 시장 경쟁력을 강화하며 지속 가능한 성장과 발전을 도모할 예정이다.그래디언트바이오컨버전스는 이달 열린 유럽종양학회(ESMO)에서 암환자 유래 오가노이드뱅킹·AI기반 신규 타깃 발굴 기술을 소개했다.그래디언트바이오컨버전스는 이번 학회에서 자체 AI 기술을 적용한 '암환자 유래 오가노이드(PDO)' 기반의 혁신신약 타깃 발굴 및 비반응성 바이오마커 발굴 플랫폼을 소개하고, 각 PDO 별로 환자 임상정보를 비롯한 약물반응성과 유전체 정보(NGS)가 매칭된 PDO 뱅킹 시스템을 선보이며 글로벌 제약바이오 관계자들로부터 큰 호응을 얻었다.2024-09-24 06:00:45노병철
R&D 혁신 이끄는 '오가노이드', 캐시카우 원동력 부상[데일리팜=노병철 기자] 국내외적으로 대체동물시험을 촉진하기 위한 법안들이 속속 등장하면서 오가노이드 기반 R&D산업이 주목받고 있다.오가노이드(organoid)는 인간의 줄기세포나 전구세포를 사용해 특정 장기의 구조와 기능을 3차원적으로 모사한 미니어처 형태의 인공 장기다.오가노이드는 실제 장기와 유사한 시험 환경을 연구원에게 제공하며, 세포 간 상호작용과 조직 특유의 구조를 재현할 수도 있다.이는 2차원 세포 배양 방식에 비해 훨씬 더 정교한 연구 모델로서 활용되고 있으며, 질병 연구나 신약 개발, 독성 평가 등에서 새로운 시험 방법으로 평가받고 있는 기술이다.대표적으로 글로벌 제약사인 로슈는 간암과 같은 특정 질병 연구에서 오가노이드를 활용해 약물의 효과와 독성을 평가하고 있으며, 머크(Merck)는 종양 오가노이드 모델을 활용해 새로운 항암제를 테스트하고 있는 것으로 알려져 있다.이외에도 아스트라제네카와 글락소스미스클라인(GSK)은 각각 폐 오가노이드 모델과 뇌 오가노이드 모델을 활용해 호흡기 질환 치료제와 신경질환 치료제 개발을 이어가고 있다.오가노이드 기술관련 국내 대표주자로는 JW중외제약, 차바이오텍, 그래디언트바이오컨버전스, 오가노이드사이언스 등 10개 안팎의 기업을 들 수 있다.먼저 JW중외제약은 신약 개발 과정에서 오가노이드를 선도적으로 도입해 활용하고 있는 제약사다.대표적으로 최근 미국 텍사스주에서 열린 미국 피부연구학회(Society of Investigative Dermatology)에서 JW중외제약은 탈모치료제 혁신 신약후보물질 ‘JW0061’에 대한 전임상 연구 결과를 발표해 참가자들의 많은 관심을 받았다.JW중외제약이 공개한 연구결과에 따르면 인간의 두피에서 JW0061이 모낭을 생성하는지 예측하기 위해 피부 오가노이드 모델을 활용해 전임상 시험을 진행, 표준치료제에 비해 약물 처리 5일째, 10일째 기준 모낭 수가 각각 7.2배, 4.0배 많다는 모낭생성 효능 시험 데이터를 확인했다.2023년에는 JW중외제약 연구법인 C&C신약연구소가 정밀의료 혁신기업 ‘엠비디’와 3D 암 오가노이드 진단 플랫폼 기반의 혁신 항암제 개발을 위한 연구 협력을 체결, 오가노이드 플랫폼을 활용해 다양한 종양 적응증을 탐색해 나가는 과제를 수행하고 있다. 차바이오텍도 오픈이노베이션과 CDMO를 통해 오가노이드 재생치료제 사업에 공을 들이고 있다.차바이오텍은 지난 3월, 재생의료용 세포치료제 개발기업 셀인셀즈와 연골질환 오가노이드치료제 위탁생산(CDMO) 계약을 했다.이번 계약으로 차바이오텍은 자회사인 차바이오랩 의약품 제조시설에서 고품질 오가노이드 재생치료제 개발용 줄기세포의 세포은행을 구축해 셀인셀즈에 제공할 예정이다.이에 따라 셀인셀즈는 줄기세포 유래 오가노이드 재생치료제 개발에 속도를 올릴 수 있게 됐고, 차바이오텍은 세포은행 구축 후 임상용 의약품 생산도 기대할 수 있게 됐다.셀인셀즈는 피부재생, 연골재생, 혈관생성 등 다양한 질환의 오가노이드 재생치료제 파이프라인을 보유, 95% 이상 확률로 균일한 오가노이드를 대량 생산할 수 있는 기술을 갖고 있다.기술 확장과 고도화를 위해 오가노이드와 인공지능(AI) 기술을 융합해 생산공정 자동화, 기준 및 시험방법 마련, 대량 생산 최적화 솔루션 개발 등을 추진 중이다.오가노이드 기반 차세대 재생치료제 개발 전문기업 오가노이드사이언스는 전략적 파트너십을 활용해 오가노이드 기반 사업을 확장하고 있다.오가노이드사이언스는 이달 중순 신약개발기업 그라스메디와 MOU를 맺고, 동물실험없는 반려동물 헬스케어시대를 앞당길 계획이다.오가노이드사이언스는 이번 전략적 파트너십을 계기로 공동 연구 프로젝트를 추진, 기술 교류 및 인재 양성 등 구체적인 협력 방안을 지속 논의할 방침이다.또, 차세대 의약외품 및 반려동물 관련 상품 개발을 가속화하고 글로벌 시장 경쟁력을 강화하며 지속 가능한 성장과 발전을 도모할 예정이다.그래디언트바이오컨버전스는 이달 열린 유럽종양학회(ESMO)에서 암환자 유래 오가노이드뱅킹·AI기반 신규 타깃 발굴 기술을 소개했다.그래디언트바이오컨버전스는 이번 학회에서 자체 AI 기술을 적용한 '암환자 유래 오가노이드(PDO)' 기반의 혁신신약 타깃 발굴 및 비반응성 바이오마커 발굴 플랫폼을 소개하고, 각 PDO 별로 환자 임상정보를 비롯한 약물반응성과 유전체 정보(NGS)가 매칭된 PDO 뱅킹 시스템을 선보이며 글로벌 제약바이오 관계자들로부터 큰 호응을 얻었다.2024-09-24 06:00:45노병철 -
 유방암 최초 AKT억제제 티루캡...치료효과 배가[데일리팜=황병우 기자] 치료제의 발전에도 불구하고 암이 전이된 이후 옵션이 부족했던 유방암에 새로운 표적 치료제인 티루캡이 등장하면서 미충족수요가 개선될 수 있을지 주목받고 있다.HR 양성/HER2음성 유방암의 2차 치료에서 절반가량을 차지하는 PIK3CA/AKT1/PTEN 변이를 표적으로 하는 만큼 다수의 환자가 혜택을 볼 수 있을 것이라는 게 전문가의 평가다.다만 염기서열 유전자패널검사(이하 NGS) 선별급여의 본인부담금이 증가하면서 환자 맞춤형 치료전략 수립을 위한 시너지 고민이 필요하다는 지적이다.12일 아스트라제네카는 국소진행성 또는 전이성 유방암 최초이자 유일한 AKT 억제제 티루캡(성분명 카피바서팁)의 국내 출시기념 간담회를 개최하고 치료제의 임상적 가치를 조명했다. 이달 12일 아스트라제네카는 국소진행성 또는 전이성 유방암 최초이자 유일한 AKT 억제제 티루캡(카피바서팁)의 국내 출시기념 간담회를 개최하고 치료제의 임상적 가치를 조명했다.티루캡은 지난 4월 호르몬수용체양성(HR+)/사람상피세포성장인자수용체2음성(HER2-)(이하, HR 양성/HER2음성)이면서 한 가지 이상의 PIK3CA/AKT1/PTEN 변이가 있는 성인의 국소 진행성 또는 전이성 유방암 치료제로 식품의약품안전처의 허가를 받았다.지난 9일부터 시장에 출시 돼 내분비 요법 중 또는 이후 진행되거나 보조요법 완료 후 12개월 이내 재발한 경우 풀베스트란트와의 병용투여 처방이 가능해졌다.티루캡의 등장이 가지는 의미는 HR 양성/HER2음성 1차 치료 후 미충족 수요가 있던 2차 치료의 선택지 증가다.발표를 맡은 박경화 고대안암병원 종양내과 교수에 따르면 HR 양성/HER2음성은 전체 유방암 환자의 70%를 차지한다.기존에 CDK4/6 억제제와 같은 1차 치료 옵션이 등장했지만, 여전히 내성 등으로 치료에 실패하는 환자가 발생하고 있다.박경화 교수는 "HR 양성/HER2음성 환자 중 약 50%를 차지하는 하나 이상의 PIK3CA/AKT1/ PTEN 변이가 있는 환자는 질병 진행이 빨라질 수 있어 해당 변이를 타깃하는 전이성 유방암 2차 표적 치료제에 대한 필요성이 지속적으로 제기돼 왔다"고 설명했다.박경화 고대안암병원 종양내과 교수는 티루캡이 질병 진행 또는 사망위험률을 50% 낮춘 부분에 주목했다. 티루캡 허가의 근거가 된 연구는 CAPItello-291다. 연구 결과 내분비요법(ET)±CDK4/6 억제제 요법 후 1차 치료에 실패한 환자를 대상으로 풀베스트란트 단독요법군 대비 무진행생존기간 중앙값(mPFS)을 약 2.5배 개선됐다.구체적으로 티루캡 풀베스트란트 병용 환자군의 mPFS 7.3개월로 풀베스트란트 단독요법 3.1개월 대비 2배 이상 높게 나타났으며, 질병 진행 또는 사망위험률을 50% 낮췄다.박 교수는 "결국 전이성 유방암에서 1차 치료제로 완치되는 환자는 아주 드물고 대부분 치료에 실패서 2차 치료 이상으로 넘어오게 된다. 티루캡이 표적으로 삼는 돌연변이가 간이나 여러 장기로 전이가 잘되는 아형이기 때문에 치료제의 긍정적인 효과가 기대된다"고 강조했다.본인부담 늘어난 유방암 NGS…"환경 변화 고민 필요해"티루캡이 가진 치료 효과와 별개로 환자를 치료하는 전문가의 고민도 존재한다.치료제 특성상 NGS 등을 통한 변이 확인이 필수지만 지난해 12월 NGS 선별급여가 본인부담금 80%로 개정되면서 환자들의 부담이 커졌기 때문이다.박경화 고대안암병원 종양내과 교수박 교수는 "2차 치료 결정을 빠르게 내리고, 적절한 치료로 치료 결과를 향상하기 위해서는 NGS를 통해 진단 시 혹은 1차 치료 중에 변이 여부 확인이 필요하다"며 "유전자 변이가 많은 유방암에서 환자 맞춤형 치료전략 수립을 위해 NGS 검사의 활성화와 지원 확대가 절실하다"고 말했다.실제 글로벌 NCCN, ASCO, ESMO 주요 가이드라인에서는 전이성 유방암 환자에서 PIK3CA, AKT1, PTEN 유전자 변이를 확인할 것을 권고하고 있다.박 교수는 "NGS 선별검사의 환자 본인부담금이 절반인 것과 80%일 때 환자가 느끼는 압박의 차이는 매우 크다"며 "꼭 신약을 사용하기 위한 것이 아니라 변이가 없는 것을 확인하고 현재 보험이 적용되는 호르몬제나 일반항암제를 선택하기 위해서라도 NGS 검사의 효과는 크다"고 밝혔다.이어 그는 "이를 위해 현재 학회를 중심으로 국내 데이터를 모아 근거를 만드는 등의 고민도 이뤄지고 있다"며 "암이 재발 또는 전이 돼서 결국 환자가 사망할 수밖에 없는 상황이 환자에게 NGS를 한번 진행하는 것이 정말 비용효과성이 떨어지는 것인가에 대해서는 다시 생각해 볼 필요가 있다"고 덧붙였다.2024-09-12 17:14:20황병우
유방암 최초 AKT억제제 티루캡...치료효과 배가[데일리팜=황병우 기자] 치료제의 발전에도 불구하고 암이 전이된 이후 옵션이 부족했던 유방암에 새로운 표적 치료제인 티루캡이 등장하면서 미충족수요가 개선될 수 있을지 주목받고 있다.HR 양성/HER2음성 유방암의 2차 치료에서 절반가량을 차지하는 PIK3CA/AKT1/PTEN 변이를 표적으로 하는 만큼 다수의 환자가 혜택을 볼 수 있을 것이라는 게 전문가의 평가다.다만 염기서열 유전자패널검사(이하 NGS) 선별급여의 본인부담금이 증가하면서 환자 맞춤형 치료전략 수립을 위한 시너지 고민이 필요하다는 지적이다.12일 아스트라제네카는 국소진행성 또는 전이성 유방암 최초이자 유일한 AKT 억제제 티루캡(성분명 카피바서팁)의 국내 출시기념 간담회를 개최하고 치료제의 임상적 가치를 조명했다. 이달 12일 아스트라제네카는 국소진행성 또는 전이성 유방암 최초이자 유일한 AKT 억제제 티루캡(카피바서팁)의 국내 출시기념 간담회를 개최하고 치료제의 임상적 가치를 조명했다.티루캡은 지난 4월 호르몬수용체양성(HR+)/사람상피세포성장인자수용체2음성(HER2-)(이하, HR 양성/HER2음성)이면서 한 가지 이상의 PIK3CA/AKT1/PTEN 변이가 있는 성인의 국소 진행성 또는 전이성 유방암 치료제로 식품의약품안전처의 허가를 받았다.지난 9일부터 시장에 출시 돼 내분비 요법 중 또는 이후 진행되거나 보조요법 완료 후 12개월 이내 재발한 경우 풀베스트란트와의 병용투여 처방이 가능해졌다.티루캡의 등장이 가지는 의미는 HR 양성/HER2음성 1차 치료 후 미충족 수요가 있던 2차 치료의 선택지 증가다.발표를 맡은 박경화 고대안암병원 종양내과 교수에 따르면 HR 양성/HER2음성은 전체 유방암 환자의 70%를 차지한다.기존에 CDK4/6 억제제와 같은 1차 치료 옵션이 등장했지만, 여전히 내성 등으로 치료에 실패하는 환자가 발생하고 있다.박경화 교수는 "HR 양성/HER2음성 환자 중 약 50%를 차지하는 하나 이상의 PIK3CA/AKT1/ PTEN 변이가 있는 환자는 질병 진행이 빨라질 수 있어 해당 변이를 타깃하는 전이성 유방암 2차 표적 치료제에 대한 필요성이 지속적으로 제기돼 왔다"고 설명했다.박경화 고대안암병원 종양내과 교수는 티루캡이 질병 진행 또는 사망위험률을 50% 낮춘 부분에 주목했다. 티루캡 허가의 근거가 된 연구는 CAPItello-291다. 연구 결과 내분비요법(ET)±CDK4/6 억제제 요법 후 1차 치료에 실패한 환자를 대상으로 풀베스트란트 단독요법군 대비 무진행생존기간 중앙값(mPFS)을 약 2.5배 개선됐다.구체적으로 티루캡 풀베스트란트 병용 환자군의 mPFS 7.3개월로 풀베스트란트 단독요법 3.1개월 대비 2배 이상 높게 나타났으며, 질병 진행 또는 사망위험률을 50% 낮췄다.박 교수는 "결국 전이성 유방암에서 1차 치료제로 완치되는 환자는 아주 드물고 대부분 치료에 실패서 2차 치료 이상으로 넘어오게 된다. 티루캡이 표적으로 삼는 돌연변이가 간이나 여러 장기로 전이가 잘되는 아형이기 때문에 치료제의 긍정적인 효과가 기대된다"고 강조했다.본인부담 늘어난 유방암 NGS…"환경 변화 고민 필요해"티루캡이 가진 치료 효과와 별개로 환자를 치료하는 전문가의 고민도 존재한다.치료제 특성상 NGS 등을 통한 변이 확인이 필수지만 지난해 12월 NGS 선별급여가 본인부담금 80%로 개정되면서 환자들의 부담이 커졌기 때문이다.박경화 고대안암병원 종양내과 교수박 교수는 "2차 치료 결정을 빠르게 내리고, 적절한 치료로 치료 결과를 향상하기 위해서는 NGS를 통해 진단 시 혹은 1차 치료 중에 변이 여부 확인이 필요하다"며 "유전자 변이가 많은 유방암에서 환자 맞춤형 치료전략 수립을 위해 NGS 검사의 활성화와 지원 확대가 절실하다"고 말했다.실제 글로벌 NCCN, ASCO, ESMO 주요 가이드라인에서는 전이성 유방암 환자에서 PIK3CA, AKT1, PTEN 유전자 변이를 확인할 것을 권고하고 있다.박 교수는 "NGS 선별검사의 환자 본인부담금이 절반인 것과 80%일 때 환자가 느끼는 압박의 차이는 매우 크다"며 "꼭 신약을 사용하기 위한 것이 아니라 변이가 없는 것을 확인하고 현재 보험이 적용되는 호르몬제나 일반항암제를 선택하기 위해서라도 NGS 검사의 효과는 크다"고 밝혔다.이어 그는 "이를 위해 현재 학회를 중심으로 국내 데이터를 모아 근거를 만드는 등의 고민도 이뤄지고 있다"며 "암이 재발 또는 전이 돼서 결국 환자가 사망할 수밖에 없는 상황이 환자에게 NGS를 한번 진행하는 것이 정말 비용효과성이 떨어지는 것인가에 대해서는 다시 생각해 볼 필요가 있다"고 덧붙였다.2024-09-12 17:14:20황병우 -
 "담관암, 치료옵션 부족...효과좋은 새 표적치료제 기대"오도연 서울대병원 혈액종양내과 교수 [데일리팜=손형민 기자] “최근 들어 많은 회사들이 담관암 분야에서 다양한 연구들을 진행하면서 팁소보 등 효과적인 약물들이 점차 출시되고 있습니다. 담관암도 폐암처럼 표적치료제 개발이 가능한 암이었으나 그동안 연구와 투자가 충분하지 않았는데, 최근 좋은 임상 결과들이 점점 나오고 있는 상황입니다.”오도연 서울대병원 혈액종양내과 교수는 최근 데일리팜과 만난 자리에서 그간 치료옵션이 부족했던 담관암에 효과 좋은 표적치료제가 속속 등장하고 있다는 기대감을 내비쳤다.담관암은 간에서 만들어진 담즙이 십이지장까지 가는 경로인 담도에서 암세포들이 형성하는 종괴다. 지난해 발표된 중앙암등록본부 자료에 의하면 담관암 환자의 수는 2011년 5444명에서 2021년 7617명으로 10년 새 40% 가까이 증가했다.담관암은 환자 수가 비교적 적은 편이지만 조기 진단이 어렵고 주변 장기로의 빠른 전이와 재발로 인해 5년 상대생존율(2017~2021년)은 28.9%에 불과하다. 환자 10명 중 7명이 담관암으로 사망하고 있다.담관암 환자의 생존율이 낮은 또 다른 이유는 치료옵션이 제한적이기 때문이다. 수술이 불가능한 국소 진행형 또는 전이성 담관암에서 1차 치료에 실패한 경우 2차 치료제로 국내에서 허가된 표적치료제가 없었다.이런 상황에서 세르비에의 팁소보(성분명 이보시데닙)라는 새로운 표적치료옵션이 지난 5월 국내 허가됐다. 이번 허가로 팁소보는 이소시트르산 탈수소효소-1(IDH1) 변이 양성인 이전 치료 경험이 있는 국소 진행성 또는 전이성 담관암 성인 환자에서 사용이 가능해졌다.오 교수는 새로운 약물이 환자들에게 새로운 기회를 제공하고 삶의 질을 바꿀 수 있다며 표적치료제 옵션에 대한 접근성이 높아져야 한다고 강조했다. 표적치료제 팁소보 등장…IDH1 변이 담관암서 허가된 유일한 표적치료제담관암 분야에서 최초로 글로벌 임상3상 연구에 성공한 표적치료제는 IDH1을 타깃한 팁소보다. IDH1 유전자 변이는 전체 고형암 중 주로 신경교종(glioma)과 담관암에서 발현된다. 담관암 중에서는 간내 담관암에서 주로 IDH1 변이가 보고되는 것으로 알려진다.오 교수는 “일반적인 특성이 없으면 담관암 2차 치료옵션은 세포 독성 항암화학요법과 FOLFOX(플루오로우라실·류코보린·옥살리플라틴) 크게 두 가지로 제한된다. 3차부터는 표준 약이 없다”며 “다만 IDH1 변이와 같은 특성이 있는 환자들에게는 표적치료제 사용도 가능하다. 환자가 좋은 컨디션을 유지한다면 담관암에서도 다양한 치료옵션을 시도해 볼 수 있다”고 전했다.이어 “간내 담관암, 간외 담관암, 담낭암 등 담도암 전체를 포함해 분석할 경우 차세대염기서열분석(NGS) 결과에서 IDH1 변이가 빈번하게 나타나지 않는다. 다만 간내 담관암만 보면 IDH1 변이의 빈도가 약 10% 전후로 높아진다”고 덧붙였다.팁소보는 이전에 치료를 받은 IDH1 변이 담관암 환자를 대상으로 실시된 무작위 임상3상 ClarIDHy 연구에서 유효성을 확인했다. 팁소보는 1차 평가변수인 독립적 검토위원회의 무진행 생존기간(PFS)을 통계적으로 유의하게 개선시킨 것으로 나타났다.오 교수는 “현재도 2차 치료에서 표준요법이라고 할 만한 것은 없지만 팁소보 연구가 진행됐을 때는 FOLFOX 요법의 연구 결과도 나오기 전이었다. 이에 대조군을 위약군으로 설정할 수밖에 없었다”고 전했다.이어 “연구의 1차 평가지표는 무진행생존기간(PFS)으로 진행됐다. 위약군에서 질병이 진행(PD)됐을 때, 환자들이 팁소보군으로 교차 투여할 수 있도록 설계됐기 때문이다. 만약 전체생존기간(OS)를 주요 평가변수로 설정했더라면, 교차 치료로 인해 OS 데이터가 혼합돼 연구 결과가 희석(dilution) 될 수 있기 때문”이라고 덧붙였다.임상 결과, 팁소보 치료군의 PFS 중앙값은 2.7개월, 위약군은 1.4개월로 분석됐다. 팁소보 치료군에서 6개월 차와 12개월 차에 질병이 진행되지 않거나 사망하지 않은 환자의 비율은 각각 32%, 22%이었으며 위약군에서는 이러한 환자가 없었다.팁소보는 임상시험의 주요 2차 평가변수인 OS에 대해서도 긍정적인 결과를 보였다. 팁소보 치료군의 OS 중앙값은 10.3개월이었으며, 위약군은 7.5개월로 나타났다.오 교수는 “위약군의 OS는 7.5개월 정도였지만 이 수치는 환자가 팁소보 교체투여를 실시해서 증가된 것이다. 이를 보정하기 위해 RPFST(rank-preserving structural failure time) 방법을 사용해 측정된 위약군의 OS는 5.1개월이다. 10.3개월과 5.1개월의 OS 차이를 비교했을 때 위험비는 유의미하게 나타났다(HR 0.49).”고 전했다.이어 “처방 결과를 돌이켜보면 팁소보를 사용했을 때 독성 관련 이상반응은 크게 발견되지 않았다. 예를 들어 FGFR2 억제제들은 손가락이 갈라지거나 피가 나고 피부가 벗겨지거나 손톱이 빠지는 등 특징적인 부작용들이 있다. 팁소보의 경우 특별히 주의해야 하는 부작용은 없었다. 그렇기 때문에 환자가 편하게 약을 사용할 수 있다”고 강조했다.효과 좋은 표적치료제 연구 계속…"신약 접근성 높여야"최근들어 많은 회사들에서 담관암에 대한 투자를 늘리고 여러 연구들을 진행하게 되면서 효과적인 약물들이 점차 출시되고 있는 상황이다. 최근 1차 치료제에 면역항암제 아스트라제네카의 임핀지, MSD의 키트루다가 추가됐으며 2차 치료제에는 팁소보가 생존기간을 늘렸다.오 교수는 “흔히 사람들이 담관암을 비소세포폐암에 비유하곤 한다. 폐암은 유전적 아형(genetic subset)이 많은데, 담관암 역시 이러한 특성을 가지고 있다는 점에서 유사하다. 폐암처럼 담관암도 다양한 표적치료제 개발이 가능한 암이었으나 환자 수가 부족해 그간 연구와 투자가 충분하지 않았다. 다만 최근 제약업계의 관심이 높아져 좋은 연구 결과들이 점점 나오고 있는 상황”이라고 전했다.하지만 약의 효과를 입증하고 허가되더라도 환자들이 해당 약을 실질적으로 사용하기 위해서는 오랜 시간이 걸린다. 환자들에게 약에 대한 데이터를 잘 이해시켜야 하고 약을 편하게 사용할 수 있게끔 환경이 뒷받침돼야 한다는 게 오 교수의 의견이다.오 교수는 “담관암의 경우 치료 옵션이 부족하기 때문에 기존 약제 대비 효과의 차이가 가지는 의미와 가치는 다른 암종들에 비해 크다. 데이터를 해석할 때에는 각 암 종류의 고유한 환경과 생물학적 특성에 맞춰서 진행해야 한다. 정부에서도 암종의 특수성을 감안해 데이터를 분석하고 해석했으면 한다”며 “치료 옵션이 제한적인 암종에서 약이 가지는 의미는 치료 옵션이 많은 암과 차이가 있을 수 있다는 점을 이해하고 급여 기준을 잡아야 할 것으로 본다”고 전했다.이어 “최근 5년 사이에 담관암 관련 약물 개발이 매우 빨라졌다. 새로운 약들이 개발되는 것과 함께 많은 회사들도 담관암 약제 개발을 위해 힘쓰고 있는 상황이다. 담관암 환자들이 좌절하기 보다는 의료진의 가이드에 따라 치료를 잘 받아 임상 참여 등 새로운 기회를 얻는 것이 중요하다”고 강조했다.2024-09-06 06:17:06손형민
"담관암, 치료옵션 부족...효과좋은 새 표적치료제 기대"오도연 서울대병원 혈액종양내과 교수 [데일리팜=손형민 기자] “최근 들어 많은 회사들이 담관암 분야에서 다양한 연구들을 진행하면서 팁소보 등 효과적인 약물들이 점차 출시되고 있습니다. 담관암도 폐암처럼 표적치료제 개발이 가능한 암이었으나 그동안 연구와 투자가 충분하지 않았는데, 최근 좋은 임상 결과들이 점점 나오고 있는 상황입니다.”오도연 서울대병원 혈액종양내과 교수는 최근 데일리팜과 만난 자리에서 그간 치료옵션이 부족했던 담관암에 효과 좋은 표적치료제가 속속 등장하고 있다는 기대감을 내비쳤다.담관암은 간에서 만들어진 담즙이 십이지장까지 가는 경로인 담도에서 암세포들이 형성하는 종괴다. 지난해 발표된 중앙암등록본부 자료에 의하면 담관암 환자의 수는 2011년 5444명에서 2021년 7617명으로 10년 새 40% 가까이 증가했다.담관암은 환자 수가 비교적 적은 편이지만 조기 진단이 어렵고 주변 장기로의 빠른 전이와 재발로 인해 5년 상대생존율(2017~2021년)은 28.9%에 불과하다. 환자 10명 중 7명이 담관암으로 사망하고 있다.담관암 환자의 생존율이 낮은 또 다른 이유는 치료옵션이 제한적이기 때문이다. 수술이 불가능한 국소 진행형 또는 전이성 담관암에서 1차 치료에 실패한 경우 2차 치료제로 국내에서 허가된 표적치료제가 없었다.이런 상황에서 세르비에의 팁소보(성분명 이보시데닙)라는 새로운 표적치료옵션이 지난 5월 국내 허가됐다. 이번 허가로 팁소보는 이소시트르산 탈수소효소-1(IDH1) 변이 양성인 이전 치료 경험이 있는 국소 진행성 또는 전이성 담관암 성인 환자에서 사용이 가능해졌다.오 교수는 새로운 약물이 환자들에게 새로운 기회를 제공하고 삶의 질을 바꿀 수 있다며 표적치료제 옵션에 대한 접근성이 높아져야 한다고 강조했다. 표적치료제 팁소보 등장…IDH1 변이 담관암서 허가된 유일한 표적치료제담관암 분야에서 최초로 글로벌 임상3상 연구에 성공한 표적치료제는 IDH1을 타깃한 팁소보다. IDH1 유전자 변이는 전체 고형암 중 주로 신경교종(glioma)과 담관암에서 발현된다. 담관암 중에서는 간내 담관암에서 주로 IDH1 변이가 보고되는 것으로 알려진다.오 교수는 “일반적인 특성이 없으면 담관암 2차 치료옵션은 세포 독성 항암화학요법과 FOLFOX(플루오로우라실·류코보린·옥살리플라틴) 크게 두 가지로 제한된다. 3차부터는 표준 약이 없다”며 “다만 IDH1 변이와 같은 특성이 있는 환자들에게는 표적치료제 사용도 가능하다. 환자가 좋은 컨디션을 유지한다면 담관암에서도 다양한 치료옵션을 시도해 볼 수 있다”고 전했다.이어 “간내 담관암, 간외 담관암, 담낭암 등 담도암 전체를 포함해 분석할 경우 차세대염기서열분석(NGS) 결과에서 IDH1 변이가 빈번하게 나타나지 않는다. 다만 간내 담관암만 보면 IDH1 변이의 빈도가 약 10% 전후로 높아진다”고 덧붙였다.팁소보는 이전에 치료를 받은 IDH1 변이 담관암 환자를 대상으로 실시된 무작위 임상3상 ClarIDHy 연구에서 유효성을 확인했다. 팁소보는 1차 평가변수인 독립적 검토위원회의 무진행 생존기간(PFS)을 통계적으로 유의하게 개선시킨 것으로 나타났다.오 교수는 “현재도 2차 치료에서 표준요법이라고 할 만한 것은 없지만 팁소보 연구가 진행됐을 때는 FOLFOX 요법의 연구 결과도 나오기 전이었다. 이에 대조군을 위약군으로 설정할 수밖에 없었다”고 전했다.이어 “연구의 1차 평가지표는 무진행생존기간(PFS)으로 진행됐다. 위약군에서 질병이 진행(PD)됐을 때, 환자들이 팁소보군으로 교차 투여할 수 있도록 설계됐기 때문이다. 만약 전체생존기간(OS)를 주요 평가변수로 설정했더라면, 교차 치료로 인해 OS 데이터가 혼합돼 연구 결과가 희석(dilution) 될 수 있기 때문”이라고 덧붙였다.임상 결과, 팁소보 치료군의 PFS 중앙값은 2.7개월, 위약군은 1.4개월로 분석됐다. 팁소보 치료군에서 6개월 차와 12개월 차에 질병이 진행되지 않거나 사망하지 않은 환자의 비율은 각각 32%, 22%이었으며 위약군에서는 이러한 환자가 없었다.팁소보는 임상시험의 주요 2차 평가변수인 OS에 대해서도 긍정적인 결과를 보였다. 팁소보 치료군의 OS 중앙값은 10.3개월이었으며, 위약군은 7.5개월로 나타났다.오 교수는 “위약군의 OS는 7.5개월 정도였지만 이 수치는 환자가 팁소보 교체투여를 실시해서 증가된 것이다. 이를 보정하기 위해 RPFST(rank-preserving structural failure time) 방법을 사용해 측정된 위약군의 OS는 5.1개월이다. 10.3개월과 5.1개월의 OS 차이를 비교했을 때 위험비는 유의미하게 나타났다(HR 0.49).”고 전했다.이어 “처방 결과를 돌이켜보면 팁소보를 사용했을 때 독성 관련 이상반응은 크게 발견되지 않았다. 예를 들어 FGFR2 억제제들은 손가락이 갈라지거나 피가 나고 피부가 벗겨지거나 손톱이 빠지는 등 특징적인 부작용들이 있다. 팁소보의 경우 특별히 주의해야 하는 부작용은 없었다. 그렇기 때문에 환자가 편하게 약을 사용할 수 있다”고 강조했다.효과 좋은 표적치료제 연구 계속…"신약 접근성 높여야"최근들어 많은 회사들에서 담관암에 대한 투자를 늘리고 여러 연구들을 진행하게 되면서 효과적인 약물들이 점차 출시되고 있는 상황이다. 최근 1차 치료제에 면역항암제 아스트라제네카의 임핀지, MSD의 키트루다가 추가됐으며 2차 치료제에는 팁소보가 생존기간을 늘렸다.오 교수는 “흔히 사람들이 담관암을 비소세포폐암에 비유하곤 한다. 폐암은 유전적 아형(genetic subset)이 많은데, 담관암 역시 이러한 특성을 가지고 있다는 점에서 유사하다. 폐암처럼 담관암도 다양한 표적치료제 개발이 가능한 암이었으나 환자 수가 부족해 그간 연구와 투자가 충분하지 않았다. 다만 최근 제약업계의 관심이 높아져 좋은 연구 결과들이 점점 나오고 있는 상황”이라고 전했다.하지만 약의 효과를 입증하고 허가되더라도 환자들이 해당 약을 실질적으로 사용하기 위해서는 오랜 시간이 걸린다. 환자들에게 약에 대한 데이터를 잘 이해시켜야 하고 약을 편하게 사용할 수 있게끔 환경이 뒷받침돼야 한다는 게 오 교수의 의견이다.오 교수는 “담관암의 경우 치료 옵션이 부족하기 때문에 기존 약제 대비 효과의 차이가 가지는 의미와 가치는 다른 암종들에 비해 크다. 데이터를 해석할 때에는 각 암 종류의 고유한 환경과 생물학적 특성에 맞춰서 진행해야 한다. 정부에서도 암종의 특수성을 감안해 데이터를 분석하고 해석했으면 한다”며 “치료 옵션이 제한적인 암종에서 약이 가지는 의미는 치료 옵션이 많은 암과 차이가 있을 수 있다는 점을 이해하고 급여 기준을 잡아야 할 것으로 본다”고 전했다.이어 “최근 5년 사이에 담관암 관련 약물 개발이 매우 빨라졌다. 새로운 약들이 개발되는 것과 함께 많은 회사들도 담관암 약제 개발을 위해 힘쓰고 있는 상황이다. 담관암 환자들이 좌절하기 보다는 의료진의 가이드에 따라 치료를 잘 받아 임상 참여 등 새로운 기회를 얻는 것이 중요하다”고 강조했다.2024-09-06 06:17:06손형민 -
 "ADC신약 엔허투 희소폐암 허가...새 치료기회 확보"안명주 삼성서울병원 혈액종양내과 교수 [데일리팜=손형민 기자] “기존에는 환자들이 일부 상급종합병원에서 진행하는 임상에서만 엔허투를 사용할 수 있었지만 이번 국내 허가를 통해 HER2 변이 전이성 비소세포폐암 환자들에게 새로운 치료 기회가 생기게 됐습니다. 폐암 환자의 특성상 뇌 전이가 흔히 나타나는데 엔허투는 이같은 환자에서도 효과를 나타내 임상적 의미가 큽니다.”안명주 삼성서울병원 혈액종양내과 교수는 최근 데일리팜과 만난 자리에서 엔허투(성분명 트라스투주맙데룩스테칸)의 임상적 가치를 호평했다.엔허투는 다이이찌산쿄와 아스트라제네카가 공동개발한 항체약물접합체(ADC)로 지난 2022년 HER2 양성 유방암과 위암 치료에 허가됐다. 이후 엔허투는 HER2 변이 비소세포폐암과 저발현 유방암에도 효과를 나타내며 지난 5월 적응증이 확대됐다.HER2 변이 전이성 비소세포폐암은 환자의 약 2%에서 4%가량 발생하는 희소암이다. 이 암은 기존 항암화학요법과 면역항암제에 효능이 제한적이었고 HER2 표적치료제도 일관되지 않은 결과를 보여 환자의 생존율을 높일 수 있는 효과적인 옵션에 대한 미충족 수요가 존재했다.한미약품의 포지오티닙 등 여러 표적 치료옵션들이 HER2 변이 비소세포폐암에 도전장을 내밀었지만 번번이 유효성 입증에 실패했다. 엔허투의 등장은 희소암으로 분류되는 HER2 비소세포폐암 환자에게 새로운 희망이 될 것으로 전망된다.안 교수는 차세대염기서열분석(NGS) 검사의 보편화와 엔허투와 같은 표적치료제의 등장으로 비소세포폐암에서 HER2 변이가 주목을 받기 시작했다며 비소세포폐암 환자들에게도 새로운 치료 기회가 생기게 됐다고 전했다.엔허투, 임상2상 연구로 국내 허가엔허투는 HER2 변이를 타깃 하는 항체와 종양 세포를 사멸시키는 페이로드를 링커로 연결한 ADC다. 이 치료제는 항체가 특정 항원에 결합해 ADCC(Antibody Dependent Cellular Cytotoxicity) 반응과 함께 페이로드가 종양 세포에 들어가 세포막으로 나오는 기전을 갖고 있다. 이에 HER2 변이가 나타나지 않은 암 세포까지 사멸시키는 바이스탠더(Bystander) 효과를 나타내 항종양 효과를 나타낸다.이에 엔허투는 유방암, 위암, 대장암, 비소세포폐암 등 다양한 영역에서 효과를 나타내고 있다.엔허투는 DESTINY-Lung02 연구를 통해 HER2 변이 전이성 비소세포폐암 2차 치료에 항종양 반응을 입증했다.연구는 이전에 백금 기반 항암화학요법을 포함한 1회 이상의 전신요법 치료 이후 질병이 진행된 절제 불가능한 또는 전이성 비소세포폐암 환자를 대상으로 엔허투의 효능과 안전성을 평가했다.임상 결과, 엔허투 투여군은 종양 크기의 감소를 의미하는 객관적반응률(ORR)이 49%로 집계됐다. 그중 암이 완전히 사라진 완전반응(CR)은 1%, 일정 부분 종양크기가 줄어든 부분반응(PR)은 48%로 나타났다. 반응지속기간(DOR) 중앙값은 16.8개월이었다.안 교수는 “기존 2차 치료제인 도세탁셀은 반응률이 10~15%, 질병이 악화되지 않은 기간인 무진행생존기간(PFS) 중앙값이 5~6개월에 불과하지만 엔허투는 반응률이 50%, 반응지속기간이 16개월에 달한다. 또 폐암 특성상 뇌 전이가 흔히 나타나는데 엔허투는 뇌 전이 환자에서도 뇌속 반응률을 측정하는 두개내 반응률(IC-cORR)이 50% 이상이었다”고 전했다.이어 “HER2 양성 유방암에 사용되던 캐싸일라는 비소세포폐암에서 약 50% 이상의 반응률을 보여줬지만 반응지속기간이 짧다는 한계가 있었다. 이러한 상황에서 최근 엔허투가 HER2 변이 전이성 비소세포폐암 환자에서 효과를 보여주며 주목받게 됐다”며 “단일군(single-arm) 대상 임상2상 연구이긴 하지만 기존 약제가 보여왔던 데이터에 비해서는 매우 효과가 좋은 것이기 때문에 급여 적용이 될 필요가 있다고 생각한다”고 덧붙였다.비소세포폐암에서는 흔하지 않은 HER2…"엔허투 활용도 커질 것"HER2 변이 전이성 비소세포폐암의 경우 전체 비소세포폐암 환자의 2~4% 정도로 적다. 이 암은 선암(adenocarcinoma), 비흡연자, 여성, 그리고 일본과 한국을 포함한 동양인 환자가 많다는 특징이 있다. 또 뇌 전이 발생 비율도 높은 편이다.HER2 이상은 ‘유전자 변이(mutations)’, ‘유전자 증폭(amplification)’, ‘단백질 과발현(overexpression)’ 세 가지로 구분된다. 일반적으로 위암이나 유방암 등의 암종에서 HER2 유전자 이상은 대부분 HER2 단백질 과발현의 형태로 나타난다. 그러나 기존 비소세포폐암의 경우 HER2 과발현 유전자 이상이 큰 역할을 하지 않는다고 여겨졌다.기존 HER2 변이 비소세포폐암의 표준치료요법에는 1세대 항암제인 백금기반 항암화학요법이 주로 사용됐다. 최근에는 백금기반 항암화학요법과 면역항암제를 병용요법도 사용된다. 다만 비흡연자는 면역항암제로 효과를 잘 보지 못해 예후가 더 나쁜 것으로 알려져 있다.안 교수는 “그동안 HER2 변이 전이성 비소세포폐암에는 EGFR(Epidermal Growth Factor Receptor) 계열의 변이를 치료하기 위해 개발된 지오트립(아파티닙)과 같은 약물을 사용했지만, HER2 변이에서는 반응률이 약 10% 정도로 낮았다”며 “포지오티닙은 그보다 나은 약 27% 정도의 반응률을 보였지만 독성과 부작용이 심해서 사용하기에 어려움이 있었다”고 전했다.이에 안 교수는 엔허투의 등장으로 비소세포폐암의 치료 환경에 많은 변화가 있을 것으로 예상한다고 전했다.안 교수는 “미국의 경우 HER2 변이 전이성 비소세포폐암 적응증에 대해 미국 식품의약국(FDA) 허가와 급여 적용을 받아 이미 널리 사용되고 있다. 기준이 까다로운 유럽에서도 비소세포폐암 환자는 HER2 변이 검사를 반드시 실시하고 HER2 변이가 나타난 환자들에게는 엔허투를 사용하도록 권고하고 있다”고 말했다.이어 “엔허투로 치료를 받으면 1년 이상 일상생활을 충분히 유지할 수 있는 환자들이 한 달에 최대 800만원 정도가 되는 치료제를 부담하기에 무리가 돼 사용하지 못하는 것을 보면 안타깝다. 때문에 정부가 선별 급여 등 다양한 방안을 강구해 환자가 부담하는 비율을 조금 높여서라도 급여가 적용되면 좋겠다”고 피력했다.2024-07-11 06:18:17손형민
"ADC신약 엔허투 희소폐암 허가...새 치료기회 확보"안명주 삼성서울병원 혈액종양내과 교수 [데일리팜=손형민 기자] “기존에는 환자들이 일부 상급종합병원에서 진행하는 임상에서만 엔허투를 사용할 수 있었지만 이번 국내 허가를 통해 HER2 변이 전이성 비소세포폐암 환자들에게 새로운 치료 기회가 생기게 됐습니다. 폐암 환자의 특성상 뇌 전이가 흔히 나타나는데 엔허투는 이같은 환자에서도 효과를 나타내 임상적 의미가 큽니다.”안명주 삼성서울병원 혈액종양내과 교수는 최근 데일리팜과 만난 자리에서 엔허투(성분명 트라스투주맙데룩스테칸)의 임상적 가치를 호평했다.엔허투는 다이이찌산쿄와 아스트라제네카가 공동개발한 항체약물접합체(ADC)로 지난 2022년 HER2 양성 유방암과 위암 치료에 허가됐다. 이후 엔허투는 HER2 변이 비소세포폐암과 저발현 유방암에도 효과를 나타내며 지난 5월 적응증이 확대됐다.HER2 변이 전이성 비소세포폐암은 환자의 약 2%에서 4%가량 발생하는 희소암이다. 이 암은 기존 항암화학요법과 면역항암제에 효능이 제한적이었고 HER2 표적치료제도 일관되지 않은 결과를 보여 환자의 생존율을 높일 수 있는 효과적인 옵션에 대한 미충족 수요가 존재했다.한미약품의 포지오티닙 등 여러 표적 치료옵션들이 HER2 변이 비소세포폐암에 도전장을 내밀었지만 번번이 유효성 입증에 실패했다. 엔허투의 등장은 희소암으로 분류되는 HER2 비소세포폐암 환자에게 새로운 희망이 될 것으로 전망된다.안 교수는 차세대염기서열분석(NGS) 검사의 보편화와 엔허투와 같은 표적치료제의 등장으로 비소세포폐암에서 HER2 변이가 주목을 받기 시작했다며 비소세포폐암 환자들에게도 새로운 치료 기회가 생기게 됐다고 전했다.엔허투, 임상2상 연구로 국내 허가엔허투는 HER2 변이를 타깃 하는 항체와 종양 세포를 사멸시키는 페이로드를 링커로 연결한 ADC다. 이 치료제는 항체가 특정 항원에 결합해 ADCC(Antibody Dependent Cellular Cytotoxicity) 반응과 함께 페이로드가 종양 세포에 들어가 세포막으로 나오는 기전을 갖고 있다. 이에 HER2 변이가 나타나지 않은 암 세포까지 사멸시키는 바이스탠더(Bystander) 효과를 나타내 항종양 효과를 나타낸다.이에 엔허투는 유방암, 위암, 대장암, 비소세포폐암 등 다양한 영역에서 효과를 나타내고 있다.엔허투는 DESTINY-Lung02 연구를 통해 HER2 변이 전이성 비소세포폐암 2차 치료에 항종양 반응을 입증했다.연구는 이전에 백금 기반 항암화학요법을 포함한 1회 이상의 전신요법 치료 이후 질병이 진행된 절제 불가능한 또는 전이성 비소세포폐암 환자를 대상으로 엔허투의 효능과 안전성을 평가했다.임상 결과, 엔허투 투여군은 종양 크기의 감소를 의미하는 객관적반응률(ORR)이 49%로 집계됐다. 그중 암이 완전히 사라진 완전반응(CR)은 1%, 일정 부분 종양크기가 줄어든 부분반응(PR)은 48%로 나타났다. 반응지속기간(DOR) 중앙값은 16.8개월이었다.안 교수는 “기존 2차 치료제인 도세탁셀은 반응률이 10~15%, 질병이 악화되지 않은 기간인 무진행생존기간(PFS) 중앙값이 5~6개월에 불과하지만 엔허투는 반응률이 50%, 반응지속기간이 16개월에 달한다. 또 폐암 특성상 뇌 전이가 흔히 나타나는데 엔허투는 뇌 전이 환자에서도 뇌속 반응률을 측정하는 두개내 반응률(IC-cORR)이 50% 이상이었다”고 전했다.이어 “HER2 양성 유방암에 사용되던 캐싸일라는 비소세포폐암에서 약 50% 이상의 반응률을 보여줬지만 반응지속기간이 짧다는 한계가 있었다. 이러한 상황에서 최근 엔허투가 HER2 변이 전이성 비소세포폐암 환자에서 효과를 보여주며 주목받게 됐다”며 “단일군(single-arm) 대상 임상2상 연구이긴 하지만 기존 약제가 보여왔던 데이터에 비해서는 매우 효과가 좋은 것이기 때문에 급여 적용이 될 필요가 있다고 생각한다”고 덧붙였다.비소세포폐암에서는 흔하지 않은 HER2…"엔허투 활용도 커질 것"HER2 변이 전이성 비소세포폐암의 경우 전체 비소세포폐암 환자의 2~4% 정도로 적다. 이 암은 선암(adenocarcinoma), 비흡연자, 여성, 그리고 일본과 한국을 포함한 동양인 환자가 많다는 특징이 있다. 또 뇌 전이 발생 비율도 높은 편이다.HER2 이상은 ‘유전자 변이(mutations)’, ‘유전자 증폭(amplification)’, ‘단백질 과발현(overexpression)’ 세 가지로 구분된다. 일반적으로 위암이나 유방암 등의 암종에서 HER2 유전자 이상은 대부분 HER2 단백질 과발현의 형태로 나타난다. 그러나 기존 비소세포폐암의 경우 HER2 과발현 유전자 이상이 큰 역할을 하지 않는다고 여겨졌다.기존 HER2 변이 비소세포폐암의 표준치료요법에는 1세대 항암제인 백금기반 항암화학요법이 주로 사용됐다. 최근에는 백금기반 항암화학요법과 면역항암제를 병용요법도 사용된다. 다만 비흡연자는 면역항암제로 효과를 잘 보지 못해 예후가 더 나쁜 것으로 알려져 있다.안 교수는 “그동안 HER2 변이 전이성 비소세포폐암에는 EGFR(Epidermal Growth Factor Receptor) 계열의 변이를 치료하기 위해 개발된 지오트립(아파티닙)과 같은 약물을 사용했지만, HER2 변이에서는 반응률이 약 10% 정도로 낮았다”며 “포지오티닙은 그보다 나은 약 27% 정도의 반응률을 보였지만 독성과 부작용이 심해서 사용하기에 어려움이 있었다”고 전했다.이에 안 교수는 엔허투의 등장으로 비소세포폐암의 치료 환경에 많은 변화가 있을 것으로 예상한다고 전했다.안 교수는 “미국의 경우 HER2 변이 전이성 비소세포폐암 적응증에 대해 미국 식품의약국(FDA) 허가와 급여 적용을 받아 이미 널리 사용되고 있다. 기준이 까다로운 유럽에서도 비소세포폐암 환자는 HER2 변이 검사를 반드시 실시하고 HER2 변이가 나타난 환자들에게는 엔허투를 사용하도록 권고하고 있다”고 말했다.이어 “엔허투로 치료를 받으면 1년 이상 일상생활을 충분히 유지할 수 있는 환자들이 한 달에 최대 800만원 정도가 되는 치료제를 부담하기에 무리가 돼 사용하지 못하는 것을 보면 안타깝다. 때문에 정부가 선별 급여 등 다양한 방안을 강구해 환자가 부담하는 비율을 조금 높여서라도 급여가 적용되면 좋겠다”고 피력했다.2024-07-11 06:18:17손형민 -
 '유사 장기'로 난치성질환 정복…진화하는 오가노이드[데일리팜=손형민 기자] 장기유사체 오가노이드의 활용도가 난치성질환 영역까지 확대되고 있다. 오가노이드는 줄기세포를 3차원적으로 배양하거나 재조합해 만든 장기유사체로, '미니 장기', '유사 장기' 등으로 불린다.오가노이드는 인체 장기의 기능을 나타낼 수 있을 뿐만 아니라 장기에서 발생할 수 있는 다양한 질환의 특성까지 모사할 수 있다. 이를 통해 신약개발 및 질병치료와 인공장기 개발 등의 목적으로 활용이 가능하다.국내 제약바이오업계는 오가노이드를 활용해 난치성 질환으로 여겨지는 항암신약, 뇌질환신약 등에 도전장을 내밀었다.오가노이드 활용도 극대화…임상에서 대거 적용나선다27일 관련 업계에 따르면 그래디언트 바이오컨버전스는 최근 HLB바이오스텝과 암 환자 유래 오가노이드(patient-derived organoid, PDO) 이식 동물 모델 공동 연구 계약을 체결했다. 이번 업무협약으로 양사는 암 환자 유래 오가노이드를 마우스에 이식할 수 있는 생산 라인을 구축한다.폐암, 대장암, 위암 등 다양한 암에 대한 오가노이드 마우스 모델을 제작해 글로벌 전임상 시험 분야에서 입지를 구축하겠다는 게 양사의 목표다.그래디언트 바이오컨버전스는 HLB바이오스텝뿐만 아니라 신테카바이오 등과 협력해 오가노이드 활용 항암신약을 개발 중이다.그래디언트 바이오컨버전스는 오가노이드 뱅크와 자체 개발한 AI 알고리즘을 융합해 신규 항암 타깃을 발굴한다. 최근 이 회사는 미국에서 발굴한 유전자 치료제 디스커버리 결과와 오가노이드 기반의 유전자 치료제 안정성 평가 플랫폼과 유도만능줄기세포(iPCS)를 활용한 희귀 질환 질병 모델링 플랫폼을 소개하기도 했다.유전자 교정 기술을 사용한 유전자 치료제는 표적 DNA 외의 유전자를 편집하는 ‘오프타깃 효과'를 유발해 암 유전자를 활성화시키거나 생식세포까지 편집할 수 있다. 그래디언트 바이오컨버전스가 구축한 700종 이상의 암환자 유래 오가노이드는 정상 오가노이드를 페어로 보유하고 있어 약효 평가는 물론 안정성 평가까지 수행할 수 있는 특징이 있다.이와 함께 그래디언트 바이오컨버전스는 PDO 뱅킹 시스템과 AI 기반의 신약 타깃 발굴 플랫폼에 주력하여 사업 확장에 나서고 있다. 지난 2월에는 미국의 스트랜드 테라퓨틱스(Strand Therapeutics)와 차세대 메신저리보핵산(mRNA) 치료제를 위한 개발을 시작했으며, 닥터노아바이오텍과는 적합한 동물 모델이 없어 연구 개발에 어려움을 겪고 있는 희귀질환 치료제 개발을 위해 협력한다. 같은 달 싸이토젠과도 순환종양세포(CTC) 기반의 오가노이드 제작을 위한 업무협약을 체결한 바 있다.그래디언트 바이오컨버전스는 800여 종의 PDO 뱅킹을 구축하고, 이를 신약개발 및 약효평가 등에 활용한다. 그래디언트 바이오컨버전스가 수립한 각각의 PDO는 차세대염기서열(NGS) 및 약물반응성 등의 특성 정보와 함께 축적되며, 자체 개발한 AI 알고리즘은 다양한 환자의 입체적인 정보를 통합해 혁신 항암 타깃을 발굴한다.뇌질환 영역에서도 오가노이드 활용오가노이드는 항암신약 외에 뇌질환 영역에서도 활용되고 있다.넥스트앤바이오는 지난 2월 뇌질환 신약 개발 기업인 소바젠과 뇌 오가노이드를 활용한 난치성 치료제 개발에 나섰다. 소바젠은 뇌전증 치료제 SVG101 등 다양한 뇌질환을 타깃하는 신약개발 임상을 진행하고 있다.넥스트앤바이오는 소바젠이 개발 중인 뇌질환 치료 약물의 효능을 평가하기 위해 유도만능줄기세포(iPSC)에서 유래한 뇌 오가노이드를 활용할 방침이다. 유도만능줄기세포는 피부세포와 동일한 체세포가 배아줄기세포와 같은 역할을 할 수 있게 한다.이 회사에 따르면 배아줄기세포에서 뇌가 형성되는 과정을 유도만능줄기세포에 재현하는 방식으로 뇌 오가노이드를 배양할 수 있다.오가노이드사이언스는 오가노이드 재생치료제 개발에 뛰어들었다. 오가노이드 기반 재생치료제는 손상 조직 내 생착 및 분화에 의한 직접 조직 재생이 가능하다. 이 치료제는 줄기세포에서 분비되는 성장인자와 사이토카인으로 간접적 재생 효과가 나타나는 1세대 재생치료제 대비 차별성을 가져갈 수 있다.이 회사는 오가노이드 기반 물질평가 플랫폼 ‘ODISEI’를 보유하고 있다. 해당 플랫폼은 암, 뇌질환 및 감염병을 비롯한 대부분의 질병에 대응하는 신약의 효능을 정확하게 평가할 수 있다.이를 통해 오가노이드사이언스는 장, 침샘, 간, 자궁내막 등 장기와 질환별 오가노이드 모델을 기반으로 난치성 질환 치료제를 개발 중이다.오가노이드사이언스는 해당 플랫폼을 통해 재생치료제 후보물질 ‘ATORM’을 도출해 냈다. 장 오가노이드 치료제 ATORM-C는 연내 임상1상 진입을 목표하고 있다. 또 침샘 오가노이드 치료제 ATORM-S, 간 오가노이드 치료제 ATORM-L 등도 개발이 진행되고 있다.2024-06-27 12:08:54손형민
'유사 장기'로 난치성질환 정복…진화하는 오가노이드[데일리팜=손형민 기자] 장기유사체 오가노이드의 활용도가 난치성질환 영역까지 확대되고 있다. 오가노이드는 줄기세포를 3차원적으로 배양하거나 재조합해 만든 장기유사체로, '미니 장기', '유사 장기' 등으로 불린다.오가노이드는 인체 장기의 기능을 나타낼 수 있을 뿐만 아니라 장기에서 발생할 수 있는 다양한 질환의 특성까지 모사할 수 있다. 이를 통해 신약개발 및 질병치료와 인공장기 개발 등의 목적으로 활용이 가능하다.국내 제약바이오업계는 오가노이드를 활용해 난치성 질환으로 여겨지는 항암신약, 뇌질환신약 등에 도전장을 내밀었다.오가노이드 활용도 극대화…임상에서 대거 적용나선다27일 관련 업계에 따르면 그래디언트 바이오컨버전스는 최근 HLB바이오스텝과 암 환자 유래 오가노이드(patient-derived organoid, PDO) 이식 동물 모델 공동 연구 계약을 체결했다. 이번 업무협약으로 양사는 암 환자 유래 오가노이드를 마우스에 이식할 수 있는 생산 라인을 구축한다.폐암, 대장암, 위암 등 다양한 암에 대한 오가노이드 마우스 모델을 제작해 글로벌 전임상 시험 분야에서 입지를 구축하겠다는 게 양사의 목표다.그래디언트 바이오컨버전스는 HLB바이오스텝뿐만 아니라 신테카바이오 등과 협력해 오가노이드 활용 항암신약을 개발 중이다.그래디언트 바이오컨버전스는 오가노이드 뱅크와 자체 개발한 AI 알고리즘을 융합해 신규 항암 타깃을 발굴한다. 최근 이 회사는 미국에서 발굴한 유전자 치료제 디스커버리 결과와 오가노이드 기반의 유전자 치료제 안정성 평가 플랫폼과 유도만능줄기세포(iPCS)를 활용한 희귀 질환 질병 모델링 플랫폼을 소개하기도 했다.유전자 교정 기술을 사용한 유전자 치료제는 표적 DNA 외의 유전자를 편집하는 ‘오프타깃 효과'를 유발해 암 유전자를 활성화시키거나 생식세포까지 편집할 수 있다. 그래디언트 바이오컨버전스가 구축한 700종 이상의 암환자 유래 오가노이드는 정상 오가노이드를 페어로 보유하고 있어 약효 평가는 물론 안정성 평가까지 수행할 수 있는 특징이 있다.이와 함께 그래디언트 바이오컨버전스는 PDO 뱅킹 시스템과 AI 기반의 신약 타깃 발굴 플랫폼에 주력하여 사업 확장에 나서고 있다. 지난 2월에는 미국의 스트랜드 테라퓨틱스(Strand Therapeutics)와 차세대 메신저리보핵산(mRNA) 치료제를 위한 개발을 시작했으며, 닥터노아바이오텍과는 적합한 동물 모델이 없어 연구 개발에 어려움을 겪고 있는 희귀질환 치료제 개발을 위해 협력한다. 같은 달 싸이토젠과도 순환종양세포(CTC) 기반의 오가노이드 제작을 위한 업무협약을 체결한 바 있다.그래디언트 바이오컨버전스는 800여 종의 PDO 뱅킹을 구축하고, 이를 신약개발 및 약효평가 등에 활용한다. 그래디언트 바이오컨버전스가 수립한 각각의 PDO는 차세대염기서열(NGS) 및 약물반응성 등의 특성 정보와 함께 축적되며, 자체 개발한 AI 알고리즘은 다양한 환자의 입체적인 정보를 통합해 혁신 항암 타깃을 발굴한다.뇌질환 영역에서도 오가노이드 활용오가노이드는 항암신약 외에 뇌질환 영역에서도 활용되고 있다.넥스트앤바이오는 지난 2월 뇌질환 신약 개발 기업인 소바젠과 뇌 오가노이드를 활용한 난치성 치료제 개발에 나섰다. 소바젠은 뇌전증 치료제 SVG101 등 다양한 뇌질환을 타깃하는 신약개발 임상을 진행하고 있다.넥스트앤바이오는 소바젠이 개발 중인 뇌질환 치료 약물의 효능을 평가하기 위해 유도만능줄기세포(iPSC)에서 유래한 뇌 오가노이드를 활용할 방침이다. 유도만능줄기세포는 피부세포와 동일한 체세포가 배아줄기세포와 같은 역할을 할 수 있게 한다.이 회사에 따르면 배아줄기세포에서 뇌가 형성되는 과정을 유도만능줄기세포에 재현하는 방식으로 뇌 오가노이드를 배양할 수 있다.오가노이드사이언스는 오가노이드 재생치료제 개발에 뛰어들었다. 오가노이드 기반 재생치료제는 손상 조직 내 생착 및 분화에 의한 직접 조직 재생이 가능하다. 이 치료제는 줄기세포에서 분비되는 성장인자와 사이토카인으로 간접적 재생 효과가 나타나는 1세대 재생치료제 대비 차별성을 가져갈 수 있다.이 회사는 오가노이드 기반 물질평가 플랫폼 ‘ODISEI’를 보유하고 있다. 해당 플랫폼은 암, 뇌질환 및 감염병을 비롯한 대부분의 질병에 대응하는 신약의 효능을 정확하게 평가할 수 있다.이를 통해 오가노이드사이언스는 장, 침샘, 간, 자궁내막 등 장기와 질환별 오가노이드 모델을 기반으로 난치성 질환 치료제를 개발 중이다.오가노이드사이언스는 해당 플랫폼을 통해 재생치료제 후보물질 ‘ATORM’을 도출해 냈다. 장 오가노이드 치료제 ATORM-C는 연내 임상1상 진입을 목표하고 있다. 또 침샘 오가노이드 치료제 ATORM-S, 간 오가노이드 치료제 ATORM-L 등도 개발이 진행되고 있다.2024-06-27 12:08:54손형민 -
 'mRNA·ADC' 등 신기술 풍성…주목받는 '문정 바이오'조용준 문정바이오CEO포럼 회장. [데일리팜=손형민 기자] 메신저리보핵산(mRNA), 항체약물접합체(ADC), 이중항체 등 문정 소재 제약바이오기업들의 유망 파이프라인을 소개하는 자리가 마련됐다.17일 서울시 송파구 문정동에 위치한 한스바이오메드에서 올해 첫 문정바이오 CEO 포럼이 개최됐다. 문정바이오 CEO 포럼은 지난해 9월 문정동 입주 바이오벤처 CEO들이 정기적으로 모여 정보교류, 협업, 투자 유치 등을 모색하기 위해 발족했다.이번 포럼에는 회장을 맡고 있는 조용준 동구바이오제약 대표와 1대 회장인 이병건 지아이이노베이션 회장을 비롯해 관련 업계 관계자 60여 명이 참석했다.mRNA·AI·ADC 등 신기술 파이프라인 소개…투자 유치전 활발알엔에이진, 메디사피엔스, 에임드바이오, 일리미스, 에이피트바이오, 등 여러 바이오기업들의 CEO들은 이번 포럼에서 각기 보유한 유망 파이프라인을 소개했다.알엔에이진은 mRNA 기술 관련 신약 플랫폼을 공개했다. 이 회사는 2018년부터 국내 기업 최초로 mRNA 플랫폼을 구축하고 관련 백신을 개발 중이다.특히 알엔에이진은 mRNA 플랫폼을 통해 세포치료제, 반려동물용 바이러스 백신 독감, 암백신 등으로 사업영역을 확대해 나가고 있다.메디사피엔스는 희귀질환 변이를 분석하는 인공지능(AI) 솔루션을 소개했다. 메디사피엔스는 신생아 희귀질환 250여종을 판별하는 진단키트 ‘네오seq_액션’을 개발했다.NGS 데이터를 통해 분석된 데이터는 메디사피엔스가 개발한 유전변이 분석 소프트웨어 메디CVi로 분석한다. 이를 통해 희귀질환을 조기에 진단할 수 있다. 메디사피엔스는 서울대병원 등 희귀질환 연구센터에 연구용으로 소프트웨어 서비스를 제공할 예정이다.권태혁 메디사피엔스 상무는 “서울대병원 진단검사의학과와 공동 프로젝트를 진행 중이다. 프로젝트가 잘 완료되면 해외 진출도 순조로울 것이라고 생각한다”고 전했다. 에임드바이오는 글로벌제약 핫 트렌드로 급부상한 ADC 파이프라인에 대해 소개하는 시간을 가졌다. ADC는 엔허투, 트로델비, 파드셉 등 상용화된 파이프라인이 임상에서 큰 효과를 발휘하며 주목되고 있다.에임드바이오는 방광암에서 주로 발현되는 바이오머커인 FGFR3를 타깃하는 ADC 후보물질 ABM302를 보유하고 있다. ABM302는 중국 진퀸텀 헬스케어와 공동개발하고 있으며 에임드바이오가 개발한 FGFR3 항체에 진?텀의 링커-페이로드 기술이 접목됐다.에임드바이오의 ADC 기술은 항체와 페이로드의 비율(DAR)을 조절할 수 있는 것이 특징이다. FGFR3은 고형암 치료를 위한 주요 단백질이지만 해당 기전 ADC로 개발된 의약품은 아직까지 없다. 에임드바이오의 기술력을 알아본 삼성그룹은 지난해 9월 투자를 진행하기도 했다.알츠하이머 신약·이중항체 개발 위한 플랫폼 소개도알츠하이머 신약과 이중항체 플랫폼에 대한 내용도 공개됐다.일리미스테라퓨틱스는 이중융합단백질을 통해 알츠하이머 신약 상용화 가능성을 확인하고 있다. 이 회사는 현재 가이아(GAIA) 플랫폼을 구축해 아밀로이드베타 기전을 타깃하는 알츠하이머 신약을 개발 중이다. 현재까지 상용화된 알츠하미머 신약은 아밀로이드베타 기전을 타깃하고 있다.이 회사가 개발 중인 신약후보물질 ILM01은 뇌염증을 유발하지 않아 기존 항체의약품에서 발견되는 ARIA 및 뇌수축의 부작용을 해결할 수 있다는 강점이 있다.박상훈 일리미스테라퓨틱스 대표. 박상훈 일리미스 대표는 “가이아 플랫폼은 FC수용체가 아닌 TAM 수용체를 이용해 질병원의 원인물질을 염증없이 제거할 수 있다. 알츠하미어 뿐만 아니라 염증 조절이 필수적인 난치성 질환 치료제 개발로 사업 영역을 확장하고 있다”고 전했다.에이피트바이오는 난치성 고형암 항체를 개발하고 있다. 에이피트바이오가 개발하고 있는 단일클론항체는 APB-A001, APB-A101, APB-A002 등이다. 그중 APB-A001은 국내 임상1상에 진입했다.APB-A001은 췌장암, 담도암, 난소암 등 난치성 고형암에서 주로 발현되는 단백질인 CD171(L1CAM)을 타깃으로 하는 완전 인간 단클론항체 치료제다.윤선주 에이피트바이오 대표는 “단일클론항체뿐만 아니라 이중항체, ADC 후보물질도 개발하고 있다”며 “국내 파트너사와 협업해 상용화 가능성을 확인해 볼 것”이라고 전했다.조용준 포럼회장은 “분기별로 관심있는 분야에 맞게 기술 피칭을 진행할 예정이다. 포럼을 통해 문정 소재 제약기업들과 바이오기업들의 협업기회를 찾겠다. 회원사들의 많은 관심을 부탁한다”고 전했다.2024-04-18 06:18:46손형민
'mRNA·ADC' 등 신기술 풍성…주목받는 '문정 바이오'조용준 문정바이오CEO포럼 회장. [데일리팜=손형민 기자] 메신저리보핵산(mRNA), 항체약물접합체(ADC), 이중항체 등 문정 소재 제약바이오기업들의 유망 파이프라인을 소개하는 자리가 마련됐다.17일 서울시 송파구 문정동에 위치한 한스바이오메드에서 올해 첫 문정바이오 CEO 포럼이 개최됐다. 문정바이오 CEO 포럼은 지난해 9월 문정동 입주 바이오벤처 CEO들이 정기적으로 모여 정보교류, 협업, 투자 유치 등을 모색하기 위해 발족했다.이번 포럼에는 회장을 맡고 있는 조용준 동구바이오제약 대표와 1대 회장인 이병건 지아이이노베이션 회장을 비롯해 관련 업계 관계자 60여 명이 참석했다.mRNA·AI·ADC 등 신기술 파이프라인 소개…투자 유치전 활발알엔에이진, 메디사피엔스, 에임드바이오, 일리미스, 에이피트바이오, 등 여러 바이오기업들의 CEO들은 이번 포럼에서 각기 보유한 유망 파이프라인을 소개했다.알엔에이진은 mRNA 기술 관련 신약 플랫폼을 공개했다. 이 회사는 2018년부터 국내 기업 최초로 mRNA 플랫폼을 구축하고 관련 백신을 개발 중이다.특히 알엔에이진은 mRNA 플랫폼을 통해 세포치료제, 반려동물용 바이러스 백신 독감, 암백신 등으로 사업영역을 확대해 나가고 있다.메디사피엔스는 희귀질환 변이를 분석하는 인공지능(AI) 솔루션을 소개했다. 메디사피엔스는 신생아 희귀질환 250여종을 판별하는 진단키트 ‘네오seq_액션’을 개발했다.NGS 데이터를 통해 분석된 데이터는 메디사피엔스가 개발한 유전변이 분석 소프트웨어 메디CVi로 분석한다. 이를 통해 희귀질환을 조기에 진단할 수 있다. 메디사피엔스는 서울대병원 등 희귀질환 연구센터에 연구용으로 소프트웨어 서비스를 제공할 예정이다.권태혁 메디사피엔스 상무는 “서울대병원 진단검사의학과와 공동 프로젝트를 진행 중이다. 프로젝트가 잘 완료되면 해외 진출도 순조로울 것이라고 생각한다”고 전했다. 에임드바이오는 글로벌제약 핫 트렌드로 급부상한 ADC 파이프라인에 대해 소개하는 시간을 가졌다. ADC는 엔허투, 트로델비, 파드셉 등 상용화된 파이프라인이 임상에서 큰 효과를 발휘하며 주목되고 있다.에임드바이오는 방광암에서 주로 발현되는 바이오머커인 FGFR3를 타깃하는 ADC 후보물질 ABM302를 보유하고 있다. ABM302는 중국 진퀸텀 헬스케어와 공동개발하고 있으며 에임드바이오가 개발한 FGFR3 항체에 진?텀의 링커-페이로드 기술이 접목됐다.에임드바이오의 ADC 기술은 항체와 페이로드의 비율(DAR)을 조절할 수 있는 것이 특징이다. FGFR3은 고형암 치료를 위한 주요 단백질이지만 해당 기전 ADC로 개발된 의약품은 아직까지 없다. 에임드바이오의 기술력을 알아본 삼성그룹은 지난해 9월 투자를 진행하기도 했다.알츠하이머 신약·이중항체 개발 위한 플랫폼 소개도알츠하이머 신약과 이중항체 플랫폼에 대한 내용도 공개됐다.일리미스테라퓨틱스는 이중융합단백질을 통해 알츠하이머 신약 상용화 가능성을 확인하고 있다. 이 회사는 현재 가이아(GAIA) 플랫폼을 구축해 아밀로이드베타 기전을 타깃하는 알츠하이머 신약을 개발 중이다. 현재까지 상용화된 알츠하미머 신약은 아밀로이드베타 기전을 타깃하고 있다.이 회사가 개발 중인 신약후보물질 ILM01은 뇌염증을 유발하지 않아 기존 항체의약품에서 발견되는 ARIA 및 뇌수축의 부작용을 해결할 수 있다는 강점이 있다.박상훈 일리미스테라퓨틱스 대표. 박상훈 일리미스 대표는 “가이아 플랫폼은 FC수용체가 아닌 TAM 수용체를 이용해 질병원의 원인물질을 염증없이 제거할 수 있다. 알츠하미어 뿐만 아니라 염증 조절이 필수적인 난치성 질환 치료제 개발로 사업 영역을 확장하고 있다”고 전했다.에이피트바이오는 난치성 고형암 항체를 개발하고 있다. 에이피트바이오가 개발하고 있는 단일클론항체는 APB-A001, APB-A101, APB-A002 등이다. 그중 APB-A001은 국내 임상1상에 진입했다.APB-A001은 췌장암, 담도암, 난소암 등 난치성 고형암에서 주로 발현되는 단백질인 CD171(L1CAM)을 타깃으로 하는 완전 인간 단클론항체 치료제다.윤선주 에이피트바이오 대표는 “단일클론항체뿐만 아니라 이중항체, ADC 후보물질도 개발하고 있다”며 “국내 파트너사와 협업해 상용화 가능성을 확인해 볼 것”이라고 전했다.조용준 포럼회장은 “분기별로 관심있는 분야에 맞게 기술 피칭을 진행할 예정이다. 포럼을 통해 문정 소재 제약기업들과 바이오기업들의 협업기회를 찾겠다. 회원사들의 많은 관심을 부탁한다”고 전했다.2024-04-18 06:18:46손형민
오늘의 TOP 10
- 1급여 생존의 대가...애엽 위염약 약가인하 손실 연 150억
- 2개설허가 7개월 만에 제1호 창고형약국 개설자 변경
- 3약국서 카드 15만원+현금 5만원 결제, 현금영수증은?
- 4부광, 유니온제약 인수…공장은 얻었지만 부채는 부담
- 51호 창고형약국 불법 전용 논란 일단락…위반건축물 해제
- 6P-CAB 3종 경쟁력 제고 박차…자큐보, 구강붕해정 탑재
- 7발사르탄 원료 사기 사건 2심으로...민사소송 확전될까
- 8GC녹십자 코로나19 mRNA 백신, 임상1상 승인
- 9의협, 대통령 의료정책 인식 '엄지척'...저수가 해결 기대감
- 10파마리서치, 약국 기반 ‘리쥬비-에스 앰플’ 출시
-
상품명최고최저평균
-
케토톱플라스타(34매)13,00013,00013,000
-
게보린(10정)4,0003,0003,620
-
노스카나겔(20g)22,00018,00020,703
-
베나치오에프액(75ml)1,0008001,000
-
비코그린에스(20정)5,0004,0004,417













![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
