총 48건
-
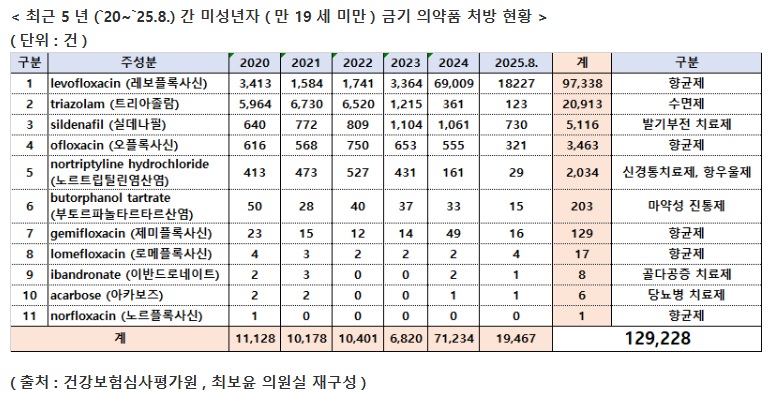 비아그라 등 미성년 금기약 처방, 5년간 13만건 육박[데일리팜=이정환 기자] 최근 5년간 미성년자에게 투여가 금지된 의약품의 처방 건수가 13만건에 육박한 것으로 집계됐다.소아·청소년에게 사용이 제한된 약물이 의료현장에서 반복 처방된 셈이다. 의약품 안전관리 체계가 제대로 작동하지 않았다는 지적이 나온다.13일 최보윤 국민의힘 의원이 건강보험심사평가원으로부터 제출받은 약품 처방 현황 자료를 분석한 결과 지난 2020 년부터 올해 8월까지 미성년자에게 투여 금지된 약물의 처방 건수는 총 12만9228건에 달했다.2020년 1만1128건에 불과했던 금기 약물 처방은 지난해 7만1234건으로 6배 이상 증가 했다. 올해 1월~8월 집계분만 따져도 이미 1만9467건이 추가됐다 . 현재 만 19세 미만 금기 의약품은 총 22종이다. 이 가운데 11종이 실제 의료기관에서 의사 처방으로 청구된 것으로 확인됐다.가장 많이 처방된 의약품은 항균제 레보플록사신으로 9만7338건을 차지했다. 이어 수면제 트리아졸람 2만913건, 발기부전 치료제 실데나필 5116건이 뒤를 이었다이 밖에도 마약성 진통제 부토르파놀 203건, 항우울제 노르트립틸린 2034건, 골다공증 치료제 이반드로네이트 8 건 등도 포함됐다.특히 레보플록사신은 2023년 12월 보건복지부 고시를 통해 '마이코플라즈마 폐렴 등 기존 항생제로 증상이 개선되지 않는 소아'에 한해 급여가 예외적으로 인정되면서 처방이 급증했다.그러나 약물 자체는 여전히 식품의약품안전처가 지정한 연령금기 의약품이다. 예외적 급여가 인정된 의약품이 변동없이 연령금기 약으로 지정되면서 혼란이 유발될 수 있다는 지적이다.트리아졸람은 다른 수면제인 졸피뎀보다 의존성과 인지장애 위험이 높아 18 세 미만 사용이 금지된다. 비아그라 주성분인 실데나필 역시 심혈관계 부작용 위험으로 소아 투여가 불가하다.식약처와 한국의약품안전관리원은 약품의 안전하고 적정한 사용을 위해 병용금기·임부금기·특정 연령대 금기 의약품을 지정·관리하고 있다.이 가운데 '특정 연령대 금기' 의약품은 일부 연령층, 특히 소아·청소년에서 심각한 부작용을 유발하거나 안전성이 확보되지 않아 처방 또는 조제해서는 안 되는 약물로 분류된다.이들 약제는 의약품 적정사용(Drug Utilization Review, DUR)시스템을 통해 사전에 처방이 차단되거나 경고가 표시되도록 관리된다.최보윤 의원은 "의사의 처방권은 최대한 존중돼야 하지만, 그와 별개로 행정당국의 안전관리 시스템이 제 역할을 하지 못한 것은 분명한 문제"라며 "식약처는 DUR시스템을 통해 금기 처방을 사전에 차단·경고하는 기능을 강화하고, 심평원은 '처방해서는 안 되는 약품'의 급여 기준을 다시 정비해야 한다"고 말했다.2025-10-13 18:56:34이정환
비아그라 등 미성년 금기약 처방, 5년간 13만건 육박[데일리팜=이정환 기자] 최근 5년간 미성년자에게 투여가 금지된 의약품의 처방 건수가 13만건에 육박한 것으로 집계됐다.소아·청소년에게 사용이 제한된 약물이 의료현장에서 반복 처방된 셈이다. 의약품 안전관리 체계가 제대로 작동하지 않았다는 지적이 나온다.13일 최보윤 국민의힘 의원이 건강보험심사평가원으로부터 제출받은 약품 처방 현황 자료를 분석한 결과 지난 2020 년부터 올해 8월까지 미성년자에게 투여 금지된 약물의 처방 건수는 총 12만9228건에 달했다.2020년 1만1128건에 불과했던 금기 약물 처방은 지난해 7만1234건으로 6배 이상 증가 했다. 올해 1월~8월 집계분만 따져도 이미 1만9467건이 추가됐다 . 현재 만 19세 미만 금기 의약품은 총 22종이다. 이 가운데 11종이 실제 의료기관에서 의사 처방으로 청구된 것으로 확인됐다.가장 많이 처방된 의약품은 항균제 레보플록사신으로 9만7338건을 차지했다. 이어 수면제 트리아졸람 2만913건, 발기부전 치료제 실데나필 5116건이 뒤를 이었다이 밖에도 마약성 진통제 부토르파놀 203건, 항우울제 노르트립틸린 2034건, 골다공증 치료제 이반드로네이트 8 건 등도 포함됐다.특히 레보플록사신은 2023년 12월 보건복지부 고시를 통해 '마이코플라즈마 폐렴 등 기존 항생제로 증상이 개선되지 않는 소아'에 한해 급여가 예외적으로 인정되면서 처방이 급증했다.그러나 약물 자체는 여전히 식품의약품안전처가 지정한 연령금기 의약품이다. 예외적 급여가 인정된 의약품이 변동없이 연령금기 약으로 지정되면서 혼란이 유발될 수 있다는 지적이다.트리아졸람은 다른 수면제인 졸피뎀보다 의존성과 인지장애 위험이 높아 18 세 미만 사용이 금지된다. 비아그라 주성분인 실데나필 역시 심혈관계 부작용 위험으로 소아 투여가 불가하다.식약처와 한국의약품안전관리원은 약품의 안전하고 적정한 사용을 위해 병용금기·임부금기·특정 연령대 금기 의약품을 지정·관리하고 있다.이 가운데 '특정 연령대 금기' 의약품은 일부 연령층, 특히 소아·청소년에서 심각한 부작용을 유발하거나 안전성이 확보되지 않아 처방 또는 조제해서는 안 되는 약물로 분류된다.이들 약제는 의약품 적정사용(Drug Utilization Review, DUR)시스템을 통해 사전에 처방이 차단되거나 경고가 표시되도록 관리된다.최보윤 의원은 "의사의 처방권은 최대한 존중돼야 하지만, 그와 별개로 행정당국의 안전관리 시스템이 제 역할을 하지 못한 것은 분명한 문제"라며 "식약처는 DUR시스템을 통해 금기 처방을 사전에 차단·경고하는 기능을 강화하고, 심평원은 '처방해서는 안 되는 약품'의 급여 기준을 다시 정비해야 한다"고 말했다.2025-10-13 18:56:34이정환 -
 삼일제약, CNS 라인업 강화…500억 사업부 탄생 초읽기삼일제약 본사.[데일리팜=이석준 기자] 삼일제약이 CNS 라인업을 강화하고 있다. 파킨슨병치료제 허가를 받고 연간 100억원 시장에 도전장을 내민다.삼일제약 CNS 사업은 2021년 67억원 수준에서 지난해 365억원 정도로 커진 상태다. 조만간 연 500억원 돌파가 점쳐진다. 지난해 회사 매출(연결 기준)이 2200억원 정도인 점을 감안하면 CNS 사업이 삼일제약의 또 다른 중심축이 되는 모양새다.식약처에 따르면 삼일제약 파킨슨병치료제 '원도파정'이 24일 허가를 받았다. 벤세라지드와 레보도파 복합제로 오리지널 '마도파정'와 명인제약 '명도파정'과 동일 계열의 약물이다.관련 시장은 오리지널 마도파정이 국내 시장에서 철수하면서 명도파정이 그 자리를 대체하고 있다. 국내 급여 수준과 파킨슨병 환자수와 처방량을 감안하면 연간 시장 규모는 약 80억~100억원대로 추산된다.삼일제약은 후발주자로 유통 전략, 가격 경쟁력 등을 내세워 시장을 공략할 것으로 판단된다.2021년 67억→2024년 365억→2026년 500억?삼일제약은 주력 안과 사업 외에도 CNS 사업을 미래 성장 동력으로 육성하고 있다.수년간 국내외 제약사로부터 CNS 계열 품목(항우울제, 항정신병, 수면제류 등)을 도입하거나 유통권을 확보해 단기간에 제품 포트폴리오를 확장했다.실제 삼일제약은 비아트리스와 공동 판매 중인 CNS 품목(항우울제 졸로푸트, 항불안제 자낙스, 항조현병제 젤독스 등)에 산도스 CNS 라인까지 도입하면서 해당 분야 신흥 강자로 떠오르고 있다.산도스 품목은 항우울제 미트락스, 산도스에스시탈로프람, 산도스파록세틴, 산도스설트랄린, 조현변치료제 산도스올라자핀, 불면증 치료제 산도스졸피뎀, 전신마취 회복제 산도스슈가마덱스 등이다.삼일제약은 영업본부 중 한 곳을 CNS로 두며 주력 사업으로 육성시키고 있다. 2021년 하반기에는 CNS 사업부를 출범하며 처방·유통을 확대했다. 실제 사업보고서를 보면 CNS는 ETC, 안과와 함께 세 개의 영업본부 중 하나로 포함돼 있다. 회사에서 또 다른 주력 사업으로 밀고 있다는 방증이다.성과도 내고 있다. CNS 매출은 2021년 67억→2024년 365억으로 수직상승했다. 조만간 연 500억원을 넘어설 수 있다는 전망이 나온다. 이 경우 지난해 매출액(2197억원)을 감안하면 약 4분의 1에 해당되는 수치다.업계는 삼일제약의 CNS 사업이 궤도에 올랐다는 평가를 내놓는다. 라인업 확보, 영업력, 시장 트렌드 등에서 3박자를 내고 있어서다.시장 관계자는 "삼일제약은 라인업 확대, 유통망 강점, 빠른 성장 속도로 CNS 시장에서 기존 강자를 위협하고 있다. 단기간에 많은 제품을 확보하고 전담 영업 조직 및 마케팅 역량 투자를 통해 시장 침투율을 높이고 있다"고 진단했다.2025-09-25 06:12:43이석준
삼일제약, CNS 라인업 강화…500억 사업부 탄생 초읽기삼일제약 본사.[데일리팜=이석준 기자] 삼일제약이 CNS 라인업을 강화하고 있다. 파킨슨병치료제 허가를 받고 연간 100억원 시장에 도전장을 내민다.삼일제약 CNS 사업은 2021년 67억원 수준에서 지난해 365억원 정도로 커진 상태다. 조만간 연 500억원 돌파가 점쳐진다. 지난해 회사 매출(연결 기준)이 2200억원 정도인 점을 감안하면 CNS 사업이 삼일제약의 또 다른 중심축이 되는 모양새다.식약처에 따르면 삼일제약 파킨슨병치료제 '원도파정'이 24일 허가를 받았다. 벤세라지드와 레보도파 복합제로 오리지널 '마도파정'와 명인제약 '명도파정'과 동일 계열의 약물이다.관련 시장은 오리지널 마도파정이 국내 시장에서 철수하면서 명도파정이 그 자리를 대체하고 있다. 국내 급여 수준과 파킨슨병 환자수와 처방량을 감안하면 연간 시장 규모는 약 80억~100억원대로 추산된다.삼일제약은 후발주자로 유통 전략, 가격 경쟁력 등을 내세워 시장을 공략할 것으로 판단된다.2021년 67억→2024년 365억→2026년 500억?삼일제약은 주력 안과 사업 외에도 CNS 사업을 미래 성장 동력으로 육성하고 있다.수년간 국내외 제약사로부터 CNS 계열 품목(항우울제, 항정신병, 수면제류 등)을 도입하거나 유통권을 확보해 단기간에 제품 포트폴리오를 확장했다.실제 삼일제약은 비아트리스와 공동 판매 중인 CNS 품목(항우울제 졸로푸트, 항불안제 자낙스, 항조현병제 젤독스 등)에 산도스 CNS 라인까지 도입하면서 해당 분야 신흥 강자로 떠오르고 있다.산도스 품목은 항우울제 미트락스, 산도스에스시탈로프람, 산도스파록세틴, 산도스설트랄린, 조현변치료제 산도스올라자핀, 불면증 치료제 산도스졸피뎀, 전신마취 회복제 산도스슈가마덱스 등이다.삼일제약은 영업본부 중 한 곳을 CNS로 두며 주력 사업으로 육성시키고 있다. 2021년 하반기에는 CNS 사업부를 출범하며 처방·유통을 확대했다. 실제 사업보고서를 보면 CNS는 ETC, 안과와 함께 세 개의 영업본부 중 하나로 포함돼 있다. 회사에서 또 다른 주력 사업으로 밀고 있다는 방증이다.성과도 내고 있다. CNS 매출은 2021년 67억→2024년 365억으로 수직상승했다. 조만간 연 500억원을 넘어설 수 있다는 전망이 나온다. 이 경우 지난해 매출액(2197억원)을 감안하면 약 4분의 1에 해당되는 수치다.업계는 삼일제약의 CNS 사업이 궤도에 올랐다는 평가를 내놓는다. 라인업 확보, 영업력, 시장 트렌드 등에서 3박자를 내고 있어서다.시장 관계자는 "삼일제약은 라인업 확대, 유통망 강점, 빠른 성장 속도로 CNS 시장에서 기존 강자를 위협하고 있다. 단기간에 많은 제품을 확보하고 전담 영업 조직 및 마케팅 역량 투자를 통해 시장 침투율을 높이고 있다"고 진단했다.2025-09-25 06:12:43이석준 -
 첫 RNA 기반 ATTR-CM 치료제 '암부트라'④최초의 RNAi 기반 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 치료제, ‘암부트라(Vutrisiran)’암부트라(Amvuttra®, 성분명: 부트리시란 Vutrisiran, Alnylam Pharmaceuticals)는 소간섭 RNA(small interfering RNA, siRNA) 치료제로, 2022년 6월 미국 FDA에서 유전성 트랜스티레틴 매개 아밀로이드 다발신경병증(hATTR-PN) 치료제로 최초 승인되었다. 이어 2025년 3월에는 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 환자의 심혈관 사망, 입원 및 응급실 방문을 감소시키는 최초의 RNAi 치료제로 추가 승인을 받았다.Alnylam Pharmaceuticals는 siRNA 기술을 기반으로 간세포 내 TTR 합성을 직접 억제하는 신약 개발을 선도해 왔으며, 2018년 파티시란(Patisiran, Onpattro®)이 hATTR-PN 치료제로 최초 승인되었다. 이후 이를 개량한 2세대 제형인 부트리시란(Amvuttra®)이 개발되어 hATTR-PN과 ATTR-CM 모두에 사용 가능하게 되었다.트랜스티레틴 매개 아밀로이드증(ATTR amyloidosis)은 간에서 합성되는 단백질인 트랜스티레틴(TTR)의 구조적 불안정성에 의해 발생한다. 불안정한 TTR 사량체(tetramer)는 쉽게 해리되어 아밀로이드 형성 성향(amyloidogenic)을 띠는 잘못 접힌 단량체(misfolded monomer)로 전환된다. 이 단량체들이 서로 응집해 β-sheet 구조를 형성하면서 아밀로이드 섬유(amyloid fibril)로 축적되고, 신경·심장·소화관 등 다양한 장기에 침착되어 임상 증상을 유발한다.유전성 ATTR 다발신경병증(hATTR-PN)은 TTR 유전자 변이에 의해 발생하며, 주로 말초 및 자율신경에 침착해 신경병증을 유발한다.ATTR 심근병증(ATTR-CM)은 유전성(hATTR-CM) 또는 노화와 관련된 야생형(wild-type ATTR-CM)으로 발생할 수 있으며, 주 침착 부위는 심근이다.부트리시란은 RNAi 치료제로, 3개월 간격으로 1회 피하주사한다. 특정 mRNA를 표적·침묵시켜 야생형과 변이형 모두의 TTR 생성을 차단한다.HELIOS-A 시험은 hATTR-PN 환자를 대상으로 한 무작위 배정, 공개라벨, 다국가 3상 임상으로 진행되었다. 환자들은 3개월마다 피하로 부트리시란을 투여받거나 대조군으로 파티시란 정맥주사를 투여받았다.주요 유효성 평가는 mNIS+7 점수, Norfolk QoL-DN 설문, 보행 검사 등이었으며, 외부 위약군(APOLLO 연구 placebo arm)과의 비교를 통해 신뢰성을 보강하였다. 그 결과, 부트리시란 투여군은 신경학적 기능 악화를 유의하게 억제했으며 삶의 질과 신체 기능이 향상되는 양상을 보였다. 안전성 측면에서도 대부분의 이상반응은 경미하거나 중등도 수준에 그쳐 장기 투여의 내약성이 입증되었다.HELIOS-B 시험은 hATTR-CM뿐 아니라 야생형 ATTR-CM 환자를 포함한 심근병증 환자군을 대상으로 수행된 무작위 배정, 이중맹검, 위약 대조 3상 임상시험이다. ATTR-CM 환자에서 부트리시란의 심혈관 사망 및 입원 위험 감소 효과를 평가하는 데 중점을 두었으며, 1차 종료점으로 심혈관 사망률과 심부전 입원율이 설정되었다.연구 결과, 부트리시란은 ATTR-CM 환자에서 주요 심혈관 사건의 발생을 줄이는 경향을 보였고, 타파미디스(Tafamidis) 치료 경험 여부와 무관하게 일관된 효과를 나타냈다.트랜스티레틴(Transthyretin, TTR)은 무엇인가? 트랜스티레틴(Transthyretin)은 그 명칭이 transport + thyroxin + retinol에서 유래하였으며, 혈액과 뇌척수액에서 갑상선 호르몬과 비타민 A를 운반하는 필수 단백질이다.분자량 약 55kDa의 사량체(tetramer) 구조를 가진 TTR은 주로 간세포에서 합성되어 혈장으로 분비되며, 전체의 90% 이상이 간에서 생산된다. 혈중 TTR은 전체 단백질의 약 0.1–0.3%를 차지하며, 갑상선 호르몬 및 비타민 A 운반뿐 아니라 단백-에너지 영양 상태를 반영하는 민감한 지표로 활용된다.간 외에도 뇌의 맥락얼기(choroid plexus) 상피세포와 망막색소상피(retinal pigment epithelium, RPE)에서 국소적으로 합성된다. 맥락얼기에서 생성된 TTR은 뇌척수액 내에 풍부하게 존재하며, thyroxine(T4)의 주요 운반체로 기능한다. 혈액-뇌 장벽을 통한 갑상선 호르몬의 직접적 이동이 제한적이라는 점을 고려할 때, TTR은 중추신경계 발달과 대사 항상성 유지에 핵심적 역할을 한다.망막에서 합성된 TTR은 retinol-binding protein(RBP)과 결합하여 레티놀을 안정적으로 운반하고, RBP의 신장 여과를 방지함으로써 시각 회로 유지와 비타민 A 항상성 조절에 기여한다. TTR의 주요 기능은 세 가지로 요약된다. 첫째, 갑상선 호르몬 운반으로 혈중 thyroxine 운반의 약 15%를 담당하며, 알부민과 티록신 결합 글로불린(TBG)과 보완적으로 작용한다. 특히 뇌척수액에서는 TTR이 유일한 주요 운반 단백질이다. 둘째, 비타민 A 대사 및 운반으로 RBP와의 결합을 통해 레티놀을 안정화시키고 체내 항상성을 유지한다. 셋째, 대사적 지표 기능으로 혈중 농도가 영양 상태 및 단백질 합성 능력을 반영하여 임상적으로 영양평가의 바이오마커로 활용된다.한편, TTR은 구조적 불안정성으로 인해 단량체(monomer)로 분리되면 잘못 접힘(misfolding)이 발생하고, 이는 β-sheet 기반의 아밀로이드 섬유를 형성하여 조직에 침착할 수 있다. 이러한 병리적 변화가 트랜스티레틴 아밀로이드증(ATTR amyloidosis)의 기전이며, 연령 증가에 따른 야생형(wild-type) TTR의 불안정성은 심근병증(ATTR-CM)과 연관되고, 특정 유전자 변이에 의한 변이형 TTR은 다발신경병증(ATTR-PN)의 주요 원인으로 작용한다.트랜스티레틴 매개 아밀로이드증(Transthyretin-mediated amyloidosis, ATTR 아밀로이드증)이란 어떤 질환인가? ATTR 아밀로이드증은 트랜스티레틴(TTR)의 구조적 불안정성으로 인해 발생하는 전신성 단백질 침착 질환이다.TTR은 간에서 주로 합성되는 사량체 운반 단백질로, 정상 상태에서는 갑상선 호르몬과 비타민 A를 안정적으로 운반한다. 그러나 유전적 변이나 노화로 인해 단백질의 안정성이 저하되면 사량체(tetramer)가 단량체(monomer)로 해리되고, 이 단량체가 잘못 접힘(misfolding)을 거쳐 β-sheet 구조의 불용성 아밀로이드 섬유(amyloid fibril)로 전환된다. 축적된 아밀로이드 섬유는 다양한 장기에 침착하여 구조적 손상과 기능 저하를 유발한다.ATTR 아밀로이드증은 원인에 따라 변이형(hereditary ATTR, ATTRv)과 야생형(wild-type ATTR, ATTRwt)으로 구분된다. 변이형 ATTR은 TTR 유전자 변이에 의해 사량체의 안정성이 손상되면서 발생하며, 현재까지 120개 이상의 병인성 변이가 보고되어 있다. 임상 양상은 돌연변이 유형에 따라 다르지만, 크게 두 가지 표현형으로 나눌 수 있다.다발신경병증형(ATTR-PN, familial amyloid polyneuropathy, FAP)는 말초 및 자율신경계를 침범하며, 감각·운동 신경병증, 기립성 저혈압, 위장관 운동장애, 체중 감소 등을 동반한다.심근병증형(ATTR-CM, familial amyloid cardiomyopathy, FAC)는 심장 침착을 특징으로 하며, 심실 비후, 이완기 기능장애, 진행성 심부전 및 부정맥을 유발한다. 일부 변이는 신장, 안구, 연부조직을 동시에 침범해 복합적인 임상 양상을 보인다.ATTRv는 주로 성인기에 발병하며, 발현 연령과 진행 속도는 변이 종류와 지역적 특성에 따라 다양하다.야생형 ATTR은 유전자 이상이 없는 정상 TTR이 노화 과정에서 불안정해지며 발생한다. 과거에는 노인성 전신 아밀로이드증(senile systemic amyloidosis)으로 불렸으며, 주로 65세 이상 고령 남성에서 발견된다. 임상적으로는 대부분 심장을 침범하여 심근병증(ATTRwt-CM)의 형태로 발현되고, 진행성 심부전, 심실 비후, 전도장애, 심방세동이 주요 특징이다. 또한 손목터널증후군, 이두근건 파열, 척추관 협착증 등 근골격계 질환이 전구 증상으로 나타날 수 있으나, 비특이적인 증상과 고령 발병 특성으로 인해 과소진단되는 경우가 많다.ATTR 아밀로이드증의 치료는 이러한 발병 기전에 착안해 개발되었으며, 현재는 간에서 TTR 합성을 억제하는 RNA 기반 치료제, 사량체의 해리를 방지하는 안정화제, 그리고 이미 형성된 아밀로이드 침착을 제거하려는 면역학적 접근이 임상에 적용되고 있다.ATTR 아밀로이드증 치료에는 어떤 방법이 있는가? ATTR 아밀로이드증의 치료는 크게 두 축으로 발전해 왔다. 첫 번째는 증상을 조절하고 삶의 질을 유지하기 위한 기본 유지요법이며, 두 번째는 병태생리 자체를 교정하려는 표적 치료 전략이다.기본 유지요법은 질환의 근본적 진행을 막을 수는 없지만 환자의 기능 상태를 유지하고 합병증을 최소화하는 데 필수적이다. 울혈성 심부전 관리에는 루프 이뇨제가 주로 사용되며, 심방세동 및 전도 장애는 항응고제 투여와 함께 페이스메이커나 삽입형 제세동기(ICD)로 조절할 수 있다.신경병증성 통증은 가바펜티노이드, 삼환계 항우울제, SNRIs로 관리하며, 물리·재활 치료가 보조적 역할을 한다. 또한 기립성 저혈압과 같은 자율신경계 증상은 미도드린이나 플루드로코르티손으로 개선할 수 있고, 위장관 증상은 식이 조절 및 약물 치료로 완화할 수 있다.무엇보다 ATTR 아밀로이드증은 다장기 질환의 특성을 지니므로, 심장내과·신경과·소화기내과·재활의학과를 포함한 다학제적 접근이 필수적이다.병태생리 기반의 표적 치료는 TTR 단백질의 안정화, 합성 억제, 축적된 아밀로이드 제거, 그리고 간이식으로 구분된다. TTR 안정화제인 타파미디스(Tafamidis)는 사량체의 안정성을 높여 해체와 잘못 접힘을 억제하며, 임상시험에서 ATTR-CM 환자의 사망률과 입원율을 의미 있게 감소시켰다.RNA 기반 치료제는 TTR 합성을 근본적으로 차단하는 전략으로, siRNA 계열(파티시란, 부트리시란)과 ASO 계열(이노테르센, 에플로네르센)이 대표적이다. 이들 약제는 특히 hATTR-PN 환자에서 신경병증 진행을 억제하였고, 일부는 심근 침범 환자에서도 임상적 유효성이 입증되었다. 이미 형성된 아밀로이드 섬유를 제거하기 위한 항체 기반 치료도 연구되었으나 일부는 임상시험에서 실패하였고, 최근 새로운 접근법이 다시 모색되고 있다.마지막으로, 과거 hATTR 치료의 중요한 축이었던 간이식은 변이 TTR 합성을 근본적으로 차단할 수 있다는 장점이 있었으나, 이미 침착된 아밀로이드는 제거되지 않으며 야생형(wt) TTR에 의한 진행이 지속될 수 있다. 이러한 한계로 인해 현재는 RNA 기반 치료제의 도입과 함께 그 역할이 크게 줄어든 상태이다.TTR 안정화제(TTR stabilizer)는 어떤 약제인가? 최초의 트랜스티레틴 안정화제 타파미디스(Tafamidis)는 빈다켈(VyndaqelⓇ) 캡슐 20mg과 빈다맥스(VyndamaxⓇ) 캡슐 61mg 제형으로 출시되었다. 국내에서는 빈다켈이 ‘트랜스티레틴 가족성 아밀로이드성 다발신경병증(ATTR-PN)’ 치료제로, 빈다맥스가 ‘정상형(wild type) 또는 유전성 트랜스티레틴 아밀로이드성 심근병증(ATTR-CM) 성인 환자의 심혈관계 사망률 및 심혈관계 관련 입원 감소’ 적응증으로 각각 승인되어 있다.타파미디스는 TTR 단백질 사량체(tetramer)의 티록신 결합 부위에 선택적으로 결합하여 단량체(monomer)로의 해체를 억제한다. 이를 통해 잘못 접힌 단량체의 발생을 차단하고 아밀로이드 섬유 형성을 예방한다.두 번째 트랜스티레틴 안정화제 아코라미디스(Acoramidis, AttrubyⓇ)는 2024년 11월 미국 FDA에서 ‘정상형(wild type) 또는 유전성 트랜스티레틴 아밀로이드성 심근병증(ATTR-CM) 성인 환자의 심혈관계 사망률 및 심혈관계 관련 입원 감소’ 적응증으로 승인되었다.아코라미디스는 타파미디스 이후 처음 승인된 고강도 TTR 안정화제이자 경구 투여가 가능한 최신 치료제로, ATTR-CM 환자에서 생존률 및 입원율을 유의하게 개선한 점에서 임상적 의의가 크다.그러나 TTR 안정화제는 근본적으로 새로운 TTR 단백질 합성을 억제하지 못하고, 이미 형성된 아밀로이드 침착을 제거하지 못한다는 한계가 있다. 따라서 질환의 진행을 완전히 억제하기 어렵고, 특히 신경병증 환자에서는 RNAi 제제나 안티센스 올리고뉴클레오타이드(ASO) 제제에 비해 상대적으로 제한적인 효과를 보일 수 있다.트랜스티레틴 억제제(Transthyretin silencers)는 어떤 약제인가? TTR 억제제는 트랜스티레틴(TTR) 발현을 감소시키거나 제거함으로써 ATTR-CM의 진행을 늦추는 치료 전략이다. 이 접근법은 혈중 TTR 수치를 효과적으로 낮출 수 있으나, 동시에 TTR이 정상적으로 수행하는 운반 단백질로서의 기능까지 억제하게 된다는 한계를 지닌다.TTR 억제 요법에는 크게 두 가지 계열이 있다. 소간섭 RNA(siRNA)와 안티센스 올리고뉴클레오타이드(ASO) 모두 TTR mRNA에 결합하여 분해를 유도하지만, 세포 내에서 작용하는 기전에는 차이가 있다. siRNA는 표적 mRNA의 sense 가닥과 antisense 가닥으로 이루어진 이중가닥 RNA이다. 세포 내로 유입된 siRNA는 RNA-induced silencing complex(RISC)에 탑재되며, Ago2 엔도뉴클레아제가 sense 가닥을 제거하면 antisense 가닥이 노출되어 표적 mRNA와 상보적으로 결합한다. 이로 인해 해당 mRNA가 분해되어 유전자 발현이 억제된다.이러한 RNA 간섭 기전을 통해 siRNA는 특정 단백질 합성을 효과적으로 차단할 수 있으나, 세포 내 흡수율이 낮고 장기 특이성이 부족하다는 한계가 있다. 따라서 임상 적용을 위해서는 지질 나노입자(lipid nanoparticle, LNP)와 같은 전달체가 필요하다.이 문제를 해결하기 위해 개발된 첫 번째 상용화 약제가 파티시란(Patisiran)이다. 파티시란은 LNP 기반 전달체를 이용해 간세포 표적화를 가능하게 하였으며, 2015년 제2상 임상시험에서 3주 간격 투여 시 혈중 트랜스티레틴(TTR) 농도를 평균 약 80%까지 감소시켰다. 이어진 제3상 APOLLO 시험에서는 좌심실 벽 두께 감소(약 1 mm)와 NT-proBNP 수치 약 55% 감소가 확인되어, 신경병증뿐만 아니라 심혈관계 지표 개선 효과도 입증되었다.후속 약제인 부트리시란(Vutrisiran)은 2세대 siRNA 치료제로, LNP 대신 N-아세틸갈락토사민(GalNAc) 결합체를 적용하여 간세포 선택성을 높이고 약효 지속성을 강화하였다. 투여 용량은 파티시란보다 현저히 적으며, 3개월마다 피하주사 1회로 충분한 효과를 유지할 수 있다. 제1상 임상시험에서는 단일 투여 후 6주 시점에 혈중 TTR 농도가 약 83% 감소하였고, 이 억제 효과는 약 90일간 지속된 뒤 점진적으로 회복되는 양상이 관찰되었다.결론적으로, siRNA 기반 TTR 억제제는 ATTR 아밀로이드증 환자에서 혈중 TTR 농도를 크게 낮추고, 신경학적·심혈관학적 임상 지표를 개선하는 효과를 보인다. 특히 부트리시란은 투여 편의성과 안전성에서 진전을 이루어 ATTR-CM을 포함한 다양한 임상 영역에서 활용 가능성이 확대되고 있다.안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, ASO) ASO는 특정 mRNA에 직접 결합하여 RNase H 매개 절단을 유도하거나 스플라이싱을 조절함으로써 단백질 발현을 억제한다. 트랜스티레틴 아밀로이드증에서는 간세포에서 합성되는 TTR mRNA를 표적으로 하여 혈중 TTR 단백질 농도를 감소시킴으로써 질병의 진행을 억제한다.이러한 접근법은 RNA 간섭 기전을 활용하는 siRNA 기반 약물과 달리, RISC 복합체를 필요로 하지 않고 단일가닥 핵산 서열을 통해 작용한다는 점에서 차별성을 가진다.현재 승인된 대표적인 ASO 약제로는 이노테르센(Inotersen, TegsediⓇ)과 에플로네르센(Eplontersen, WainuaⓇ)이 있다. 미국 FDA는 이노테르센을 2018년 10월, 에플로네르센을 2023년 12월에 각각 ‘ATTRv-PN’ 치료제로 승인하였지만, 국내에는 아직 소개되지 않았다. 두 약제 모두 간에서 TTR 합성을 억제하여 혈중 TTR 농도를 낮추고, 아밀로이드 침착을 줄여 질환의 진행을 늦추거나 증상을 개선한다.이노테르센은 주 1회 피하주사로 투여되며, 임상시험에서 혈중 TTR 농도를 평균 70~80% 감소시키고 신경병증 점수 및 삶의 질 지표를 개선하는 효과가 확인되었다. 그러나 치료 과정에서 혈소판 감소와 신장 이상이 보고되어 정기적인 모니터링이 필요하다는 한계가 있다.이러한 안전성 문제와 투여 편의성의 제약을 개선하기 위해 개발된 차세대 약제가 에플로네르센이다. 에플로네르센은 N-아세틸갈락토사민(GalNAc) 결합체를 도입하여 간세포 특이적 흡수 효율을 높임으로써 약효를 극대화하는 동시에 부작용을 줄이도록 설계되었다.또한 이노테르센이 주 1회 투여를 필요로 하는 반면, 에플로네르센은 월 1회 피하주사만으로도 충분한 효과를 유지할 수 있어 환자 순응도를 크게 향상시켰다.부티리시란(Vutrisiran)는 어떤 약제인가? 부트리시란은 GalNAc(N-acetylgalactosamine) 플랫폼을 적용한 차세대 소간섭 RNA(siRNA) 치료제로, hATTR-PN과 ATTR-CM 환자 모두에서 사용 가능한 약제이다.이 약제는 기존의 파티시란(Patisiran)과 동일하게 TTR mRNA를 표적하여 단백질 발현을 억제하지만, 약리학적 특성에서 중요한 차별성을 지닌다. 먼저, 인산다이에스터(phosphodiester) 결합을 인산티오에이트(phosphorothioate) 결합으로 치환하여 핵산 분해효소에 대한 저항성을 강화하고 분자의 전신 안정성을 크게 향상시켰다. 이를 통해 보다 적은 용량으로도 지속적이고 강력한 TTR 억제 효과를 유지할 수 있게 되었다.또한 siRNA 분자와 삼분지(triantennary) N-아세틸갈락토사민(GalNAc) 리간드의 공유결합은 간세포 표면의 아실로글리코단백질 수용체(asialoglycoprotein receptor, ASGPR)를 통한 고효율적 내재화를 유도한다. 이로써 간세포 특이적 전달이 극대화되고 전신적 비특이적 분포가 최소화되어 약효의 선택성과 안전성이 동시에 확보된다.GalNAc 플랫폼의 도입은 정맥투여 대신 피하주사(SC) 제형을 가능하게 하였으며, 결과적으로 짧은 시간 내 간단한 투여가 가능해졌다. 부트리시란은 3개월마다 한 번의 피하 투여만으로 효과를 유지할 수 있어 환자의 치료 편의성과 순응도를 획기적으로 개선하였다. 더불어, 투여 전 스테로이드나 항히스타민제와 같은 항염증 전처치가 필요하지 않아 안전성과 내약성 측면에서도 우수한 특성을 보인다.임상적으로, 부트리시란은 HELIOS-A 3상 시험에서 파티시란과 동등한 수준의 신경학적 개선 효과를 보였으며, 주사 경로가 단순화되었음에도 불구하고 안전성 측면에서 우수한 결과를 나타냈다. 이어서 HELIOS-B 연구에서는 ATTR-CM 환자를 대상으로 심혈관 사망률과 입원율을 유의하게 감소시키는 효과가 확인되었고, 이를 근거로 2025년 FDA는 부트리시란의 적응증을 ATTR-CM으로 확장 승인하였다.부티리시란(Vutrisiran)의 약리 기전은? 부티시란은 소간섭 RNA(siRNA) 기술을 기반으로 트랜스티레틴(TTR) 단백질 합성을 근본적으로 억제하는 기전을 가진다. 일반적으로 siRNA는 이중가닥 구조를 이루어 세포 내로 유입된 뒤 RNA-induced silencing complex(RISC)에 탑재된다.이 과정에서 비표적 가닥(sense strand)은 분해되고, 표적을 인식하는 가닥(antisense strand)이 노출되어 상보적인 TTR mRNA와 결합한다. 결합된 mRNA는 Ago2와 같은 효소에 의해 절단·분해되며, 결과적으로 TTR 단백질 합성이 차단된다. 부티시란은 이러한 RNA 간섭(RNAi) 경로를 통해 병태생리의 근본 원인인 TTR 단백질 축적을 억제한다.특히 부티시란은 TTR 합성이 주로 일어나는 간세포로 siRNA를 선택적으로 전달함으로써 약효를 극대화하고 전신적 부작용을 최소화한다. 또한 화학적 변형인 인산티오에이트(phosphorothioate)를 도입하여 체내 핵산 분해효소에 대한 저항성을 강화하고, 안정성을 향상시켰다.이러한 최적화된 설계는 낮은 용량에서도 장기간 TTR 억제를 가능하게 하며, 3개월마다 한 번의 피하 투여만으로도 안정적인 약리 효과를 유지할 수 있게 한다.부트리시란(AMVUTTRA)의 허가임상은 어떠한가? -Polyneuropathy of Hereditary Transthyretin-mediated AmyloidosisAMVUTTRA(부트리시란, vutrisiran)의 유효성은 hATTR-PN 성인 환자를 대상으로 한 무작위 배정, 공개 임상시험(HELIOS-A; NCT03759379)에서 평가되었다.환자들은 3:1의 비율로 무작위 배정되어, 25mg의 AMVUTTRA를 3개월마다 피하 투여받은 군(N=122)과, 대조(reference)군으로서 0.3mg/kg의 파티시란(Patisiran)을 3주마다 정맥 투여받은 군(N=42)에 배정되었다. AMVUTTRA 투여군 환자의 97%, 파티시란 투여군 환자의 93%가 최소 9개월 동안 배정된 치료를 완료하였다.유효성 평가는 hATTR 아밀로이드증에 의한 다발신경병증(PN)을 가진 성인 환자군으로 구성된 외부 위약 대조군과 HELIOS-A 시험의 AMVUTTRA 투여군을 비교하는 방식으로 이루어졌다.주요 유효성 평가 변수는 기저치 대비 9개월 시점의 수정된 신경병증 장애 점수+7(modified Neuropathy Impairment Score +7, mNIS+7)의 변화였다. mNIS+7은 객관적인 신경병증 평가 도구로, 기본 NIS와 Modified +7 복합 점수로 구성된다.본 시험에서 사용된 mNIS+7 버전은, NIS가 뇌신경 기능, 근력, 반사 기능의 장애를 객관적으로 측정하고, +7 항목이 기립성 혈압(postural blood pressure), 정량적 감각 검사(quantitative sensory testing), 말초신경 전기생리학(peripheral nerve electrophysiology)을 평가하도록 설계되었다. mNIS+7은 총 0~304점 범위를 가지며, 점수가 높을수록 질환의 중증도가 크다는 것을 의미한다.mNIS+7 효과의 임상적 유의성은 기저치 대비 9개월 시점의 Norfolk 삶의 질-당뇨병성 신경병증(Norfolk Quality of Life-Diabetic Neuropathy, QoL-DN)총점 변화를 통해 추가적으로 평가되었다.Norfolk QoL-DN 척도는 환자 보고 기반 평가(patient-reported outcome)로서, 신경병증의 주관적 경험을 평가하며, 대섬유 신경병증/신체 기능(physical functioning/large fiber neuropathy), 일상생활 수행능력(activities of daily living), 증상(symptoms), 소섬유 신경병증(small fiber neuropathy), 자율신경병증(autonomic neuropathy) 영역을 포함한다. Norfolk QoL-DN의 총점 범위는 -4~136점이며, 점수가 높을수록 삶의 질 저하와 신경병증의 심각성이 큼을 의미한다.추가 평가 변수로는 10미터 보행 검사(10-meter walk test, 10MWT)를 통한 보행 속도와, 수정 체질량지수(modified body mass index, mBMI)가 포함되었다.HELIOS-A 시험에서 AMVUTTRA 치료는 위약군과 비교했을 때, 9개월 시점의 mNIS+7, Norfolk QoL-DN 총점, 10MWT에서 통계적으로 유의한 개선을 보였다(p2025-09-19 06:01:02최병철 박사
첫 RNA 기반 ATTR-CM 치료제 '암부트라'④최초의 RNAi 기반 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 치료제, ‘암부트라(Vutrisiran)’암부트라(Amvuttra®, 성분명: 부트리시란 Vutrisiran, Alnylam Pharmaceuticals)는 소간섭 RNA(small interfering RNA, siRNA) 치료제로, 2022년 6월 미국 FDA에서 유전성 트랜스티레틴 매개 아밀로이드 다발신경병증(hATTR-PN) 치료제로 최초 승인되었다. 이어 2025년 3월에는 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 환자의 심혈관 사망, 입원 및 응급실 방문을 감소시키는 최초의 RNAi 치료제로 추가 승인을 받았다.Alnylam Pharmaceuticals는 siRNA 기술을 기반으로 간세포 내 TTR 합성을 직접 억제하는 신약 개발을 선도해 왔으며, 2018년 파티시란(Patisiran, Onpattro®)이 hATTR-PN 치료제로 최초 승인되었다. 이후 이를 개량한 2세대 제형인 부트리시란(Amvuttra®)이 개발되어 hATTR-PN과 ATTR-CM 모두에 사용 가능하게 되었다.트랜스티레틴 매개 아밀로이드증(ATTR amyloidosis)은 간에서 합성되는 단백질인 트랜스티레틴(TTR)의 구조적 불안정성에 의해 발생한다. 불안정한 TTR 사량체(tetramer)는 쉽게 해리되어 아밀로이드 형성 성향(amyloidogenic)을 띠는 잘못 접힌 단량체(misfolded monomer)로 전환된다. 이 단량체들이 서로 응집해 β-sheet 구조를 형성하면서 아밀로이드 섬유(amyloid fibril)로 축적되고, 신경·심장·소화관 등 다양한 장기에 침착되어 임상 증상을 유발한다.유전성 ATTR 다발신경병증(hATTR-PN)은 TTR 유전자 변이에 의해 발생하며, 주로 말초 및 자율신경에 침착해 신경병증을 유발한다.ATTR 심근병증(ATTR-CM)은 유전성(hATTR-CM) 또는 노화와 관련된 야생형(wild-type ATTR-CM)으로 발생할 수 있으며, 주 침착 부위는 심근이다.부트리시란은 RNAi 치료제로, 3개월 간격으로 1회 피하주사한다. 특정 mRNA를 표적·침묵시켜 야생형과 변이형 모두의 TTR 생성을 차단한다.HELIOS-A 시험은 hATTR-PN 환자를 대상으로 한 무작위 배정, 공개라벨, 다국가 3상 임상으로 진행되었다. 환자들은 3개월마다 피하로 부트리시란을 투여받거나 대조군으로 파티시란 정맥주사를 투여받았다.주요 유효성 평가는 mNIS+7 점수, Norfolk QoL-DN 설문, 보행 검사 등이었으며, 외부 위약군(APOLLO 연구 placebo arm)과의 비교를 통해 신뢰성을 보강하였다. 그 결과, 부트리시란 투여군은 신경학적 기능 악화를 유의하게 억제했으며 삶의 질과 신체 기능이 향상되는 양상을 보였다. 안전성 측면에서도 대부분의 이상반응은 경미하거나 중등도 수준에 그쳐 장기 투여의 내약성이 입증되었다.HELIOS-B 시험은 hATTR-CM뿐 아니라 야생형 ATTR-CM 환자를 포함한 심근병증 환자군을 대상으로 수행된 무작위 배정, 이중맹검, 위약 대조 3상 임상시험이다. ATTR-CM 환자에서 부트리시란의 심혈관 사망 및 입원 위험 감소 효과를 평가하는 데 중점을 두었으며, 1차 종료점으로 심혈관 사망률과 심부전 입원율이 설정되었다.연구 결과, 부트리시란은 ATTR-CM 환자에서 주요 심혈관 사건의 발생을 줄이는 경향을 보였고, 타파미디스(Tafamidis) 치료 경험 여부와 무관하게 일관된 효과를 나타냈다.트랜스티레틴(Transthyretin, TTR)은 무엇인가? 트랜스티레틴(Transthyretin)은 그 명칭이 transport + thyroxin + retinol에서 유래하였으며, 혈액과 뇌척수액에서 갑상선 호르몬과 비타민 A를 운반하는 필수 단백질이다.분자량 약 55kDa의 사량체(tetramer) 구조를 가진 TTR은 주로 간세포에서 합성되어 혈장으로 분비되며, 전체의 90% 이상이 간에서 생산된다. 혈중 TTR은 전체 단백질의 약 0.1–0.3%를 차지하며, 갑상선 호르몬 및 비타민 A 운반뿐 아니라 단백-에너지 영양 상태를 반영하는 민감한 지표로 활용된다.간 외에도 뇌의 맥락얼기(choroid plexus) 상피세포와 망막색소상피(retinal pigment epithelium, RPE)에서 국소적으로 합성된다. 맥락얼기에서 생성된 TTR은 뇌척수액 내에 풍부하게 존재하며, thyroxine(T4)의 주요 운반체로 기능한다. 혈액-뇌 장벽을 통한 갑상선 호르몬의 직접적 이동이 제한적이라는 점을 고려할 때, TTR은 중추신경계 발달과 대사 항상성 유지에 핵심적 역할을 한다.망막에서 합성된 TTR은 retinol-binding protein(RBP)과 결합하여 레티놀을 안정적으로 운반하고, RBP의 신장 여과를 방지함으로써 시각 회로 유지와 비타민 A 항상성 조절에 기여한다. TTR의 주요 기능은 세 가지로 요약된다. 첫째, 갑상선 호르몬 운반으로 혈중 thyroxine 운반의 약 15%를 담당하며, 알부민과 티록신 결합 글로불린(TBG)과 보완적으로 작용한다. 특히 뇌척수액에서는 TTR이 유일한 주요 운반 단백질이다. 둘째, 비타민 A 대사 및 운반으로 RBP와의 결합을 통해 레티놀을 안정화시키고 체내 항상성을 유지한다. 셋째, 대사적 지표 기능으로 혈중 농도가 영양 상태 및 단백질 합성 능력을 반영하여 임상적으로 영양평가의 바이오마커로 활용된다.한편, TTR은 구조적 불안정성으로 인해 단량체(monomer)로 분리되면 잘못 접힘(misfolding)이 발생하고, 이는 β-sheet 기반의 아밀로이드 섬유를 형성하여 조직에 침착할 수 있다. 이러한 병리적 변화가 트랜스티레틴 아밀로이드증(ATTR amyloidosis)의 기전이며, 연령 증가에 따른 야생형(wild-type) TTR의 불안정성은 심근병증(ATTR-CM)과 연관되고, 특정 유전자 변이에 의한 변이형 TTR은 다발신경병증(ATTR-PN)의 주요 원인으로 작용한다.트랜스티레틴 매개 아밀로이드증(Transthyretin-mediated amyloidosis, ATTR 아밀로이드증)이란 어떤 질환인가? ATTR 아밀로이드증은 트랜스티레틴(TTR)의 구조적 불안정성으로 인해 발생하는 전신성 단백질 침착 질환이다.TTR은 간에서 주로 합성되는 사량체 운반 단백질로, 정상 상태에서는 갑상선 호르몬과 비타민 A를 안정적으로 운반한다. 그러나 유전적 변이나 노화로 인해 단백질의 안정성이 저하되면 사량체(tetramer)가 단량체(monomer)로 해리되고, 이 단량체가 잘못 접힘(misfolding)을 거쳐 β-sheet 구조의 불용성 아밀로이드 섬유(amyloid fibril)로 전환된다. 축적된 아밀로이드 섬유는 다양한 장기에 침착하여 구조적 손상과 기능 저하를 유발한다.ATTR 아밀로이드증은 원인에 따라 변이형(hereditary ATTR, ATTRv)과 야생형(wild-type ATTR, ATTRwt)으로 구분된다. 변이형 ATTR은 TTR 유전자 변이에 의해 사량체의 안정성이 손상되면서 발생하며, 현재까지 120개 이상의 병인성 변이가 보고되어 있다. 임상 양상은 돌연변이 유형에 따라 다르지만, 크게 두 가지 표현형으로 나눌 수 있다.다발신경병증형(ATTR-PN, familial amyloid polyneuropathy, FAP)는 말초 및 자율신경계를 침범하며, 감각·운동 신경병증, 기립성 저혈압, 위장관 운동장애, 체중 감소 등을 동반한다.심근병증형(ATTR-CM, familial amyloid cardiomyopathy, FAC)는 심장 침착을 특징으로 하며, 심실 비후, 이완기 기능장애, 진행성 심부전 및 부정맥을 유발한다. 일부 변이는 신장, 안구, 연부조직을 동시에 침범해 복합적인 임상 양상을 보인다.ATTRv는 주로 성인기에 발병하며, 발현 연령과 진행 속도는 변이 종류와 지역적 특성에 따라 다양하다.야생형 ATTR은 유전자 이상이 없는 정상 TTR이 노화 과정에서 불안정해지며 발생한다. 과거에는 노인성 전신 아밀로이드증(senile systemic amyloidosis)으로 불렸으며, 주로 65세 이상 고령 남성에서 발견된다. 임상적으로는 대부분 심장을 침범하여 심근병증(ATTRwt-CM)의 형태로 발현되고, 진행성 심부전, 심실 비후, 전도장애, 심방세동이 주요 특징이다. 또한 손목터널증후군, 이두근건 파열, 척추관 협착증 등 근골격계 질환이 전구 증상으로 나타날 수 있으나, 비특이적인 증상과 고령 발병 특성으로 인해 과소진단되는 경우가 많다.ATTR 아밀로이드증의 치료는 이러한 발병 기전에 착안해 개발되었으며, 현재는 간에서 TTR 합성을 억제하는 RNA 기반 치료제, 사량체의 해리를 방지하는 안정화제, 그리고 이미 형성된 아밀로이드 침착을 제거하려는 면역학적 접근이 임상에 적용되고 있다.ATTR 아밀로이드증 치료에는 어떤 방법이 있는가? ATTR 아밀로이드증의 치료는 크게 두 축으로 발전해 왔다. 첫 번째는 증상을 조절하고 삶의 질을 유지하기 위한 기본 유지요법이며, 두 번째는 병태생리 자체를 교정하려는 표적 치료 전략이다.기본 유지요법은 질환의 근본적 진행을 막을 수는 없지만 환자의 기능 상태를 유지하고 합병증을 최소화하는 데 필수적이다. 울혈성 심부전 관리에는 루프 이뇨제가 주로 사용되며, 심방세동 및 전도 장애는 항응고제 투여와 함께 페이스메이커나 삽입형 제세동기(ICD)로 조절할 수 있다.신경병증성 통증은 가바펜티노이드, 삼환계 항우울제, SNRIs로 관리하며, 물리·재활 치료가 보조적 역할을 한다. 또한 기립성 저혈압과 같은 자율신경계 증상은 미도드린이나 플루드로코르티손으로 개선할 수 있고, 위장관 증상은 식이 조절 및 약물 치료로 완화할 수 있다.무엇보다 ATTR 아밀로이드증은 다장기 질환의 특성을 지니므로, 심장내과·신경과·소화기내과·재활의학과를 포함한 다학제적 접근이 필수적이다.병태생리 기반의 표적 치료는 TTR 단백질의 안정화, 합성 억제, 축적된 아밀로이드 제거, 그리고 간이식으로 구분된다. TTR 안정화제인 타파미디스(Tafamidis)는 사량체의 안정성을 높여 해체와 잘못 접힘을 억제하며, 임상시험에서 ATTR-CM 환자의 사망률과 입원율을 의미 있게 감소시켰다.RNA 기반 치료제는 TTR 합성을 근본적으로 차단하는 전략으로, siRNA 계열(파티시란, 부트리시란)과 ASO 계열(이노테르센, 에플로네르센)이 대표적이다. 이들 약제는 특히 hATTR-PN 환자에서 신경병증 진행을 억제하였고, 일부는 심근 침범 환자에서도 임상적 유효성이 입증되었다. 이미 형성된 아밀로이드 섬유를 제거하기 위한 항체 기반 치료도 연구되었으나 일부는 임상시험에서 실패하였고, 최근 새로운 접근법이 다시 모색되고 있다.마지막으로, 과거 hATTR 치료의 중요한 축이었던 간이식은 변이 TTR 합성을 근본적으로 차단할 수 있다는 장점이 있었으나, 이미 침착된 아밀로이드는 제거되지 않으며 야생형(wt) TTR에 의한 진행이 지속될 수 있다. 이러한 한계로 인해 현재는 RNA 기반 치료제의 도입과 함께 그 역할이 크게 줄어든 상태이다.TTR 안정화제(TTR stabilizer)는 어떤 약제인가? 최초의 트랜스티레틴 안정화제 타파미디스(Tafamidis)는 빈다켈(VyndaqelⓇ) 캡슐 20mg과 빈다맥스(VyndamaxⓇ) 캡슐 61mg 제형으로 출시되었다. 국내에서는 빈다켈이 ‘트랜스티레틴 가족성 아밀로이드성 다발신경병증(ATTR-PN)’ 치료제로, 빈다맥스가 ‘정상형(wild type) 또는 유전성 트랜스티레틴 아밀로이드성 심근병증(ATTR-CM) 성인 환자의 심혈관계 사망률 및 심혈관계 관련 입원 감소’ 적응증으로 각각 승인되어 있다.타파미디스는 TTR 단백질 사량체(tetramer)의 티록신 결합 부위에 선택적으로 결합하여 단량체(monomer)로의 해체를 억제한다. 이를 통해 잘못 접힌 단량체의 발생을 차단하고 아밀로이드 섬유 형성을 예방한다.두 번째 트랜스티레틴 안정화제 아코라미디스(Acoramidis, AttrubyⓇ)는 2024년 11월 미국 FDA에서 ‘정상형(wild type) 또는 유전성 트랜스티레틴 아밀로이드성 심근병증(ATTR-CM) 성인 환자의 심혈관계 사망률 및 심혈관계 관련 입원 감소’ 적응증으로 승인되었다.아코라미디스는 타파미디스 이후 처음 승인된 고강도 TTR 안정화제이자 경구 투여가 가능한 최신 치료제로, ATTR-CM 환자에서 생존률 및 입원율을 유의하게 개선한 점에서 임상적 의의가 크다.그러나 TTR 안정화제는 근본적으로 새로운 TTR 단백질 합성을 억제하지 못하고, 이미 형성된 아밀로이드 침착을 제거하지 못한다는 한계가 있다. 따라서 질환의 진행을 완전히 억제하기 어렵고, 특히 신경병증 환자에서는 RNAi 제제나 안티센스 올리고뉴클레오타이드(ASO) 제제에 비해 상대적으로 제한적인 효과를 보일 수 있다.트랜스티레틴 억제제(Transthyretin silencers)는 어떤 약제인가? TTR 억제제는 트랜스티레틴(TTR) 발현을 감소시키거나 제거함으로써 ATTR-CM의 진행을 늦추는 치료 전략이다. 이 접근법은 혈중 TTR 수치를 효과적으로 낮출 수 있으나, 동시에 TTR이 정상적으로 수행하는 운반 단백질로서의 기능까지 억제하게 된다는 한계를 지닌다.TTR 억제 요법에는 크게 두 가지 계열이 있다. 소간섭 RNA(siRNA)와 안티센스 올리고뉴클레오타이드(ASO) 모두 TTR mRNA에 결합하여 분해를 유도하지만, 세포 내에서 작용하는 기전에는 차이가 있다. siRNA는 표적 mRNA의 sense 가닥과 antisense 가닥으로 이루어진 이중가닥 RNA이다. 세포 내로 유입된 siRNA는 RNA-induced silencing complex(RISC)에 탑재되며, Ago2 엔도뉴클레아제가 sense 가닥을 제거하면 antisense 가닥이 노출되어 표적 mRNA와 상보적으로 결합한다. 이로 인해 해당 mRNA가 분해되어 유전자 발현이 억제된다.이러한 RNA 간섭 기전을 통해 siRNA는 특정 단백질 합성을 효과적으로 차단할 수 있으나, 세포 내 흡수율이 낮고 장기 특이성이 부족하다는 한계가 있다. 따라서 임상 적용을 위해서는 지질 나노입자(lipid nanoparticle, LNP)와 같은 전달체가 필요하다.이 문제를 해결하기 위해 개발된 첫 번째 상용화 약제가 파티시란(Patisiran)이다. 파티시란은 LNP 기반 전달체를 이용해 간세포 표적화를 가능하게 하였으며, 2015년 제2상 임상시험에서 3주 간격 투여 시 혈중 트랜스티레틴(TTR) 농도를 평균 약 80%까지 감소시켰다. 이어진 제3상 APOLLO 시험에서는 좌심실 벽 두께 감소(약 1 mm)와 NT-proBNP 수치 약 55% 감소가 확인되어, 신경병증뿐만 아니라 심혈관계 지표 개선 효과도 입증되었다.후속 약제인 부트리시란(Vutrisiran)은 2세대 siRNA 치료제로, LNP 대신 N-아세틸갈락토사민(GalNAc) 결합체를 적용하여 간세포 선택성을 높이고 약효 지속성을 강화하였다. 투여 용량은 파티시란보다 현저히 적으며, 3개월마다 피하주사 1회로 충분한 효과를 유지할 수 있다. 제1상 임상시험에서는 단일 투여 후 6주 시점에 혈중 TTR 농도가 약 83% 감소하였고, 이 억제 효과는 약 90일간 지속된 뒤 점진적으로 회복되는 양상이 관찰되었다.결론적으로, siRNA 기반 TTR 억제제는 ATTR 아밀로이드증 환자에서 혈중 TTR 농도를 크게 낮추고, 신경학적·심혈관학적 임상 지표를 개선하는 효과를 보인다. 특히 부트리시란은 투여 편의성과 안전성에서 진전을 이루어 ATTR-CM을 포함한 다양한 임상 영역에서 활용 가능성이 확대되고 있다.안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, ASO) ASO는 특정 mRNA에 직접 결합하여 RNase H 매개 절단을 유도하거나 스플라이싱을 조절함으로써 단백질 발현을 억제한다. 트랜스티레틴 아밀로이드증에서는 간세포에서 합성되는 TTR mRNA를 표적으로 하여 혈중 TTR 단백질 농도를 감소시킴으로써 질병의 진행을 억제한다.이러한 접근법은 RNA 간섭 기전을 활용하는 siRNA 기반 약물과 달리, RISC 복합체를 필요로 하지 않고 단일가닥 핵산 서열을 통해 작용한다는 점에서 차별성을 가진다.현재 승인된 대표적인 ASO 약제로는 이노테르센(Inotersen, TegsediⓇ)과 에플로네르센(Eplontersen, WainuaⓇ)이 있다. 미국 FDA는 이노테르센을 2018년 10월, 에플로네르센을 2023년 12월에 각각 ‘ATTRv-PN’ 치료제로 승인하였지만, 국내에는 아직 소개되지 않았다. 두 약제 모두 간에서 TTR 합성을 억제하여 혈중 TTR 농도를 낮추고, 아밀로이드 침착을 줄여 질환의 진행을 늦추거나 증상을 개선한다.이노테르센은 주 1회 피하주사로 투여되며, 임상시험에서 혈중 TTR 농도를 평균 70~80% 감소시키고 신경병증 점수 및 삶의 질 지표를 개선하는 효과가 확인되었다. 그러나 치료 과정에서 혈소판 감소와 신장 이상이 보고되어 정기적인 모니터링이 필요하다는 한계가 있다.이러한 안전성 문제와 투여 편의성의 제약을 개선하기 위해 개발된 차세대 약제가 에플로네르센이다. 에플로네르센은 N-아세틸갈락토사민(GalNAc) 결합체를 도입하여 간세포 특이적 흡수 효율을 높임으로써 약효를 극대화하는 동시에 부작용을 줄이도록 설계되었다.또한 이노테르센이 주 1회 투여를 필요로 하는 반면, 에플로네르센은 월 1회 피하주사만으로도 충분한 효과를 유지할 수 있어 환자 순응도를 크게 향상시켰다.부티리시란(Vutrisiran)는 어떤 약제인가? 부트리시란은 GalNAc(N-acetylgalactosamine) 플랫폼을 적용한 차세대 소간섭 RNA(siRNA) 치료제로, hATTR-PN과 ATTR-CM 환자 모두에서 사용 가능한 약제이다.이 약제는 기존의 파티시란(Patisiran)과 동일하게 TTR mRNA를 표적하여 단백질 발현을 억제하지만, 약리학적 특성에서 중요한 차별성을 지닌다. 먼저, 인산다이에스터(phosphodiester) 결합을 인산티오에이트(phosphorothioate) 결합으로 치환하여 핵산 분해효소에 대한 저항성을 강화하고 분자의 전신 안정성을 크게 향상시켰다. 이를 통해 보다 적은 용량으로도 지속적이고 강력한 TTR 억제 효과를 유지할 수 있게 되었다.또한 siRNA 분자와 삼분지(triantennary) N-아세틸갈락토사민(GalNAc) 리간드의 공유결합은 간세포 표면의 아실로글리코단백질 수용체(asialoglycoprotein receptor, ASGPR)를 통한 고효율적 내재화를 유도한다. 이로써 간세포 특이적 전달이 극대화되고 전신적 비특이적 분포가 최소화되어 약효의 선택성과 안전성이 동시에 확보된다.GalNAc 플랫폼의 도입은 정맥투여 대신 피하주사(SC) 제형을 가능하게 하였으며, 결과적으로 짧은 시간 내 간단한 투여가 가능해졌다. 부트리시란은 3개월마다 한 번의 피하 투여만으로 효과를 유지할 수 있어 환자의 치료 편의성과 순응도를 획기적으로 개선하였다. 더불어, 투여 전 스테로이드나 항히스타민제와 같은 항염증 전처치가 필요하지 않아 안전성과 내약성 측면에서도 우수한 특성을 보인다.임상적으로, 부트리시란은 HELIOS-A 3상 시험에서 파티시란과 동등한 수준의 신경학적 개선 효과를 보였으며, 주사 경로가 단순화되었음에도 불구하고 안전성 측면에서 우수한 결과를 나타냈다. 이어서 HELIOS-B 연구에서는 ATTR-CM 환자를 대상으로 심혈관 사망률과 입원율을 유의하게 감소시키는 효과가 확인되었고, 이를 근거로 2025년 FDA는 부트리시란의 적응증을 ATTR-CM으로 확장 승인하였다.부티리시란(Vutrisiran)의 약리 기전은? 부티시란은 소간섭 RNA(siRNA) 기술을 기반으로 트랜스티레틴(TTR) 단백질 합성을 근본적으로 억제하는 기전을 가진다. 일반적으로 siRNA는 이중가닥 구조를 이루어 세포 내로 유입된 뒤 RNA-induced silencing complex(RISC)에 탑재된다.이 과정에서 비표적 가닥(sense strand)은 분해되고, 표적을 인식하는 가닥(antisense strand)이 노출되어 상보적인 TTR mRNA와 결합한다. 결합된 mRNA는 Ago2와 같은 효소에 의해 절단·분해되며, 결과적으로 TTR 단백질 합성이 차단된다. 부티시란은 이러한 RNA 간섭(RNAi) 경로를 통해 병태생리의 근본 원인인 TTR 단백질 축적을 억제한다.특히 부티시란은 TTR 합성이 주로 일어나는 간세포로 siRNA를 선택적으로 전달함으로써 약효를 극대화하고 전신적 부작용을 최소화한다. 또한 화학적 변형인 인산티오에이트(phosphorothioate)를 도입하여 체내 핵산 분해효소에 대한 저항성을 강화하고, 안정성을 향상시켰다.이러한 최적화된 설계는 낮은 용량에서도 장기간 TTR 억제를 가능하게 하며, 3개월마다 한 번의 피하 투여만으로도 안정적인 약리 효과를 유지할 수 있게 한다.부트리시란(AMVUTTRA)의 허가임상은 어떠한가? -Polyneuropathy of Hereditary Transthyretin-mediated AmyloidosisAMVUTTRA(부트리시란, vutrisiran)의 유효성은 hATTR-PN 성인 환자를 대상으로 한 무작위 배정, 공개 임상시험(HELIOS-A; NCT03759379)에서 평가되었다.환자들은 3:1의 비율로 무작위 배정되어, 25mg의 AMVUTTRA를 3개월마다 피하 투여받은 군(N=122)과, 대조(reference)군으로서 0.3mg/kg의 파티시란(Patisiran)을 3주마다 정맥 투여받은 군(N=42)에 배정되었다. AMVUTTRA 투여군 환자의 97%, 파티시란 투여군 환자의 93%가 최소 9개월 동안 배정된 치료를 완료하였다.유효성 평가는 hATTR 아밀로이드증에 의한 다발신경병증(PN)을 가진 성인 환자군으로 구성된 외부 위약 대조군과 HELIOS-A 시험의 AMVUTTRA 투여군을 비교하는 방식으로 이루어졌다.주요 유효성 평가 변수는 기저치 대비 9개월 시점의 수정된 신경병증 장애 점수+7(modified Neuropathy Impairment Score +7, mNIS+7)의 변화였다. mNIS+7은 객관적인 신경병증 평가 도구로, 기본 NIS와 Modified +7 복합 점수로 구성된다.본 시험에서 사용된 mNIS+7 버전은, NIS가 뇌신경 기능, 근력, 반사 기능의 장애를 객관적으로 측정하고, +7 항목이 기립성 혈압(postural blood pressure), 정량적 감각 검사(quantitative sensory testing), 말초신경 전기생리학(peripheral nerve electrophysiology)을 평가하도록 설계되었다. mNIS+7은 총 0~304점 범위를 가지며, 점수가 높을수록 질환의 중증도가 크다는 것을 의미한다.mNIS+7 효과의 임상적 유의성은 기저치 대비 9개월 시점의 Norfolk 삶의 질-당뇨병성 신경병증(Norfolk Quality of Life-Diabetic Neuropathy, QoL-DN)총점 변화를 통해 추가적으로 평가되었다.Norfolk QoL-DN 척도는 환자 보고 기반 평가(patient-reported outcome)로서, 신경병증의 주관적 경험을 평가하며, 대섬유 신경병증/신체 기능(physical functioning/large fiber neuropathy), 일상생활 수행능력(activities of daily living), 증상(symptoms), 소섬유 신경병증(small fiber neuropathy), 자율신경병증(autonomic neuropathy) 영역을 포함한다. Norfolk QoL-DN의 총점 범위는 -4~136점이며, 점수가 높을수록 삶의 질 저하와 신경병증의 심각성이 큼을 의미한다.추가 평가 변수로는 10미터 보행 검사(10-meter walk test, 10MWT)를 통한 보행 속도와, 수정 체질량지수(modified body mass index, mBMI)가 포함되었다.HELIOS-A 시험에서 AMVUTTRA 치료는 위약군과 비교했을 때, 9개월 시점의 mNIS+7, Norfolk QoL-DN 총점, 10MWT에서 통계적으로 유의한 개선을 보였다(p2025-09-19 06:01:02최병철 박사 -
 표준치료 없는 치료저항성 우울증…스프라바토 해법될까[데일리팜=황병우 기자] 한국이 OECD 국가중 자살률 1위를 기록하고 있는 가운데 '치료저항성 우울증' 치료지원의 필요성이 강조되고 있다.특히 일반적인 우울증보다 자살 시도가 7배 더 높은 것으로 알려진 치료저항성 우울증 치료를 위한 대안이 필요하다는 게 전문가의 입장이다.한국얀센은 9일 세계 자살예방의 날을 맞아 마스터클래스를 열고 치료저항성 우울증(TRD)의 실태와 최신 치료지견을 공유했다.조성준 강북삼성병원 정신건강의학과 교수통계청 '2023년 사망원인통계'에 따르면 2023년 한 해 자살로 1만3978명이 사망했다. 2023년의 인구 10만 명당 자살률은 27.3명으로, 2022년 대비 8.5% 증가했다. 이는 OECD 국가 중 자살률 1위에 해당하며, OECD 평균의 두 배 이상에 달하는 수준이다.자살 위험을 높이는 주요 요인 중 하나로는 우울증이 꼽힌다. 2015년부터 2023년까지 9개년에 걸쳐 자살사망자 1099례를 대상으로 한 심리부검 결과(보건복지부∙한국생명존중희망재단 2023 심리부검 면담 결과 보고서) 86.3%가 사망 전 정신질환을 앓았을 것으로 추정되며, 이 중 74.5%는 우울장애로 파악됐다.또 정신질환이 있었던 것으로 추정된 자살사망자 중 60.5%는 사망 전 정신건강 문제로 치료 또는 상담받은 경험이 있었다.조성준 강북삼성병원 정신건강의학과 교수는 "한국에서 우울증 100만명 시대를 넘어서는 등 다른 국가에 비해 훨씬 높은 것을 볼수가 있다"며 "우울증의 경우 병의 유무를 정확하게 딱 떨어지는 것이 어렵기 때문에 치료에서도 어려움이 있다"고 설명했다.조 교수에 따르면 주요 우울장애란 최소 2주 이상 지속되는 우울감 및 흥미 저하를 비롯한 여러 신체 증상으로 심각한 일상적 기능 저하가 동반되는 것을 의미한다. 이들 가운데 약 3명 중 1명은 다양한 항우울제 치료에 반응하지 않는 치료저항성 우울증 환자일 수 있다.치료저항성 우울증은 보편적으로는 '최소 두 가지 이상의 경구 항우울제를 충분한 용량으로 적절한 기간 동안 투여하였음에도 불구하고 임상적 반응이 나타나지 않는 경우'로 정의된다.조 교수는 "TRD 환자는 일반 우울증환자보다 40% 이상의 의료비를 더 지출하고, 치료가 어려울뿐만 아니라 재발률또한 일반우울증 환자에 비해 높게 나타난다"며 "직업 유지가 어려운 중증의 환자는 경제적 부담이 더 커지는 악순환이 발생할 수 있다"고 말했다.다만, 치료저항성 우울증에는 현재까지 보편적으로 표준화된 치료법이 존재하지 않는다.치료저항성 우울증의 치료에는 항우울제의 최적화, 교체 혹은 병합, 강화요법 등의 약물치료를 비롯하여 경두개자기자극술(rTMS), 전기경련치료(ECT)등을 사용할 수 있다. 그러나 기존 약물치료는 관해에 도달하기까지 시간이 걸려 자살 충동에 대한 즉각적인 대응을 기대하기 어려운 상황이다.기존의 우울증 치료는 관해에 도달하기까지 약 37일~51일이 소요되어 치료의 골든 타임을 놓치기 쉬우며, 치료가 실패를 겪을수록 관해율이 크게 감소했다.치료저항성 우울증 치료에 대한 빠르고 효과적인 치료의 필요성이 높아지고 있는 가운데 스프라바토(에스케타민염산염)의 역할도 주목받고 있다.국내에서 치료저항성 우울증을 적응증으로 허가받은 유일한 약제다. 스프라바토는 세로토닌, 노르에피네프린을 타깃으로 하는 기존 항우울제들과 다르게 NMDA 수용체에 작용하는 새로운 기전의 항우울제다.스프라바토는 연구 결과 치료 저항성 우울증 환자에서 투여 후 24시간 내에 임상적으로 의미 있는 증상 개선을 나타냈으며, 투여 28일 차 52.5%의 관해율을 보였다. 또 16주간 스프라바토 투여 후 안정적인 관해를 보였던 환자군에서 약제를 지속 투여할 경우, 재발 위험을 51% 감소시켰다.조 교수는 "스프라바토를 투여하고 한 달 정도 지났을 대 유도기를 지났을 때 절반 이상의 환자가 반응을 보인걸 넘어서 관해상태에 도달했다"며 "특히 투여 직후 혹은 다음날부터 증상이 개선되는 등 효과가 빠르게 나타나는 점도 주목되는 부분"이라고 말했다.하지만 비급여로 스프라바토는 1회당 약 40만원의 비용이 드는것으로 알려져 있다.통상 한 번 치료 시 2개가 투여되어 한 회에 약 80만 원이 들며, 초기에는 주 2회 투여가 일반적이므로 1주일 치료 비용이 약 160만원 달해 환자 입장에서는 접근성에 제한이 생길 수 밖에 없다.현재 국내 자살예방정책에서 자살 고위험군에 대한 관리는 자살 시도에 따른 손상 치료비 지원, 자살시도자 및 유족의 상담 및 사례관리에 그치는 상황이다.장기적으로 자살 예방에 이를 수 있는 실질적인 치료까지 이어지는 통합적인 보건 서비스의 제공이 필요하다는 게 조 교수의 의견이다.조 교수는 "임상현장에서 스프라바토가 현실적으로 자살률을 낮추는데 기여할 수 있을 것 같다는 이야기를 한다"며 "하지만 실제 처방으로 연결되기까지 비용적인 측면에서 처방의 허들이 존재할수밖에 없다"고 밝혔다.이어 그는 "국내에서도 전라북도정신건강복지센터에서 주요 우울장애 환자를 대상으로 스프라바토 치료비 지원사업을 시행하는 등 변화가 나타나고 있다. 적극적인 치료를 이어나갈 수 있는 변화가 필요하다"고 덧붙였다.2025-09-10 06:08:47황병우
표준치료 없는 치료저항성 우울증…스프라바토 해법될까[데일리팜=황병우 기자] 한국이 OECD 국가중 자살률 1위를 기록하고 있는 가운데 '치료저항성 우울증' 치료지원의 필요성이 강조되고 있다.특히 일반적인 우울증보다 자살 시도가 7배 더 높은 것으로 알려진 치료저항성 우울증 치료를 위한 대안이 필요하다는 게 전문가의 입장이다.한국얀센은 9일 세계 자살예방의 날을 맞아 마스터클래스를 열고 치료저항성 우울증(TRD)의 실태와 최신 치료지견을 공유했다.조성준 강북삼성병원 정신건강의학과 교수통계청 '2023년 사망원인통계'에 따르면 2023년 한 해 자살로 1만3978명이 사망했다. 2023년의 인구 10만 명당 자살률은 27.3명으로, 2022년 대비 8.5% 증가했다. 이는 OECD 국가 중 자살률 1위에 해당하며, OECD 평균의 두 배 이상에 달하는 수준이다.자살 위험을 높이는 주요 요인 중 하나로는 우울증이 꼽힌다. 2015년부터 2023년까지 9개년에 걸쳐 자살사망자 1099례를 대상으로 한 심리부검 결과(보건복지부∙한국생명존중희망재단 2023 심리부검 면담 결과 보고서) 86.3%가 사망 전 정신질환을 앓았을 것으로 추정되며, 이 중 74.5%는 우울장애로 파악됐다.또 정신질환이 있었던 것으로 추정된 자살사망자 중 60.5%는 사망 전 정신건강 문제로 치료 또는 상담받은 경험이 있었다.조성준 강북삼성병원 정신건강의학과 교수는 "한국에서 우울증 100만명 시대를 넘어서는 등 다른 국가에 비해 훨씬 높은 것을 볼수가 있다"며 "우울증의 경우 병의 유무를 정확하게 딱 떨어지는 것이 어렵기 때문에 치료에서도 어려움이 있다"고 설명했다.조 교수에 따르면 주요 우울장애란 최소 2주 이상 지속되는 우울감 및 흥미 저하를 비롯한 여러 신체 증상으로 심각한 일상적 기능 저하가 동반되는 것을 의미한다. 이들 가운데 약 3명 중 1명은 다양한 항우울제 치료에 반응하지 않는 치료저항성 우울증 환자일 수 있다.치료저항성 우울증은 보편적으로는 '최소 두 가지 이상의 경구 항우울제를 충분한 용량으로 적절한 기간 동안 투여하였음에도 불구하고 임상적 반응이 나타나지 않는 경우'로 정의된다.조 교수는 "TRD 환자는 일반 우울증환자보다 40% 이상의 의료비를 더 지출하고, 치료가 어려울뿐만 아니라 재발률또한 일반우울증 환자에 비해 높게 나타난다"며 "직업 유지가 어려운 중증의 환자는 경제적 부담이 더 커지는 악순환이 발생할 수 있다"고 말했다.다만, 치료저항성 우울증에는 현재까지 보편적으로 표준화된 치료법이 존재하지 않는다.치료저항성 우울증의 치료에는 항우울제의 최적화, 교체 혹은 병합, 강화요법 등의 약물치료를 비롯하여 경두개자기자극술(rTMS), 전기경련치료(ECT)등을 사용할 수 있다. 그러나 기존 약물치료는 관해에 도달하기까지 시간이 걸려 자살 충동에 대한 즉각적인 대응을 기대하기 어려운 상황이다.기존의 우울증 치료는 관해에 도달하기까지 약 37일~51일이 소요되어 치료의 골든 타임을 놓치기 쉬우며, 치료가 실패를 겪을수록 관해율이 크게 감소했다.치료저항성 우울증 치료에 대한 빠르고 효과적인 치료의 필요성이 높아지고 있는 가운데 스프라바토(에스케타민염산염)의 역할도 주목받고 있다.국내에서 치료저항성 우울증을 적응증으로 허가받은 유일한 약제다. 스프라바토는 세로토닌, 노르에피네프린을 타깃으로 하는 기존 항우울제들과 다르게 NMDA 수용체에 작용하는 새로운 기전의 항우울제다.스프라바토는 연구 결과 치료 저항성 우울증 환자에서 투여 후 24시간 내에 임상적으로 의미 있는 증상 개선을 나타냈으며, 투여 28일 차 52.5%의 관해율을 보였다. 또 16주간 스프라바토 투여 후 안정적인 관해를 보였던 환자군에서 약제를 지속 투여할 경우, 재발 위험을 51% 감소시켰다.조 교수는 "스프라바토를 투여하고 한 달 정도 지났을 대 유도기를 지났을 때 절반 이상의 환자가 반응을 보인걸 넘어서 관해상태에 도달했다"며 "특히 투여 직후 혹은 다음날부터 증상이 개선되는 등 효과가 빠르게 나타나는 점도 주목되는 부분"이라고 말했다.하지만 비급여로 스프라바토는 1회당 약 40만원의 비용이 드는것으로 알려져 있다.통상 한 번 치료 시 2개가 투여되어 한 회에 약 80만 원이 들며, 초기에는 주 2회 투여가 일반적이므로 1주일 치료 비용이 약 160만원 달해 환자 입장에서는 접근성에 제한이 생길 수 밖에 없다.현재 국내 자살예방정책에서 자살 고위험군에 대한 관리는 자살 시도에 따른 손상 치료비 지원, 자살시도자 및 유족의 상담 및 사례관리에 그치는 상황이다.장기적으로 자살 예방에 이를 수 있는 실질적인 치료까지 이어지는 통합적인 보건 서비스의 제공이 필요하다는 게 조 교수의 의견이다.조 교수는 "임상현장에서 스프라바토가 현실적으로 자살률을 낮추는데 기여할 수 있을 것 같다는 이야기를 한다"며 "하지만 실제 처방으로 연결되기까지 비용적인 측면에서 처방의 허들이 존재할수밖에 없다"고 밝혔다.이어 그는 "국내에서도 전라북도정신건강복지센터에서 주요 우울장애 환자를 대상으로 스프라바토 치료비 지원사업을 시행하는 등 변화가 나타나고 있다. 적극적인 치료를 이어나갈 수 있는 변화가 필요하다"고 덧붙였다.2025-09-10 06:08:47황병우 -
 '브린텔릭스', 10년 간 항우울제 시장 입지 굳건[데일리팜=어윤호 기자] '브린텔릭스'가 항우울제 시장에서 10년 간 굳건한 입지를 구축하고 있다. 제네릭 진입 등 이슈에도 흔들리지 않는 모양새다.관련 업계에 따르면 한국룬드벡의 브린텔릭스(보티옥세틴)는 항우울제 시장에서 지난 10년간 지속적으로 성장을 해왔으며, 2025년 1분기 IQVIA 데이터 기준, 항우울제 시장에서 매출 2위를 기록했다.2015년 국내에 처음 도입된 브린텔릭스는 기존 항우울제인 선택적 세로토닌재흡수억제제(SSRI)나 세로토닌노르에피네프린재흡수억제제(SNRI)가 세로토닌 또는 노르에피네프린의 재흡수를 차단해 항우울 작용을 나타내던 것과는 차별화된다.브린텔릭스는 다양한 세로토닌 수용체에 작용함과 동시에 세로토닌 재흡수 억제를 하는 새로운 기전의 항우울제이다. 이를 통해 세로토닌뿐만 아니라 다양한 신경전달물질의 균형을 맞춰주고, 주요우울장애 환자의 우울 증상 개선뿐 아니라 인지 증상(집중력, 주의력, 학습 능력, 실행 능력) 개선 효과를 보여준다.실제 브린텔릭스는 주요우울장애 환자에서 나타나는 주의력 저하, 집중력 부족, 기억력 감퇴 등 인지 증상을 유의하게 개선하는 효과를 입증했다.아울러 우울증 환자의 동기부여 저하 및 에너지 부족 증상을 유의하게 개선하였고, 감정적 둔화 역시 통계적으로 의미 있게 개선하는 것으로 확인됐다.이러한 인지적·정서적 증상 개선 효과는 단기간 치료에만 국한되지 않았다. 브린텔릭스는 52주에 이르는 장기 연구를 통해 지속적인 항우울 효과를 입증했으며, 주요우울장애 환자의 재발률을 위약 대비 약 50% 낮춘 것으로 보고됐다.회사 관계자는 "브린텔릭스는 올해 국내 출시 10주년을 맞아, 축적된 임상 경험과 제품 신뢰를 바탕으로 더 많은 환자에게 도움을 줄 수 있도록 다양한 활동을 준비하고 있다. 앞으로도 환자 중심의 치료 옵션으로서 우울증 치료에 기여해 나갈 것이다"라고 밝혔다.2025-08-07 06:00:33어윤호
'브린텔릭스', 10년 간 항우울제 시장 입지 굳건[데일리팜=어윤호 기자] '브린텔릭스'가 항우울제 시장에서 10년 간 굳건한 입지를 구축하고 있다. 제네릭 진입 등 이슈에도 흔들리지 않는 모양새다.관련 업계에 따르면 한국룬드벡의 브린텔릭스(보티옥세틴)는 항우울제 시장에서 지난 10년간 지속적으로 성장을 해왔으며, 2025년 1분기 IQVIA 데이터 기준, 항우울제 시장에서 매출 2위를 기록했다.2015년 국내에 처음 도입된 브린텔릭스는 기존 항우울제인 선택적 세로토닌재흡수억제제(SSRI)나 세로토닌노르에피네프린재흡수억제제(SNRI)가 세로토닌 또는 노르에피네프린의 재흡수를 차단해 항우울 작용을 나타내던 것과는 차별화된다.브린텔릭스는 다양한 세로토닌 수용체에 작용함과 동시에 세로토닌 재흡수 억제를 하는 새로운 기전의 항우울제이다. 이를 통해 세로토닌뿐만 아니라 다양한 신경전달물질의 균형을 맞춰주고, 주요우울장애 환자의 우울 증상 개선뿐 아니라 인지 증상(집중력, 주의력, 학습 능력, 실행 능력) 개선 효과를 보여준다.실제 브린텔릭스는 주요우울장애 환자에서 나타나는 주의력 저하, 집중력 부족, 기억력 감퇴 등 인지 증상을 유의하게 개선하는 효과를 입증했다.아울러 우울증 환자의 동기부여 저하 및 에너지 부족 증상을 유의하게 개선하였고, 감정적 둔화 역시 통계적으로 의미 있게 개선하는 것으로 확인됐다.이러한 인지적·정서적 증상 개선 효과는 단기간 치료에만 국한되지 않았다. 브린텔릭스는 52주에 이르는 장기 연구를 통해 지속적인 항우울 효과를 입증했으며, 주요우울장애 환자의 재발률을 위약 대비 약 50% 낮춘 것으로 보고됐다.회사 관계자는 "브린텔릭스는 올해 국내 출시 10주년을 맞아, 축적된 임상 경험과 제품 신뢰를 바탕으로 더 많은 환자에게 도움을 줄 수 있도록 다양한 활동을 준비하고 있다. 앞으로도 환자 중심의 치료 옵션으로서 우울증 치료에 기여해 나갈 것이다"라고 밝혔다.2025-08-07 06:00:33어윤호 -
 화이자 비강분무제 급성 편두통 치료제 '자브즈프렛'7편: 비강분무 편두통 치료, 3세대 CGRP 수용체 길항제 자브즈프렛(Zavegepant)자브즈프렛(ZavzpretⓇ, zav-spret, 성분명: 자베게판트, Zavegepant, 화이자)은 3세대 칼시토닌 유전자 관련 펩타이드(calcitonin gene-related peptide, CGRP) 수용체 길항제로 2023년 3월 미국 FDA에서 편두통 급성치료에 승인을 받았다. 하지만 유럽 EMA에서는 아직 승인되지 않았다.편두통은 전 세계적으로 높은 유병률을 보이는 신경혈관성 질환으로, 삶의 질 저하와 함께 사회경제적 부담을 초래하는 주요 질환 중 하나이다. 이러한 편두통의 병태생리에는 다양한 신경전달물질과 경로가 관여한다. 이에 따라 칼시토닌 유전자 관련 펩타이드(CGRP)의 중심적인 역할이 주목받고 있다.CGRP는 강력한 혈관확장 작용을 지닌 신경펩타이드로, 삼차신경혈관계(trigeminovascular system)의 활성화와 함께 방출된다. 이어 경막혈관의 확장, 혈관주변 염증(perivascular inflammation) 및 통각수용체를 활성화시켜 편두통을 유발한다.이러한 CGRP를 표적으로 하는 약제로는 소분자 CGRP 수용체 길항제(Gepants)와 CGRP 수용체를 표적하는 단클론 항체(monoclonal Antibody)가 있다. 최초의 Gepant는 2019년 미국 FDA 승인을 받은 유브로게판트(Ubrogepant)이며, 이후, 리메게판트(Rimegepant), 아토게판트(Atogepant) 및 자베게판트(Zavegepant)가 승인되었다.자베게판트는 편두통 급성치료제로 승인 근거가 된 3상 임상에서, 1차 평가변수인 투약 2시간 후 통증의 완전한 개선을 달성한 환자의 비율이 자베게판트군에서 24%, 위약군에서 15%였다. 편두통 완화 효과는 빠르면 투약 15분 만에 나타났으며, 경구제제에 비해 빠른 효과를 보였다.Gepant 계열 약제는 스테로이드를 기반으로 하지 않으며, CGRP 수용체를 선택적으로 차단한다. 이들은 기존 Triptan 계열 약제와 달리 혈관 평활근의 5-HT₁B 수용체를 자극하지 않아 직접적인 혈관수축을 유발하지 않으며, 심혈관계 질환자에게서도 비교적 안전한 치료 대안으로 간주된다. 이러한 약리학적 특성은 편두통 치료에 있어 비스테로이드성, 비혈관수축성 기전에 기반한 새로운 치료 전략을 가능하게 하였다.편두통의 발생 기전은 무엇인가?전통적으로는 혈관 확장이 편두통의 주요 원인으로 간주되었으나, 최근의 연구들은 신경계의 기능적 이상, 혈관 반응, 면역계 및 후성유전적 조절이 상호 작용하는 복합 질환임으로 설명하고 있다.현대 편두통 기전의 핵심은 삼차신경혈관계(trigeminovascular system, TGVS)의 활성화이다. TGVS는 해부학적으로 경막 혈관을 지배하는 감각 신경들로 이루어져 있으며, 이 감각 신경들의 세포체는 삼차신경절(trigeminal ganglion)에 위치한다.(Figure 1)기능적으로 TGVS는 혈관 및 경막의 감각 자극을 감지하고, 이 정보를 중추신경계로 전달하며, 동시에 칼시토닌 유전자 관련 펩타이드(calcitonin gene-related peptide, CGRP)와 같은 염증 매개 신경펩타이드를 방출하여 신경성 염증 및 통증 전달을 조절하는 역할을 수행한다. 이 체계가 활성화되면 CGRP의 분비가 증가하고, 경막혈관의 확장이 유도된다. 얼굴과 머리의 통증은 주로 삼차신경의 첫 번째 가지인 눈신경(ophthalmic division)의 통각 구심성 신경(nociceptive afferents)에 의해 매개된다. 경막 감각 신경(meningeal sensory afferents)이 활성화되면, 이 자극은 삼차신경 척수핵(trigeminal nucleus caudalis)로 전달되며, 이후 통증 지각에 관여하는 전방 뇌 구조물(rostral brain structures)까지 전달된다.이 과정에서 삼차신경 말단에서 CGRP, Substance P, Neurokinin A와 같은 신경펩타이드가 방출되며, 혈관 확장과 함께 신경인성 염증(neurogenic inflammation)을 유발한다.이러한 신경-혈관 반응은 말초 통각 수용기의 민감도를 증가시키고, 시간이 경과함에 따라 중추 감작(central sensitization)으로 진행되어 두통의 지속 시간과 통증 강도를 증가시킨다. 중추 감작은 시상, 대뇌피질, 삼차신경계 신경핵에서 일어나며, 이로 인해 광선공포증, 음향공포증, 피부 과민(allodynia)과 같은 감각 과민 증상이 동반된다.또한 일부 환자에서 관찰되는 전조증상(aura)은 대뇌 피질에서 시작되는 피질 확산성 탈분극(cortical spreading depression, CSD)과 연관되며, 이는 시각피질에서부터 후두엽을 따라 진행되는 전기적 흥분 억제 현상으로 정의된다. CSD는 삼차신경계 자극과 혈관 반응을 촉진하며, 전조가 없는 환자에서도 유사한 신경생리학적 현상이 존재할 수 있음이 보고되고 있다.따라서, 삼차신경 내에서 가장 풍부하게 발현되는 신경펩타이드는 CGRP이며, 이는 삼차신경절 뉴런의 약 35~50%에서 발현된다. CGRP는 편두통 발작 중 정맥 내 농도가 유의하게 증가함이 확인되면서 중요한 병태생리적 매개 인자로 주목받고 있다. CGRP는 혈관을 확장시키고, 비만세포로부터 히스타민 분비를 유도하며, 신경절 내 질산 생성도 촉진하는 역할을 한다.CGRP(Calcitonin gene-related peptide, 칼시토닌 유전자-관련 펩타이드)는 어떤 물질인가?CGRP는 1982년, 칼시토닌 유전자(CALCA)의 mRNA 대체 스플라이싱을 통해 신경조직에서 유래된 37개의 아미노산 잔기로 구성된 신경펩타이드로 처음 분리되었으며, α-CGRP로 명명되었다.이후 CALCB 유전자로부터 유래되는 β-CGRP가 추가로 밝혀졌고, 인간에서는 이 두 아이소폼이 모두 존재한다. 이 중 병리적 의미에서 가장 주목받는 형태는 α-CGRP이며, 이는 특히 삼차신경 감각 신경계 및 통각 전달 경로에서 핵심적인 역할을 하는 것으로 알려져 있다.CGRP는 중추신경계(CNS)와 장신경계(enteric nervous system)에 광범위하게 발현되며, 수용체와의 결합을 위해 8~18번째 아미노산에 걸쳐 형성된 양친매성(양소수성) α-나선(amphiphilic α-helix) 구조를 가진다. CGRP 수용체는 조직별로 다양한 아형(subtypes)을 가지는 것으로 밝혀졌으며, 이는 약리학적 반응의 차이를 설명한다.분자생물학적으로는 G 단백질 연결 수용체(GPCR) B 계열에 속하는 칼시토닌 유사 수용체(calcitonin-like receptor, CLR)가 RAMP(receptor activity-modifying protein)와 이합체를 형성하여 수용체의 기능적 특성이 결정된다.예를 들어, CLR–RAMP1 복합체는 CGRP 수용체로, CLR–RAMP2 복합체는 아드레노메둘린(adrenomedullin) 수용체로 작용한다. 또한 RCP(receptor component protein)는 cAMP 신호전달 경로 활성화에 필수적인 요소로 작용한다.편두통 병태생리에서 CGRP는 특히 삼차혈관계와 밀접하게 연관된다. 삼차신경절(trigeminal ganglion)에 위치한 감각성 위단극성 뉴런(pseudounipolar sensory neuron)은 두개내 혈관 및 경막(dura)을 지배하며, 중심축삭은 삼차경부 복합체(trigeminocervical complex)로 투사되어 시상(thalamus) 및 고차 대뇌 피질로 통각 정보를 전달한다.CGRP의 분비는 주로 Ca²⁺-의존적인 소포성 경로를 통해 이루어진다. 감각 신경 말단에 활동전위가 도달하면 전압의존성 칼슘 채널이 개방되고, 세포 내 Ca²⁺ 농도가 급증한다. 이는 SNARE(soluble NSF attachment protein receptor) 복합체를 활성화시켜, CGRP가 저장된 소포가 세포막과 융합한 후, 외포작용(exocytosis)을 통해 CGRP가 분비된다.이러한 기전을 표적으로 한 여러 치료 전략이 임상적으로 활용되고 있다. 예를 들어, 트립탄 계열 약물은 세로토닌 5-HT₁B/₁D 수용체를 자극하여 presynaptic 칼슘 유입을 차단함으로써 CGRP 분비를 억제한다. 또한 보툴리눔 톡신 A형은 SNARE 복합체의 핵심 구성요소인 SNAP-25를 절단하여 소포 융합 자체를 저해함으로써 CGRP의 방출을 차단한다.그러나 최근 연구에서는 이러한 전통적인 Ca²⁺ 및 SNARE 의존 경로와는 별개의 CGRP 분비 경로의 존재 가능성이 제기되고 있다. 특히 감각 신경의 근위 축삭 말단(proximal axon terminal)에서는 외포 경로에 의존하지 않는 CGRP 분비가 확인되었으며, 이 부위에서는 트립탄(Triptan)이나 보툴리눔 톡신(botulinum toxin)에 대한 반응성이 낮은 것으로 나타났다.이러한 발견은 기존 치료제에 반응하지 않는 일부 편두통 환자의 존재를 설명하며, 단순한 분비 차단을 넘어, 수용체 수준에서의 CGRP 신호 전달 억제가 보다 효과적인 치료 전략이 될 수 있음을 시사한다.CGRP는 편두통에 어떤 영향을 미치는가?삼차신경혈관계(TGVS)를 구성하는 비수초화 감각 C 섬유(unmyelinated sensory C fibers)는 주로 경막과 뇌혈관에 분포하며, 그 축삭은 척수 및 뇌간의 삼차신경 척수로핵(spinal trigeminal nucleus caudalis)까지 연장되어 시냅스를 형성한다. 이들 섬유는 CGRP를 풍부하게 발현하고 있으며, 편두통 발작 시 CGRP의 방출이 핵심 병태생리 기전이라는 가설을 뒷받침한다.실제로 편두통 환자에서는 혈중 CGRP 농도가 유의하게 상승하며, 건강한 피험자에게 외인성 CGRP를 투여할 경우 편두통 유사 증상이 유발된다는 보고를 통해, CGRP의 병인적 역할이 점차 명확히 규명되고 있다.CGRP는 주로 혈관 평활근과 삼차신경 말단에 존재하는 CGRP 수용체(CGRP receptor, CGRP-R)를 통해 작용한다. 이러한 수용체는 중간 경막 동맥, 중대뇌동맥, 연질막 동맥, 천측 측두 동맥 등 주요 뇌혈관뿐만 아니라, 경막과 비강 부위를 지배하는 삼차신경 말단에도 분포하고 있어, CGRP가 말초에서 직접 작용하여 편두통을 유발함을 시사한다.편두통 발작 시 CGRP는 삼차신경계의 다양한 부위(경막의 구심성 말단, 삼차신경절 내 세포체, 연수 및 척수로 투사되는 원심성 섬유)에서 방출된다. 이 과정은 신경성 염증과 통증 전달 경로의 활성을 유도하는 중요한 기전으로 작용한다. 특히 CGRP는 경막 내 비만세포(mast cells) 및 대식세포(macrophages)를 유인하고, 국소 염증 반응을 촉진하여 통증 유발 환경을 조성한다.또한 CGRP는 삼차신경절 내 뉴런과 교세포(glial cells)를 활성화시켜 역행성 신호 전달(retrograde signaling)을 유도하고, 이는 말초 통각 수용기의 민감도를 증가시켜 말초 감작(peripheral sensitization)을 유발한다. 이러한 변화는 척수 배측각(dorsal horn)과 삼차신경 척수로핵에서의 중추 감작(central sensitization)으로 이어져, 통증 역치의 저하 및 과민 반응(hypersensitivity)을 유발하게 된다.더 나아가, CGRP는 삼차신경절 내 위성 교세포(satellite glial cells)를 자극하여 염증성 사이토카인과 신경영양인자(예: BDNF)의 분비를 촉진하고, 이들 분비물은 다시 뉴런의 CGRP 발현을 증가시키는 파라크린(paracrine) 기전을 형성하여 삼차신경계의 흥분성과 감작을 증폭시킨다.CGRP는 혈액-뇌 장벽(BBB)을 직접 통과하지는 않지만, 말초에서의 작용을 통해 중추 통각 경로(시상, 대상회, 대뇌 피질 등)에 간접적으로 영향을 미치며, 삼차신경핵 후방부(nucleus caudalis)로의 투사를 통해 글루타메이트(glutamate) 방출을 증가시켜 통증 전달을 더욱 강화하는 것으로 알려져 있다.편두통 치료제 중 국내에서 승인된 어떤 약제들이 있는가?편두통 치료에는 다양한 약제가 사용되며, 급성기 치료에는 비스테로이드성 항염증제(NSAIDs)와 경구용 세로토닌(5-하이드록시트립타민) 수용체 1B/1D 작용제인 트립탄이 사용된다. 반면, 항경련제, 항우울제, 항고혈압제, 보툴리눔 독소 등의 약물은 편두통 예방 목적으로 사용된다. 이러한 약제 중 상당수는 편두통 치료를 위해 특별히 개발된 것이 아니며, 다양한 부작용을 유발할 수 있고 작용 기전도 명확하지 않다. 또한 복약 순응도의 저하와 잦은 치료 변경으로 인해 이들 약물의 효과적인 사용에는 한계가 있다.1. 예방 치료토피라메이트(Topiramate)토피라메이트는 편두통 예방 치료의 1차 선택약제로 고려되며, 전간 치료에 사용하는 용량보다 낮은 1일 용량에서도 효과를 보인다. 이 약제는 삽화 편두통(episodic migraine)뿐만 아니라 만성 편두통 환자의 예방 치료에도 효과적인 것으로 입증되었으며, 약물 과용 두통이 동반된 경우에도 유용하게 사용될 수 있다.가장 흔한 부작용은 손발 저림(paresthesia)이며, 이 외에도 집중력 저하, 피로, 식욕 감소, 구역, 설사, 감각 저하, 복통 등의 부작용이 나타날 수 있다. 장기간 투여 시 체중 감소와 신결석이 발생할 수 있다.플루나리진(Flunarizine) 플루나리진은 칼슘채널차단제 중 비선택적 칼슘 통로 차단제로, 편두통 치료에 승인된 약물이다. 이 약제는 여러 임상시험에서 그 효과가 입증되었으며, 부작용으로는 체중 증가, 졸림, 구강 건조, 어지러움, 저혈압 등이 나타날 수 있다. 특히 장기간 투여 시 약물 유발 파킨슨 증후군(추체외로계 부작용)을 유발할 수 있으므로, 보행이 느려지거나 손떨림 증상이 발생하면 즉시 투약을 중단해야 한다.보툴리눔 독소 A형(Botulinum toxin A, BoNT-A) 보툴리눔 독소 A형(botulinum neurotoxin type A, BoNT-A)은 강력한 신경독소로, 혐기성 세균인 Clostridium botulinum에 의해 생성된다. 이 독소는 신경근 접합부에서 아세틸콜린의 분비를 차단함으로써 이완성 근마비를 유발한다. BoNT-A는 미국 FDA 및 국내에서 만성 편두통의 예방 치료제로 승인되었으며, 기존의 예방 약물에 반응하지 않는 만성 편두통 환자에서 선택적 치료 옵션이 될 수 있다.BoNT-A는 수개월간 지속되는 일시적인 화학적 탈신경(chemodenervation)을 유도하여, 전신적 부작용 위험은 최소화하면서 국소적으로 근육, 한선, 수축근 등의 기능을 감소시키거나 억제한다. 이 약제는 최초로 원숭이 모델에서 사시의 비수술적 치료를 위한 연구 중에 임상 적용 가능성이 보고되었다.BoNT-A는 연접전 신경 종말에 결합하여 아세틸콜린 분비를 차단함으로써 사시, 안검경련, 편측 안면경련, 경부 근긴장이상 등 과도한 근수축과 관련된 질환에 효과적이다. 최근에는 편두통을 포함한 다양한 형태의 두통, 요부 통증, 근막통증 증후군 등의 치료에 적용되고 있으며, 이는 단순한 근육 이완에 따른 이차적 진통 효과를 넘어서는 추가적인 작용 기전이 있음을 시사한다.BoNT-A는 말초 구심성 신경 말단에서 CGRP, substance P, glutamate 등의 통각 매개 물질 분비를 억제함으로써, 중추 삼차신경혈관계의 감작(sensitization)을 차단하는 기전을 통해 편두통 치료 효과를 발휘하는 것으로 알려져 있다.2. 급성기 치료 에르고타민(Ergotamine) 복합제 국내에서는 단일 성분의 Ergotamine 제제는 없으며, Ergotamine tartrate와 Caffeine의 복합제 형태로만 처방된다. 이 약제는 세로토닌 수용체인 5-HT₁ 및 5-HT₂ 수용체에 작용하여 혈관을 수축시키고, 경막의 신경성 염증을 억제하는 효과가 있다.혈관 수축 및 평활근 수축 작용을 가지므로, 말초혈관질환, 관상동맥질환, 신장 또는 간 기능 이상, 임신, 조절되지 않는 고혈압 등의 기저 질환이 있는 환자에게는 사용을 피해야 한다.경구 투여 시 흡수가 느리며, 구역, 구토, 복통, 손 저림, 설사 등의 위장관계 및 말초신경계 부작용이 나타날 수 있고, 드물게 사지 괴사와 같은 중대한 이상반응이 발생할 수 있다. 남용 시 약물 과용 두통(medication-overuse headache, MOH)으로 진행할 수 있으므로, 사용 빈도는 1주일에 2회 이하로 제한하는 것이 권장된다.이 약제는 편두통 급성기 치료에서 작용 지속 시간이 길어 재발률이 낮기 때문에, Triptan 제제를 사용한 후 재발이 문제가 되는 경우 효과적인 대안이 될 수 있다. 그러나 구역 및 구토 등 부작용이 흔하고, 독성 및 오용의 위험이 더 높다. Triptan 제제와는 병용해서는 안 되며, Triptan 복용 후 12시간이 경과한 이후에만 안전하게 사용할 수 있다. Triptan제(5-HT1B/1D 수용체 작용제) Triptan 계열 약제에는 수마트립탄(Sumatriptan), 졸미트립탄(Zolmitriptan), 나라트립탄(Naratriptan), 프로바트립탄(Frovatriptan), 알모트립탄(Almotriptan) 등이 있으며, 경구제, 피하주사제, 비강 내 투여제 등 다양한 제형으로 제공된다. 이들 약제는 세로토닌 수용체인 5-HT₁B/₁D 수용체에 선택적으로 작용하여, 확장된 두개혈관을 수축시키고, 혈관 주위 삼차신경 말단에서 신경펩타이드의 방출 및 삼차신경원의 활성화를 억제함으로써 신경인성 염증반응을 차단한다.이들 약제는 유사한 약리학적 기전을 공유하지만, 생체이용률(bioavailability), 혈중 반감기(half-life), 지방 친화도(lipophilicity), 약물상호작용(drug interactions) 등 약동학적 특성에서 차이를 보이므로, 각 환자의 편두통 양상에 따라 개별적으로 선택되어야 한다. 예를 들어, Tmax(최고 혈중농도에 도달하는 시간)가 짧을수록 약효 발현이 빠르고 급성기에 효과적이며, 반감기가 길수록 재발 빈도가 낮아지는 경향이 있다.Triptan 계열 약제는 모두 5-HT₁B/₁D 수용체에 선택적으로 작용하기 때문에, 기존의 비특이적 편두통 치료제에 비해 전신적 부작용이 적은 것이 장점이다. 그러나, 일시적으로 박동감, 저림, 비정상적인 감각, 흉부 압박감, 열감, 작열감, 냉감 등의 감각 이상 증상과 함께, 구역, 어지러움, 졸음, 피로감 등이 발생할 수 있다.이들 약제는 심장 관상동맥의 수축을 유발할 수 있으므로, 허혈성 심질환(협심증, 심근경색, 심근 허혈 등), 심장판막 질환, 부정맥(특히 빈맥) 등의 심혈관 질환이 있는 환자에게는 투여하지 않는다. 또한, 관상동맥 질환의 위험인자(당뇨병, 고혈압, 고지혈증, 가족력, 흡연 등)를 보유한 환자에게는 주의하여 사용하거나 가능한 경우 다른 약제로 대체하는 것이 바람직하다.또한, 에르고타민과 병용하거나 짧은 간격을 두고 투여하면 심각한 혈관 수축이 발생할 수 있으므로, 이들 약물과의 중복 투여는 피해야 한다. 아울러, SSRI(선택적 세로토닌 재흡수 억제제) 또는 SNRI(세로토닌-노르에피네프린 재흡수 억제제)를 복용 중인 환자에게는 세로토닌 증후군(serotonin syndrome) 발생 위험이 있으므로 주의가 필요하다. 이 증후군은 마비, 과다 반사, 운동 실조, 빈맥, 진전, 발한, 불안초조 등의 증상으로 나타날 수 있다.Ditan제(5-HT1F 수용체 작용제) 라스미디탄(Lasmiditan, 제품명: 레이보우정, LeyvowⓇ)은 최초의 경구용 선택적 5-HT₁F 수용체 작용제(Ditan 계열)로, 현재 국내에서는 ‘전조 증상의 동반 여부와 관계없이 편두통의 급성 치료’ 적응증으로 승인되어 있다.5-HT₁F 수용체는 삼차신경절, 삼차신경핵, 뇌혈관 등에 분포하며, 5-HT₁B 수용체와 달리 혈관 수축을 유발하지 않는 선택성을 가지기 때문에, Triptan 계열 약제에 비해 심혈관계 안전성이 높은 것이 특징이다. 또한, 5-HT₁F 수용체는 경막 주위에서의 신경인성 염증 억제와 삼차신경핵 내 신경세포 활성도 감소를 통해 항편두통 효과를 발휘한다.라스미디탄은 두통 완화율 및 완전 관해율 측면에서 위약 대비 유의한 치료 효과를 보였으며, 기존 Triptan 계열 약제에 반응하지 않던 환자군에서도 효과가 입증되었다. 무엇보다 Triptan 계열에서 흔히 나타나는 혈관 수축에 의한 심혈관계 부작용의 위험이 현저히 낮은 것이 중요한 장점으로 평가된다.CGRP 관련 약제 편두통 발병 과정에서 CGRP의 역할에 대한 이해는 CGRP 및 그 수용체를 표적으로 하는 약물의 개발로 이어졌다. 여기에는 CGRP 수용체를 표적하는 단클론 항체들과 CGRP 수용체 길항제 계열약제(Gepants)가 있다.(Figure 3)이들 약제는 표적 분자 및 치료 전략은 유사하지만, 약물 구조, 투여 방식, 작용 지속 시간 및 대사 경로 등에서 본질적인 차이를 보인다. 단클론 항체는 생물학적 제제로서 한 달 이상 작용할 수 있으며, 피하주사로 투여되며 면역학적 반응을 유발할 가능성이 있다.반면 소분자 약제는 빠른 작용과 경구/비강 투여의 편의성을 바탕으로 급성기 치료에 적합하며, 간에서 대사되고 전신 반감기가 짧은 특징이 있다.이들 약제는 Triptan과 작용 기전이 달라, 기존 약물에 반응이 없거나 부작용·금기가 있는 환자에서 대안으로 고려될 수 있다.CGRP 단클론 항체(monoclonal antibody, mAb)는 어떤 약제인가?CGRP는 말초뿐 아니라 중추신경계에서도 편두통의 유발 및 지속에 기여하는 신경펩타이드이다. 편두통 발작 시 환자의 혈중 및 타액 내 CGRP 농도가 유의하게 상승하는 것이 보고되었으며, 이러한 병태생리적 기전을 바탕으로 개발된 CGRP 표적 단클론 항체(mAb는 편두통 예방 치료에 새로운 전기를 마련한 치료 전략으로 주목받고 있다.이들 단클론 항체는 분자량이 매우 커 혈액-뇌 장벽(BBB)을 거의 통과하지 못하며, 주로 경막, 뇌혈관, 삼차신경절 등 말초 삼차신경계 구조를 표적으로 작용한다. 이러한 특성은 중추신경계에 대한 비특이적 영향을 최소화하면서 병리적 말초 경로에 선택적으로 작용할 수 있는 기전을 제공하며, 이에 따라 중추 관련 부작용을 감소시킬 수 있다는 중요한 임상적 이점을 갖는다.현재까지 개발된 CGRP 관련 항체는 크게 두 가지 계열로 나뉜다. CGRP 수용체를 표적으로 하는 에레누맙(Erenumab)은 수용체에 가역적으로 결합하여 리간드와의 결합을 차단하고, 반면 CGRP 리간드 자체를 중화하는 프레마네주맙(Fremanezumab), 갈카네주맙(Galcanezumab), 엡티네주맙(Eptinezumab)은 CGRP 펩타이드에 직접 결합하여 기능적 차단을 유도한다.이들 약제는 모두 미국 FDA로부터 편두통 예방 치료제로 승인되었으며, 특히 에레누맙은 2018년, 만성 및 삽화성 편두통 모두에 대해 최초로 승인된 단클론 항체이다. 국내에서는 프레마네주맙(아조비Ⓡ)과 갈카네주맙(앰갈리티Ⓡ)이 편두통 예방 적응증으로 승인되어 사용되고 있다.단클론 항체의 월 1회 또는 분기 1회 투여만으로도 치료 효과를 유지할 수 있다는 점이며, 이는 기존 예방 약제에 비해 복약 순응도 향상 및 지속적 관리의 용이성 측면에서 큰 이점을 제공한다. 또한, 높은 선택성과 긴 반감기를 기반으로 비특이적 신경계 억제 없이 표적 경로에 집중된 효과를 유도한다는 점에서 기존 예방제들과 차별화된다.CGRP는 강력한 혈관 확장 작용 외에도 혈류 조절, 염증 반응 조절, 조직 보호 등 다양한 생리적 기능에 관여한다. 일부 연구에서는 CGRP가 고혈압 상태에서 혈관을 보호하는 보상 기전으로 작용할 수 있으며, 이에 따라 고혈압 환자에서의 장기적 차단이 잠재적 위험이 될 수 있다는 우려가 제시되고 있다.그럼에도 불구하고, 현재까지의 임상시험 결과는 이러한 항체 치료제가 Triptan 또는 CGRP 길항제와 비교해도 관상동맥 연축이나 심혈관계 중대한 부작용 없이 안전하게 사용 가능함을 보여주고 있다.이처럼 CGRP 단클론 항체 치료제는 높은 표적 선택성, 낮은 투여 빈도, 우수한 안전성 프로파일을 바탕으로 편두통 예방 치료의 새로운 기준을 제시하고 있으며, 향후에는 장기적 안전성 평가 및 고위험군 환자에 대한 적용 가능성에 대한 후속 연구가 요구된다.CGRP 수용체 길항제(CGRP receptor antagonists)는 어떤 약제인가?기존의 대부분 편두통 예방 치료제는 흥분성 신경전달물질(예: glutamate)의 방출을 억제하거나 신경세포의 흥분성을 낮추어 빠른 시냅스 전달(fast synaptic transmission)을 차단함으로써 효과를 나타낸다. 반면, CGRP 경로를 표적으로 하는 약제는 느린 신경조절(slow neuromodulation)에 관여하며, 신경활성도 자체를 조절함으로써 편두통의 발생을 억제하는 새로운 작용 기전을 가진다.CGRP는 일반적으로 세포 내 Ca²⁺ 유입에 의해 활성화되는 SNARE 단백질 복합체를 통해 분비되며, 이는 소포의 세포막 도킹 및 융합을 통한 Ca²⁺ 의존적 외포(exocytosis) 과정이다.Triptan 계열 약제는 Ca²⁺ 신호전달을 억제하고, 보툴리눔 톡신 A형은 SNARE 복합체의 핵심인 SNAP-25 단백질을 절단하여 CGRP 분비를 차단한다. 그러나 일부 감각 신경 말단에서는 이와 무관한 비전형적 CGRP 분비 경로가 존재하는 것으로 보고되어, 기존 약제가 효과를 보이지 않는 일부 환자군의 기전을 설명하는 데 기여하고 있다.이러한 한계를 극복하기 위해 개발된 것이 Gepant 계열의 약제들이다. Gepants는 소분자 CGRP 수용체 길항제로서, 주 수용체 복합체인 CLR:RAMP1(canonical CGRP receptor)에 대해 높은 친화도를 가지며, 아드레노메둘린 수용체(adrenomedullin receptors, CLR:RAMP2 또는 CLR:RAMP3)에는 거의 결합하지 않는다.1세대 Gepant인 텔카게판트(Telcagepant)와 올세게판트(Olcegepant)는 CGRP 수용체에 대한 효능을 입증했으나, 간독성 문제와 제형 개발의 어려움으로 인해 상용화되지 못했다. 이후 개발된 2세대 gepants는 간 독성이 없고 경구용 제형으로 임상적 유용성이 높아졌다.2세대 Gepant인 유브로게판트(Ubrogepant), 리메게판트(Rimegepant), 아토게판트(Atogepant)는 경구 투여 제형이며, 각각 급성 치료(유브로게판트), 예방 치료(아토게판트), 또는 두 가지 모두(리메게판트)를 위해 개발되었다. 이들 약제는 효과적이며 간 독성을 보이지 않는다.미국 FDA는 2019년 우브로게판트(Ubrogepant)를 ‘급성 편두통 치료’, 2020년 리메가판트(Rimegepant)를 ‘편두통 예방 및 급성 치료’, 2021년 아토게판트(Atogepant)를 ‘편두통 예방’에 승인하였다. 국내에서는 리메게판트(Rimegepant, 제품명: 너텍 구강붕해정, Nurtec ODTⓇ)는 ‘1. 성인에서의 전조증상을 수반하거나 수반하지 않는 편두통의 급성치료 2. 성인에서의 삽화성 편두통의 예방’, 아토게팜트(Atogepant, 제픔명: 아큅타, AquiptaⓇ)는 ‘성인 18세 이상)에서의 편두통의 예방’에 승인되어 있다.3세대 Gepant로 분류되는 자베게판트(Zavegepant)는 최초의 비강 분무형 CGRP 수용체 길항제로 개발되었으며, 2023년 3월 미국 FDA로부터 급성기 편두통 치료제로 승인되었다. 이 약제는 비강분무제형(nasal spray)으로 속효성을 장점으로 하며 리메가판트(Rimegepant)와 동일 회사 약제이다.ODT(Orally Disintegrating Tablet)는 경구 투여제형으로 편리성과 예방/치료의 이중 용도가 장점인 반면, 급성 발작 시 구토, 오심 등으로 경구 복용이 어려운 환자가 존재한다. 이에 반해 구강 흡수가 필요 없는 비강분무제는 급성기에서 더 빠르고 효과적으로 작용한다.자베게판트는 어떤 약제인가? 자베게판트(Zavegepant, 제품명: 자브즈프렛 비강분무제, ZavzpretⓇ)는 CGRP 수용체에 선택적으로 결합하는 3세대 소분자 비펩타이드형 길항제(small-molecule non-peptide antagonist)로, 비강 투여(intranasal administration)를 목적으로 개발된 최초의 Gepant 계열 약제이다.자베게판트는 기존 Gepant 계열 약제들과 유사한 구조적 골격을 공유하지만, 비강용 스프레이(nasal spray) 제형으로 개발되어 속효성(rapid onset)을 극대화하기 위한 약물 전달 전략(drug delivery strategy)의 일환으로 설계되었다. 이는 특히 편두통 발작 시 구역 및 구토 증상으로 인해 경구 약물 복용이 어려운 환자군에서 유용한 치료 대안으로 평가된다.전임상 연구에서는 자베게판트가 인간 세포막에 발현된 CGRP 수용체에 대한 강력한 결합 억제 활성을 나타냈으며, 또한 인간 두개내 동맥(intracranial artery)의 ex vivo 모델에서 CGRP 유도 혈관 확장을 완전하고 강력하게 억제하는 효과가 확인되었다.자베게판트는 1회 투여량 10mg으로, 하루 1회 사용이 권장되며, 월 8회 초과 사용 시 안정성은 아직 확립되지 않았다. 따라서 사용 빈도에 대한 주의가 필요하다.자베게판트의 약리 기전은?자베게판트(Zavegepant)는 이 CGRP 수용체에 대해 고친화성(high affinity) 및 고선택성(high selectivity)을 나타내는 경쟁적 길항제(competitive antagonist)로, CGRP의 결합을 방해하여 해당 신호전달 경로(signal transduction pathway)를 차단한다.수용체 차단 시, Gαs 단백질을 통한 아데닐산 고리화효소(adenylyl cyclase) 활성화가 저해되고, 이로 인한 세포내 cAMP 생성 감소는 혈관 확장을 억제하며, substance P, neurokinin A 등의 염증성 신경전달물질의 방출을 저해하는 효과를 나타낸다.자베게판트는 기존의 경구용 Gepant 계열 약제와 달리, 비강 점막(nasal mucosa)을 통한 투과율이 우수하도록 설계되었다. 비강 분무 후 15~30분 이내에 혈중 최고 농도(Cmax)에 도달하며, 일회통과 대사(first-pass metabolism)를 회피함으로써 절대 생체이용률(bioavailability)이 높고, 보다 빠른 약효 발현이 가능하다.또한 Gepant 계열 약제는 일반적으로 지용성(lipophilic)이 강해 체내 지방조직에 축적되는 경향이 있으며, 이로 인해 고체중 환자에서 유효 혈중 농도 감소 및 치료 반응 저하가 보고될 수 있다. 반면, 자베게판트는 비강 점막을 통한 국소 삼차신경 말단 전달이 가능하므로, 체중에 영향을 받지 않는 균일한 치료 효과가 기대된다.자베게판트는 일부 혈액-뇌장벽(BBB)을 통과할 수 있는 것으로 알려져 있으며, 이에 따라 말초뿐 아니라 중추의 CGRP 수용체에도 작용 가능성이 제기되고 있다. 그러나 대부분의 약리 작용은 말초 삼차신경계 및 경막혈관계 수준에서 이루어진다. 혈장 단백 결합율은 중등도(moderate)이며, 체내 조직 분포(distribution)는 빠르고 광범위한 것으로 보고되었다. 자베게판트(ZAVZPRETⓇ)의 허가임상은 어떠한가?성인에서 전조(aura)의 유무와 관계없이 급성 편두통 치료를 위한 ZAVZPRET의 유효성은, 두 건의 무작위배정, 이중눈가림, 위약대조 임상시험(Study 1 및 Study 2)을 통해 입증되었다.두 연구 모두에서, 환자들은 중등도에서 중증의 편두통 발작 발생 시 시험약을 투여하도록 지시받았으며, 구제 약물(예: NSAIDs, 아세트아미노펜, 항구토제)은 초기 투여 후 2시간 이후부터 허용되었다. 반면, Triptan 등 다른 형태의 구제 약물은 초기 투여 후 48시간 이내 사용이 제한되었다.Study 1 및 Study 2에서 각각 13.4% 및 13.6%의 환자가 연구 시작 당시 편두통 예방 약물을 복용 중이었으나, CGRP 경로에 작용하는 예방 치료제는 포함되지 않았다.Study 1에서는 환자들이 ZAVZPRET 10mg(n=623) 또는 위약(n=646)을 단회 투여받도록 무작위 배정되었다. ZAVZPRET의 유효성은 투여 후 2시간 시점에서의 두통 완전 소실(pain freedom)과 가장 성가신 증상(MBS, Most Bothersome Symptom) 소실이라는 공동 주요 평가변수(co-primary endpoints)에서 위약 대비 통계적으로 유의한 개선 효과를 보이며 입증되었다.두통 완전 소실은 중등도 또는 중증의 두통이 무통 상태로 완화된 것으로 정의되며, MBS 소실은 환자가 사전에 보고한 가장 성가신 증상(예: 광공포증, 음향공포증, 오심) 중 해당 증상이 투여 2시간 후 소실된 경우로 정의되었다.투약 직전 가장 흔한 MBS는 광공포증(photophobia, 55%), 오심(nausea, 28%), 음향공포증(phonophobia, 16%) 순으로 보고되었다.결과적으로, Study 1에서 ZAVZPRET를 투여받은 환자군은 위약군에 비해 단일 투여 2시간 후 두통 완전 소실 및 MBS 소실을 달성한 비율이 통계적으로 유의하게 높았다(Table 2 참조). Study 1에서는 ZAVZPRET가 위약에 비해 다음과 같은 추가적인 유효성 평가 지표에서도 통계적으로 유의한 효과를 보였다: 투여 2시간 후 통증 완화, 투여 2시간 후 정상적인 기능 회복, 투여 2~48시간 동안 지속적인 통증 소실(Table 3 참조), 투여 2시간 후 음향과민 및 광과민 소실.여기서 통증 완화(pain relief)는 편두통 통증의 강도가 중등도 또는 중증에서 경도 또는 무통 상태로 완화된 것을 의미한다.또한, 투여 2시간 후 정상적인 기능 회복(normal function)에 대한 평가는 단일 항목 설문지를 통해 측정되었으며, 환자들은 아래 네 가지 중 하나를 선택하도록 하였다: 정상적인 기능(normal function), 경미한 기능 장애(mild impairment), 심한 기능 장애(severe impairment), 침상 안정이 필요한 상태(required bedrest). ZAVZPRET 10mg 투여 후 광공포증 및 음향공포증의 발생률은 위약에 비해 감소하였다.Study 2에서는 환자들이 ZAVZPRET 10mg(n=391) 또는 위약(n=401)을 단회 투여받도록 무작위 배정되었다. Study 2에서도 ZAVZPRET 10mg은 단일 투여 2시간 후 두통 완전 소실(pain freedom) 및 가장 성가신 증상(MBS: Most Bothersome Symptom) 소실이라는 공동 주요 평가변수에서 위약 대비 통계적으로 유의한 유효성을 보였다.두통 완전 소실은 ZAVZPRET 투여군에서 22.5%, 위약군에서 15.5%의 환자에서 관찰되었으며, 통계적으로 유의한 차이를 보였다(p=0.011).MBS 소실은 ZAVZPRET 투여군에서 41.9%, 위약군에서 33.7%로 나타났으며, 역시 유의한 차이를 보였다(p=0.016).투약 전 환자들이 보고한 가장 흔한 MBS는 광공포증(53%), 오심(31%), 음향공포증(15%) 순이었다. 자베게판트의 예상되는 쟁점은?Gepant 계열 약제는 심혈관계 부작용이 거의 없는 새로운 작용기전을 가지며, CGRP 수용체를 직접 차단함으로써 보다 선택적인 신경조절을 가능하게 한다. 이로 인해 Triptan 계열 약제의 사용이 제한되는 환자군에게 있어 안전하고 효과적인 대체 치료제이다.이 중 자베게판트는 유일하게 비강 분무 제형(nasal spray)으로 개발된 약제로 주목받고 있다. 편두통 발작 시 자주 동반되는 구역감, 구토 등으로 인한 경구 약제 복용의 어려움을 극복할 수 있는 대안으로, 비강 점막을 통한 약물 전달은 빠른 흡수 및 작용 발현을 가능하게 하여, 급성기 치료에서 임상적으로 유의미한 이점을 제공할 수 있다.그러나 이러한 비강 제형의 우월성에 대한 근거는 아직 제한적이다. 현재까지 Gepant 계열 약제 간의 직접 비교 임상시험(head-to-head trial)은 수행되지 않았으며, 약물동태학적 특성의 차이와 임상 반응성 간의 상관관계에 대한 연구 역시 부족하다. 특히 성별, 체질량지수(BMI), 유전적 요인 등 개별 환자 특성에 따라 이들 약제의 효과 및 부작용 프로파일이 어떻게 달라질 수 있는지에 대한 정보는 충분하지 않다.자베게판트의 비강 분무 제형은 약물이 간에서 분해되거나 체중에 따라 흡수 속도가 달라지는 문제를 어느 정도 줄일 수 있는 장점이 있다. 그러나 실제 임상 현장에서 이 약제가 얼마나 효과적이고 안전한지는 앞으로 더 많은 연구를 통해 확인될 필요가 있다.자베게판트의 임상시험에서는 미각 장애, 비강 불편감, 인후 자극감 등의 경미한 이상반응이 보고되었으며, 장기적인 비점막에 대한 영향은 아직 충분히 규명되지 않았다. 또한, CGRP가 비강 점막 혈관에 미치는 생리적 기능에 대한 이해도 제한적인 상황이다.따라서 비강 제형 자베게판트의 효과와 안전성에 대한 종합적인 평가, 투여 대상 환자군의 최적화, 그리고 개별 맞춤 치료 전략의 수립은 향후 편두통 치료의 패러다임을 확장하는 데 있어 중요한 과제가 될 것이다.참고문헌 1. Andrew Blumenfeld et al. “Hypervigilance, Allostatic Load, and Migraine Prevention: Antibodies to CGRP or Receptor” Neurol Ther. Volume 10, 469–497(2021). 2. Tessa de Vries et al. “Pharmacological treatment of migraine: CGRP and 5-HT beyond the triptans” Pharmacology & Therapeutics Volume 211, July 2020, Page 107528. 3. F A Russell et al. “Calcitonin gene-related peptide: physiology and pathophysiology” Physiol Rev 94: 1099–1142,(2014). 4. Boucherie et al. “Comparison of gepant effects at therapeutic plasma concentrations: connecting” The Journal of Headache and Pain (2024) 25:141. 5. Michael Thomas Eller et al. “Novel Calcitonin Gene-Related Peptide (CGRP) Interfering Migraine Therapies and Stroke—A Review” Int. J. Mol. Sci. 2024, 25(21), 11685. 6. Andrew F. Russo “ CALCITONIN GENE-RELATED PEPTIDE: A New Target for Migraine” Annu Rev Pharmacol Toxicol. 2015 ; 55: 533–552. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등).2025-07-11 06:47:54최병철 박사
화이자 비강분무제 급성 편두통 치료제 '자브즈프렛'7편: 비강분무 편두통 치료, 3세대 CGRP 수용체 길항제 자브즈프렛(Zavegepant)자브즈프렛(ZavzpretⓇ, zav-spret, 성분명: 자베게판트, Zavegepant, 화이자)은 3세대 칼시토닌 유전자 관련 펩타이드(calcitonin gene-related peptide, CGRP) 수용체 길항제로 2023년 3월 미국 FDA에서 편두통 급성치료에 승인을 받았다. 하지만 유럽 EMA에서는 아직 승인되지 않았다.편두통은 전 세계적으로 높은 유병률을 보이는 신경혈관성 질환으로, 삶의 질 저하와 함께 사회경제적 부담을 초래하는 주요 질환 중 하나이다. 이러한 편두통의 병태생리에는 다양한 신경전달물질과 경로가 관여한다. 이에 따라 칼시토닌 유전자 관련 펩타이드(CGRP)의 중심적인 역할이 주목받고 있다.CGRP는 강력한 혈관확장 작용을 지닌 신경펩타이드로, 삼차신경혈관계(trigeminovascular system)의 활성화와 함께 방출된다. 이어 경막혈관의 확장, 혈관주변 염증(perivascular inflammation) 및 통각수용체를 활성화시켜 편두통을 유발한다.이러한 CGRP를 표적으로 하는 약제로는 소분자 CGRP 수용체 길항제(Gepants)와 CGRP 수용체를 표적하는 단클론 항체(monoclonal Antibody)가 있다. 최초의 Gepant는 2019년 미국 FDA 승인을 받은 유브로게판트(Ubrogepant)이며, 이후, 리메게판트(Rimegepant), 아토게판트(Atogepant) 및 자베게판트(Zavegepant)가 승인되었다.자베게판트는 편두통 급성치료제로 승인 근거가 된 3상 임상에서, 1차 평가변수인 투약 2시간 후 통증의 완전한 개선을 달성한 환자의 비율이 자베게판트군에서 24%, 위약군에서 15%였다. 편두통 완화 효과는 빠르면 투약 15분 만에 나타났으며, 경구제제에 비해 빠른 효과를 보였다.Gepant 계열 약제는 스테로이드를 기반으로 하지 않으며, CGRP 수용체를 선택적으로 차단한다. 이들은 기존 Triptan 계열 약제와 달리 혈관 평활근의 5-HT₁B 수용체를 자극하지 않아 직접적인 혈관수축을 유발하지 않으며, 심혈관계 질환자에게서도 비교적 안전한 치료 대안으로 간주된다. 이러한 약리학적 특성은 편두통 치료에 있어 비스테로이드성, 비혈관수축성 기전에 기반한 새로운 치료 전략을 가능하게 하였다.편두통의 발생 기전은 무엇인가?전통적으로는 혈관 확장이 편두통의 주요 원인으로 간주되었으나, 최근의 연구들은 신경계의 기능적 이상, 혈관 반응, 면역계 및 후성유전적 조절이 상호 작용하는 복합 질환임으로 설명하고 있다.현대 편두통 기전의 핵심은 삼차신경혈관계(trigeminovascular system, TGVS)의 활성화이다. TGVS는 해부학적으로 경막 혈관을 지배하는 감각 신경들로 이루어져 있으며, 이 감각 신경들의 세포체는 삼차신경절(trigeminal ganglion)에 위치한다.(Figure 1)기능적으로 TGVS는 혈관 및 경막의 감각 자극을 감지하고, 이 정보를 중추신경계로 전달하며, 동시에 칼시토닌 유전자 관련 펩타이드(calcitonin gene-related peptide, CGRP)와 같은 염증 매개 신경펩타이드를 방출하여 신경성 염증 및 통증 전달을 조절하는 역할을 수행한다. 이 체계가 활성화되면 CGRP의 분비가 증가하고, 경막혈관의 확장이 유도된다. 얼굴과 머리의 통증은 주로 삼차신경의 첫 번째 가지인 눈신경(ophthalmic division)의 통각 구심성 신경(nociceptive afferents)에 의해 매개된다. 경막 감각 신경(meningeal sensory afferents)이 활성화되면, 이 자극은 삼차신경 척수핵(trigeminal nucleus caudalis)로 전달되며, 이후 통증 지각에 관여하는 전방 뇌 구조물(rostral brain structures)까지 전달된다.이 과정에서 삼차신경 말단에서 CGRP, Substance P, Neurokinin A와 같은 신경펩타이드가 방출되며, 혈관 확장과 함께 신경인성 염증(neurogenic inflammation)을 유발한다.이러한 신경-혈관 반응은 말초 통각 수용기의 민감도를 증가시키고, 시간이 경과함에 따라 중추 감작(central sensitization)으로 진행되어 두통의 지속 시간과 통증 강도를 증가시킨다. 중추 감작은 시상, 대뇌피질, 삼차신경계 신경핵에서 일어나며, 이로 인해 광선공포증, 음향공포증, 피부 과민(allodynia)과 같은 감각 과민 증상이 동반된다.또한 일부 환자에서 관찰되는 전조증상(aura)은 대뇌 피질에서 시작되는 피질 확산성 탈분극(cortical spreading depression, CSD)과 연관되며, 이는 시각피질에서부터 후두엽을 따라 진행되는 전기적 흥분 억제 현상으로 정의된다. CSD는 삼차신경계 자극과 혈관 반응을 촉진하며, 전조가 없는 환자에서도 유사한 신경생리학적 현상이 존재할 수 있음이 보고되고 있다.따라서, 삼차신경 내에서 가장 풍부하게 발현되는 신경펩타이드는 CGRP이며, 이는 삼차신경절 뉴런의 약 35~50%에서 발현된다. CGRP는 편두통 발작 중 정맥 내 농도가 유의하게 증가함이 확인되면서 중요한 병태생리적 매개 인자로 주목받고 있다. CGRP는 혈관을 확장시키고, 비만세포로부터 히스타민 분비를 유도하며, 신경절 내 질산 생성도 촉진하는 역할을 한다.CGRP(Calcitonin gene-related peptide, 칼시토닌 유전자-관련 펩타이드)는 어떤 물질인가?CGRP는 1982년, 칼시토닌 유전자(CALCA)의 mRNA 대체 스플라이싱을 통해 신경조직에서 유래된 37개의 아미노산 잔기로 구성된 신경펩타이드로 처음 분리되었으며, α-CGRP로 명명되었다.이후 CALCB 유전자로부터 유래되는 β-CGRP가 추가로 밝혀졌고, 인간에서는 이 두 아이소폼이 모두 존재한다. 이 중 병리적 의미에서 가장 주목받는 형태는 α-CGRP이며, 이는 특히 삼차신경 감각 신경계 및 통각 전달 경로에서 핵심적인 역할을 하는 것으로 알려져 있다.CGRP는 중추신경계(CNS)와 장신경계(enteric nervous system)에 광범위하게 발현되며, 수용체와의 결합을 위해 8~18번째 아미노산에 걸쳐 형성된 양친매성(양소수성) α-나선(amphiphilic α-helix) 구조를 가진다. CGRP 수용체는 조직별로 다양한 아형(subtypes)을 가지는 것으로 밝혀졌으며, 이는 약리학적 반응의 차이를 설명한다.분자생물학적으로는 G 단백질 연결 수용체(GPCR) B 계열에 속하는 칼시토닌 유사 수용체(calcitonin-like receptor, CLR)가 RAMP(receptor activity-modifying protein)와 이합체를 형성하여 수용체의 기능적 특성이 결정된다.예를 들어, CLR–RAMP1 복합체는 CGRP 수용체로, CLR–RAMP2 복합체는 아드레노메둘린(adrenomedullin) 수용체로 작용한다. 또한 RCP(receptor component protein)는 cAMP 신호전달 경로 활성화에 필수적인 요소로 작용한다.편두통 병태생리에서 CGRP는 특히 삼차혈관계와 밀접하게 연관된다. 삼차신경절(trigeminal ganglion)에 위치한 감각성 위단극성 뉴런(pseudounipolar sensory neuron)은 두개내 혈관 및 경막(dura)을 지배하며, 중심축삭은 삼차경부 복합체(trigeminocervical complex)로 투사되어 시상(thalamus) 및 고차 대뇌 피질로 통각 정보를 전달한다.CGRP의 분비는 주로 Ca²⁺-의존적인 소포성 경로를 통해 이루어진다. 감각 신경 말단에 활동전위가 도달하면 전압의존성 칼슘 채널이 개방되고, 세포 내 Ca²⁺ 농도가 급증한다. 이는 SNARE(soluble NSF attachment protein receptor) 복합체를 활성화시켜, CGRP가 저장된 소포가 세포막과 융합한 후, 외포작용(exocytosis)을 통해 CGRP가 분비된다.이러한 기전을 표적으로 한 여러 치료 전략이 임상적으로 활용되고 있다. 예를 들어, 트립탄 계열 약물은 세로토닌 5-HT₁B/₁D 수용체를 자극하여 presynaptic 칼슘 유입을 차단함으로써 CGRP 분비를 억제한다. 또한 보툴리눔 톡신 A형은 SNARE 복합체의 핵심 구성요소인 SNAP-25를 절단하여 소포 융합 자체를 저해함으로써 CGRP의 방출을 차단한다.그러나 최근 연구에서는 이러한 전통적인 Ca²⁺ 및 SNARE 의존 경로와는 별개의 CGRP 분비 경로의 존재 가능성이 제기되고 있다. 특히 감각 신경의 근위 축삭 말단(proximal axon terminal)에서는 외포 경로에 의존하지 않는 CGRP 분비가 확인되었으며, 이 부위에서는 트립탄(Triptan)이나 보툴리눔 톡신(botulinum toxin)에 대한 반응성이 낮은 것으로 나타났다.이러한 발견은 기존 치료제에 반응하지 않는 일부 편두통 환자의 존재를 설명하며, 단순한 분비 차단을 넘어, 수용체 수준에서의 CGRP 신호 전달 억제가 보다 효과적인 치료 전략이 될 수 있음을 시사한다.CGRP는 편두통에 어떤 영향을 미치는가?삼차신경혈관계(TGVS)를 구성하는 비수초화 감각 C 섬유(unmyelinated sensory C fibers)는 주로 경막과 뇌혈관에 분포하며, 그 축삭은 척수 및 뇌간의 삼차신경 척수로핵(spinal trigeminal nucleus caudalis)까지 연장되어 시냅스를 형성한다. 이들 섬유는 CGRP를 풍부하게 발현하고 있으며, 편두통 발작 시 CGRP의 방출이 핵심 병태생리 기전이라는 가설을 뒷받침한다.실제로 편두통 환자에서는 혈중 CGRP 농도가 유의하게 상승하며, 건강한 피험자에게 외인성 CGRP를 투여할 경우 편두통 유사 증상이 유발된다는 보고를 통해, CGRP의 병인적 역할이 점차 명확히 규명되고 있다.CGRP는 주로 혈관 평활근과 삼차신경 말단에 존재하는 CGRP 수용체(CGRP receptor, CGRP-R)를 통해 작용한다. 이러한 수용체는 중간 경막 동맥, 중대뇌동맥, 연질막 동맥, 천측 측두 동맥 등 주요 뇌혈관뿐만 아니라, 경막과 비강 부위를 지배하는 삼차신경 말단에도 분포하고 있어, CGRP가 말초에서 직접 작용하여 편두통을 유발함을 시사한다.편두통 발작 시 CGRP는 삼차신경계의 다양한 부위(경막의 구심성 말단, 삼차신경절 내 세포체, 연수 및 척수로 투사되는 원심성 섬유)에서 방출된다. 이 과정은 신경성 염증과 통증 전달 경로의 활성을 유도하는 중요한 기전으로 작용한다. 특히 CGRP는 경막 내 비만세포(mast cells) 및 대식세포(macrophages)를 유인하고, 국소 염증 반응을 촉진하여 통증 유발 환경을 조성한다.또한 CGRP는 삼차신경절 내 뉴런과 교세포(glial cells)를 활성화시켜 역행성 신호 전달(retrograde signaling)을 유도하고, 이는 말초 통각 수용기의 민감도를 증가시켜 말초 감작(peripheral sensitization)을 유발한다. 이러한 변화는 척수 배측각(dorsal horn)과 삼차신경 척수로핵에서의 중추 감작(central sensitization)으로 이어져, 통증 역치의 저하 및 과민 반응(hypersensitivity)을 유발하게 된다.더 나아가, CGRP는 삼차신경절 내 위성 교세포(satellite glial cells)를 자극하여 염증성 사이토카인과 신경영양인자(예: BDNF)의 분비를 촉진하고, 이들 분비물은 다시 뉴런의 CGRP 발현을 증가시키는 파라크린(paracrine) 기전을 형성하여 삼차신경계의 흥분성과 감작을 증폭시킨다.CGRP는 혈액-뇌 장벽(BBB)을 직접 통과하지는 않지만, 말초에서의 작용을 통해 중추 통각 경로(시상, 대상회, 대뇌 피질 등)에 간접적으로 영향을 미치며, 삼차신경핵 후방부(nucleus caudalis)로의 투사를 통해 글루타메이트(glutamate) 방출을 증가시켜 통증 전달을 더욱 강화하는 것으로 알려져 있다.편두통 치료제 중 국내에서 승인된 어떤 약제들이 있는가?편두통 치료에는 다양한 약제가 사용되며, 급성기 치료에는 비스테로이드성 항염증제(NSAIDs)와 경구용 세로토닌(5-하이드록시트립타민) 수용체 1B/1D 작용제인 트립탄이 사용된다. 반면, 항경련제, 항우울제, 항고혈압제, 보툴리눔 독소 등의 약물은 편두통 예방 목적으로 사용된다. 이러한 약제 중 상당수는 편두통 치료를 위해 특별히 개발된 것이 아니며, 다양한 부작용을 유발할 수 있고 작용 기전도 명확하지 않다. 또한 복약 순응도의 저하와 잦은 치료 변경으로 인해 이들 약물의 효과적인 사용에는 한계가 있다.1. 예방 치료토피라메이트(Topiramate)토피라메이트는 편두통 예방 치료의 1차 선택약제로 고려되며, 전간 치료에 사용하는 용량보다 낮은 1일 용량에서도 효과를 보인다. 이 약제는 삽화 편두통(episodic migraine)뿐만 아니라 만성 편두통 환자의 예방 치료에도 효과적인 것으로 입증되었으며, 약물 과용 두통이 동반된 경우에도 유용하게 사용될 수 있다.가장 흔한 부작용은 손발 저림(paresthesia)이며, 이 외에도 집중력 저하, 피로, 식욕 감소, 구역, 설사, 감각 저하, 복통 등의 부작용이 나타날 수 있다. 장기간 투여 시 체중 감소와 신결석이 발생할 수 있다.플루나리진(Flunarizine) 플루나리진은 칼슘채널차단제 중 비선택적 칼슘 통로 차단제로, 편두통 치료에 승인된 약물이다. 이 약제는 여러 임상시험에서 그 효과가 입증되었으며, 부작용으로는 체중 증가, 졸림, 구강 건조, 어지러움, 저혈압 등이 나타날 수 있다. 특히 장기간 투여 시 약물 유발 파킨슨 증후군(추체외로계 부작용)을 유발할 수 있으므로, 보행이 느려지거나 손떨림 증상이 발생하면 즉시 투약을 중단해야 한다.보툴리눔 독소 A형(Botulinum toxin A, BoNT-A) 보툴리눔 독소 A형(botulinum neurotoxin type A, BoNT-A)은 강력한 신경독소로, 혐기성 세균인 Clostridium botulinum에 의해 생성된다. 이 독소는 신경근 접합부에서 아세틸콜린의 분비를 차단함으로써 이완성 근마비를 유발한다. BoNT-A는 미국 FDA 및 국내에서 만성 편두통의 예방 치료제로 승인되었으며, 기존의 예방 약물에 반응하지 않는 만성 편두통 환자에서 선택적 치료 옵션이 될 수 있다.BoNT-A는 수개월간 지속되는 일시적인 화학적 탈신경(chemodenervation)을 유도하여, 전신적 부작용 위험은 최소화하면서 국소적으로 근육, 한선, 수축근 등의 기능을 감소시키거나 억제한다. 이 약제는 최초로 원숭이 모델에서 사시의 비수술적 치료를 위한 연구 중에 임상 적용 가능성이 보고되었다.BoNT-A는 연접전 신경 종말에 결합하여 아세틸콜린 분비를 차단함으로써 사시, 안검경련, 편측 안면경련, 경부 근긴장이상 등 과도한 근수축과 관련된 질환에 효과적이다. 최근에는 편두통을 포함한 다양한 형태의 두통, 요부 통증, 근막통증 증후군 등의 치료에 적용되고 있으며, 이는 단순한 근육 이완에 따른 이차적 진통 효과를 넘어서는 추가적인 작용 기전이 있음을 시사한다.BoNT-A는 말초 구심성 신경 말단에서 CGRP, substance P, glutamate 등의 통각 매개 물질 분비를 억제함으로써, 중추 삼차신경혈관계의 감작(sensitization)을 차단하는 기전을 통해 편두통 치료 효과를 발휘하는 것으로 알려져 있다.2. 급성기 치료 에르고타민(Ergotamine) 복합제 국내에서는 단일 성분의 Ergotamine 제제는 없으며, Ergotamine tartrate와 Caffeine의 복합제 형태로만 처방된다. 이 약제는 세로토닌 수용체인 5-HT₁ 및 5-HT₂ 수용체에 작용하여 혈관을 수축시키고, 경막의 신경성 염증을 억제하는 효과가 있다.혈관 수축 및 평활근 수축 작용을 가지므로, 말초혈관질환, 관상동맥질환, 신장 또는 간 기능 이상, 임신, 조절되지 않는 고혈압 등의 기저 질환이 있는 환자에게는 사용을 피해야 한다.경구 투여 시 흡수가 느리며, 구역, 구토, 복통, 손 저림, 설사 등의 위장관계 및 말초신경계 부작용이 나타날 수 있고, 드물게 사지 괴사와 같은 중대한 이상반응이 발생할 수 있다. 남용 시 약물 과용 두통(medication-overuse headache, MOH)으로 진행할 수 있으므로, 사용 빈도는 1주일에 2회 이하로 제한하는 것이 권장된다.이 약제는 편두통 급성기 치료에서 작용 지속 시간이 길어 재발률이 낮기 때문에, Triptan 제제를 사용한 후 재발이 문제가 되는 경우 효과적인 대안이 될 수 있다. 그러나 구역 및 구토 등 부작용이 흔하고, 독성 및 오용의 위험이 더 높다. Triptan 제제와는 병용해서는 안 되며, Triptan 복용 후 12시간이 경과한 이후에만 안전하게 사용할 수 있다. Triptan제(5-HT1B/1D 수용체 작용제) Triptan 계열 약제에는 수마트립탄(Sumatriptan), 졸미트립탄(Zolmitriptan), 나라트립탄(Naratriptan), 프로바트립탄(Frovatriptan), 알모트립탄(Almotriptan) 등이 있으며, 경구제, 피하주사제, 비강 내 투여제 등 다양한 제형으로 제공된다. 이들 약제는 세로토닌 수용체인 5-HT₁B/₁D 수용체에 선택적으로 작용하여, 확장된 두개혈관을 수축시키고, 혈관 주위 삼차신경 말단에서 신경펩타이드의 방출 및 삼차신경원의 활성화를 억제함으로써 신경인성 염증반응을 차단한다.이들 약제는 유사한 약리학적 기전을 공유하지만, 생체이용률(bioavailability), 혈중 반감기(half-life), 지방 친화도(lipophilicity), 약물상호작용(drug interactions) 등 약동학적 특성에서 차이를 보이므로, 각 환자의 편두통 양상에 따라 개별적으로 선택되어야 한다. 예를 들어, Tmax(최고 혈중농도에 도달하는 시간)가 짧을수록 약효 발현이 빠르고 급성기에 효과적이며, 반감기가 길수록 재발 빈도가 낮아지는 경향이 있다.Triptan 계열 약제는 모두 5-HT₁B/₁D 수용체에 선택적으로 작용하기 때문에, 기존의 비특이적 편두통 치료제에 비해 전신적 부작용이 적은 것이 장점이다. 그러나, 일시적으로 박동감, 저림, 비정상적인 감각, 흉부 압박감, 열감, 작열감, 냉감 등의 감각 이상 증상과 함께, 구역, 어지러움, 졸음, 피로감 등이 발생할 수 있다.이들 약제는 심장 관상동맥의 수축을 유발할 수 있으므로, 허혈성 심질환(협심증, 심근경색, 심근 허혈 등), 심장판막 질환, 부정맥(특히 빈맥) 등의 심혈관 질환이 있는 환자에게는 투여하지 않는다. 또한, 관상동맥 질환의 위험인자(당뇨병, 고혈압, 고지혈증, 가족력, 흡연 등)를 보유한 환자에게는 주의하여 사용하거나 가능한 경우 다른 약제로 대체하는 것이 바람직하다.또한, 에르고타민과 병용하거나 짧은 간격을 두고 투여하면 심각한 혈관 수축이 발생할 수 있으므로, 이들 약물과의 중복 투여는 피해야 한다. 아울러, SSRI(선택적 세로토닌 재흡수 억제제) 또는 SNRI(세로토닌-노르에피네프린 재흡수 억제제)를 복용 중인 환자에게는 세로토닌 증후군(serotonin syndrome) 발생 위험이 있으므로 주의가 필요하다. 이 증후군은 마비, 과다 반사, 운동 실조, 빈맥, 진전, 발한, 불안초조 등의 증상으로 나타날 수 있다.Ditan제(5-HT1F 수용체 작용제) 라스미디탄(Lasmiditan, 제품명: 레이보우정, LeyvowⓇ)은 최초의 경구용 선택적 5-HT₁F 수용체 작용제(Ditan 계열)로, 현재 국내에서는 ‘전조 증상의 동반 여부와 관계없이 편두통의 급성 치료’ 적응증으로 승인되어 있다.5-HT₁F 수용체는 삼차신경절, 삼차신경핵, 뇌혈관 등에 분포하며, 5-HT₁B 수용체와 달리 혈관 수축을 유발하지 않는 선택성을 가지기 때문에, Triptan 계열 약제에 비해 심혈관계 안전성이 높은 것이 특징이다. 또한, 5-HT₁F 수용체는 경막 주위에서의 신경인성 염증 억제와 삼차신경핵 내 신경세포 활성도 감소를 통해 항편두통 효과를 발휘한다.라스미디탄은 두통 완화율 및 완전 관해율 측면에서 위약 대비 유의한 치료 효과를 보였으며, 기존 Triptan 계열 약제에 반응하지 않던 환자군에서도 효과가 입증되었다. 무엇보다 Triptan 계열에서 흔히 나타나는 혈관 수축에 의한 심혈관계 부작용의 위험이 현저히 낮은 것이 중요한 장점으로 평가된다.CGRP 관련 약제 편두통 발병 과정에서 CGRP의 역할에 대한 이해는 CGRP 및 그 수용체를 표적으로 하는 약물의 개발로 이어졌다. 여기에는 CGRP 수용체를 표적하는 단클론 항체들과 CGRP 수용체 길항제 계열약제(Gepants)가 있다.(Figure 3)이들 약제는 표적 분자 및 치료 전략은 유사하지만, 약물 구조, 투여 방식, 작용 지속 시간 및 대사 경로 등에서 본질적인 차이를 보인다. 단클론 항체는 생물학적 제제로서 한 달 이상 작용할 수 있으며, 피하주사로 투여되며 면역학적 반응을 유발할 가능성이 있다.반면 소분자 약제는 빠른 작용과 경구/비강 투여의 편의성을 바탕으로 급성기 치료에 적합하며, 간에서 대사되고 전신 반감기가 짧은 특징이 있다.이들 약제는 Triptan과 작용 기전이 달라, 기존 약물에 반응이 없거나 부작용·금기가 있는 환자에서 대안으로 고려될 수 있다.CGRP 단클론 항체(monoclonal antibody, mAb)는 어떤 약제인가?CGRP는 말초뿐 아니라 중추신경계에서도 편두통의 유발 및 지속에 기여하는 신경펩타이드이다. 편두통 발작 시 환자의 혈중 및 타액 내 CGRP 농도가 유의하게 상승하는 것이 보고되었으며, 이러한 병태생리적 기전을 바탕으로 개발된 CGRP 표적 단클론 항체(mAb는 편두통 예방 치료에 새로운 전기를 마련한 치료 전략으로 주목받고 있다.이들 단클론 항체는 분자량이 매우 커 혈액-뇌 장벽(BBB)을 거의 통과하지 못하며, 주로 경막, 뇌혈관, 삼차신경절 등 말초 삼차신경계 구조를 표적으로 작용한다. 이러한 특성은 중추신경계에 대한 비특이적 영향을 최소화하면서 병리적 말초 경로에 선택적으로 작용할 수 있는 기전을 제공하며, 이에 따라 중추 관련 부작용을 감소시킬 수 있다는 중요한 임상적 이점을 갖는다.현재까지 개발된 CGRP 관련 항체는 크게 두 가지 계열로 나뉜다. CGRP 수용체를 표적으로 하는 에레누맙(Erenumab)은 수용체에 가역적으로 결합하여 리간드와의 결합을 차단하고, 반면 CGRP 리간드 자체를 중화하는 프레마네주맙(Fremanezumab), 갈카네주맙(Galcanezumab), 엡티네주맙(Eptinezumab)은 CGRP 펩타이드에 직접 결합하여 기능적 차단을 유도한다.이들 약제는 모두 미국 FDA로부터 편두통 예방 치료제로 승인되었으며, 특히 에레누맙은 2018년, 만성 및 삽화성 편두통 모두에 대해 최초로 승인된 단클론 항체이다. 국내에서는 프레마네주맙(아조비Ⓡ)과 갈카네주맙(앰갈리티Ⓡ)이 편두통 예방 적응증으로 승인되어 사용되고 있다.단클론 항체의 월 1회 또는 분기 1회 투여만으로도 치료 효과를 유지할 수 있다는 점이며, 이는 기존 예방 약제에 비해 복약 순응도 향상 및 지속적 관리의 용이성 측면에서 큰 이점을 제공한다. 또한, 높은 선택성과 긴 반감기를 기반으로 비특이적 신경계 억제 없이 표적 경로에 집중된 효과를 유도한다는 점에서 기존 예방제들과 차별화된다.CGRP는 강력한 혈관 확장 작용 외에도 혈류 조절, 염증 반응 조절, 조직 보호 등 다양한 생리적 기능에 관여한다. 일부 연구에서는 CGRP가 고혈압 상태에서 혈관을 보호하는 보상 기전으로 작용할 수 있으며, 이에 따라 고혈압 환자에서의 장기적 차단이 잠재적 위험이 될 수 있다는 우려가 제시되고 있다.그럼에도 불구하고, 현재까지의 임상시험 결과는 이러한 항체 치료제가 Triptan 또는 CGRP 길항제와 비교해도 관상동맥 연축이나 심혈관계 중대한 부작용 없이 안전하게 사용 가능함을 보여주고 있다.이처럼 CGRP 단클론 항체 치료제는 높은 표적 선택성, 낮은 투여 빈도, 우수한 안전성 프로파일을 바탕으로 편두통 예방 치료의 새로운 기준을 제시하고 있으며, 향후에는 장기적 안전성 평가 및 고위험군 환자에 대한 적용 가능성에 대한 후속 연구가 요구된다.CGRP 수용체 길항제(CGRP receptor antagonists)는 어떤 약제인가?기존의 대부분 편두통 예방 치료제는 흥분성 신경전달물질(예: glutamate)의 방출을 억제하거나 신경세포의 흥분성을 낮추어 빠른 시냅스 전달(fast synaptic transmission)을 차단함으로써 효과를 나타낸다. 반면, CGRP 경로를 표적으로 하는 약제는 느린 신경조절(slow neuromodulation)에 관여하며, 신경활성도 자체를 조절함으로써 편두통의 발생을 억제하는 새로운 작용 기전을 가진다.CGRP는 일반적으로 세포 내 Ca²⁺ 유입에 의해 활성화되는 SNARE 단백질 복합체를 통해 분비되며, 이는 소포의 세포막 도킹 및 융합을 통한 Ca²⁺ 의존적 외포(exocytosis) 과정이다.Triptan 계열 약제는 Ca²⁺ 신호전달을 억제하고, 보툴리눔 톡신 A형은 SNARE 복합체의 핵심인 SNAP-25 단백질을 절단하여 CGRP 분비를 차단한다. 그러나 일부 감각 신경 말단에서는 이와 무관한 비전형적 CGRP 분비 경로가 존재하는 것으로 보고되어, 기존 약제가 효과를 보이지 않는 일부 환자군의 기전을 설명하는 데 기여하고 있다.이러한 한계를 극복하기 위해 개발된 것이 Gepant 계열의 약제들이다. Gepants는 소분자 CGRP 수용체 길항제로서, 주 수용체 복합체인 CLR:RAMP1(canonical CGRP receptor)에 대해 높은 친화도를 가지며, 아드레노메둘린 수용체(adrenomedullin receptors, CLR:RAMP2 또는 CLR:RAMP3)에는 거의 결합하지 않는다.1세대 Gepant인 텔카게판트(Telcagepant)와 올세게판트(Olcegepant)는 CGRP 수용체에 대한 효능을 입증했으나, 간독성 문제와 제형 개발의 어려움으로 인해 상용화되지 못했다. 이후 개발된 2세대 gepants는 간 독성이 없고 경구용 제형으로 임상적 유용성이 높아졌다.2세대 Gepant인 유브로게판트(Ubrogepant), 리메게판트(Rimegepant), 아토게판트(Atogepant)는 경구 투여 제형이며, 각각 급성 치료(유브로게판트), 예방 치료(아토게판트), 또는 두 가지 모두(리메게판트)를 위해 개발되었다. 이들 약제는 효과적이며 간 독성을 보이지 않는다.미국 FDA는 2019년 우브로게판트(Ubrogepant)를 ‘급성 편두통 치료’, 2020년 리메가판트(Rimegepant)를 ‘편두통 예방 및 급성 치료’, 2021년 아토게판트(Atogepant)를 ‘편두통 예방’에 승인하였다. 국내에서는 리메게판트(Rimegepant, 제품명: 너텍 구강붕해정, Nurtec ODTⓇ)는 ‘1. 성인에서의 전조증상을 수반하거나 수반하지 않는 편두통의 급성치료 2. 성인에서의 삽화성 편두통의 예방’, 아토게팜트(Atogepant, 제픔명: 아큅타, AquiptaⓇ)는 ‘성인 18세 이상)에서의 편두통의 예방’에 승인되어 있다.3세대 Gepant로 분류되는 자베게판트(Zavegepant)는 최초의 비강 분무형 CGRP 수용체 길항제로 개발되었으며, 2023년 3월 미국 FDA로부터 급성기 편두통 치료제로 승인되었다. 이 약제는 비강분무제형(nasal spray)으로 속효성을 장점으로 하며 리메가판트(Rimegepant)와 동일 회사 약제이다.ODT(Orally Disintegrating Tablet)는 경구 투여제형으로 편리성과 예방/치료의 이중 용도가 장점인 반면, 급성 발작 시 구토, 오심 등으로 경구 복용이 어려운 환자가 존재한다. 이에 반해 구강 흡수가 필요 없는 비강분무제는 급성기에서 더 빠르고 효과적으로 작용한다.자베게판트는 어떤 약제인가? 자베게판트(Zavegepant, 제품명: 자브즈프렛 비강분무제, ZavzpretⓇ)는 CGRP 수용체에 선택적으로 결합하는 3세대 소분자 비펩타이드형 길항제(small-molecule non-peptide antagonist)로, 비강 투여(intranasal administration)를 목적으로 개발된 최초의 Gepant 계열 약제이다.자베게판트는 기존 Gepant 계열 약제들과 유사한 구조적 골격을 공유하지만, 비강용 스프레이(nasal spray) 제형으로 개발되어 속효성(rapid onset)을 극대화하기 위한 약물 전달 전략(drug delivery strategy)의 일환으로 설계되었다. 이는 특히 편두통 발작 시 구역 및 구토 증상으로 인해 경구 약물 복용이 어려운 환자군에서 유용한 치료 대안으로 평가된다.전임상 연구에서는 자베게판트가 인간 세포막에 발현된 CGRP 수용체에 대한 강력한 결합 억제 활성을 나타냈으며, 또한 인간 두개내 동맥(intracranial artery)의 ex vivo 모델에서 CGRP 유도 혈관 확장을 완전하고 강력하게 억제하는 효과가 확인되었다.자베게판트는 1회 투여량 10mg으로, 하루 1회 사용이 권장되며, 월 8회 초과 사용 시 안정성은 아직 확립되지 않았다. 따라서 사용 빈도에 대한 주의가 필요하다.자베게판트의 약리 기전은?자베게판트(Zavegepant)는 이 CGRP 수용체에 대해 고친화성(high affinity) 및 고선택성(high selectivity)을 나타내는 경쟁적 길항제(competitive antagonist)로, CGRP의 결합을 방해하여 해당 신호전달 경로(signal transduction pathway)를 차단한다.수용체 차단 시, Gαs 단백질을 통한 아데닐산 고리화효소(adenylyl cyclase) 활성화가 저해되고, 이로 인한 세포내 cAMP 생성 감소는 혈관 확장을 억제하며, substance P, neurokinin A 등의 염증성 신경전달물질의 방출을 저해하는 효과를 나타낸다.자베게판트는 기존의 경구용 Gepant 계열 약제와 달리, 비강 점막(nasal mucosa)을 통한 투과율이 우수하도록 설계되었다. 비강 분무 후 15~30분 이내에 혈중 최고 농도(Cmax)에 도달하며, 일회통과 대사(first-pass metabolism)를 회피함으로써 절대 생체이용률(bioavailability)이 높고, 보다 빠른 약효 발현이 가능하다.또한 Gepant 계열 약제는 일반적으로 지용성(lipophilic)이 강해 체내 지방조직에 축적되는 경향이 있으며, 이로 인해 고체중 환자에서 유효 혈중 농도 감소 및 치료 반응 저하가 보고될 수 있다. 반면, 자베게판트는 비강 점막을 통한 국소 삼차신경 말단 전달이 가능하므로, 체중에 영향을 받지 않는 균일한 치료 효과가 기대된다.자베게판트는 일부 혈액-뇌장벽(BBB)을 통과할 수 있는 것으로 알려져 있으며, 이에 따라 말초뿐 아니라 중추의 CGRP 수용체에도 작용 가능성이 제기되고 있다. 그러나 대부분의 약리 작용은 말초 삼차신경계 및 경막혈관계 수준에서 이루어진다. 혈장 단백 결합율은 중등도(moderate)이며, 체내 조직 분포(distribution)는 빠르고 광범위한 것으로 보고되었다. 자베게판트(ZAVZPRETⓇ)의 허가임상은 어떠한가?성인에서 전조(aura)의 유무와 관계없이 급성 편두통 치료를 위한 ZAVZPRET의 유효성은, 두 건의 무작위배정, 이중눈가림, 위약대조 임상시험(Study 1 및 Study 2)을 통해 입증되었다.두 연구 모두에서, 환자들은 중등도에서 중증의 편두통 발작 발생 시 시험약을 투여하도록 지시받았으며, 구제 약물(예: NSAIDs, 아세트아미노펜, 항구토제)은 초기 투여 후 2시간 이후부터 허용되었다. 반면, Triptan 등 다른 형태의 구제 약물은 초기 투여 후 48시간 이내 사용이 제한되었다.Study 1 및 Study 2에서 각각 13.4% 및 13.6%의 환자가 연구 시작 당시 편두통 예방 약물을 복용 중이었으나, CGRP 경로에 작용하는 예방 치료제는 포함되지 않았다.Study 1에서는 환자들이 ZAVZPRET 10mg(n=623) 또는 위약(n=646)을 단회 투여받도록 무작위 배정되었다. ZAVZPRET의 유효성은 투여 후 2시간 시점에서의 두통 완전 소실(pain freedom)과 가장 성가신 증상(MBS, Most Bothersome Symptom) 소실이라는 공동 주요 평가변수(co-primary endpoints)에서 위약 대비 통계적으로 유의한 개선 효과를 보이며 입증되었다.두통 완전 소실은 중등도 또는 중증의 두통이 무통 상태로 완화된 것으로 정의되며, MBS 소실은 환자가 사전에 보고한 가장 성가신 증상(예: 광공포증, 음향공포증, 오심) 중 해당 증상이 투여 2시간 후 소실된 경우로 정의되었다.투약 직전 가장 흔한 MBS는 광공포증(photophobia, 55%), 오심(nausea, 28%), 음향공포증(phonophobia, 16%) 순으로 보고되었다.결과적으로, Study 1에서 ZAVZPRET를 투여받은 환자군은 위약군에 비해 단일 투여 2시간 후 두통 완전 소실 및 MBS 소실을 달성한 비율이 통계적으로 유의하게 높았다(Table 2 참조). Study 1에서는 ZAVZPRET가 위약에 비해 다음과 같은 추가적인 유효성 평가 지표에서도 통계적으로 유의한 효과를 보였다: 투여 2시간 후 통증 완화, 투여 2시간 후 정상적인 기능 회복, 투여 2~48시간 동안 지속적인 통증 소실(Table 3 참조), 투여 2시간 후 음향과민 및 광과민 소실.여기서 통증 완화(pain relief)는 편두통 통증의 강도가 중등도 또는 중증에서 경도 또는 무통 상태로 완화된 것을 의미한다.또한, 투여 2시간 후 정상적인 기능 회복(normal function)에 대한 평가는 단일 항목 설문지를 통해 측정되었으며, 환자들은 아래 네 가지 중 하나를 선택하도록 하였다: 정상적인 기능(normal function), 경미한 기능 장애(mild impairment), 심한 기능 장애(severe impairment), 침상 안정이 필요한 상태(required bedrest). ZAVZPRET 10mg 투여 후 광공포증 및 음향공포증의 발생률은 위약에 비해 감소하였다.Study 2에서는 환자들이 ZAVZPRET 10mg(n=391) 또는 위약(n=401)을 단회 투여받도록 무작위 배정되었다. Study 2에서도 ZAVZPRET 10mg은 단일 투여 2시간 후 두통 완전 소실(pain freedom) 및 가장 성가신 증상(MBS: Most Bothersome Symptom) 소실이라는 공동 주요 평가변수에서 위약 대비 통계적으로 유의한 유효성을 보였다.두통 완전 소실은 ZAVZPRET 투여군에서 22.5%, 위약군에서 15.5%의 환자에서 관찰되었으며, 통계적으로 유의한 차이를 보였다(p=0.011).MBS 소실은 ZAVZPRET 투여군에서 41.9%, 위약군에서 33.7%로 나타났으며, 역시 유의한 차이를 보였다(p=0.016).투약 전 환자들이 보고한 가장 흔한 MBS는 광공포증(53%), 오심(31%), 음향공포증(15%) 순이었다. 자베게판트의 예상되는 쟁점은?Gepant 계열 약제는 심혈관계 부작용이 거의 없는 새로운 작용기전을 가지며, CGRP 수용체를 직접 차단함으로써 보다 선택적인 신경조절을 가능하게 한다. 이로 인해 Triptan 계열 약제의 사용이 제한되는 환자군에게 있어 안전하고 효과적인 대체 치료제이다.이 중 자베게판트는 유일하게 비강 분무 제형(nasal spray)으로 개발된 약제로 주목받고 있다. 편두통 발작 시 자주 동반되는 구역감, 구토 등으로 인한 경구 약제 복용의 어려움을 극복할 수 있는 대안으로, 비강 점막을 통한 약물 전달은 빠른 흡수 및 작용 발현을 가능하게 하여, 급성기 치료에서 임상적으로 유의미한 이점을 제공할 수 있다.그러나 이러한 비강 제형의 우월성에 대한 근거는 아직 제한적이다. 현재까지 Gepant 계열 약제 간의 직접 비교 임상시험(head-to-head trial)은 수행되지 않았으며, 약물동태학적 특성의 차이와 임상 반응성 간의 상관관계에 대한 연구 역시 부족하다. 특히 성별, 체질량지수(BMI), 유전적 요인 등 개별 환자 특성에 따라 이들 약제의 효과 및 부작용 프로파일이 어떻게 달라질 수 있는지에 대한 정보는 충분하지 않다.자베게판트의 비강 분무 제형은 약물이 간에서 분해되거나 체중에 따라 흡수 속도가 달라지는 문제를 어느 정도 줄일 수 있는 장점이 있다. 그러나 실제 임상 현장에서 이 약제가 얼마나 효과적이고 안전한지는 앞으로 더 많은 연구를 통해 확인될 필요가 있다.자베게판트의 임상시험에서는 미각 장애, 비강 불편감, 인후 자극감 등의 경미한 이상반응이 보고되었으며, 장기적인 비점막에 대한 영향은 아직 충분히 규명되지 않았다. 또한, CGRP가 비강 점막 혈관에 미치는 생리적 기능에 대한 이해도 제한적인 상황이다.따라서 비강 제형 자베게판트의 효과와 안전성에 대한 종합적인 평가, 투여 대상 환자군의 최적화, 그리고 개별 맞춤 치료 전략의 수립은 향후 편두통 치료의 패러다임을 확장하는 데 있어 중요한 과제가 될 것이다.참고문헌 1. Andrew Blumenfeld et al. “Hypervigilance, Allostatic Load, and Migraine Prevention: Antibodies to CGRP or Receptor” Neurol Ther. Volume 10, 469–497(2021). 2. Tessa de Vries et al. “Pharmacological treatment of migraine: CGRP and 5-HT beyond the triptans” Pharmacology & Therapeutics Volume 211, July 2020, Page 107528. 3. F A Russell et al. “Calcitonin gene-related peptide: physiology and pathophysiology” Physiol Rev 94: 1099–1142,(2014). 4. Boucherie et al. “Comparison of gepant effects at therapeutic plasma concentrations: connecting” The Journal of Headache and Pain (2024) 25:141. 5. Michael Thomas Eller et al. “Novel Calcitonin Gene-Related Peptide (CGRP) Interfering Migraine Therapies and Stroke—A Review” Int. J. Mol. Sci. 2024, 25(21), 11685. 6. Andrew F. Russo “ CALCITONIN GENE-RELATED PEPTIDE: A New Target for Migraine” Annu Rev Pharmacol Toxicol. 2015 ; 55: 533–552. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등).2025-07-11 06:47:54최병철 박사 -
 항우울제 프리스틱 염변경 제제, 저용량으로 경쟁력 강화[데일리팜=이탁순 기자] 항우울제 프리스틱(데스벤라팍신숙신산염일수화물) 염변경 약제들이 오리지널과 제네릭 약제에는 없는 25mg 저용량 제품으로 시장 경쟁력을 강화하고 있다.제네릭 진입에 따른 약가 조정이 예고된 상황에서 이들 염변경 약제의 승부수가 통할지 주목된다.6일 업계에 따르면 이달 넥스팜코리아 데스베라서방정25mg, 명인제약 에스벤서방정25mg, 한림제약 프리넥사서방정25mg 등 3개 품목이 급여 등재됐다.이들 품목의 성분명은 데스벤라팍신벤조산염으로, 오리지널 프리스틱의 염변경 약제다. 오리지널과 제네릭 약제에는 25m 용량이 없다.이에 앞서 환인제약은 지난 2022년 6월 데팍신서방정25mg(데스벤라팍신)을 출시했다.항우울제의 경우 갑자기 투여를 중단할 경우 금단증상, 구역, 현기증, 불안, 등 이상반응이 나타날 수 있다. 이에 단계적인 복용량 감소가 필요하다. 그런 의미에서 데스벤라팍신 25mg 저용량을 잘 활용하면 점차적인 용량 감소에 유용할 것으로 전망된다.데스벤라팍신 제제는 제네릭 약제가 나온 지 1년째가 되면서 올해 8월 53.55% 수준으로 약가 조정이 예정돼 있다. 이에 가산을 받은 염변경 약제도 약가가 인하될 수 있다.이번에 급여 등재된 데스벤라팍벤조산염 25mg 제제도 이에 발맞춰 한 달 후 약가 조정이 예정돼 있다.약가 조정이 현실화된다면 한 달 안에 현재 약가로 시장 선점에 나서야 한다. 현재 상한금액은 넥스팜코리아 데스베라서방정25mg은 469원, 명인제약 에스벤서방정25mg은 468원, 한림제약 프리넥사서방정25mg은 450원이다. 한림은 산정가보다 가격을 낮췄다.한 달 뒤에는 약가 조정으로 데스베라서방정25mg가 359원, 나머지 2개 제품은 358원으로 비슷해진다.3개 브랜드는 작년 유비스트 기준 명인제약 에스벤이 11억2976만원, 넥스팜코리아 데스베라 5억981만원, 한림제약 프리넥사가 3억9380만원의 원외처방액을 기록했다. 오리지널 프리스틱서방정이 22억원, 환인제약 데팍신서방정은 16억원으로 선두권을 형성하고 있다.2025-07-06 14:22:04이탁순
항우울제 프리스틱 염변경 제제, 저용량으로 경쟁력 강화[데일리팜=이탁순 기자] 항우울제 프리스틱(데스벤라팍신숙신산염일수화물) 염변경 약제들이 오리지널과 제네릭 약제에는 없는 25mg 저용량 제품으로 시장 경쟁력을 강화하고 있다.제네릭 진입에 따른 약가 조정이 예고된 상황에서 이들 염변경 약제의 승부수가 통할지 주목된다.6일 업계에 따르면 이달 넥스팜코리아 데스베라서방정25mg, 명인제약 에스벤서방정25mg, 한림제약 프리넥사서방정25mg 등 3개 품목이 급여 등재됐다.이들 품목의 성분명은 데스벤라팍신벤조산염으로, 오리지널 프리스틱의 염변경 약제다. 오리지널과 제네릭 약제에는 25m 용량이 없다.이에 앞서 환인제약은 지난 2022년 6월 데팍신서방정25mg(데스벤라팍신)을 출시했다.항우울제의 경우 갑자기 투여를 중단할 경우 금단증상, 구역, 현기증, 불안, 등 이상반응이 나타날 수 있다. 이에 단계적인 복용량 감소가 필요하다. 그런 의미에서 데스벤라팍신 25mg 저용량을 잘 활용하면 점차적인 용량 감소에 유용할 것으로 전망된다.데스벤라팍신 제제는 제네릭 약제가 나온 지 1년째가 되면서 올해 8월 53.55% 수준으로 약가 조정이 예정돼 있다. 이에 가산을 받은 염변경 약제도 약가가 인하될 수 있다.이번에 급여 등재된 데스벤라팍벤조산염 25mg 제제도 이에 발맞춰 한 달 후 약가 조정이 예정돼 있다.약가 조정이 현실화된다면 한 달 안에 현재 약가로 시장 선점에 나서야 한다. 현재 상한금액은 넥스팜코리아 데스베라서방정25mg은 469원, 명인제약 에스벤서방정25mg은 468원, 한림제약 프리넥사서방정25mg은 450원이다. 한림은 산정가보다 가격을 낮췄다.한 달 뒤에는 약가 조정으로 데스베라서방정25mg가 359원, 나머지 2개 제품은 358원으로 비슷해진다.3개 브랜드는 작년 유비스트 기준 명인제약 에스벤이 11억2976만원, 넥스팜코리아 데스베라 5억981만원, 한림제약 프리넥사가 3억9380만원의 원외처방액을 기록했다. 오리지널 프리스틱서방정이 22억원, 환인제약 데팍신서방정은 16억원으로 선두권을 형성하고 있다.2025-07-06 14:22:04이탁순 -
 높은 자살률 관심 보인 이 대통령…약국 자살예방 사업 주목[데일리팜=김지은 기자] 이재명 대통령이 한국의 높은 자살률에 관심을 보이면서 지역 약국을 중심으로 수년째 이어지고 있는 자살예방사업도 새롭게 조명되고 있다.이 대통령은 지난 5일 용산 대통령실에서 열린 새정부 첫 국무회의에서 조규홍 복지부장관에게 자살률 관련 질문을 한 것으로 알려졌다. 정치권에 따르면 같은 날 열린 안전치안점검회의에서도 이 대통령은 우리나라 자살률이 높다며 대응을 주문했다.이 대통령이 자살률과 그에 따른 대응에 대해 높은 관심을 보이면서 그에 따른 후속조치로 복지부는 조만간 대통령실에 자살예방 대책 추진 경과 등을 보고할 것으로 알려졌다.정치권에서는 이 대통령이 자살률 문제를 지속 언급하고 높은 관심을 보이고 있는 만큼 관련 예방 사업이나 정책의 재정비나 예산 확충 등이 이뤄질 수 있을 것으로 보고 있다.이런 가운데 대한약사회가 참여 중인 민관협력 자살예방사업에 대해서도 관심이 모아진다. 복지부가 민관기관에서 수행 중인 각종 자살예방사업에 예산을 지원하는 것으로, 약사회는 2017년부터 매년 사업에 참여하고 있다.올해 사업에는 약사회를 비롯해 10개 기관이 참여 중이며 약사회의 올해 사업명은 ‘생명지킴이 약사로서 지역약국 자살예방 강화’다.해당 사업을 통해 약사회는 전국 2만여곳 약국에 생명존중 문화 정착을 위한 포스터를 배포해 홍보에 나서는 한편, 참여 약국들은 항우울제 복용 환자를 모니터링해 자살 고위험군을 조기 발굴, 치료기관과 정신건강복지센터에 연계하는 활동 등을 시행하고 있다.약사회는 9년 넘게 이번 사업에 참여한 공로를 인정받아 지난해 보건복지부장관 기관 표창을 수상하기도 했다. 올해는 사업 확대 방안으로 약사의 자살예방 역량을 체계적으로 높이기 위해 자살예방교육을 연수교육 프로그램에 포함하고 최대 1평점까지 인정하는 방안을 마련하기도 했다.이 외에도 지역 별로 지자체와 지역 약사회 간 협약을 통해 자살예방을 위한 생명사랑약국 사업이 진행되는 곳들도 있다.인천시의 경우 지난 2019년부터 인천시자살예방센터와 연계돼 약국에 방문한 시민들에게 정신건강정보를 전달하고 의약품 복약지도를 하면서 정신건강 상의 문제나 자살 위기를 겪는 환자를 발견해 관련 기관에 연계하는 역할을 하고 있다.시에서는 약국에 생명사랑약국 안내 현판과 홍보용 전단, 상담소 연락처가 적힌 생분해성 봉투 등을 지속해서 지원하며 홍보에도 일조하고 있다.약사회에서는 자살예방과 관련해 민관기관 중 약사회와 일선 약국들이 중요한 역할을 해 왔던 만큼 관련 사업이 더 확장될 수 있는 방안을 찾을 예정이다.약사회 관계자는 “지역 약국은 자살 예방 관련 역할을 하기에 가장 적합한 것도 사실”이라며 “이번 민주당 대선 공약에 단골약국제도가 포함돼 있었던 만큼 동네 약국이 자살예방사업을 비롯해 금연, 만성질환, 다제약물관리 등 새로운 서비스에 대한 실행 모델 개발을 고민할 시점이 됐다”고 말했다.이어 “복지부, 국회와 긴밀히 소통하며 실행 가능한 것부터 순차적으로 진행할 수 있는 방안을 고려하고 있다”고 덧붙였다.2025-06-11 17:05:04김지은
높은 자살률 관심 보인 이 대통령…약국 자살예방 사업 주목[데일리팜=김지은 기자] 이재명 대통령이 한국의 높은 자살률에 관심을 보이면서 지역 약국을 중심으로 수년째 이어지고 있는 자살예방사업도 새롭게 조명되고 있다.이 대통령은 지난 5일 용산 대통령실에서 열린 새정부 첫 국무회의에서 조규홍 복지부장관에게 자살률 관련 질문을 한 것으로 알려졌다. 정치권에 따르면 같은 날 열린 안전치안점검회의에서도 이 대통령은 우리나라 자살률이 높다며 대응을 주문했다.이 대통령이 자살률과 그에 따른 대응에 대해 높은 관심을 보이면서 그에 따른 후속조치로 복지부는 조만간 대통령실에 자살예방 대책 추진 경과 등을 보고할 것으로 알려졌다.정치권에서는 이 대통령이 자살률 문제를 지속 언급하고 높은 관심을 보이고 있는 만큼 관련 예방 사업이나 정책의 재정비나 예산 확충 등이 이뤄질 수 있을 것으로 보고 있다.이런 가운데 대한약사회가 참여 중인 민관협력 자살예방사업에 대해서도 관심이 모아진다. 복지부가 민관기관에서 수행 중인 각종 자살예방사업에 예산을 지원하는 것으로, 약사회는 2017년부터 매년 사업에 참여하고 있다.올해 사업에는 약사회를 비롯해 10개 기관이 참여 중이며 약사회의 올해 사업명은 ‘생명지킴이 약사로서 지역약국 자살예방 강화’다.해당 사업을 통해 약사회는 전국 2만여곳 약국에 생명존중 문화 정착을 위한 포스터를 배포해 홍보에 나서는 한편, 참여 약국들은 항우울제 복용 환자를 모니터링해 자살 고위험군을 조기 발굴, 치료기관과 정신건강복지센터에 연계하는 활동 등을 시행하고 있다.약사회는 9년 넘게 이번 사업에 참여한 공로를 인정받아 지난해 보건복지부장관 기관 표창을 수상하기도 했다. 올해는 사업 확대 방안으로 약사의 자살예방 역량을 체계적으로 높이기 위해 자살예방교육을 연수교육 프로그램에 포함하고 최대 1평점까지 인정하는 방안을 마련하기도 했다.이 외에도 지역 별로 지자체와 지역 약사회 간 협약을 통해 자살예방을 위한 생명사랑약국 사업이 진행되는 곳들도 있다.인천시의 경우 지난 2019년부터 인천시자살예방센터와 연계돼 약국에 방문한 시민들에게 정신건강정보를 전달하고 의약품 복약지도를 하면서 정신건강 상의 문제나 자살 위기를 겪는 환자를 발견해 관련 기관에 연계하는 역할을 하고 있다.시에서는 약국에 생명사랑약국 안내 현판과 홍보용 전단, 상담소 연락처가 적힌 생분해성 봉투 등을 지속해서 지원하며 홍보에도 일조하고 있다.약사회에서는 자살예방과 관련해 민관기관 중 약사회와 일선 약국들이 중요한 역할을 해 왔던 만큼 관련 사업이 더 확장될 수 있는 방안을 찾을 예정이다.약사회 관계자는 “지역 약국은 자살 예방 관련 역할을 하기에 가장 적합한 것도 사실”이라며 “이번 민주당 대선 공약에 단골약국제도가 포함돼 있었던 만큼 동네 약국이 자살예방사업을 비롯해 금연, 만성질환, 다제약물관리 등 새로운 서비스에 대한 실행 모델 개발을 고민할 시점이 됐다”고 말했다.이어 “복지부, 국회와 긴밀히 소통하며 실행 가능한 것부터 순차적으로 진행할 수 있는 방안을 고려하고 있다”고 덧붙였다.2025-06-11 17:05:04김지은 -
 한국룬드벡, 첫 외국인 CEO 브래드 애드워즈 선임브래드 애드워즈 한국룬드벡 신임 대표 [데일리팜=황병우 기자] 글로벌 뇌질환 치료제 전문 기업 한국룬드벡이 지난 1일 한국 법인 설립 이후 23년 만에 최초 외국인 최고경영자(CEO)로 브래드 애드워즈(Brad Edwards)를 선임했다고 16일 밝혔다.브래드 애드워즈 신임 대표는 쉐링플라우, 화이자, 샤이어, 다케다 등 다양한 다국적 제약회사에서 근무하며 약 25년 동안 폭넓은 경험과 전문성을 쌓은 전문가다.최근에는 싱가포르에서 다케다의 혈장 유래 치료제(plasma derived-therapies) 신규 시장 발굴 책임자로 근무했다.브래드 애드워즈 대표는 지난 2014년 희귀(특수)질환 전문제약사 샤이어로 이직 후, 샤이어의 풍부한 희귀질환 포트폴리오를 통해 많은 경험을 쌓았다.이후 다케다 호주와 뉴질랜드의 총괄 책임자를 역임했으며, 산업 협회 이사회 멤버로서 호주에서 환자들의 희귀질환 치료제 접근성 개선을 위한 외부 정책 환경 형성에 기여한 바 있다.이번 신임 대표 선임을 통해 룬드벡은 그의 폭넓은 경험과 희귀질환 분야에서의 깊이 있는 지식이 한국룬드벡의 신경계 희귀질환(Neuro-rare) 분야로의 확장을 준비하는 데 있어 매우 중요한 역할을 할 것으로 기대하고 있다.브래드 애드워즈 대표는 "룬드벡에 합류하여 한국에서 일할 기회를 가지게 되어 영광이고 룬드벡의 ‘Focused Innovator’ 전략 여정에 함께하게 되어 기대된다"며 "신경과학 분야에서 한국룬드벡의 입지를 강화하고, 충족되지 않는 의료 수요가 있는 다른 분야로의 확장을 이끌겠다"고 말했다.이어 그는 "한국 문화를 더 많이 배우고, 룬드벡 동료들과 긴밀히 협력하며, 무엇보다도 한국 환자들에게 실질적인 영향을 미치는 치료제를 제공하는 데 일조하고 싶다"고 덧붙였다.한편, 한국룬드벡은 덴마크 코펜하겐에 본사를 둔 다국적 제약회사로서 신경·정신과 질환 치료제를 연구·개발하는 뇌질환 치료제 전문 기업이다.대표적으로 항우울제 렉사프로(에스시탈로프람옥살산염)와 브린텔릭스(보티옥세틴브롬화수소산염), 알츠하이머병 치료제 에빅사(메만틴염산염), 파킨슨병 치료제 아질렉트(라사길린메실산염)을 보유하고 있다.2025-04-16 14:11:52황병우
한국룬드벡, 첫 외국인 CEO 브래드 애드워즈 선임브래드 애드워즈 한국룬드벡 신임 대표 [데일리팜=황병우 기자] 글로벌 뇌질환 치료제 전문 기업 한국룬드벡이 지난 1일 한국 법인 설립 이후 23년 만에 최초 외국인 최고경영자(CEO)로 브래드 애드워즈(Brad Edwards)를 선임했다고 16일 밝혔다.브래드 애드워즈 신임 대표는 쉐링플라우, 화이자, 샤이어, 다케다 등 다양한 다국적 제약회사에서 근무하며 약 25년 동안 폭넓은 경험과 전문성을 쌓은 전문가다.최근에는 싱가포르에서 다케다의 혈장 유래 치료제(plasma derived-therapies) 신규 시장 발굴 책임자로 근무했다.브래드 애드워즈 대표는 지난 2014년 희귀(특수)질환 전문제약사 샤이어로 이직 후, 샤이어의 풍부한 희귀질환 포트폴리오를 통해 많은 경험을 쌓았다.이후 다케다 호주와 뉴질랜드의 총괄 책임자를 역임했으며, 산업 협회 이사회 멤버로서 호주에서 환자들의 희귀질환 치료제 접근성 개선을 위한 외부 정책 환경 형성에 기여한 바 있다.이번 신임 대표 선임을 통해 룬드벡은 그의 폭넓은 경험과 희귀질환 분야에서의 깊이 있는 지식이 한국룬드벡의 신경계 희귀질환(Neuro-rare) 분야로의 확장을 준비하는 데 있어 매우 중요한 역할을 할 것으로 기대하고 있다.브래드 애드워즈 대표는 "룬드벡에 합류하여 한국에서 일할 기회를 가지게 되어 영광이고 룬드벡의 ‘Focused Innovator’ 전략 여정에 함께하게 되어 기대된다"며 "신경과학 분야에서 한국룬드벡의 입지를 강화하고, 충족되지 않는 의료 수요가 있는 다른 분야로의 확장을 이끌겠다"고 말했다.이어 그는 "한국 문화를 더 많이 배우고, 룬드벡 동료들과 긴밀히 협력하며, 무엇보다도 한국 환자들에게 실질적인 영향을 미치는 치료제를 제공하는 데 일조하고 싶다"고 덧붙였다.한편, 한국룬드벡은 덴마크 코펜하겐에 본사를 둔 다국적 제약회사로서 신경·정신과 질환 치료제를 연구·개발하는 뇌질환 치료제 전문 기업이다.대표적으로 항우울제 렉사프로(에스시탈로프람옥살산염)와 브린텔릭스(보티옥세틴브롬화수소산염), 알츠하이머병 치료제 에빅사(메만틴염산염), 파킨슨병 치료제 아질렉트(라사길린메실산염)을 보유하고 있다.2025-04-16 14:11:52황병우 -
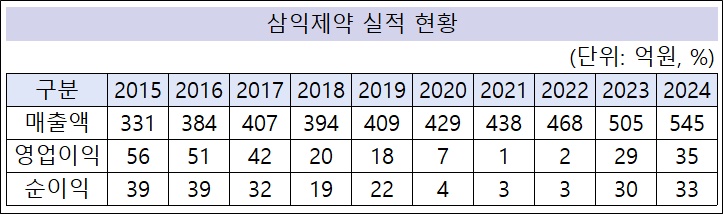 삼익제약, 지난해 매출 545억 '최대'…하반기 IPO 예열[데일리팜=이석준 기자] 삼익제약 매출이 545억을 달성하며 역대 최대치 기록했다. 외형은 2019년부터 매년 확대되고 있다. 약점이던 수익성은 업계 평균으로 올라섰다.회사는 이르면 올 하반기 코스닥 입성에 도전한다. 자금조달을 통해 대상포진 후 신경통(PHN) 치료제 등 미래성장동력에 투자할 계획이다. 삼익제약의 지난해 매출액은 545억원으로 전년(505억원) 대비 7.9% 증가했다. 같은기간 영업이익(29억→35억원)과 순이익(30억→33억원)도 20.7%, 10% 늘었다.외형은 매년 확대되고 있다. 드라마틱한 변화는 아니지만 2019년부터 5% 안팎의 성장을 이뤄내고 있다.수익성도 개선됐다. 2023년과 2024년 영업이익률은 각각 5.74%, 6.42%를 달성했다. 업계 평균 수준이다.삼익제약은 당뇨병치료제를 앞세워 매출 확대를 꾀하고 있다.대표적으로 피오시타정은 시타글립틴+피오글리타존 최초 복합제로 2023년 11월 급여를 받고 시장에 진입하고 있다.세브란스병원(강남/용인)과 성심병원(강남/동탄), 서울의료원, 상계백병원 포함 주요 병원 8곳에서 처방이 시작됐으며 서울아산병원, 서울대학교병원, 한양대학교병원 등 20여개 병원에서 연내 DC 상정을 준비 중이다. 삼익제약은 이를 통해 전국 50여 병원에서 피오시타정의 처방이 이뤄질 것으로 예상하고 있다.위수탁 매출도 발생하고 있다. 피오글리타존과 시타글립틴 조합인 마더스제약 '시타디온정 100/15mg·시타디온정100/30mg', 한국휴텍스제약 '피오비아정100/15mg·피오비아정100/30mg', 메디카코리아 '피오글시타정100/15mg·피오글시타정100/30mg 등은 삼익제약이 생산한다.이외도 삼익제약은 SGLT-2i와 DPP-4i 복합제 '포르자듀오정(다파글리플로진/시타글립틴)', DPP-4i와 Met XR 복합제 '자누맥스엠엑스알서방정(시타글립틴/메트포르민)', DDP-4i와 TZD 복합제 '피오시타정(시타글립틴/피오글리타존) 등 당뇨병치료제 라인업을 갖추고 있다.하반기 코스닥 노크업계에 따르면 삼익제약은 하반기 코스닥 입성에 도전한다. 하나증권을 단독 주관사로 선정했다. 상장 목표 시기는 10월이다. 삼익제약 최대주주는 오너 2세 이충환(28.47%) 대표다. 창업주 이세영 회장은 15.19% 지분을 보유중이다.IPO 조달 자금은 연구개발 등에 활용될 계획이다. 대표적으로 2상 중인 대상포진 후 신경통(PHN) 치료제 'SIKD1977'이다.해당 약물은 약물재창출(Drug repositioning) 기술을 적용한 천연물의약품이다. 그동안 환자들은 항우울제·항경련제·아편유사제·국소마취제·스테로이드 복용 등 임시방편적 방법에 의존해 왔다.임상은 동국대학교분당한방병원, 강동경희대학교한방병원, 자생한방병원 등 3개 병원에서 표준 치료제를 1개월 이상 투여했음에도 통증이 지속되는 PHN 환자를 대상으로 이중맹검, 위약대조, 무작위배정 방법으로 7주간 실시한다.삼익제약 관계자는 "SIKD1977의 임상시험이 성공한다면 PHN 환자들의 치료적 선택지와 미충족 수요 모두를 만족시킬 수 있는 안전성이 확보된 신약으로 환자 삶의 질을 높이는데 기여하게 될 것"이라고 강조했다.2025-04-11 06:00:09이석준
삼익제약, 지난해 매출 545억 '최대'…하반기 IPO 예열[데일리팜=이석준 기자] 삼익제약 매출이 545억을 달성하며 역대 최대치 기록했다. 외형은 2019년부터 매년 확대되고 있다. 약점이던 수익성은 업계 평균으로 올라섰다.회사는 이르면 올 하반기 코스닥 입성에 도전한다. 자금조달을 통해 대상포진 후 신경통(PHN) 치료제 등 미래성장동력에 투자할 계획이다. 삼익제약의 지난해 매출액은 545억원으로 전년(505억원) 대비 7.9% 증가했다. 같은기간 영업이익(29억→35억원)과 순이익(30억→33억원)도 20.7%, 10% 늘었다.외형은 매년 확대되고 있다. 드라마틱한 변화는 아니지만 2019년부터 5% 안팎의 성장을 이뤄내고 있다.수익성도 개선됐다. 2023년과 2024년 영업이익률은 각각 5.74%, 6.42%를 달성했다. 업계 평균 수준이다.삼익제약은 당뇨병치료제를 앞세워 매출 확대를 꾀하고 있다.대표적으로 피오시타정은 시타글립틴+피오글리타존 최초 복합제로 2023년 11월 급여를 받고 시장에 진입하고 있다.세브란스병원(강남/용인)과 성심병원(강남/동탄), 서울의료원, 상계백병원 포함 주요 병원 8곳에서 처방이 시작됐으며 서울아산병원, 서울대학교병원, 한양대학교병원 등 20여개 병원에서 연내 DC 상정을 준비 중이다. 삼익제약은 이를 통해 전국 50여 병원에서 피오시타정의 처방이 이뤄질 것으로 예상하고 있다.위수탁 매출도 발생하고 있다. 피오글리타존과 시타글립틴 조합인 마더스제약 '시타디온정 100/15mg·시타디온정100/30mg', 한국휴텍스제약 '피오비아정100/15mg·피오비아정100/30mg', 메디카코리아 '피오글시타정100/15mg·피오글시타정100/30mg 등은 삼익제약이 생산한다.이외도 삼익제약은 SGLT-2i와 DPP-4i 복합제 '포르자듀오정(다파글리플로진/시타글립틴)', DPP-4i와 Met XR 복합제 '자누맥스엠엑스알서방정(시타글립틴/메트포르민)', DDP-4i와 TZD 복합제 '피오시타정(시타글립틴/피오글리타존) 등 당뇨병치료제 라인업을 갖추고 있다.하반기 코스닥 노크업계에 따르면 삼익제약은 하반기 코스닥 입성에 도전한다. 하나증권을 단독 주관사로 선정했다. 상장 목표 시기는 10월이다. 삼익제약 최대주주는 오너 2세 이충환(28.47%) 대표다. 창업주 이세영 회장은 15.19% 지분을 보유중이다.IPO 조달 자금은 연구개발 등에 활용될 계획이다. 대표적으로 2상 중인 대상포진 후 신경통(PHN) 치료제 'SIKD1977'이다.해당 약물은 약물재창출(Drug repositioning) 기술을 적용한 천연물의약품이다. 그동안 환자들은 항우울제·항경련제·아편유사제·국소마취제·스테로이드 복용 등 임시방편적 방법에 의존해 왔다.임상은 동국대학교분당한방병원, 강동경희대학교한방병원, 자생한방병원 등 3개 병원에서 표준 치료제를 1개월 이상 투여했음에도 통증이 지속되는 PHN 환자를 대상으로 이중맹검, 위약대조, 무작위배정 방법으로 7주간 실시한다.삼익제약 관계자는 "SIKD1977의 임상시험이 성공한다면 PHN 환자들의 치료적 선택지와 미충족 수요 모두를 만족시킬 수 있는 안전성이 확보된 신약으로 환자 삶의 질을 높이는데 기여하게 될 것"이라고 강조했다.2025-04-11 06:00:09이석준 -
 메네스에스·에나폰 불순물 이슈, 수급 불안정 '불똥'[데일리팜=강혜경 기자] '불순물 이슈'로 인한 의약품 수급 불안정 문제가 현실화되고 있다.한시적 허용기준 초과 검출에 따른 사전 예방적 조치로 인한 영업자 회수, 선제적 안전조치로 인한 출하 중지 등이 원인인데 불순물 이슈가 늘어남에 따라 의약품 수급에 까지 영향이 불가피해 지고 있다는 게 약국가 전반의 얘기다.불순물 이슈로 회수 내지는 출하중지가 이뤄지면서, 수급 불안정이 불가피한 약들. 회수가 대체품목 수요 반등으로 이어지고, 결국에는 품절 사태까지 악순환을 만들고 있다는 것이다.3월 바로팜 품절입고알림 신청현황을 살펴보면 불순물 이슈에서 기인한 품절과 수급 불안정이 눈에 띄었다.바로팜 3월 품절입고알림 신청현황. 대표적인 품목이 신청횟수 1만2393회로 2위를 차지한 '메네스에스정'이다. 동구바이오제약은 어지럼증 치료제로 사용되는 메네스에스정에 대한 출하 중지를 지난 달 결정했다.'베타히스틴 함유 의약품에서 니트로사민류 불순물(N-nitroso-betahistine)이 검출됐다는 안정성 정보가 확인돼 베타히스틴 함유 완제의약품에 대해 선제적 안전조치로 출하를 중지한다'는 이유에서였다. 아직까지 식약처 지침 등은 없지만 선제적 조치의 일환으로 한시적 허용기준이 적용될 때까지 제품 출하를 중지한다는 것.제약사가 출하 중지 결정을 내리면서 이명 등에 대신 쓸 수 있는 유턴정과 메네스정, 메네신정도 수급이 불안정해졌다.신청현황에 따르면 유턴정은 3630회로 21위에 이름을 올렸으며 메네스정과 메네신정도 각각 39위와 45위에 랭크됐다.불순물 이슈로 인한 항우울제 수급도 한 달 넘게 비상이다. 일성아이엔스 센시발정(노르트립틸린염산염) 25mg·10mg, 환인제약 에나폰정(아미트리프틸린염산염), 동화약품 에트라빌(아미트리프틸린염산염) 25mg·10mg에 대한 회수가 내려지면서 수급 차질이 빚어지고 있는 것.회수 사유는 '불순물(N-nitroso-nortriptyline) 한시적 허용 기준 초과 검출에 따른 사전 예방적 조치로 시중 유통품에 대한 영엉자 회수'다.에나폰정10mg은 전 달 대비 신청횟수가 8734회 늘어 3위에 이름을 올렸으며, 에나폰정5mg도 7위에 새롭게 이름을 등재했다. 명인 아미트리프틸린염산염정10mg과 환인클로나제팜정0.5mg, 아티반정1mg, 한독 세로자트정10mg, 아티반정0.5mg은 항우울제 수급 불안정에 따른 영향으로 각각 26위와 27위, 40위, 61위, 62위에 이름을 올렸다.이번에도 가장 많은 수요가 몰린 약은 종근당 골관절염치료제 이모튼이었다. 이모튼 신청횟수는 5만3673회로 약국당 한 달 기준 3.6회 입고알림 신청을 한 것으로 나타났으며, 광범위 피부질환 치료제인 라벤다크림도 1만1803회로 4위에 올랐다.봄철 안구건조증 증가에 따라 안과용제에서도 줄줄이 수급불안정이 나타났다. 퀴놀론계 항균제 에펙신안연고가 11위에 집계됐으며, 안구건조증에 사용되는 리포직점안겔과 히아레인미니점안액0.1%가 각각 19위와 31위에 랭크됐다.또한 ▲유한 메트포르민서방정 ▲안국록소프로펜나트륨정 ▲글리티아연질캡슐 ▲리큅정 ▲프레리카캡슐 ▲토레스판연질캡슐 ▲페북트정 ▲아페린정 ▲보송크림 ▲메디키넷리타드캡슐 ▲세레타이드디스커스 등이 새롭게 수급불안정 의약품 리스트에 모습을 드러냈다.감기관련 제제 수요는 감소했는데 시네츄라시럽, 코대원포르테시럽, 펜잘8시간이알서방정 등의 순위가 하락세로 돌아섰다.2025-04-08 18:32:57강혜경
메네스에스·에나폰 불순물 이슈, 수급 불안정 '불똥'[데일리팜=강혜경 기자] '불순물 이슈'로 인한 의약품 수급 불안정 문제가 현실화되고 있다.한시적 허용기준 초과 검출에 따른 사전 예방적 조치로 인한 영업자 회수, 선제적 안전조치로 인한 출하 중지 등이 원인인데 불순물 이슈가 늘어남에 따라 의약품 수급에 까지 영향이 불가피해 지고 있다는 게 약국가 전반의 얘기다.불순물 이슈로 회수 내지는 출하중지가 이뤄지면서, 수급 불안정이 불가피한 약들. 회수가 대체품목 수요 반등으로 이어지고, 결국에는 품절 사태까지 악순환을 만들고 있다는 것이다.3월 바로팜 품절입고알림 신청현황을 살펴보면 불순물 이슈에서 기인한 품절과 수급 불안정이 눈에 띄었다.바로팜 3월 품절입고알림 신청현황. 대표적인 품목이 신청횟수 1만2393회로 2위를 차지한 '메네스에스정'이다. 동구바이오제약은 어지럼증 치료제로 사용되는 메네스에스정에 대한 출하 중지를 지난 달 결정했다.'베타히스틴 함유 의약품에서 니트로사민류 불순물(N-nitroso-betahistine)이 검출됐다는 안정성 정보가 확인돼 베타히스틴 함유 완제의약품에 대해 선제적 안전조치로 출하를 중지한다'는 이유에서였다. 아직까지 식약처 지침 등은 없지만 선제적 조치의 일환으로 한시적 허용기준이 적용될 때까지 제품 출하를 중지한다는 것.제약사가 출하 중지 결정을 내리면서 이명 등에 대신 쓸 수 있는 유턴정과 메네스정, 메네신정도 수급이 불안정해졌다.신청현황에 따르면 유턴정은 3630회로 21위에 이름을 올렸으며 메네스정과 메네신정도 각각 39위와 45위에 랭크됐다.불순물 이슈로 인한 항우울제 수급도 한 달 넘게 비상이다. 일성아이엔스 센시발정(노르트립틸린염산염) 25mg·10mg, 환인제약 에나폰정(아미트리프틸린염산염), 동화약품 에트라빌(아미트리프틸린염산염) 25mg·10mg에 대한 회수가 내려지면서 수급 차질이 빚어지고 있는 것.회수 사유는 '불순물(N-nitroso-nortriptyline) 한시적 허용 기준 초과 검출에 따른 사전 예방적 조치로 시중 유통품에 대한 영엉자 회수'다.에나폰정10mg은 전 달 대비 신청횟수가 8734회 늘어 3위에 이름을 올렸으며, 에나폰정5mg도 7위에 새롭게 이름을 등재했다. 명인 아미트리프틸린염산염정10mg과 환인클로나제팜정0.5mg, 아티반정1mg, 한독 세로자트정10mg, 아티반정0.5mg은 항우울제 수급 불안정에 따른 영향으로 각각 26위와 27위, 40위, 61위, 62위에 이름을 올렸다.이번에도 가장 많은 수요가 몰린 약은 종근당 골관절염치료제 이모튼이었다. 이모튼 신청횟수는 5만3673회로 약국당 한 달 기준 3.6회 입고알림 신청을 한 것으로 나타났으며, 광범위 피부질환 치료제인 라벤다크림도 1만1803회로 4위에 올랐다.봄철 안구건조증 증가에 따라 안과용제에서도 줄줄이 수급불안정이 나타났다. 퀴놀론계 항균제 에펙신안연고가 11위에 집계됐으며, 안구건조증에 사용되는 리포직점안겔과 히아레인미니점안액0.1%가 각각 19위와 31위에 랭크됐다.또한 ▲유한 메트포르민서방정 ▲안국록소프로펜나트륨정 ▲글리티아연질캡슐 ▲리큅정 ▲프레리카캡슐 ▲토레스판연질캡슐 ▲페북트정 ▲아페린정 ▲보송크림 ▲메디키넷리타드캡슐 ▲세레타이드디스커스 등이 새롭게 수급불안정 의약품 리스트에 모습을 드러냈다.감기관련 제제 수요는 감소했는데 시네츄라시럽, 코대원포르테시럽, 펜잘8시간이알서방정 등의 순위가 하락세로 돌아섰다.2025-04-08 18:32:57강혜경 -
 노보 63%↑·릴리 2%↓...비만약 열풍에 한국법인 희비[데일리팜=손형민 기자] 글루카곤 유사 펩타이드(GLP-1) 계열 비만신약 출시 여부가 노보노디스크와 한국릴리의 실적에 큰 영향을 미쳤다. 지난해 노보노디스크는 위고비를 국내 시장에 내놓으며 매출이 63% 올랐다. 한국릴리의 경우 2023년 허가된 마운자로의 출시가 늦어지고 일부 품목들의 부진으로 매출이 소폭 감소했다.3일 금융감독원에 따르면 노보노디스크 한국법인의 매출은 2023년 2302억원에서 지난해 3747억원으로 63% 증가했다. 같은 기간 영업이익은 83억원에서 137억원으로 65% 올랐다.노보노디스크의 매출 성장은 위고비가 견인했다. 시장조사기관 아이큐비아에 따르면 위고비는 지난해 10월 출시 이후 같은 분기에만 매출 603억원을 기록했다.지난 2023년 4월 국내 허가된 위고비는 당화혈색소, 체중 감소 효과가 확인된 세마글루타이드 성분으로 구성된 GLP-1 제제다. 노보노디스크는 GLP-1 계열 당뇨병 치료제 후보물질들의 임상 도중 환자 체중 감량 효과를 확인하고 세마글루타이드 성분으로 주 1회 투여 용법 비만치료제 위고비를 개발했다. 노보노디스크의 인슐린 제제들도 매출 성장세에 힘을 보탰다. 시장조사기관 유비스트에 따르면 GLP-1 계열 리라글루타이드와 인슐린 데글루덱 복합제인 줄토피는 지난해 151억원의 매출을 기록하며 전년 대비 26% 늘었다.또 주 1회 투여 인슐린 제제 트레시바와 인슐린 복합제 리조덱도 지난해 매출 380억원과 313억원을 기록하며 각각 3%, 7% 증가했다.노보노디스크는 비만 분야에서 입지를 더욱 강화하겠다는 계획이다. 현재 노보노디스크는 위고비, 삭센다에 이어 새로운 비만 신약 ‘카그리세마’의 글로벌 임상3상 연구를 진행 중이다. 카그리세마는 위고비의 주성분인 세마글루타이드 2.4 mg과 지속형 아밀린 유사체 카그릴린타이드 2.4 mg 복합제다.이 치료제는 차세대 비만신약으로 평가된다. 카그리세마는 임상에서 기존 세마글루타이드 단일제 등과 비교했을 때 체중 감량 효과를 23% 확인한 바 있다. 임상 예상 종료 시점은 내년 1분기로, 이후 노보노디스크는 전 세계 주요 규제기관에 허가 신청을 진행할 계획이다.릴리 실적 주춤…마운자로 미출시반면 같은 GLP-1 계열 당뇨·비만신약 마운자로를 보유한 한국릴리의 실적은 소폭 감소한 것으로 나타났다.한국릴리는 지난해 매출 1642억원을 기록하며 전년 1678억원 대비 2% 감소했다. 영업이익은 103억원으로 2023년 대비 1% 줄었다.한국릴리의 경우 마운자로의 출시가 늦어지고 있어 매출이 큰 폭으로 늘어나지 못하고 있는 것으로 분석된다.마운자로는 릴리가 개발한 당뇨병 신약이다. 마운자로는 인슐린 분비 자극 펩타이드(GIP) 수용체와 GLP-1 수용체에 모두 작용해 인슐린 분비 촉진, 인슐린 저항성 개선, 글루카곤 분비 감소 등으로 식전과 식후 혈당 감소를 유도한다.비만치료제 위고비·젭바운드·삭센다 마운자로는 혈당조절뿐 아니라 체중감량 효과가 뛰어나다는 장점이 있다. 마운자로는 주 1회 투여 만으로 당뇨병이 없고 체질량지수(BMI)가 30kg/㎡ 이상이거나 동반질환이 하나 이상 있는 과체중 성인환자를 대상으로 진행한 SURMOUNT-1 임상3상 결과를 통해 체중 감소 효과를 입증했다.릴리는 마운자로의 임상에서 체중 감량 효과를 확인한 만큼 동일 성분 비만치료제 젭바운드를 지난 2023년 11월 미국 시장에 출시한 바 있다. 국내에서 마운자로는 2023년 6월 당뇨병 치료제로 허가됐고 지난해 8월에는 동일 제품명 비만신약으로 추가 적응증을 확보했다. 다만 국내 시장 출시는 아직 진행되지 않고 있다.또 트루리시티와 심발타의 지난해 매출도 부진했다. GLP-1 계열 당뇨병 치료제 트루리시티의 매출은 372억원을 기록하며 전년 444억원 대비 16% 떨어졌다. 항우울제 심발타의 작년 매출은 51억원으로 2023년보다 52% 감소했다.한국릴리는 SGLT-2 억제제 자디앙의 활약을 기대하고 있다. 자디앙은 지난해 매출 663억원으로 전년 대비 14% 올랐다. 경쟁 품목인 포시가가 지난해 시장에서 이탈하며 수혜를 고스란히 입게 됐다. 또 올해 1월 이 회사는 아토피피부염 신약 엡글리스도 시장에 출시하며 반등을 노리고 있다.릴리 역시 차세대 당뇨병·비만 신약도 준비하고 있다. 릴리가 개발 중인 레타트루타이드는 GLP-1과 GIP, GCG(글루카곤) 등 세 가지 수용체에 작용하는 차세대 당뇨병·비만 치료제다. 현재까지 해당 기전으로 상용화된 비만신약은 없다.임상2상에서 레타트루타이드는 48주차에 8mg와 12mg을 투여했을 때 각각 22.8%와 24.2%의 체중 감소 효과가 입증됐다. 이는 기존 GLP-1과 GIP를 타깃하는 마운자로의 20.2% 대비 더 높은 체중 감소 효과다. 현재 릴리는 레타트루타이드를 비만뿐만 아니라 당뇨병, 간질환 등에서 다양한 만성질환 영역에서 가능성을 확인하고 있다.2025-04-03 12:00:52손형민
노보 63%↑·릴리 2%↓...비만약 열풍에 한국법인 희비[데일리팜=손형민 기자] 글루카곤 유사 펩타이드(GLP-1) 계열 비만신약 출시 여부가 노보노디스크와 한국릴리의 실적에 큰 영향을 미쳤다. 지난해 노보노디스크는 위고비를 국내 시장에 내놓으며 매출이 63% 올랐다. 한국릴리의 경우 2023년 허가된 마운자로의 출시가 늦어지고 일부 품목들의 부진으로 매출이 소폭 감소했다.3일 금융감독원에 따르면 노보노디스크 한국법인의 매출은 2023년 2302억원에서 지난해 3747억원으로 63% 증가했다. 같은 기간 영업이익은 83억원에서 137억원으로 65% 올랐다.노보노디스크의 매출 성장은 위고비가 견인했다. 시장조사기관 아이큐비아에 따르면 위고비는 지난해 10월 출시 이후 같은 분기에만 매출 603억원을 기록했다.지난 2023년 4월 국내 허가된 위고비는 당화혈색소, 체중 감소 효과가 확인된 세마글루타이드 성분으로 구성된 GLP-1 제제다. 노보노디스크는 GLP-1 계열 당뇨병 치료제 후보물질들의 임상 도중 환자 체중 감량 효과를 확인하고 세마글루타이드 성분으로 주 1회 투여 용법 비만치료제 위고비를 개발했다. 노보노디스크의 인슐린 제제들도 매출 성장세에 힘을 보탰다. 시장조사기관 유비스트에 따르면 GLP-1 계열 리라글루타이드와 인슐린 데글루덱 복합제인 줄토피는 지난해 151억원의 매출을 기록하며 전년 대비 26% 늘었다.또 주 1회 투여 인슐린 제제 트레시바와 인슐린 복합제 리조덱도 지난해 매출 380억원과 313억원을 기록하며 각각 3%, 7% 증가했다.노보노디스크는 비만 분야에서 입지를 더욱 강화하겠다는 계획이다. 현재 노보노디스크는 위고비, 삭센다에 이어 새로운 비만 신약 ‘카그리세마’의 글로벌 임상3상 연구를 진행 중이다. 카그리세마는 위고비의 주성분인 세마글루타이드 2.4 mg과 지속형 아밀린 유사체 카그릴린타이드 2.4 mg 복합제다.이 치료제는 차세대 비만신약으로 평가된다. 카그리세마는 임상에서 기존 세마글루타이드 단일제 등과 비교했을 때 체중 감량 효과를 23% 확인한 바 있다. 임상 예상 종료 시점은 내년 1분기로, 이후 노보노디스크는 전 세계 주요 규제기관에 허가 신청을 진행할 계획이다.릴리 실적 주춤…마운자로 미출시반면 같은 GLP-1 계열 당뇨·비만신약 마운자로를 보유한 한국릴리의 실적은 소폭 감소한 것으로 나타났다.한국릴리는 지난해 매출 1642억원을 기록하며 전년 1678억원 대비 2% 감소했다. 영업이익은 103억원으로 2023년 대비 1% 줄었다.한국릴리의 경우 마운자로의 출시가 늦어지고 있어 매출이 큰 폭으로 늘어나지 못하고 있는 것으로 분석된다.마운자로는 릴리가 개발한 당뇨병 신약이다. 마운자로는 인슐린 분비 자극 펩타이드(GIP) 수용체와 GLP-1 수용체에 모두 작용해 인슐린 분비 촉진, 인슐린 저항성 개선, 글루카곤 분비 감소 등으로 식전과 식후 혈당 감소를 유도한다.비만치료제 위고비·젭바운드·삭센다 마운자로는 혈당조절뿐 아니라 체중감량 효과가 뛰어나다는 장점이 있다. 마운자로는 주 1회 투여 만으로 당뇨병이 없고 체질량지수(BMI)가 30kg/㎡ 이상이거나 동반질환이 하나 이상 있는 과체중 성인환자를 대상으로 진행한 SURMOUNT-1 임상3상 결과를 통해 체중 감소 효과를 입증했다.릴리는 마운자로의 임상에서 체중 감량 효과를 확인한 만큼 동일 성분 비만치료제 젭바운드를 지난 2023년 11월 미국 시장에 출시한 바 있다. 국내에서 마운자로는 2023년 6월 당뇨병 치료제로 허가됐고 지난해 8월에는 동일 제품명 비만신약으로 추가 적응증을 확보했다. 다만 국내 시장 출시는 아직 진행되지 않고 있다.또 트루리시티와 심발타의 지난해 매출도 부진했다. GLP-1 계열 당뇨병 치료제 트루리시티의 매출은 372억원을 기록하며 전년 444억원 대비 16% 떨어졌다. 항우울제 심발타의 작년 매출은 51억원으로 2023년보다 52% 감소했다.한국릴리는 SGLT-2 억제제 자디앙의 활약을 기대하고 있다. 자디앙은 지난해 매출 663억원으로 전년 대비 14% 올랐다. 경쟁 품목인 포시가가 지난해 시장에서 이탈하며 수혜를 고스란히 입게 됐다. 또 올해 1월 이 회사는 아토피피부염 신약 엡글리스도 시장에 출시하며 반등을 노리고 있다.릴리 역시 차세대 당뇨병·비만 신약도 준비하고 있다. 릴리가 개발 중인 레타트루타이드는 GLP-1과 GIP, GCG(글루카곤) 등 세 가지 수용체에 작용하는 차세대 당뇨병·비만 치료제다. 현재까지 해당 기전으로 상용화된 비만신약은 없다.임상2상에서 레타트루타이드는 48주차에 8mg와 12mg을 투여했을 때 각각 22.8%와 24.2%의 체중 감소 효과가 입증됐다. 이는 기존 GLP-1과 GIP를 타깃하는 마운자로의 20.2% 대비 더 높은 체중 감소 효과다. 현재 릴리는 레타트루타이드를 비만뿐만 아니라 당뇨병, 간질환 등에서 다양한 만성질환 영역에서 가능성을 확인하고 있다.2025-04-03 12:00:52손형민 -
 유유제약, 타나민 신경과 치료 전략 공유[데일리팜=이석준 기자] 유유제약은 의료 전문가들과 함께 신경과 질환 최신 지견 및 치료 전략을 공유하는 심포지엄을 진행했다고 31일 밝혔다.심포지엄은 유유제약 뇌∙말초순환 개선제 ‘타나민’, 항혈소판제 ‘유크리드’, 생약성 항우울제 ‘노이로민’ 등을 학술적으로 조명하고자 개최됐다. 주요 대학병원 신경과 전문의들의 강연 및 Q&A가 진행됐다.서울아산병원 임재성 교수는 ‘Next Neuroprotective Agent : Differentiating EGb 761®’을 주제로 인지기능개선제로써 타나민(EGb761®)의 신경보호 효과 및 임상적 유용성을 집조명했다. 경도인지장애(MCI) 단계에서 초기 치료 중요성과 콜린 알포세레이트 대비 EGb 761®’의 임상 결과를 소개했다.EGb 761®은 독일 슈바베 그룹이 세계 최초로 개발한 오리지널 고순도 은행엽 추출물로 500편 이상의 연구 문헌을 통해 효능과 안전성을 입증했다. 유유제약이 1993년도부터 타나민이라는 제품명으로 국내에 선보이고 있으며 치매성 증상(기억력 감퇴 등)을 수반하는 기질성 뇌기능 장애, 어지러움, 말초동맥 순환장애(간헐성 파행증), 혈관성 및 퇴행성 이명에 효과가 있다.국제성모병원 안상준 교수는 ‘CYP2C19 Genotype을 고려한 항혈소판제 선택’을 주제로 아시아인에서 다빈도로 나타나는 클로피도그렐 저항성 환자에서 유크리드정의 항혈전 효과와 안전성에 대한 정보를 공유했다.노원을지대학교병원 이웅우 교수는 ‘신경과 Part에서의 노이로민의 임상적 활용’을 주제로 신경계 질환과 연관되어 나타날 수 있는 우울 증상을 중심으로, 노이로민의 임상적 유효성과 처방 Case에 대한 강연을 진행했다.삼성서울병원 서우근 교수는 ‘Medication Before and After Neurointervention’ 강연을 통해 중재적 시술 전후 약물 관리의 중요성을 공유했다.유유제약 ETC마케팅실 임현수 실장은 “이번 심포지엄은 의료 전문가들과 함께 당사의 대표 제품들을 학술적으로 조명하고 최신 지견을 교류하는 소중한 자리였다. 특히 타나민의 과학적 근거와 차별성에 대한 의료진의 깊은 관심을 확인할 수 있었으며 향후에도 근거 기반 마케팅 활동을 진행하겠다”고 말했다.2025-03-31 08:47:55이석준
유유제약, 타나민 신경과 치료 전략 공유[데일리팜=이석준 기자] 유유제약은 의료 전문가들과 함께 신경과 질환 최신 지견 및 치료 전략을 공유하는 심포지엄을 진행했다고 31일 밝혔다.심포지엄은 유유제약 뇌∙말초순환 개선제 ‘타나민’, 항혈소판제 ‘유크리드’, 생약성 항우울제 ‘노이로민’ 등을 학술적으로 조명하고자 개최됐다. 주요 대학병원 신경과 전문의들의 강연 및 Q&A가 진행됐다.서울아산병원 임재성 교수는 ‘Next Neuroprotective Agent : Differentiating EGb 761®’을 주제로 인지기능개선제로써 타나민(EGb761®)의 신경보호 효과 및 임상적 유용성을 집조명했다. 경도인지장애(MCI) 단계에서 초기 치료 중요성과 콜린 알포세레이트 대비 EGb 761®’의 임상 결과를 소개했다.EGb 761®은 독일 슈바베 그룹이 세계 최초로 개발한 오리지널 고순도 은행엽 추출물로 500편 이상의 연구 문헌을 통해 효능과 안전성을 입증했다. 유유제약이 1993년도부터 타나민이라는 제품명으로 국내에 선보이고 있으며 치매성 증상(기억력 감퇴 등)을 수반하는 기질성 뇌기능 장애, 어지러움, 말초동맥 순환장애(간헐성 파행증), 혈관성 및 퇴행성 이명에 효과가 있다.국제성모병원 안상준 교수는 ‘CYP2C19 Genotype을 고려한 항혈소판제 선택’을 주제로 아시아인에서 다빈도로 나타나는 클로피도그렐 저항성 환자에서 유크리드정의 항혈전 효과와 안전성에 대한 정보를 공유했다.노원을지대학교병원 이웅우 교수는 ‘신경과 Part에서의 노이로민의 임상적 활용’을 주제로 신경계 질환과 연관되어 나타날 수 있는 우울 증상을 중심으로, 노이로민의 임상적 유효성과 처방 Case에 대한 강연을 진행했다.삼성서울병원 서우근 교수는 ‘Medication Before and After Neurointervention’ 강연을 통해 중재적 시술 전후 약물 관리의 중요성을 공유했다.유유제약 ETC마케팅실 임현수 실장은 “이번 심포지엄은 의료 전문가들과 함께 당사의 대표 제품들을 학술적으로 조명하고 최신 지견을 교류하는 소중한 자리였다. 특히 타나민의 과학적 근거와 차별성에 대한 의료진의 깊은 관심을 확인할 수 있었으며 향후에도 근거 기반 마케팅 활동을 진행하겠다”고 말했다.2025-03-31 08:47:55이석준 -
 당뇨·혈압약·철분제·항생제 연고까지 품절…"대체 왜?"[데일리팜=강혜경 기자] '타이레놀'로 시작된 품절약 문제가 여전히 현재진행형이다.대한약사회가 11일 열린 제71차 정기총회에서 종합 대책 설립을 촉구하는 결의안을 채택한 것처럼 여전히 약국에서의 품절 문제가 심각 수준이라는 지적이다.실제 2월의 경우 비수기와 영업일수가 짧은 영향으로, 매출이 30% 가까이 줄었다는 게 정설이지만 그럼에도 불구하고 당뇨약, 혈압약, 철분제, 항생제연고 등 품절이 가시화된 것으로 나타났다.또 항우울증제 회수 영향으로 에트라빌과 에나폰 등 수요가 급증한 것으로 집계됐다. 바로팜의 2월 품절입고 신청현황에 따르면 지난달 증가했던 감기·독감 관련 수요는 전반적으로 줄어들었다. 다만 이모튼캡슐, 유한 메트로포민서방정, 현대테놀민정, 씬지로이드정, 볼그레액 같은 비감기 제제에서 수요가 늘어난 것으로 확인됐다.이번에도 품절입고 신청 1위 품목은 이모튼캡슐이었다. 2월 알림신청 횟수는 4만3591회로 전 달 4만1340회 보다 5.4% 가량 늘어났다.유한 메트포르민은 신청횟수가 24% 늘며 5위에서 '2위'로 3계단 올라섰다. 혈압강하제인 현대테놀민정25mg도 수요가 129.5% 늘며 15위에서 '3위'로 상승했다.씬지로이드정0.1mg과 볼그레액도 11위에서 '4위'로, 30위에서 '5위'로 순위를 앞당겼다. 씬지로이드0.05mg과 씬지로이드0.15mg도 37위에서 '9위'로, 86위에서 '32위'로 올라섰다.혈관보강제 베니톨정은 7위에서 '6위'로 순위가 상승했지만 알림신청 횟수는 54.9% 줄어들었다. 포타겔현탁액 역시 10위에서 '7위'로 올라섰지만 알림신청 횟수는 29.2% 감소했다.변비약 실콘정도 20위에서 '10위'로 앞 순위를 받았지만, 신청 횟수는 16.6% 줄어든 것으로 나타났다.지난달 상위권을 차지하던 감기 관련 품목들도 순위가 밀려났는데, 시네츄라시럽15ml는 3위에서 '8위'로, 코대원포르테시럽은 2위에서 '11위'로, 펜잘8시간이알서방정은 19위에서 '26위'로 순위를 내어줬다.반면 소화기 질환 치료제와 소화제, 소화기관용약 등이 순위권 내에 다수 포진했다. 부광약품 알베릭스연질캡슐은 49위에서 '12위'로 상승했으며, 베아제정도 36위에서 '22위'로 순위 변동이 나타났다. 가모드정과 제스라제트연질캡슐도 새롭게 순위권에 이름을 올렸다.뇌전증약 리보트릴과 항우울제 에트라빌, 에나폰정도 수요가 증가한 것으로 확인됐다. 뇌기능장애치료제 글리틴 리드캡슐도 32위에서 '19위'로 상승했다.박테로신연고, 베아로반연고 등 항생제 연고도 23위와 47위에 이름을 올렸으며 당뇨약 글루코프리서방정, 혈압약 듀오웰정도 새롭게 순위권에 진입했다. 골격근이완제 뮤렉스정과 뮤페신정도 새롭게 이름을 올렸다.약국가는 '품절'의 원인이 다양해 지고 있는 만큼 종합적이고, 거시적인 대책 마련이 이뤄져야 한다는 주장이다.서울 A약사는 "타이레놀로 시작된 품절 문제가 혈압, 당뇨, 갑상선, 철분제 등까지 번진 지 오래다. 원인 역시 다양하다 보니 약국에서 예측이 불가한 상황"이라며 "약국에 약이 없는 문제에 대해 약사들은 물론 국민이나 정부도 익숙해 지는 게 아닌가 우려된다. 품절 문제를 약국의 문제로 치부하기 보다는 종합적인 대책 마련이 절실한 상황"이라고 말했다.B약사 역시 "2월 비수기였음에도 불구하고 품절약들이 산발적으로 생겨나고 있다. 현재는 라벤다크림이 대표적"이라면서 "품절약이 심화되는 일부 품목, 이모튼캡슐 등의 경우 부당한 조건의 거래들까지 암암리에 생겨나고 있다"고 지적했다.뿐만 아니라 중소형 도매업체가 품절약을 미끼로 최소주문금액을 맞춰 주문하게 하는 불공정 등이 행해지고 있다는 주장이다.이 약사는 "약국이 적정한 재고를 가지고 운영될 수 있도록 하는 방안이 필요하다"고 강조했다.2025-03-12 11:51:46강혜경
당뇨·혈압약·철분제·항생제 연고까지 품절…"대체 왜?"[데일리팜=강혜경 기자] '타이레놀'로 시작된 품절약 문제가 여전히 현재진행형이다.대한약사회가 11일 열린 제71차 정기총회에서 종합 대책 설립을 촉구하는 결의안을 채택한 것처럼 여전히 약국에서의 품절 문제가 심각 수준이라는 지적이다.실제 2월의 경우 비수기와 영업일수가 짧은 영향으로, 매출이 30% 가까이 줄었다는 게 정설이지만 그럼에도 불구하고 당뇨약, 혈압약, 철분제, 항생제연고 등 품절이 가시화된 것으로 나타났다.또 항우울증제 회수 영향으로 에트라빌과 에나폰 등 수요가 급증한 것으로 집계됐다. 바로팜의 2월 품절입고 신청현황에 따르면 지난달 증가했던 감기·독감 관련 수요는 전반적으로 줄어들었다. 다만 이모튼캡슐, 유한 메트로포민서방정, 현대테놀민정, 씬지로이드정, 볼그레액 같은 비감기 제제에서 수요가 늘어난 것으로 확인됐다.이번에도 품절입고 신청 1위 품목은 이모튼캡슐이었다. 2월 알림신청 횟수는 4만3591회로 전 달 4만1340회 보다 5.4% 가량 늘어났다.유한 메트포르민은 신청횟수가 24% 늘며 5위에서 '2위'로 3계단 올라섰다. 혈압강하제인 현대테놀민정25mg도 수요가 129.5% 늘며 15위에서 '3위'로 상승했다.씬지로이드정0.1mg과 볼그레액도 11위에서 '4위'로, 30위에서 '5위'로 순위를 앞당겼다. 씬지로이드0.05mg과 씬지로이드0.15mg도 37위에서 '9위'로, 86위에서 '32위'로 올라섰다.혈관보강제 베니톨정은 7위에서 '6위'로 순위가 상승했지만 알림신청 횟수는 54.9% 줄어들었다. 포타겔현탁액 역시 10위에서 '7위'로 올라섰지만 알림신청 횟수는 29.2% 감소했다.변비약 실콘정도 20위에서 '10위'로 앞 순위를 받았지만, 신청 횟수는 16.6% 줄어든 것으로 나타났다.지난달 상위권을 차지하던 감기 관련 품목들도 순위가 밀려났는데, 시네츄라시럽15ml는 3위에서 '8위'로, 코대원포르테시럽은 2위에서 '11위'로, 펜잘8시간이알서방정은 19위에서 '26위'로 순위를 내어줬다.반면 소화기 질환 치료제와 소화제, 소화기관용약 등이 순위권 내에 다수 포진했다. 부광약품 알베릭스연질캡슐은 49위에서 '12위'로 상승했으며, 베아제정도 36위에서 '22위'로 순위 변동이 나타났다. 가모드정과 제스라제트연질캡슐도 새롭게 순위권에 이름을 올렸다.뇌전증약 리보트릴과 항우울제 에트라빌, 에나폰정도 수요가 증가한 것으로 확인됐다. 뇌기능장애치료제 글리틴 리드캡슐도 32위에서 '19위'로 상승했다.박테로신연고, 베아로반연고 등 항생제 연고도 23위와 47위에 이름을 올렸으며 당뇨약 글루코프리서방정, 혈압약 듀오웰정도 새롭게 순위권에 진입했다. 골격근이완제 뮤렉스정과 뮤페신정도 새롭게 이름을 올렸다.약국가는 '품절'의 원인이 다양해 지고 있는 만큼 종합적이고, 거시적인 대책 마련이 이뤄져야 한다는 주장이다.서울 A약사는 "타이레놀로 시작된 품절 문제가 혈압, 당뇨, 갑상선, 철분제 등까지 번진 지 오래다. 원인 역시 다양하다 보니 약국에서 예측이 불가한 상황"이라며 "약국에 약이 없는 문제에 대해 약사들은 물론 국민이나 정부도 익숙해 지는 게 아닌가 우려된다. 품절 문제를 약국의 문제로 치부하기 보다는 종합적인 대책 마련이 절실한 상황"이라고 말했다.B약사 역시 "2월 비수기였음에도 불구하고 품절약들이 산발적으로 생겨나고 있다. 현재는 라벤다크림이 대표적"이라면서 "품절약이 심화되는 일부 품목, 이모튼캡슐 등의 경우 부당한 조건의 거래들까지 암암리에 생겨나고 있다"고 지적했다.뿐만 아니라 중소형 도매업체가 품절약을 미끼로 최소주문금액을 맞춰 주문하게 하는 불공정 등이 행해지고 있다는 주장이다.이 약사는 "약국이 적정한 재고를 가지고 운영될 수 있도록 하는 방안이 필요하다"고 강조했다.2025-03-12 11:51:46강혜경 -
 와이브레인 전자약 '마인드스팀', 우울증 효과 입증2월 23일부터 26일까지 일본 고베에서 진행된 국제뇌자극 컨퍼런스 내 와이브레인 부스현장 사진. [데일리팜=노병철 기자] 멘탈헬스 플랫폼기업 와이브레인(대표 이기원)이 지난주 일본 고베에서 열린 국제뇌자극 컨퍼런스에서 우울증 전자약 마인드스팀의 주산기 우울증 실증연구 및 양극성 장애 연구 결과를 발표했다고 5일 밝혔다.특히, 이번 발표에서는 서울대병원 조희영 교수 연구팀이 진행한 마인드스팀의 주산기 우울증 실증연구의 중간 결과가 큰 호응을 얻었다. 이 임상은 한국판 벡우울척도(K-BDI-II) 18-28점 범위의 경도중등도 주요 우울장애를 가진 주산기 여성 22명을 대상으로 진행 중이다. 치료방법은 마인드스팀을 통한 재택 자가 치료 방식이다.임상 중간 결과 마인드스팀을 6주간 치료받은 후 임상 참여자들은 평가지표 모두에서 유의미한 개선을 보였다. 평가지표로는K-BDI-II, 우울증중등도 지표(MADRS), 한국판 산후우울증 지표(K-EPDS), 불면증 지표(ISI-K)가 활용됐다. 특히, K-BDI-II와 K-EPDS 점수에서 각각 -6.5, -5.3의 감소가 관찰돼, 마인드스팀을 통한 재택치료가 약물치료가 제한적인 주산기 우울증 환자에게 지속적이고 안전한 치료 옵션이 될 수 있음을 제시했다.또한, 이번 발표에서는 마인드스팀의 양극성 장애 치료 임상결과도 발표됐다. 64명의 양극성 장애I/II 환자를 대상으로6주간 재택으로 마인드스팀 자가 치료를 진행한 결과 위약 대조군과 동일한 수준의 안전성을 확인했다.양극성 장애는 조울증으로 알려진 만성 정신질환으로, 기분장애 중 자살 시도가 잦아 예후가 가장 좋지 않은 질환이다. 표준 치료로는 약물요법이 흔히 쓰이지만 제한적인 효과와 부작용의 위험이 있어 대안 치료제에 대한 요구가 높은 분야다.연구팀은 소규모로 진행된 이번 임상에서 기분안정제 및 항우울제 등의 약물 복용 여부에 대한 면밀한 통제가 진행되지 않은 점을 바탕으로 향후 양극성장애에서 마인드스팀의 효과 분석을 위한 대규모 임상에 대한 계획도 발표했다.그 외에도 국내에서 진행된 허가용 임상 결과와 실제 처방 데이터 자료가 발표돼 학회 참가자들의 주목을 끌었다. 마인드스팀은 경증 및 중등증 주요 우울장애 치료제로, 2020년 국내 다기관 재택 임상에서 6주간 매일 30분씩 단독 치료했을 때 우울 증상의 관해율이 62.8%를 기록했다. 이는 기존 항우울제의 관해율(약 50%)보다 12.8% 더 높은 수치다.2021년 식약처 허가 후, 2022년에는 한국보건의료연구원(NECA)의 신의료기술 유예기술로 선정돼 국내에서 비급여로 처방 중이다. 마인드스팀은 2018년부터 2022년까지 총 4,866명의 사용자에게 172,536회 처방됐고, 중대한 부작용이 보고되지 않아 실제 임상 환경에서 안전성과 유효성이 입증됐다.와이브레인의 이기원 대표는 “인체에 안전한 미세전류(tDCS)를 우울증 치료에 처방중인 사례는 대한민국의 와이브레인이 세계 최초”라며, “이번 발표에서 마인드스팀을 활용한 주산기 우울증 및 양극성 장애 임상 데이터뿐만 아니라 실제 환자치료를 위한 처방 데이터를 통해 실제 치료효과와 임상적 유효성을 해외에 소개할 수 있어 기쁘다”고 밝혔다.2025-03-05 08:50:10노병철
와이브레인 전자약 '마인드스팀', 우울증 효과 입증2월 23일부터 26일까지 일본 고베에서 진행된 국제뇌자극 컨퍼런스 내 와이브레인 부스현장 사진. [데일리팜=노병철 기자] 멘탈헬스 플랫폼기업 와이브레인(대표 이기원)이 지난주 일본 고베에서 열린 국제뇌자극 컨퍼런스에서 우울증 전자약 마인드스팀의 주산기 우울증 실증연구 및 양극성 장애 연구 결과를 발표했다고 5일 밝혔다.특히, 이번 발표에서는 서울대병원 조희영 교수 연구팀이 진행한 마인드스팀의 주산기 우울증 실증연구의 중간 결과가 큰 호응을 얻었다. 이 임상은 한국판 벡우울척도(K-BDI-II) 18-28점 범위의 경도중등도 주요 우울장애를 가진 주산기 여성 22명을 대상으로 진행 중이다. 치료방법은 마인드스팀을 통한 재택 자가 치료 방식이다.임상 중간 결과 마인드스팀을 6주간 치료받은 후 임상 참여자들은 평가지표 모두에서 유의미한 개선을 보였다. 평가지표로는K-BDI-II, 우울증중등도 지표(MADRS), 한국판 산후우울증 지표(K-EPDS), 불면증 지표(ISI-K)가 활용됐다. 특히, K-BDI-II와 K-EPDS 점수에서 각각 -6.5, -5.3의 감소가 관찰돼, 마인드스팀을 통한 재택치료가 약물치료가 제한적인 주산기 우울증 환자에게 지속적이고 안전한 치료 옵션이 될 수 있음을 제시했다.또한, 이번 발표에서는 마인드스팀의 양극성 장애 치료 임상결과도 발표됐다. 64명의 양극성 장애I/II 환자를 대상으로6주간 재택으로 마인드스팀 자가 치료를 진행한 결과 위약 대조군과 동일한 수준의 안전성을 확인했다.양극성 장애는 조울증으로 알려진 만성 정신질환으로, 기분장애 중 자살 시도가 잦아 예후가 가장 좋지 않은 질환이다. 표준 치료로는 약물요법이 흔히 쓰이지만 제한적인 효과와 부작용의 위험이 있어 대안 치료제에 대한 요구가 높은 분야다.연구팀은 소규모로 진행된 이번 임상에서 기분안정제 및 항우울제 등의 약물 복용 여부에 대한 면밀한 통제가 진행되지 않은 점을 바탕으로 향후 양극성장애에서 마인드스팀의 효과 분석을 위한 대규모 임상에 대한 계획도 발표했다.그 외에도 국내에서 진행된 허가용 임상 결과와 실제 처방 데이터 자료가 발표돼 학회 참가자들의 주목을 끌었다. 마인드스팀은 경증 및 중등증 주요 우울장애 치료제로, 2020년 국내 다기관 재택 임상에서 6주간 매일 30분씩 단독 치료했을 때 우울 증상의 관해율이 62.8%를 기록했다. 이는 기존 항우울제의 관해율(약 50%)보다 12.8% 더 높은 수치다.2021년 식약처 허가 후, 2022년에는 한국보건의료연구원(NECA)의 신의료기술 유예기술로 선정돼 국내에서 비급여로 처방 중이다. 마인드스팀은 2018년부터 2022년까지 총 4,866명의 사용자에게 172,536회 처방됐고, 중대한 부작용이 보고되지 않아 실제 임상 환경에서 안전성과 유효성이 입증됐다.와이브레인의 이기원 대표는 “인체에 안전한 미세전류(tDCS)를 우울증 치료에 처방중인 사례는 대한민국의 와이브레인이 세계 최초”라며, “이번 발표에서 마인드스팀을 활용한 주산기 우울증 및 양극성 장애 임상 데이터뿐만 아니라 실제 환자치료를 위한 처방 데이터를 통해 실제 치료효과와 임상적 유효성을 해외에 소개할 수 있어 기쁘다”고 밝혔다.2025-03-05 08:50:10노병철 -
 항우울제 회수 쇼크…에트라빌 회수에 약국 비상[데일리팜=강혜경 기자] 잇따른 항우울제 회수에 약국가가 술렁이고 있다.이번에는 동화약품 에트라빌(아미트리프틸린염산염)에 대해 회수조치가 내려진 것인데, 처방의 대부분을 차지하는 10mg의 경우 회수범위가 '전 제조번호'인 만큼 약국에서도 타격이 크다는 설명이다.대전식품의약품안전청에 따르면 회수 사유는 '불순물(N-nitroso-nortriptyline, NNORT) 한시적 허용기준 초과 검출에 따른 사전예방적 조치로 시중 유통품에 대해 영업자 회수'다. 10mg는 전 제조번호가 대상이며, 25mg은 제조번호 '2D001', '2D002', '2D003', 'C004', 'C005', 'C006'이 대상이다.의약품 조사기관 유비스트에 따르면 2023년 외래 처방금액은 5억7006만원이다. 2022년은 5억8848만원이다.A약사는 "조제에 사용되는 에트라빌10mg 전 제품이 회수 대상에 포함된다"면서 "센시발, 에나폰에 이어 에트라빌까지 회수가 내려진 데 대해 약국들도 당황스럽다는 입장"이라고 말했다.당장 조제 불편에 대한 우려도 나오고 있다. A약사는 "항우울제가 줄줄이 품절·회수되면서 조제 불편 등이 예상된다"고 토로했다.B약사는 "21일자로 회수가 내려진 것을 24일에야 알게 됐다. 주말과 월요일 오전 조제된 부분에 대해 어떻게 해야 할지 난감하다"고 토로했다.B약사는 "항우울제 품절 이슈로 인해 교품한 제품도 회수 대상에 포함된다. 회수에 난항이 빚어졌던 센시발처럼 에트라빌 역시 회수에 차질이 빚어지는 게 아닐지 우려된다"고 전했다. 이어 "항우울제의 잇단 회수가 시장에 어떤 영향을 미칠지 지켜봐야 할 부분"이라고 덧붙였다.2025-02-24 15:59:35강혜경
항우울제 회수 쇼크…에트라빌 회수에 약국 비상[데일리팜=강혜경 기자] 잇따른 항우울제 회수에 약국가가 술렁이고 있다.이번에는 동화약품 에트라빌(아미트리프틸린염산염)에 대해 회수조치가 내려진 것인데, 처방의 대부분을 차지하는 10mg의 경우 회수범위가 '전 제조번호'인 만큼 약국에서도 타격이 크다는 설명이다.대전식품의약품안전청에 따르면 회수 사유는 '불순물(N-nitroso-nortriptyline, NNORT) 한시적 허용기준 초과 검출에 따른 사전예방적 조치로 시중 유통품에 대해 영업자 회수'다. 10mg는 전 제조번호가 대상이며, 25mg은 제조번호 '2D001', '2D002', '2D003', 'C004', 'C005', 'C006'이 대상이다.의약품 조사기관 유비스트에 따르면 2023년 외래 처방금액은 5억7006만원이다. 2022년은 5억8848만원이다.A약사는 "조제에 사용되는 에트라빌10mg 전 제품이 회수 대상에 포함된다"면서 "센시발, 에나폰에 이어 에트라빌까지 회수가 내려진 데 대해 약국들도 당황스럽다는 입장"이라고 말했다.당장 조제 불편에 대한 우려도 나오고 있다. A약사는 "항우울제가 줄줄이 품절·회수되면서 조제 불편 등이 예상된다"고 토로했다.B약사는 "21일자로 회수가 내려진 것을 24일에야 알게 됐다. 주말과 월요일 오전 조제된 부분에 대해 어떻게 해야 할지 난감하다"고 토로했다.B약사는 "항우울제 품절 이슈로 인해 교품한 제품도 회수 대상에 포함된다. 회수에 난항이 빚어졌던 센시발처럼 에트라빌 역시 회수에 차질이 빚어지는 게 아닐지 우려된다"고 전했다. 이어 "항우울제의 잇단 회수가 시장에 어떤 영향을 미칠지 지켜봐야 할 부분"이라고 덧붙였다.2025-02-24 15:59:35강혜경 -
 "품절에 가까스로 교품했더니"...센시발 회수 난항[데일리팜=강혜경 기자] 항우울제 센시발정 회수를 놓고 약국가에서 혼란이 이어지고 있다.장기품절 이슈로 인해 약국가에 남아있는 재고가 많지는 않지만, 가까스로 약국간 교품을 통해 재고를 충당해 온 약국을 중심으로 불만이 고조되고 있다. 실제 회수에 난항도 예상된다.17일 지역 약국가에 따르면 식품의약품안전처 회수조치에 따라 도매업체도 약국을 대상으로 회수 안내에 나섰다.A약사는 "회수 조치가 내려진 것을 뒤늦게 확인했다"면서 "여러 약국에서 교품을 해 사용했는데, 갑작스러운 회수 조치에 당황스러운 상황"이라고 말했다.교품한 약 가운데 완통재고도 있지만 ATC카세트에 부어둔 재고와 반티 등까지 혼재돼 있어 회수처와 회수범위 등이 고민스러울 수밖에 없다는 것.이 약사는 "메인 도매에 얘기를 했지만 아직까지 확답은 받지 못했다"면서 "장기품절에 회수까지 약국만 피해를 입어야 하는지 모르겠다"고 지적했다.회수사유가 '불순물(N-nitroso-notriptyline, NNORT) 한시적 허용기준 초과 검출에 따른 사전예방적 조치로 인한 영업자 회수'인 데다, 10mg의 경우 제조번호가 무려 133개나 해당돼 사실상 전량 회수나 다름 없다는 것.B약사는 "10mg의 경우 '23년부터 원료 수급 이슈로 장기품절 상태였다 보니 대부분 약국에서 교품으로 재고를 충당해 왔을 것"이라며 "장기품절에 25mg 반티 처방이 나오는 경우도 다반사인데, 회수가 쉽지 않을 것으로 전망된다"고 말했다.C약사는 "약국 재고를 확인해 보니 회수에서 빗겨가긴 했지만, 의원에서는 일괄회수가 아닌 일부회수에 '계속 처방을 내자'는 분위기"라며 "약이 없는 데도 처방이 나오다 보면 환자가 약을 구하기 위해 뺑뺑이를 돌아야 하는 문제가 발생할 수 있다. 나아가 불순물 이슈가 항우울증약 전체에 영향을 미칠 가능성도 배제할 수는 없는 상황"이라고 지적했다.앞서 에나폰 역시 동일한 이슈로 회수가 내려진 바 있기 때문이다.이미 조제가 완료된 건에 대한 환불조치를 놓고도 우려의 목소리가 나오고 있다. B약사는 "발사르탄 때는 조제해 간 약 까지 회수 범위에 포함됐었으나 아직까지 이렇다할 지침이 없는 것 같다"면서 "항우울제의 경우 처방 변경 등에 대한 환자 니즈가 떨어지는 만큼 약국의 부담이 더 클 수밖에 없다"고 토로했다.2025-02-17 16:41:51강혜경
"품절에 가까스로 교품했더니"...센시발 회수 난항[데일리팜=강혜경 기자] 항우울제 센시발정 회수를 놓고 약국가에서 혼란이 이어지고 있다.장기품절 이슈로 인해 약국가에 남아있는 재고가 많지는 않지만, 가까스로 약국간 교품을 통해 재고를 충당해 온 약국을 중심으로 불만이 고조되고 있다. 실제 회수에 난항도 예상된다.17일 지역 약국가에 따르면 식품의약품안전처 회수조치에 따라 도매업체도 약국을 대상으로 회수 안내에 나섰다.A약사는 "회수 조치가 내려진 것을 뒤늦게 확인했다"면서 "여러 약국에서 교품을 해 사용했는데, 갑작스러운 회수 조치에 당황스러운 상황"이라고 말했다.교품한 약 가운데 완통재고도 있지만 ATC카세트에 부어둔 재고와 반티 등까지 혼재돼 있어 회수처와 회수범위 등이 고민스러울 수밖에 없다는 것.이 약사는 "메인 도매에 얘기를 했지만 아직까지 확답은 받지 못했다"면서 "장기품절에 회수까지 약국만 피해를 입어야 하는지 모르겠다"고 지적했다.회수사유가 '불순물(N-nitroso-notriptyline, NNORT) 한시적 허용기준 초과 검출에 따른 사전예방적 조치로 인한 영업자 회수'인 데다, 10mg의 경우 제조번호가 무려 133개나 해당돼 사실상 전량 회수나 다름 없다는 것.B약사는 "10mg의 경우 '23년부터 원료 수급 이슈로 장기품절 상태였다 보니 대부분 약국에서 교품으로 재고를 충당해 왔을 것"이라며 "장기품절에 25mg 반티 처방이 나오는 경우도 다반사인데, 회수가 쉽지 않을 것으로 전망된다"고 말했다.C약사는 "약국 재고를 확인해 보니 회수에서 빗겨가긴 했지만, 의원에서는 일괄회수가 아닌 일부회수에 '계속 처방을 내자'는 분위기"라며 "약이 없는 데도 처방이 나오다 보면 환자가 약을 구하기 위해 뺑뺑이를 돌아야 하는 문제가 발생할 수 있다. 나아가 불순물 이슈가 항우울증약 전체에 영향을 미칠 가능성도 배제할 수는 없는 상황"이라고 지적했다.앞서 에나폰 역시 동일한 이슈로 회수가 내려진 바 있기 때문이다.이미 조제가 완료된 건에 대한 환불조치를 놓고도 우려의 목소리가 나오고 있다. B약사는 "발사르탄 때는 조제해 간 약 까지 회수 범위에 포함됐었으나 아직까지 이렇다할 지침이 없는 것 같다"면서 "항우울제의 경우 처방 변경 등에 대한 환자 니즈가 떨어지는 만큼 약국의 부담이 더 클 수밖에 없다"고 토로했다.2025-02-17 16:41:51강혜경 -
식약처, 염산노르트립틸린 '항우울제' 회수 명령[데일리팜=이석준 기자] 식품의약품안전처는 최근 센시발정 10mg 및 25mg(성분명: 염산노르트립틸린)에 대한 영업자 회수 조치를 명령했다.불순물 'N-nitroso-notriptyline(NNORT)'의 한시적 허용기준 초과 검출에 따른 사전예방적 조치로 시중 유통품에 대한 영업자 회수가 실시된다.센시발정 10mg의 경우 2023년 2월 24일 이후 원료 수급 문제로 장기 품절 상태였다. 식약처는 대체약 부재로 한시적 허용 기준을 설정해 공급을 허용해왔다.이번 조치는 한시적 허용 종료와 제품의 위해성을 고려해 시행됐다.본 회수 조치에 앞서 2025년 2월 12일 동일한 불순물 문제로 에나폰정(아미트리프틸린)도 회수 조치된 바 있다.항우울제 관련 회수 조치가 반복되고 있어 처방 시 주의가 요구된다.노르트립틸린 성분 제제는 현재 센시발정만이 허가를 받아 유통 중이나 아미트리프틸린 성분 제제의 경우 에나폰정 외에도 다른 제약사도 허가를 받은 상태로 회수 대상이 확대될 가능성이 있다.업계 관계자는 "항우울제의 특성상 기존 복용 품목에 대한 환자 선호도가 높아 일선 의료 현장에서의 어려움이 예상된다"고 말했다.2025-02-14 08:58:00이석준
-
 센시발에 에나폰까지 회수…항우울제 수급 비상[데일리팜=강혜경 기자] 센시발과 에나폰 등 항우울증약에 대한 회수 결정이 내려지면서, 관련 제제 수급에 비상이 걸렸다.센시발, 에나폰 등 항우울증약 품절이 장기화되고 있는 데다, 해당 품목들이 다빈도 처방품목인 만큼 약국가는 회수로 인한 영향이 적지 않을 것으로 전망하고 있다.12일과 13일부로 회수 조치가 내려진 센시발과 에나폰. 13일 식품의약품안전처에 따르면 회수 결정이 내려진 품목은 일성아이에스 센시발정(노르트립틸린염산염) 25mg·센시발정10mg, 환인제약 에나폰정(아미트리프틸린염산염) 5mg 이다. 회수사유는 '불순물(N-nitroso-notriptyline, NNORT) 한시적 허용기준 초과 검출에 따른 사전예방적 조치로 시중 유통품에 대한 영업자 회수'다.약국가는 항우울증약의 잇단 회수명령에 당혹감을 금치 못한다는 입장이다. A약사는 "센시발과 에나폰은 다빈도 처방 품목으로, 특히 센시발정의 경우 약국 내 재고가 모두 포함된다"면서 "동일성분약이 없다 보니 약국도 발만 동동 구르고 있다"고 말했다.대체품목 찾기에도 열을 올리고 있다. B약사는 "항우울증약들이 1년 넘게 품절이다 보니 약국 내 재고가 많지는 않다. 하지만 재고분이 모두 회수 대상에 포함되더라"라면서 "항우울증에 사용할 수 있는 심발타(한국릴리), 푸로작(보령)과 에트라빌(동화약품) 모두 품절 상태다 보니 대체품목을 찾기도 쉽지 않은 상황"이라고 설명했다.센시발과 삼발타 등이 장기간 품절되다 보니 약국에서 항우울증약 재고를 늘렸고, 이번 회수 대상에 포함된 사례가 전국적으로 적지 않을 것이라는 설명이다.A약사는 "장기 품절에 회수 조치까지 겹쳐지며 항우울증약 수급에 비상이 걸리는 게 아닐지 우려된다"고 전했다.한편 2023년 기준 생산실적은 센시발정25mg 1억8814만원, 센시발정10mg 22억5904만원, 에나폰 4억472만원이다. 회수대상 품목 ◆센시발정25mg 제조번호 SSB1001,SSB1005,SSB1004,SSB1003,SSB1002,SSB2005,SSB2004,SSB2003,SSB2002,SSB2001, SSB3004,SSB3003,SSB3002,SSB3001,SSB2006,SSB4004,SSB4003,SSB4002,SSB4001,SSB4005'◆센시발정10mg 제조번호 SSA1005, SSA1009, SSA1008, SSA1007, SSA1006, SSA1012, SSA1011, SSA1010, SSA1016, SSA1015, SSA1014, SSA1013, SSA1017, SSA1018, SSA1019, SSA1020, SSA1021, SSA1022, SSA1023, SSA1024, SSA1025, SSA1026, SSA1027, SSA1028, SSA1029, SSA1030, SSA1031, SSA1032, SSA1033, SSA1034, SSA1035, SSA1036, SSA1037, SSA1038, SSA1039, SSA1040, SSA1041, SSA1042, SSA1043, SSA1044, SSA1045, SSA1046, SSA1047, SSA1048, SSA1049, SSA1050, SSA1051, SSA1052, SSA1053, SSA1054, SSA1055, SSA1056, SSA1057, SSA1058, SSA1059, SSA1060, SSA1061, SSA1062, SSA1063, SSA1064, SSA2001, SSA2002, SSA2003, SSA2004, SSA2005, SSA2006, SSA2007, SSA2008, SSA2009, SSA2010, SSA2011, SSA2012, SSA2013, SSA2014, SSA2015, SSA2016, SSA2017, SSA2018, SSA2019, SSA2020, SSA2021, SSA2022, SSA2023, SSA2024, SSA2025, SSA2026, SSA2027, SSA2028, SSA2029, SSA2030, SSA2031, SSA2032, SSA2033, SSA2034, SSA2035, SSA2036, SSA2037, SSA2038, SSA2039, SSA2040, SSA2041, SSA2042, SSA2043, SSA2044, SSA2045, SSA2046, SSA2047, SSA2048, SSA3001, SSA3002, SSA3003, SSA3004, SSA3005, SSA3006, SSA3007, SSA3008, SSA3009, SSA3010, SSA3011, SSA3012, SSA3013, SSA3014, SSA3015, SSA3016, SSA3017, SSA3018, SSA3019, SSA3020, SSA3021, SSA3022, SSA3023, SSA3024, SSA3025◆에나폰정5mg 제조번호 241N01AA, 241N02AA2025-02-13 18:52:53강혜경
센시발에 에나폰까지 회수…항우울제 수급 비상[데일리팜=강혜경 기자] 센시발과 에나폰 등 항우울증약에 대한 회수 결정이 내려지면서, 관련 제제 수급에 비상이 걸렸다.센시발, 에나폰 등 항우울증약 품절이 장기화되고 있는 데다, 해당 품목들이 다빈도 처방품목인 만큼 약국가는 회수로 인한 영향이 적지 않을 것으로 전망하고 있다.12일과 13일부로 회수 조치가 내려진 센시발과 에나폰. 13일 식품의약품안전처에 따르면 회수 결정이 내려진 품목은 일성아이에스 센시발정(노르트립틸린염산염) 25mg·센시발정10mg, 환인제약 에나폰정(아미트리프틸린염산염) 5mg 이다. 회수사유는 '불순물(N-nitroso-notriptyline, NNORT) 한시적 허용기준 초과 검출에 따른 사전예방적 조치로 시중 유통품에 대한 영업자 회수'다.약국가는 항우울증약의 잇단 회수명령에 당혹감을 금치 못한다는 입장이다. A약사는 "센시발과 에나폰은 다빈도 처방 품목으로, 특히 센시발정의 경우 약국 내 재고가 모두 포함된다"면서 "동일성분약이 없다 보니 약국도 발만 동동 구르고 있다"고 말했다.대체품목 찾기에도 열을 올리고 있다. B약사는 "항우울증약들이 1년 넘게 품절이다 보니 약국 내 재고가 많지는 않다. 하지만 재고분이 모두 회수 대상에 포함되더라"라면서 "항우울증에 사용할 수 있는 심발타(한국릴리), 푸로작(보령)과 에트라빌(동화약품) 모두 품절 상태다 보니 대체품목을 찾기도 쉽지 않은 상황"이라고 설명했다.센시발과 삼발타 등이 장기간 품절되다 보니 약국에서 항우울증약 재고를 늘렸고, 이번 회수 대상에 포함된 사례가 전국적으로 적지 않을 것이라는 설명이다.A약사는 "장기 품절에 회수 조치까지 겹쳐지며 항우울증약 수급에 비상이 걸리는 게 아닐지 우려된다"고 전했다.한편 2023년 기준 생산실적은 센시발정25mg 1억8814만원, 센시발정10mg 22억5904만원, 에나폰 4억472만원이다. 회수대상 품목 ◆센시발정25mg 제조번호 SSB1001,SSB1005,SSB1004,SSB1003,SSB1002,SSB2005,SSB2004,SSB2003,SSB2002,SSB2001, SSB3004,SSB3003,SSB3002,SSB3001,SSB2006,SSB4004,SSB4003,SSB4002,SSB4001,SSB4005'◆센시발정10mg 제조번호 SSA1005, SSA1009, SSA1008, SSA1007, SSA1006, SSA1012, SSA1011, SSA1010, SSA1016, SSA1015, SSA1014, SSA1013, SSA1017, SSA1018, SSA1019, SSA1020, SSA1021, SSA1022, SSA1023, SSA1024, SSA1025, SSA1026, SSA1027, SSA1028, SSA1029, SSA1030, SSA1031, SSA1032, SSA1033, SSA1034, SSA1035, SSA1036, SSA1037, SSA1038, SSA1039, SSA1040, SSA1041, SSA1042, SSA1043, SSA1044, SSA1045, SSA1046, SSA1047, SSA1048, SSA1049, SSA1050, SSA1051, SSA1052, SSA1053, SSA1054, SSA1055, SSA1056, SSA1057, SSA1058, SSA1059, SSA1060, SSA1061, SSA1062, SSA1063, SSA1064, SSA2001, SSA2002, SSA2003, SSA2004, SSA2005, SSA2006, SSA2007, SSA2008, SSA2009, SSA2010, SSA2011, SSA2012, SSA2013, SSA2014, SSA2015, SSA2016, SSA2017, SSA2018, SSA2019, SSA2020, SSA2021, SSA2022, SSA2023, SSA2024, SSA2025, SSA2026, SSA2027, SSA2028, SSA2029, SSA2030, SSA2031, SSA2032, SSA2033, SSA2034, SSA2035, SSA2036, SSA2037, SSA2038, SSA2039, SSA2040, SSA2041, SSA2042, SSA2043, SSA2044, SSA2045, SSA2046, SSA2047, SSA2048, SSA3001, SSA3002, SSA3003, SSA3004, SSA3005, SSA3006, SSA3007, SSA3008, SSA3009, SSA3010, SSA3011, SSA3012, SSA3013, SSA3014, SSA3015, SSA3016, SSA3017, SSA3018, SSA3019, SSA3020, SSA3021, SSA3022, SSA3023, SSA3024, SSA3025◆에나폰정5mg 제조번호 241N01AA, 241N02AA2025-02-13 18:52:53강혜경 -
 보령, 1000억원에 인수한 알림타 제조 품목 급여등재[데일리팜=이탁순 기자] 보령이 약 1000억원에 인수한 비소세포폐암치료제 '알림타'의 자체 제조품목을 급여 등재하는 데 성공했다.이에따라 전략적으로 육성하고 있는 항암제 사업이 더 탄력을 받을 것으로 전망된다.21일 업계에 따르면 알림타는 내달부터 국내 제조품목이 급여목록에 오른다. 알림타는 일라이릴리가 개발한 비소세포폐암 치료제. 보령은 지난 2022년 알림타에 대한 자산 양수·양도 계약을 체결했다. 이를 통해 보령은 판권, 유통권, 허가권, 생산권, 상표권 등 한국 내 알림타에 대한 모든 권리를 확보했다. 인수계약금은 7000만달러(한화 약 1009억원)이다.이후 보령은 수입품목인 알림타를 자체 제조 품목으로 전환하는 준비를 진행했다. 그 결과 지난해 11월 제조 품목을 허가받았다. 이에 급여목록에 있던 수입 품목이 제조 품목으로 전환된 것이다. 상한금액은 기존과 동일하다.알림타는 연간 200억원대 매출을 올리는 항암제 가운데 스테디셀러 품목이다. 비소세포폐암 1차 치료제이자 최초의 유지요법 치료제로, 2017년에는 미FDA로부터 MSD 면역항암제 '키트루다(성분명 펨브롤리주맙)' 병용요법을 승인 받기도 했다. 보령은 이번 제조 전환으로 이익률은 더 향상될 전망이다.보령 측은 "폭넓은 항암 포트폴리오를 바탕으로 처방의와 환자들에게 다양한 치료옵션을 제공할 수 있도록 지속적으로 노력해나가겠다"는 방침이다.한편, 알림타 외에도 수입 오리지널 제품의 국내 전환 소식이 이어지고 있다. 환인제약의 항우울제 아고틴정25mg도 국내 제조 품목이 허가를 받으면서 2월부터 수입품목이 급여목록에 삭제된다. 이 제품은 환인제약이 프랑스 세르비에로부터 도입했다. 다만, 환인제약 제조품목은 아직 급여목록에 등재되지 않았다.셀트리온제약이 다케다로부터 인수한 네시나정125mg(알로글립틴벤조산염)과 네시나액트정25/30mg도 제조 전환이 완료됨으로 수입품목이 자진취하로 급여목록에서 삭제된다.2025-01-21 17:21:33이탁순
보령, 1000억원에 인수한 알림타 제조 품목 급여등재[데일리팜=이탁순 기자] 보령이 약 1000억원에 인수한 비소세포폐암치료제 '알림타'의 자체 제조품목을 급여 등재하는 데 성공했다.이에따라 전략적으로 육성하고 있는 항암제 사업이 더 탄력을 받을 것으로 전망된다.21일 업계에 따르면 알림타는 내달부터 국내 제조품목이 급여목록에 오른다. 알림타는 일라이릴리가 개발한 비소세포폐암 치료제. 보령은 지난 2022년 알림타에 대한 자산 양수·양도 계약을 체결했다. 이를 통해 보령은 판권, 유통권, 허가권, 생산권, 상표권 등 한국 내 알림타에 대한 모든 권리를 확보했다. 인수계약금은 7000만달러(한화 약 1009억원)이다.이후 보령은 수입품목인 알림타를 자체 제조 품목으로 전환하는 준비를 진행했다. 그 결과 지난해 11월 제조 품목을 허가받았다. 이에 급여목록에 있던 수입 품목이 제조 품목으로 전환된 것이다. 상한금액은 기존과 동일하다.알림타는 연간 200억원대 매출을 올리는 항암제 가운데 스테디셀러 품목이다. 비소세포폐암 1차 치료제이자 최초의 유지요법 치료제로, 2017년에는 미FDA로부터 MSD 면역항암제 '키트루다(성분명 펨브롤리주맙)' 병용요법을 승인 받기도 했다. 보령은 이번 제조 전환으로 이익률은 더 향상될 전망이다.보령 측은 "폭넓은 항암 포트폴리오를 바탕으로 처방의와 환자들에게 다양한 치료옵션을 제공할 수 있도록 지속적으로 노력해나가겠다"는 방침이다.한편, 알림타 외에도 수입 오리지널 제품의 국내 전환 소식이 이어지고 있다. 환인제약의 항우울제 아고틴정25mg도 국내 제조 품목이 허가를 받으면서 2월부터 수입품목이 급여목록에 삭제된다. 이 제품은 환인제약이 프랑스 세르비에로부터 도입했다. 다만, 환인제약 제조품목은 아직 급여목록에 등재되지 않았다.셀트리온제약이 다케다로부터 인수한 네시나정125mg(알로글립틴벤조산염)과 네시나액트정25/30mg도 제조 전환이 완료됨으로 수입품목이 자진취하로 급여목록에서 삭제된다.2025-01-21 17:21:33이탁순
오늘의 TOP 10
- 1"13년 전 악몽 재현되나"…유통·CSO업계 약가개편 촉각
- 2'묻지마 청약' 규제했더니...상장 바이오 공모가 안정·주가↑
- 3[기자의 눈] 절치부심 K-바이오의 긍정적 시그널
- 4의사 남편은 유령환자 처방, 약사 아내는 약제비 청구
- 5비대면 법제화 결실…성분명·한약사 등 쟁점법 발의
- 6유통협회, 대웅 거점도매 연일 비판…“약사법 위반 소지”
- 7[팜리쿠르트] 삼진제약·HLB·퍼슨 등 부문별 채용
- 8제일약품, ESG 경영 강화…환경·사회 성과 축적
- 9약사회, 청년약사들과 타운홀 미팅...무슨 이야기 오갔나
- 10"진성적혈구증가증 치료, 이제는 장기 예후 논할 시점"
-
순위상품명횟수
-
1타이레놀정500mg(10정)30,426
-
2판콜에스내복액16,732
-
3텐텐츄정(10정)13,671
-
4까스활명수큐액12,867
-
5판피린큐액12,851













![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
