㉗ RNA 표적 치료의 대표 주자, ASO 플랫폼
- 최병철 박사
- 2026-05-08 06:00:53
-
가
- 가
- 가
- 가
- 가
- 가
- 최병철 박사의 노벨드럭 인사이트
- ASO, 표적 접근성 높여 치료 범위 확장 혁신
- 신속한 약물 개발 가능 강점...간 외 조직 전달 한계
- PR
- 잘 나가는 약국은 매달 보는 신제품 정보 ‘팜노트’
- 팜스타클럽

RNA 표적 치료(RNA-targeted therapeutics)란 무엇인가?
RNA 표적 치료는 질병 관련 유전자의 발현을 RNA 수준에서 조절하여 치료 효과를 달성하는 혁신적인 약물 개발 패러다임이다. 전통적인 저분자 약물이 효소 억제제로 작용하거나 세포막 또는 세포 내 수용체를 조절하는 것과 달리, RNA 표적 치료제는 단백질 생산의 근원인 mRNA를 직접 표적으로 삼아 질병 유발 단백질의 합성 자체를 차단한다.
기존의 저분자 약물은 단백질의 특정 '주머니(pocket)'에 결합해야 작용할 수 있는데, 이러한 결합 부위가 없는 단백질은 약물로 공략할 수 없어 'undruggable(치료 불가능)'로 분류되었다. RNA 표적 치료는 단백질이 만들어지기 전 단계인 mRNA를 차단함으로써, 기존에 치료할 수 없었던 표적에 대한 개입을 가능하게 하였다.
RNA 치료제의 개념은 안티센스 RNA의 발견, RNA-단백질 직접 상호작용의 규명, 기능성 비암호화 RNA의 발견, 그리고 RNA 유도 유전자 편집 기술의 발전과 함께 반복적으로 부상하였다. 현재까지 미국 FDA는 13개의 안티센스 올리고뉴클레오타이드(ASO), 7개의 소간섭 RNA(siRNA), 2개의 앱타머를 승인하였으며, COVID-19 mRNA 백신의 성공은 RNA 치료제의 임상적 가능성을 전 세계적으로 입증하였다.
RNA 표적 치료의 핵심 원리는 Watson-Crick 염기쌍 상보성에 기반한다. 치료용 올리고뉴클레오타이드는 일반적으로 15-30개 뉴클레오타이드 길이로 설계되며, 질병 관련 단백질을 암호화하는 mRNA 또는 조절 RNA의 특정 영역에 상보적으로 결합한다. 비경구 투여 후 올리고뉴클레오타이드가 세포 내로 진입하여 상보적인 RNA에 결합하면, 이 상호작용은 표적 mRNA의 분해 또는 기능 변화를 유도하여 암호화된 단백질의 번역을 감소시킨다.
생물정보학적 분석을 통해 표적 RNA에 대해 높은 특이성을 가지면서 의도하지 않은 bystander RNA와의 교차 결합을 피하는 서열을 신중하게 설계할 수 있으며, 이를 통해 밀접하게 관련된 유전자 가족의 단일 구성원도 선택적으로 표적화할 수 있다. 올리고뉴클레오타이드 약물이 상보적 mRNA 또는 pre-mRNA에 결합한 후 발생하는 결과는 표적 서열의 특성에 따라 달라지며, 효소적 절단에 의한 mRNA 분해, pre-mRNA 스플라이싱 패턴의 변화, 또는 조절 RNA 기능의 변화를 포함한다.
RNA 표적 치료의 종류는?
RNA 표적 치료제는 작용 기전과 분자 구조에 따라 크게 안티센스 올리고뉴클레오타이드(ASO), 소간섭 RNA(siRNA), 앱타머(aptamer), 그리고 mRNA 치료제로 분류된다.
안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, ASO)
ASO는 특정 RNA 서열에 상보적으로 결합하도록 설계된 짧은 합성 핵산으로, 유전자 발현 조절을 목적으로 개발된 분자 치료 플랫폼이다. 일반적으로 길이는 약 15–25개의 뉴클레오타이드로 구성되며, DNA, RNA 또는 다양한 화학적 변형 뉴클레오타이드의 조합으로 이루어진다.
ASO는 생체 내 안정성, 결합 친화도, 약동학적 특성을 향상시키기 위해 다양한 화학적 변형이 도입된다. 대표적으로 phosphorothioate backbone, 2′-O-methoxyethyl(2′-MOE), locked nucleic acid(LNA) 등의 변형이 사용되며, 이러한 변형은 뉴클레아제 분해 저항성을 증가시키고 표적 RNA에 대한 결합력을 향상시킨다.
구조적 설계에 따라 ASO는 여러 유형으로 구분되며, 대표적으로 중앙에 DNA 구간을 포함하는 gapmer, 전 구간이 변형된 뉴클레오타이드로 구성된 fully modified ASO, 그리고 스플라이싱 조절을 목적으로 하는 splice-switching ASO 등이 있다. 이러한 구조적 다양성은 목적에 따른 기능적 최적화를 가능하게 한다.
ASO는 높은 서열 특이성을 기반으로 특정 유전자의 발현을 선택적으로 조절할 수 있어, 유전 질환, 희귀질환, 암 및 다양한 난치성 질환에서 치료 전략으로 활용되고 있다. 또한 RNA를 표적으로 한다는 특성상 단백질 기반 약물로 접근이 어려운 표적에 대해서도 적용 가능하며, 맞춤형 치료 설계가 가능한 장점을 가진다.
그러나 효율적인 세포 및 핵 내 전달, 조직 특이적 분포, 오프타겟 효과, 면역 반응 등은 여전히 해결해야 할 주요 과제로 남아 있다.
소간섭 RNA(siRNA)
siRNA는 21-23개 뉴클레오타이드 길이의 이중 가닥 RNA로, RNA 간섭(RNAi) 기전을 통해 작용한다. siRNA가 세포질로 진입하면 RNA 유도 침묵 복합체(RISC)에 로딩되고, 가이드 가닥(안티센스 가닥)이 패신저 가닥으로부터 분리되어 상보적인 표적 mRNA에 결합한다. 이후 RISC 내의 Argonaute 2(Ago2) 효소가 표적 mRNA를 효소적으로 절단하여 분해를 유도한다.
siRNA의 핵심적 장점은 촉매적 기전에 있다. 절단 후 RISC는 동일한 가이드 가닥에 의해 인식되는 추가적인 표적 mRNA를 장기간에 걸쳐 분해할 수 있다. 이러한 촉매적 특성으로 인해 siRNA는 ASO보다 더 긴 투여 간격이 가능하며, 일부 siRNA 약물은 6개월에 1회 투여로 충분한 효과를 나타낸다.
ASO와 siRNA의 작용 부위에도 차이가 있다. ASO는 주로 핵에서 pre-mRNA에 작용하여 엑손과 인트론 모두를 표적화할 수 있는 반면, siRNA는 세포질에서 성숙한 스플라이싱된 mRNA에 작용한다.
현재 미국 FDA 승인 siRNA 약물로는 patisiran, givosiran, lumasiran, inclisiran, vutrisiran, nedosiran, fitusiran 등이 있다.
앱타머(Aptamer)
앱타머는 특정 단백질 표적에 높은 친화력과 특이성으로 결합하는 단일 가닥 올리고뉴클레오타이드로, 3차원 구조를 형성하여 항체와 유사하게 작용한다. 다른 RNA 치료제가 핵산을 표적으로 하는 것과 달리, 앱타머는 단백질에 직접 결합하여 그 기능을 조절한다.
미국 FDA 승인 앱타머로는 연령 관련 황반변성 치료제인 pegaptanib과 지도모양 위축 치료제인 avacincaptad pegol이 있다. 앱타머는 종양 표적화 약물 전달 시스템에서 표적 리간드로도 활용되고 있다.
mRNA 치료제(mRNA Therapeutics)
mRNA 치료제는 세포 내에서 치료 단백질을 직접 발현시키는 접근법으로, 유전자 침묵이 아닌 단백질 생산을 목표로 한다. mRNA는 지질 나노입자(LNP)에 캡슐화되어 세포 내로 전달되며, 세포질에서 리보솜에 의해 번역되어 치료 단백질을 생산한다. COVID-19 mRNA 백신의 성공은 mRNA 플랫폼의 임상적 가능성을 전 세계적으로 입증하였다. 현재 mRNA 기술은 백신 플랫폼을 넘어 암 면역치료와 단백질 대체 요법으로 확장되고 있으며, 자가 증폭 mRNA(saRNA)와 원형 RNA(circRNA) 등 차세대 기술이 개발 중이다.
신흥 RNA 치료 기술
기존 플랫폼 외에도 CRISPR-Cas13 기반 RNA 편집, ADAR(adenosine deaminase acting on RNA) 매개 염기 편집, 소분자 스플라이싱 조절제(risdiplam 등), 그리고 RNA 표적 소분자 약물 등 새로운 기술이 부상하고 있다. 이러한 기술들은 기존 올리고뉴클레오타이드 약물의 한계를 극복하고 경구 투여가 가능한 RNA 표적 치료제 개발의 가능성을 열고 있다.
ASO는 어떤 약제인가?
비정상적인 단백질 생성이나 대사는 다양한 중증 질환 및 장애와 밀접하게 관련되어 있다. 단백질은 메신저 RNA(mRNA)에 저장된 유전 정보를 해독하는 과정을 통해 생성되므로, 비정상적인 단백질 생성 역시 mRNA를 표적으로 하여 조절할 수 있다. 또한 RNA에 대한 이해가 심화되면서 RNA가 수행하는 다양한 기능이 밝혀졌다.
비코딩 RNA(ncRNA)가 알려지기 전까지 mRNA는 단순히 DNA와 리보솜 사이에서 단백질 합성을 매개하는 역할만 하는 것으로 여겨졌다. 그러나 ncRNA의 일종인 마이크로RNA(miRNA), 전령 RNA 유래 소형 RNA, 유사유전자(pseudogene), PIWI 상호작용 RNA(piRNA), 장쇄 비코딩 RNA(lncRNA), 원형 RNA(circRNA) 등은 유전자 발현 조절을 통해 다양한 생물학적 기능의 핵심 조절자로 작용하는 것으로 확인되었다.
따라서 전령 RNA(pre-mRNA), mRNA 또는 비코딩 RNA(ncRNA)를 표적으로 하는 안티센스 전략은 질병 유발 단백질의 생성을 조절함으로써 치료에 활용될 수 있다. 소분자 기반의 단백질 표적 치료제와 달리, 안티센스 약물은 표적 RNA 서열과 Watson–Crick 염기쌍 결합 규칙에 따라 상보적으로 결합함으로써 효과를 나타낸다.
단백질을 암호화하는 핵산 서열이 밝혀져 있다면, 해당 mRNA에 결합하여 단백질 생성을 억제하는 분자를 설계할 수 있다(Figure 1). 단백질의 아미노산 서열 정보를 담고 있는 DNA 또는 RNA의 뉴클레오티드 서열을 센스(sense) 가닥이라고 하며, 이중가닥 DNA에서 이에 상보적인 서열은 안티센스(antisense) 가닥이라고 한다. 또한 RNA 또는 DNA의 센스 가닥에 높은 특이성으로 결합하는 안티센스 뉴클레오티드를 합성할 수 있다.
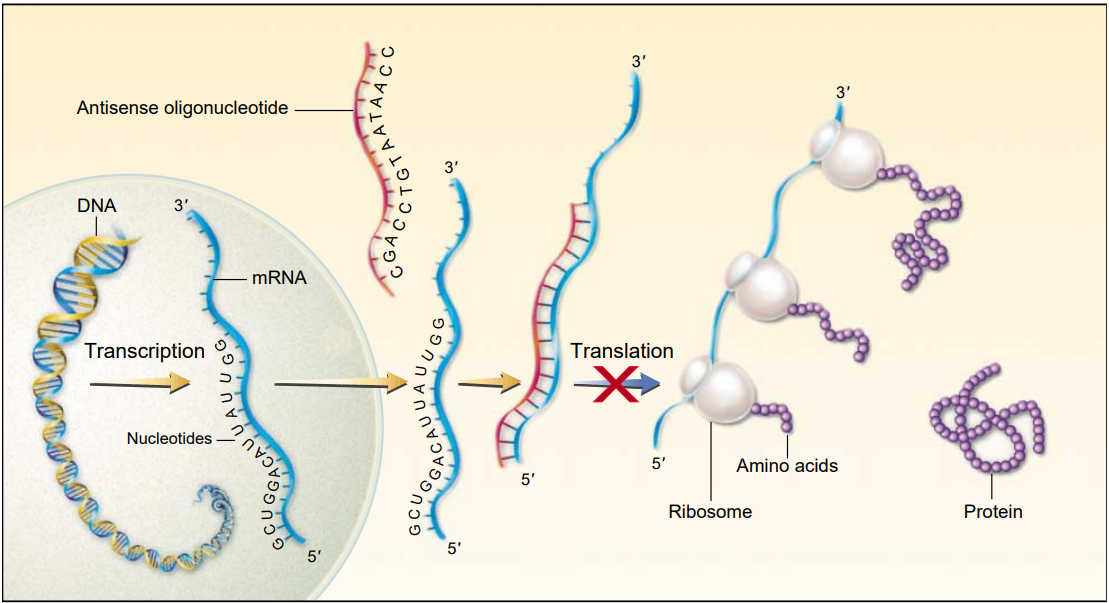
이러한 ASO는 인체 유전체뿐 아니라 바이러스 및 기타 감염성 병원체의 유전체에 의해 발현되는 유전자 산물 역시 선택적으로 차단할 수 있다.
치료용 ASO는 크게 올리고뉴클레오티드와 발현 뉴클레오티드의 두 가지 형태로 개발된다. 올리고뉴클레오티드는 일반적으로 15~20개의 핵산 염기로 이루어진 짧은 단일가닥 DNA이며, 자동 DNA 합성기를 이용해 제조할 수 있다. 반면 발현 뉴클레오티드는 아데노바이러스, 레트로바이러스 또는 플라스미드 벡터와 같은 유전자 치료용 발현 벡터를 이용해 제작된다.
이러한 벡터를 환자에게 투여하면 환자 세포 내에서 ASO가 생성된다. 발현 벡터는 수십 개에서 수천 개 길이의 다양한 안티센스 RNA를 생성하도록 설계할 수 있다. 그러나 이 접근법은 이론적으로는 매력적이지만, 안전성과 효능 측면에서 여전히 한계가 존재한다.
최근 미국 FDA가 여러 핵산 기반 치료제를 승인하면서 안티센스 연구에 대한 관심은 더욱 높아지고 있다. 현재 다양한 안티센스 치료 후보물질이 심혈관 질환, 대사질환, 내분비질환, 신경계 질환, 신경근육 질환, 염증성 질환 및 감염성 질환 치료를 목표로 임상시험 단계에서 활발히 개발되고 있다.
ASO의 작용 기전은?
약 40년 전, Zamecnik과 Stephenson은 13개 염기로 구겅된 합성 단일 가닥 ASO가 Rous 육종 바이러스 mRNA를 표적으로 하여 번역 정지를 유발할 수 있다고 처음 보고하였다. 여러 연구를 통해 활성 ASO는 일반적으로 15~20개 뉴클레오티드 길이이며 상보적 RNA를 표적으로 삼으면서도 심각한 비표적 독성을 유발하지 않는다는 것이 잘 확립되었다. 또한 포괄적인 연구를 통해 합성 ASO의 메커니즘은 RNA 절단(RNA cleavage)과 및 RNA 차단(RNA blockage)의 두 가지 유형으로 나눌 수 있다(Figure 2).
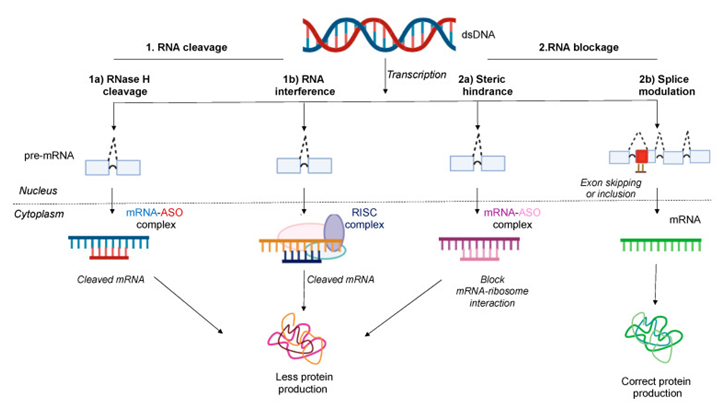
위 그림에서 1a)는 RNase H1 매개 절단, 1b)는 RNA 간섭(RNAi), 2a)는 입체적 장애, 2b) 스플라이스 조절이다. 1a)에서 ASO-mRNA 이중가닥은 RNase H1 효소를 모집하고 이 효소는 표적 mRNA를 절단한다. 1b)에서 RNA 유도 침묵 복합체(RISC)와 관련된 siRNA에 의한 mRNA을 분해한다.
2a)에서 ASO-mRNA 복합체는 mRNA와 리보솜의 상호작용을 입체적으로 차단하여 단백질 번역을 방해한다. 2b)에서는 스플라이스 스위칭 올리고뉴클레오티드(SSO)의 예이다. 사각형은 코딩 엑손(exon) 영역을 나타내고 곡선은 pre-mRNA의 비코딩 인트론(intron) 영역을 나타낸다. 붉은색 사각형은 엑손의 돌연변이 영역을 나타낸다. 점선은 전령 RNA(pre-mRNA)의 스플라이싱 패턴을 나타낸다. RNase H1 매개 절단, RNA 간섭 및 입체적 장애 메커니즘은 단백질 생성을 감소시키는 반면, 스플라이스 조절은 올바른 형태의 단백질을 생성한다.
RNase H1 매개 mRNA 분해
ASO는 표적 mRNA와의 염기서열 상보성을 이용하여 유전자 발현을 선택적으로 억제하는 합성 핵산 치료제로, 특히 RNase H1 매개 기전은 가장 대표적인 작용 방식 중 하나다. 이 기전은 주로 DNA 기반의 ‘gapmer’ 구조를 갖는 ASO에서 나타나며, 세포 내에서 mRNA 분해를 유도하는 핵심 경로이다.
ASO가 세포 내로 유입되면, 표적 mRNA와 상보적으로 결합하여 DNA-RNA hybrid를 형성한다. 이때 ASO의 중앙부는 DNA로 구성되어 있으며, 양 말단은 화학적으로 변형된 RNA 또는 유사체로 이루어져 안정성과 결합 친화도를 증가시킨다. 이러한 구조적 특징은 RNase H1 효소의 인식을 가능하게 하는 결정적 요소이다. RNase H1은 DNA-RNA 이중가닥을 특이적으로 인식하는 엔도뉴클레이스로, hybrid 상태에서 RNA 가닥만을 선택적으로 절단하는 특징을 가진다.
RNase H1이 활성화되면, ASO와 결합된 mRNA는 특정 위치에서 절단되며, 이후 세포 내 exonuclease에 의해 추가적으로 분해된다. 이 과정에서 ASO 자체는 분해되지 않고 재사용될 수 있어, 소량으로도 반복적인 mRNA 분해를 유도하는 촉매적(catalytic) 특성을 보인다. 결과적으로 해당 mRNA로부터의 단백질 번역이 억제되며, 이는 질병 관련 단백질의 발현 감소로 이어진다.
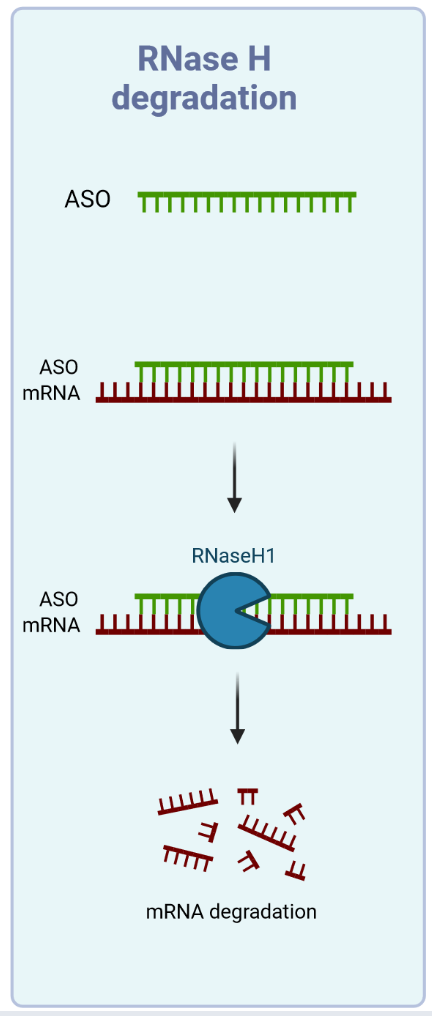
이와 같은 RNase H1 의존적 mRNA 분해 기전은 핵 내에서 주로 일어나며, 이는 RNase H1이 핵에 풍부하게 존재하기 때문이다. 따라서 ASO는 세포질뿐 아니라 핵으로의 효과적인 전달이 중요하며, 최근에는 GalNAc 결합과 같은 표적화 전략을 통해 간세포로의 선택적 전달 효율을 높이고 있다.
따라서 RNase H1 매개 ASO 작용 기전은 ASO–mRNA 결합에 의한 hybrid 형성 -> RNase H1의 선택적 RNA 절단 -> 절단된 mRNA의 추가 분해 -> 단백질 발현 억제의 단계로 이루어지며, 이는 높은 서열 특이성과 효율성을 기반으로 한 RNA 표적 치료 전략의 핵심 원리로 자리 잡고 있다.
입체적 차단(Steric hindrance)
ASO는 표적 RNA에 결합하여 효소적 절단을 유도하지 않고, 물리적 차단을 통해 유전자 발현을 조절하는 방식이다. 이러한 ASO는 일반적으로 RNase H1을 활성화하지 않도록 전 구간이 화학적으로 변형된 뉴클레오타이드로 구성되며, RNA와의 결합 안정성과 세포 내 안정성을 동시에 확보하도록 설계된다.
세포 내로 유입된 steric-blocking ASO는 표적 pre-mRNA 또는 성숙 mRNA의 특정 서열에 상보적으로 결합하여 40S 리보솜 소단위와의 상호작용을 억제하거나 40S 또는 60S 리보솜 소단위에 조립되는 것을 방지함으로써 번역 정지를 유발한다. 이는 RNA 분자의 구조적 접근성을 변화시키며, 리보솜, 스플라이싱 인자, 또는 기타 RNA 결합 단백질이 해당 부위에 접근하는 것을 물리적으로 방해한다.
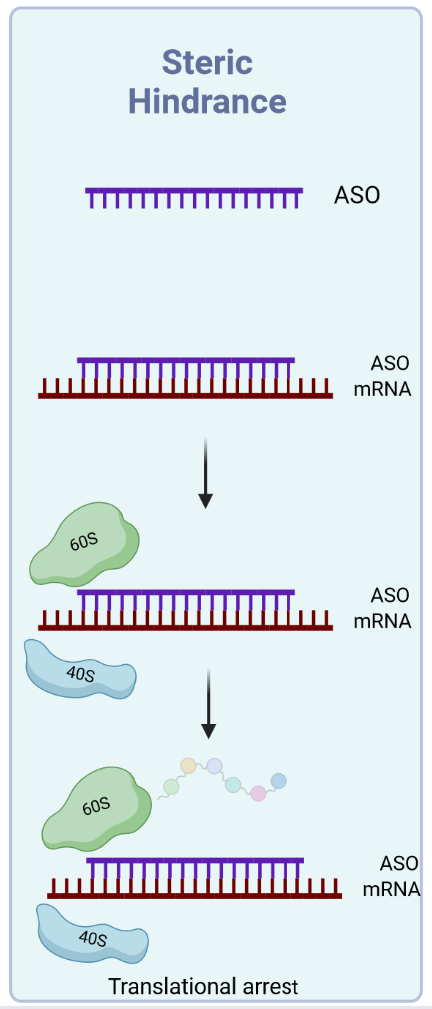
따라서 입체 차단 기반 ASO는 RNA를 직접 절단하지 않고, 특정 기능적 부위를 물리적으로 차단함으로써 스플라이싱 조절 또는 번역 억제를 유도하는 정밀한 유전자 발현 조절 전략이다. 이러한 비절단(non-cleaving) 기전은 높은 서열 특이성과 함께 다양한 RNA 단계에서의 조절 가능성을 제공하며, 차세대 핵산 치료제 개발에 중요한 기반을 형성하고 있다.
스플라이스 변조(modulation) 또는 스플라이스 스위칭(switching)
세포 핵 내에서 전사된 pre-mRNA는 intron 제거와 exon 연결을 포함하는 스플라이싱 과정을 거치며, 이 과정은 spliceosome 복합체와 다양한 splicing factor에 의해 정밀하게 조절된다. 스플라이싱 변조를 유도하는 ASO는 pre-mRNA 단계에서 작용하여 특정 exon의 제외(skipping) 또는 포함(inclusion)을 유도한다.
이 기전은 주로 입체적 차단에 기반하며, RNase H1과 같은 효소적 절단을 유도하지 않고 RNA–단백질 상호작용을 물리적으로 차단함으로써 비정상적인 단백질 생성 억제 또는 기능성 단백질 번역 조절 효과를 나타낸다.
이러한 ASO는 pre-mRNA의 특정 서열, 예를 들어 exon–intron 경계 부위, exonic splicing enhancer(ESE), 또는 intronic splicing silencer(ISS)에 상보적으로 결합한다. 이 결합은 spliceosome이나 보조 인자의 접근을 방해하여 정상적인 스플라이싱 패턴을 변화시킨다.
ASO의 결합 위치에 따라 두 가지 주요 효과가 나타난다. 먼저 exon 제외는 ASO가 전사체에 결합하여 비정상적인 해독 프레임을 교정하고, 짧지만 기능적인 단백질의 생성을 유도한다.
반면 exon 포함은 특정 부위에 결합하여 스플라이싱 억제 요소를 차단함으로써 해당 exon의 포함을 촉진한다. 이러한 전략은 돌연변이로 인해 발생한 비정상적 스플라이싱을 교정하거나, 기능적으로 유리한 isoform의 발현을 선택적으로 증가시키는 데 활용된다.

이들 ASO는 일반적으로 전 구간이 화학적으로 변형된 뉴클레오타이드로 구성되어 RNase H1 활성을 회피하며, RNA에 대한 높은 결합 친화도와 핵 내 안정성을 가진다. 또한 작용 단계가 pre-mRNA이므로 핵 내 전달 효율이 치료 효과를 결정짓는 중요한 요소로 작용한다.
ASO 설계의 특징은 무엇인가?
ASO는 일반적으로 13~30개의 뉴클레오티드 길이로 설계되며, Watson–Crick 염기쌍 결합을 통해 표적 mRNA 또는 pre-mRNA에 상보적으로 결합한다. ASO의 길이는 효능과 안전성 모두에 중요한 영향을 미친다. 짧은 올리고뉴클레오티드도 표적과 안정적으로 결합할 수 있는 충분한 친화력을 가질 수 있으나, 길이가 짧을수록 비표적(off-target) 결합 가능성이 증가하는 경향이 있다.
ASO는 일반적으로 표적 mRNA에 완전 상보적인 염기서열을 갖도록 설계되지만, 일부 염기 불일치(mismatch)가 존재하더라도 효능이 크게 저하되지 않는 경우가 있다. 그러나 이러한 불일치는 유사한 서열을 가진 비의도적 RNA에 대한 결합 가능성을 증가시켜 오프타겟 효과를 유발할 수 있다.
ASO의 효능은 부분적으로 표적 mRNA의 특정 서열에 결합할 수 있는 능력에 의해 결정된다. 단일 가닥 mRNA는 열역학적으로 안정한 2차 구조를 형성하며, 이러한 구조는 ASO의 접근성과 결합 효율을 저해할 수 있다. 일반적으로 ASO 결합이 용이한 부위는 mRNA의 말단 영역, 내부 루프(internal loop), 스플라이싱 접합 부위, 그리고 10개 이상의 연속적인 뉴클레오티드로 이루어진 단일 가닥 돌출부 등이며, 이러한 영역은 ASO 설계에서 유망한 표적 부위로 간주된다.
또한 많은 ASO는 pre-mRNA의 exon–intron 스플라이싱을 조절하도록 설계된다. 이러한 목적을 위해 ASO는 스플라이스 수용체(splice acceptor) 또는 공여체(splice donor) 부위 근처에 결합하도록 설계되는 경우가 많다. 스플라이싱 조절 ASO는 일반적으로 높은 구아닌–시토신(GC) 함량을 가지며, 결합 효능은 CCAC 및 TCCC와 같은 보존된 서열 모티프의 존재와 유의미한 상관관계를 보인다.
한편, 세포 내로 유입된 올리고뉴클레오티드는 표적에 도달하기 전에 뉴클레아제에 의해 쉽게 분해될 수 있으며, 이는 ASO 치료의 주요한 제한 요인으로 작용한다. 이를 극복하기 위해 다양한 화학적 변형이 도입되었으며, 특히 이종핵산(XNA, xeno nucleic acid)은 올리고뉴클레오타이드의 골격, 당, 또는 염기를 변형함으로써 화학적 및 생물학적 안정성을 향상시키는 전략으로 활용된다.
따라서 ASO는 일반적으로 세포 내 안정성과 표적 도달 능력을 향상시키기 위해 화학적으로 변형된 당과 염기를 포함하도록 설계된다. XNA 기반 변형은 다양한 기능적 특성을 부여할 수 있으며, ASO의 약동학적 특성과 작용 효율을 최적화하는 데 중요한 역할을 한다.
ASO의 화학적 변형은 크게 세 가지 범주로 구분된다. 첫째, phosphorothioate(PS), phosphodiamidate morpholino oligomer(PMO), peptide nucleic acis(PNA)과 같은 골격(backbone) 변형이 있다. 둘째, 2′-O-methyl(2′-OMe), 2′-O-methoxyethyl(2′-MOE), 2′-fluoro(2′-F), locked nucleic acid(LNA)과 같은 2′-당 위치 변형이 있다. 셋째, 5-methylcytosine과 같은 뉴클레오베이스 변형이 포함된다.
특히 2′-O-sugar 변형은 RNA 이중가닥의 안정성을 증가시키는 데 널리 사용된다. 그러나 이러한 변형은 RNase H에 의한 표적 RNA 절단 활성화를 저해하는 경우가 많다. 따라서 RNase H 의존적 작용을 유지하기 위해, 일반적으로 2′-sugar 변형이 없는 phosphorothioate 뉴클레오티드와 결합된 gapmer 구조로 설계되는 경우가 많다.
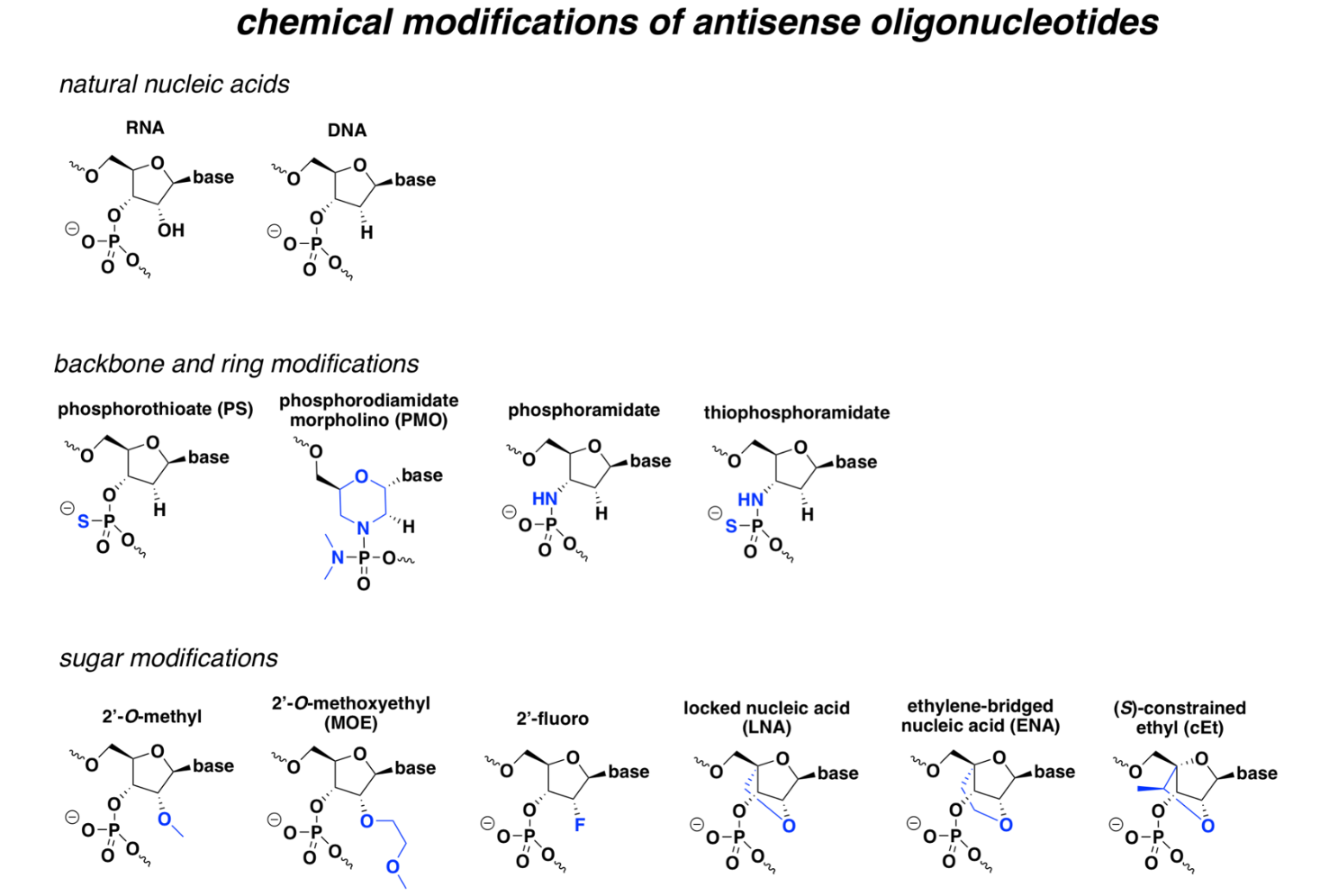
미국 FDA 승인을 받은 ASO 치료제에 사용되는 화학적 변형에는 PS 골격, 2'-MOE 치환, 5'-methylcytosine 염기 치환 및 PMO 올리고머 치환이 있다. 각 치환은 ASO에 이점을 제공하며, 일반적으로 세포 내 안정성을 증가시킨다.
ASO는 어쩐 방향으로 발전되었는가?
ASO는 초기의 단순한 핵산 기반 억제제에서 출발하여, 화학적 안정성, 전달 효율, 작용 기전, 그리고 임상 적용 범위 측면에서 단계적으로 진화해 온 치료 플랫폼이다. 이러한 진화는 크게 세대별 화학적 발전과 전달 기술, 설계 기술의 융합 과정을 통해 이루어졌다.
초기 1세대 ASO는 자연형 DNA와 유사한 구조를 기반으로 하였으나, 체내에서 뉴클레아제에 의해 빠르게 분해되고 약효 지속 시간이 짧으며, 독성 문제가 존재하는 한계를 보였다. 이를 개선하기 위해 phosphorothioate(PS) 골격이 도입되면서 혈장 단백질 결합이 증가하고 체내 안정성이 향상되었으나, 비특이적 결합과 이에 따른 독성 문제가 새로운 과제로 제기되었다.
이후 2세대 ASO에서는 2′-O-methoxyethyl(MOE)과 같은 당 구조 변형이 도입되어 결합 친화도와 안정성이 크게 향상되었으며, RNase H를 활용한 mRNA 분해 기전이 효과적으로 구현되었다. 이 시기에 gapmer 구조가 확립되면서, 중앙의 DNA 영역과 양쪽의 변형된 RNA 구조를 결합한 형태로 효능과 안정성을 동시에 확보하는 설계 전략이 정립되었다.
3세대 ASO에서는 LNA 및 cEt와 같은 고친화도 변형이 도입되어 표적 RNA에 대한 결합력이 크게 증가하였으며, 용량을 감소시키면서도 높은 효능을 달성할 수 있게 되었다. 동시에 입체적 차단 기반의 작용 기전이 발전하여 단순한 mRNA 분해를 넘어 스플라이싱 조절과 같은 다양한 기능적 조절이 가능해졌다.
최근에는 전달 기술의 혁신이 ASO 진화의 핵심 축으로 작용하고 있다. GalNAc 결합(conjugation) 기술은 간세포 특이적 전달을 가능하게 하여 효능을 획기적으로 향상시키고, 투여 용량을 크게 감소시키는 데 기여하고 있다. 또한 항체–올리고뉴클레오타이드 접합체 및 펩타이드 기반 전달 기술은 간 외 조직으로의 전달을 가능하게 하는 방향으로 발전하고 있다.
설계 기술 측면에서도 중요한 진전이 이루어지고 있다. 과거의 경험적 접근에서 벗어나 인공지능과 머신러닝을 활용한 서열 최적화가 가능해지면서, 결합 효율, 오프타겟 효과, 독성 위험 등을 사전에 예측하는 정밀 설계가 구현되고 있다. 이는 개발 효율성 향상과 함께 성공률 증가에 기여하는 중요한 변화로 평가된다.
이와 함께 ASO는 단순한 유전자 억제 도구를 넘어 다양한 치료 전략을 구현하는 플랫폼으로 확장되고 있다. RNase H 매개 분해, 스플라이싱 조절, 번역 억제 등 다양한 작용 기전을 통해 단백질 발현 감소뿐 아니라 기능 회복까지 가능해졌으며, 개인 맞춤형 치료와 같은 새로운 치료 패러다임에도 적용되고 있다.
따라서 ASO는 화학적 안정성의 개선, 전달 기술의 혁신, 설계의 지능화, 그리고 작용 기전의 다양화라는 축을 따라 지속적으로 진화해 왔으며, 현재는 정밀 유전체 의학의 핵심 치료 플랫폼으로 자리잡고 있는 기술로 평가된다.
ASO에는 어떤 약제들이 있는가?
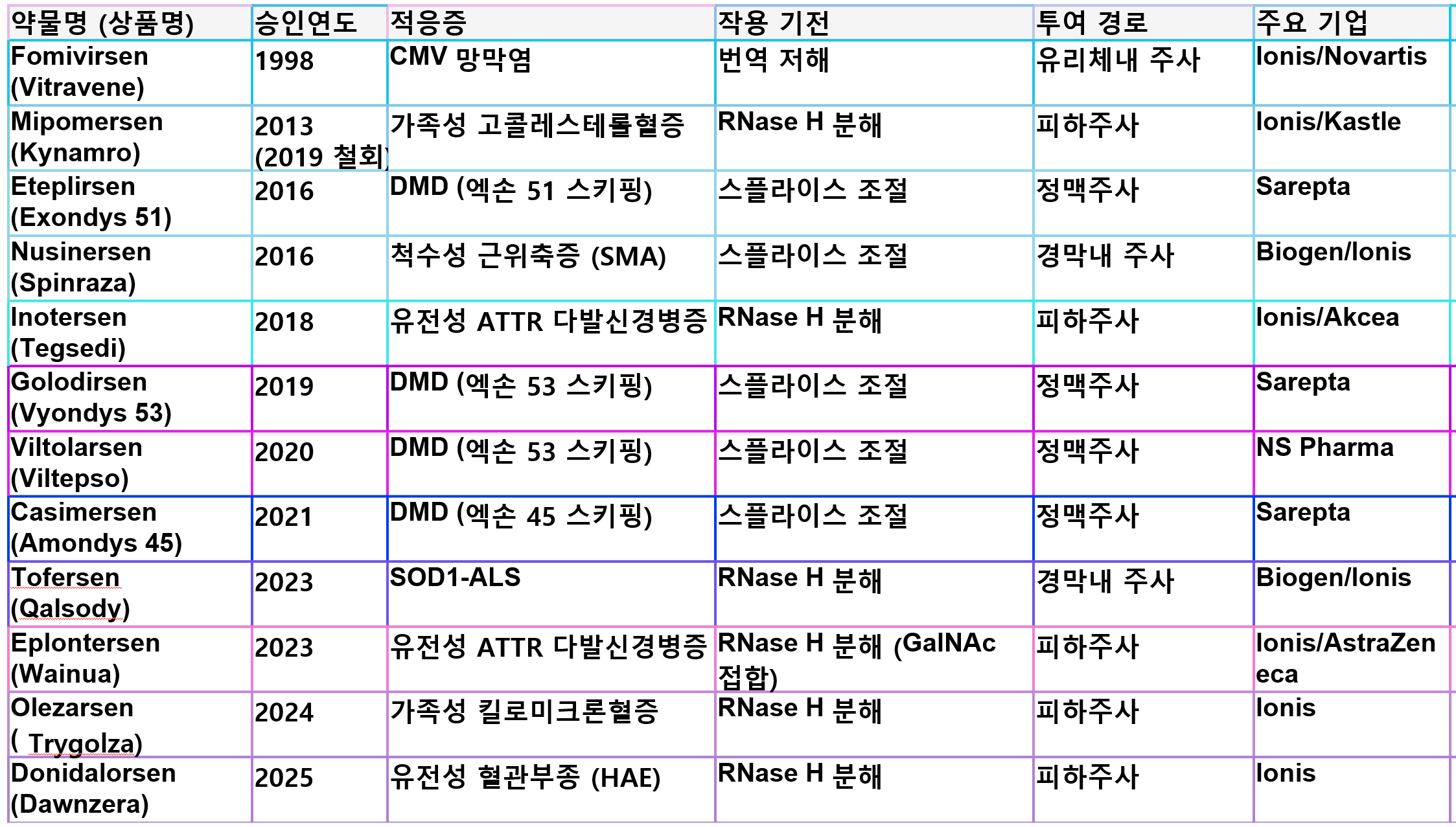
ASO는 1998년 Fomivirsen 승인 이후, 2026년 기준 U.S. Food and Drug Administration에서 다양한 적응증에 대해 다수의 약제가 승인되며 독립적인 치료 플랫폼으로 자리잡았다. ASO 약물은 작용 기전에 따라 여러 유형으로 구분되며, 이에 따라 대표적인 약제들이 존재한다.
첫 번째로, RNase H 의존적 mRNA 분해 기전을 활용하는 ASO에는 Inotersen, Eplontersen, Mipomersen, 그리고 Tofersen 등이 있다. 이들은 표적 mRNA와 상보적으로 결합한 후 RNase H를 유도하여 mRNA를 절단하고, 결과적으로 병인 단백질의 발현을 감소시키는 방식으로 작용한다. 해당 계열은 유전성 트랜스티레틴 아밀로이드증, 가족성 고콜레스테롤혈증, 그리고 SOD1 돌연변이 관련 근위축성 측삭경화증과 같은 질환에서 치료 효과를 나타낸다.
두 번째로, 스플라이싱 조절 기전을 이용하는 ASO가 있다. 이는 pre-mRNA의 스플라이싱 부위를 조절하여 특정 엑손의 포함 또는 제외를 유도하는 방식으로 작용한다. 대표적인 약제로는 Nusinersen이 있으며, Spinal Muscular Atrophy 환자에서 SMN2 유전자의 스플라이싱을 조절하여 기능적 단백질 생성을 증가시킨다.
또한 Duchenne Muscular Dystrophy 치료를 위한 exon-skipping ASO로 Eteplirsen, Golodirsen, Viltolarsen, Casimersen 등이 승인되어 있으며, 이들은 각각 특정 엑손을 선택적으로 제거함으로써 부분적으로 기능적인 dystrophin 단백질의 생성을 유도한다.
세 번째로, 입체적 방해(steric blocking) 기전을 통해 mRNA의 번역 또는 기능을 억제하는 ASO도 존재한다. 이 계열은 특정 RNA 서열에 결합하여 리보솜의 접근을 차단하거나 단백질–RNA 상호작용을 방해함으로써 작용하며, 일부 스플라이싱 조절 ASO 역시 이 범주에 포함될 수 있다.
최근에는 간세포 표적 전달을 위한 GalNAc 결합 기술이 적용된 차세대 ASO가 개발되고 있다. 이에 해당하는 약제로는 Fitusiran, Donidalorsen, Plozasiran 등이 있으며, 이들은 간 특이적 수용체를 이용하여 세포 내 전달 효율을 높인 것이 특징이다. 각각 혈우병, 유전성 혈관부종, 그리고 가족성 유미미크론혈증과 같은 질환에서 치료 효과를 나타내고 있다.
이와 같이 ASO는 작용 기전에 따라 RNase H 매개 mRNA 분해형, 스플라이싱 조절형, 그리고 입체적 방해형으로 구분되며, 각 기전에 따라 다양한 승인 약제가 존재한다. 이러한 약제들은 유전 질환, 신경계 질환, 대사 질환 등 폭넓은 영역에서 활용되고 있으며, 화학적 변형과 전달 기술의 발전을 통해 향후 더욱 다양한 치료제로 확장될 것으로 기대된다.
ASO의 장점은?
ASO는 기존 저분자 약물과 항체 치료제가 가지는 한계를 극복할 수 있는 차세대 치료 전략으로, 표적 범위의 확장성, 개발 속도, 작용 기전의 다양성, 그리고 투여 편의성 측면에서 중요한 장점을 가진다.
가장 핵심적인 장점은 이른바 “undruggable” 표적에 대한 접근 가능성이다. 저분자 약물은 특정 결합 포켓을 가진 단백질에만 작용하고, 항체는 주로 세포 외부 또는 세포막 단백질에 제한되는 반면, ASO는 mRNA 서열에 상보적으로 결합하는 방식으로 작용한다. 따라서 세포 내 단백질뿐 아니라 비암호화 RNA까지 포함한 거의 모든 유전자 산물을 표적으로 삼을 수 있다. 이는 기존 치료 접근이 어려웠던 단백질과 질환 영역까지 치료 범위를 확장할 수 있는 혁신적인 장점으로 평가된다.
또한 ASO는 신속한 약물 개발이 가능하다는 특징을 가진다. 표적 mRNA 서열 정보만 확보되면 비교적 짧은 시간 내에 후보 물질의 설계와 합성이 가능하며, 저분자 약물에서 요구되는 장기간의 구조–활성 관계 최적화 과정이 크게 단축된다. 이러한 특성은 개인 맞춤형 치료에서도 강점을 보이며, 실제로 환자 개별 돌연변이에 맞추어 단기간 내 치료제가 개발된 사례도 보고된 바 있다.
표적 특이성 또한 중요한 장점이다. Watson–Crick 염기쌍 결합 원리에 기반하여 특정 RNA 서열에 정밀하게 결합하기 때문에, 충분한 길이의 뉴클레오타이드 서열을 설계할 경우 유사 유전자 간에도 선택적 억제가 가능하다. 이는 오프타겟 효과를 최소화하고 치료 정확도를 높이는 기반이 된다.
ASO는 다양한 작용 기전을 통해 단백질 발현을 감소시키거나 복원할 수 있는 유연성을 가진다. RNase H 매개 mRNA 분해를 통해 독성 단백질 생성을 억제할 수 있으며, 스플라이싱 조절을 통해 기능성 단백질을 회복시키거나, 번역 저해를 통해 mRNA 기능을 직접 차단할 수 있다. 이러한 다층적 작용 방식은 기존 약물이 주로 억제 기능에 국한되는 것과 비교할 때 치료 전략의 폭을 크게 확장시키는 특징을 보인다.
항체 치료제와 비교하더라도 여러 장점이 존재한다. ASO는 단백질 생성 자체를 억제하기 때문에 고농도의 혈장 단백질에 대해서도 효과적으로 작용할 수 있으며, 비교적 높은 화학적 안정성을 가져 보관과 유통이 용이하다. 또한 투여 간격이 길어 월 1회 또는 그 이상의 간격으로 투여가 가능하여 환자 편의성이 향상된다. 항체 치료에서 문제될 수 있는 항약물항체 형성과 같은 적응 면역 반응이 거의 보고되지 않았다는 점 역시 중요한 차별점이다.
플랫폼 기술로서의 확장성 또한 중요한 특징이다. 하나의 ASO에서 확립된 화학적 변형 기술, 약동학 및 독성 데이터, 제조 공정은 다른 ASO 개발에 직접적으로 활용될 수 있어 후속 약물 개발의 효율성을 크게 향상시킨다. 실제로 특정 화학 플랫폼을 기반으로 용량 감소와 안전성 개선이 동시에 달성된 사례도 보고되고 있다.
또한 화학적 변형 기술을 통해 조직 내 반감기를 크게 연장할 수 있으며, 전달 기술과 결합할 경우 투여 빈도를 최소화할 수 있다. 이는 만성질환 환자에서 치료 순응도를 높이는 중요한 요소로 작용한다.
게다가 ASO는 Cytochrome P450 효소나 주요 약물 수송체에 의해 대사되지 않고, 주로 핵산 분해 효소에 의해 분해되기 때문에 약물–약물 상호작용 위험이 매우 낮다. 이는 다약제 복용이 흔한 환자군에서 안전한 병용 투여를 가능하게 하는 중요한 임상적 이점을 제공한다.
따라서 ASO 치료제는 표적 확장성, 개발 효율성, 작용 기전의 다양성, 그리고 안전성 측면에서 기존 치료제와 차별화되는 강점을 가지며, 향후 다양한 질환 영역에서 핵심 치료 플랫폼으로 발전할 가능성이 높은 기술로 평가된다.
ASO는 어떤 한계를 가지고 있는가?
ASO 치료제는 다양한 장점을 지니고 있음에도 불구하고 몇 가지 중요한 한계를 가진다. 먼저, ASO 치료제의 가장 근본적인 한계는 간(liver) 이외 조직으로 약물을 효과적으로 전달하기 어렵다는 점이다. 현재 GalNAc 결합(conjugation) 기술은 간세포 표면의 아시알로당단백질 수용체를 활용하여 간 특이적 전달을 가능하게 하며, 약 30배 수준의 효능 향상을 달성한 대표적인 성공 사례로 평가된다. 그러나 이러한 성과는 간 조직에 국한되어 있으며, 간 외 조직으로의 전달 문제는 여전히 해결되지 않은 핵심 과제로 남아 있다.
두 번째로, 미국 FDA 승인 ASO 약물 전반에서 간독성, 신독성, 혈소판 감소증, 면역 자극과 같은 다양한 부작용이 보고되고 있다. 이러한 독성은 특히 포스포로티오에이트(PS) 골격과 같은 화학적 변형과 밀접하게 연관되는 특징을 보인다. ASO의 독성은 단일 요인에 의해 결정되기보다는 서열과 화학적 변형 간의 상호작용에 의해 복합적으로 나타나는 것으로 이해되고 있다.
세 번째로, 현재 중추신경계 질환을 표적으로 하는 ASO 치료제는 대부분 경막내(intrathecal) 투여 방식을 통해 전달된다. 이는 ASO의 분자 크기와 음전하 특성으로 인해 혈액뇌장벽(BBB)를 자발적으로 통과하는 것이 근본적으로 제한되기 때문이다. 따라서 전신 투여만으로는 치료에 필요한 농도의 ASO를 뇌 조직에 전달하기 어렵고, 직접적인 중추신경계 접근 방식이 필수적으로 요구된다.
네 번째로, ASO 치료제는 매우 높은 비용으로 인해 접근성과 의료 형평성 측면에서 중요한 도전을 제기한다. 대표적인 사례로 Nusinersen이 있으며, 이는 Spinal Muscular Atrophy 치료에서 획기적인 임상적 효과를 보였음에도 불구하고 경제적 부담이 매우 큰 치료제로 평가된다. 구체적으로 미국에서 nusinersen의 가격은 1회 투여당 약 125,000달러로 설정되어 있으며, 초기 치료 단계에서는 첫 해에 6회 투여가 필요하여 약 750,000달러의 비용이 발생한다. 이러한 비용에는 시술을 위한 의료 인력, 시설 사용료, 환자 및 가족의 이동 비용과 같은 간접 비용이 포함되지 않으며, 실제 경제적 부담은 이보다 더욱 클 것으로 평가된다.
다섯 번째로, 임상 개발 과정에서의 실패 사례 또한 중요한 한계로 지적된다. Tominersen은 Huntington’s Disease 치료를 위해 변이 헌팅틴 단백질(mHTT)을 억제하도록 설계된 ASO로, 초기 임상에서 mHTT 감소에는 성공하였다. 그러나 3상 임상시험에서는 효과 부족과 안전성 문제로 인해 개발이 중단되었다. 주요 결과로는 표적 단백질 감소에도 불구하고 임상 증상이 오히려 악화되었으며, 신경손상 바이오마커 상승과 뇌실 확장 등의 이상 소견이 함께 관찰되었다. 특히 고용량·고빈도 투여군에서 이러한 악화가 더욱 뚜렷하게 나타나, 약물 노출과 독성 간의 용량 의존적 관계가 확인되었다.
이 사례는 정상 헌팅틴 단백질까지 함께 억제되는 비선택성 문제, 최적 용량 설정의 중요성, 질병 기전의 복잡성, 그리고 바이오마커 개선이 반드시 임상적 효과로 이어지지 않는다는 점을 보여주는 대표적인 예로 평가된다.
차세대 ASO는 어떻게 예상하는가?
ASO 기술은 단일 요소의 개선이 아닌 다축적 혁신을 통해 동시에 진화하고 있으며, 이러한 변화는 기존 치료제의 한계를 극복하고 적용 범위를 획기적으로 확장하는 방향으로 진행되고 있다. 특히 화학적 진화, 전달 기술 혁신, 설계 지능화, 제형 다양화, 적응증 확대, 개인화 치료라는 여섯 가지 축이 상호 보완적으로 작용하면서 ASO 플랫폼의 성능을 근본적으로 재정의하고 있다.
먼저 화학적 진화 측면에서는 GalNAc 결합(conjugation)과 cEt 변형의 조합을 통해 약물의 효능과 안정성이 크게 향상되고 있다. 이러한 접근은 간세포로의 선택적 전달과 높은 결합 친화도를 동시에 확보하여, 기존 대비 현저히 낮은 용량에서도 장기간 지속 효과를 구현할 수 있는 기반을 제공한다. 이는 약물 노출을 최소화하면서도 치료 효과를 유지할 수 있는 방향으로 기술이 발전하고 있음을 의미한다.
전달 기술 측면에서는 항체–올리고뉴클레오타이드 접합체와 펩타이드 기반 전달 시스템이 핵심적인 역할을 하고 있다. 이러한 기술은 기존 GalNAc 기반 전달이 간에 국한되었던 한계를 극복하고, 근육과 심장 등 간 외 조직으로의 전달을 가능하게 하는 방향으로 발전하고 있다. 특히 수용체 매개 전달 전략을 통해 특정 조직으로의 선택적 축적을 유도하는 기술은 향후 ASO 적용 범위를 결정짓는 핵심 요소로 평가된다.
설계 기술 또한 빠르게 진화하고 있다. 인공지능과 머신러닝 기반 플랫폼은 ASO 서열 설계 과정에서 결합 효율, 오프타겟 가능성, 독성 위험 등을 동시에 예측할 수 있게 하여 개발 효율성을 크게 향상시키고 있다. 이러한 접근은 기존의 경험적 설계 방식에서 벗어나 데이터 기반의 정밀 설계로 전환되고 있음을 의미하며, 개발 기간 단축과 성공률 향상에 중요한 기여를 하고 있다.
제형 측면에서는 경구 및 흡입 제형 개발이 중요한 변화로 나타나고 있다. 현재 대부분의 ASO가 주사 기반 투여를 필요로 하는 상황에서, 비침습적 제형은 환자 순응도를 크게 향상시키고 장기 치료의 현실적 적용 가능성을 높이는 요소로 작용한다. 이는 치료 접근성을 개선하는 중요한 기술적 진보로 평가된다.
적응증 측면에서는 희귀질환 중심에서 보다 넓은 환자군으로의 확장이 진행되고 있다. 기존 ASO 치료제는 주로 단일 유전자 이상에 기반한 희귀질환에 적용되어 왔으나, 최근에는 심혈관질환 및 만성 대사질환과 같은 대규모 질환으로 적용 범위가 확대되고 있다. 특히 지질 대사 관련 표적을 중심으로 한 임상 연구는 수억 명의 환자에게 적용 가능한 가능성을 제시하고 있다.
개인화 치료 측면에서는 유전체 진단과 ASO 설계를 통합한 N-of-1 접근이 점차 확장되고 있다. 환자의 유전적 변이를 기반으로 맞춤형 ASO를 설계하고 이를 치료에 적용하는 통합 파이프라인은 정밀의학의 궁극적 형태를 구현하는 전략으로 평가된다. 이러한 접근은 향후 개인 맞춤 치료의 새로운 표준으로 자리잡을 가능성을 시사한다.
이와 같이 다양한 기술 축의 동시적 발전은 ASO를 단순한 희귀질환 치료제를 넘어 정밀 유전체 의학의 핵심 플랫폼으로 전환시키고 있다. 특히 향후 진행 중인 대규모 임상시험 결과는 이러한 변화의 임상적 가치를 결정짓는 중요한 전환점이 될 것으로 예상되며, 치료 패러다임이 기존의 단백질 기반 접근에서 RNA 수준의 조절 중심으로 이동하는 구조적 변화를 가속화할 것으로 전망된다.
참고문헌
1. Frederick K et al. “ANTISENSE-OLIGONUCLEOTIDE THERAPY” N Engl J Med 1996 ; 334 : 316 - 318.
2. Karishma Dhuri et al. “Antisense Oligonucleotides: An Emerging Area inDrug Discovery and Development” J. Clin. Med. 2020, 9, 2004.
3. Christoph Niemietz et al. “Therapeutic Oligonucleotides Targeting Liver Disease: TTR Amyloidosis” Molecules 2015, 20, 17944-17975.
4. D. Collotta et al. “Antisense oligonucleotides: a novel Frontier in pharmacological strategy” Front. Pharmacol. 14:1304342.
5. Young-Kook Kim“RNA therapy: rich history, various applications and unlimitedfuture prospects” Experimental & Molecular Medicine (2022) 54:455–465.
6. T. Crooke “RNA-Targeted TherapeuticsStanley” Cell Metabolism 27, April 3, 2018.
7. 기타 인터넷 자료(보도 자료, 제품 설명서 등).
관련기사
-
㉖ 최초 원발성 lgA 신병증 항체치료제 '시베프렌리맙'
2026-04-17 06:00
-
㉕돋보기 대신 노안 치료 복합점안제 '유브지'
2026-04-03 06:00
-
㉔말단비대증 첫 경구용 SST2 작용제 '팔투소틴'
2026-03-20 06:00
-
㉓최초의 PDE4B 선택적 억제제 '네란도밀라스트'
2026-03-06 06:00
-
㉒인간 유래 FcRn 억제 단클론항체 '니포칼리맙'
2026-02-20 06:00
- 익명 댓글
- 실명 댓글
- 댓글 0
- 최신순
- 찬성순
- 반대순
오늘의 TOP 10
- 1"팔수록 손해라도 일단 잡자"…제약업계 변칙 영업 확산
- 2창고형 첫 폐업 사례 나오나…전북 A약국 돌연 영업중단
- 3HLB 진양곤 회장 차녀 진인혜, 차세대 항암사업 전면 배치
- 4국산 CAR-T 첫 등장…4월 의약품 허가 '봇물'
- 5LG화학, 제일약품에 28억 손해배상 소송 청구한 이유는
- 6"혁신제약, 항구적 약가우대…성분명 처방 의사 처벌 없애야"
- 7과소비 유발 창고형약국…'언젠가 쓰겠지' 소비자들 지갑 열어
- 8하이텍팜, 차현준 체제 가동…생산 안정화·수익성 회복 시동
- 9㉗ RNA 표적 치료의 대표 주자, ASO 플랫폼
- 10[팜리쿠르트] 일동·광동·제뉴원사이언스 등 약사 채용





















































![[경방신약] 방콜브이산](https://cdn.platpharm.co.kr/2025/12/2512310630020002495.webp)
![[신신제약] 모스키토 밀크](https://cdn.platpharm.co.kr/2025/10/2510150733400004067.webp)
![[유한양행] 안티푸라민 파스 시리즈](https://cdn.platpharm.co.kr/2024/05/2405280631070000069.png)
![[일양약품] 프로엑스피](https://cdn.platpharm.co.kr/2026/01/2601221008450010125.webp)
![[신신제약] 아렉스마일드](https://cdn.platpharm.co.kr/2023/11/2311300927130000133.jpg)
![[옵투스] 오에수 시리즈](https://cdn.platpharm.co.kr/2026/02/2602130209000031633.webp)
![[리쥬올] PDLLA 퍼밍 크림 30ml](https://cdn.platpharm.co.kr/2026/04/2604070229110000386.webp)
![[종근당] 브레이닝캡슐](https://cdn.platpharm.co.kr/2025/06/2506040708450012544.png)
![[일양약품] 도담도담 시리즈](https://cdn.platpharm.co.kr/2024/02/2402020935180000240.jpg)
![[삼진제약] 게보핏 시리즈](https://cdn.platpharm.co.kr/2024/07/2407100728250000386.png)
![[노보노디스크] 위고비](https://cdn.platpharm.co.kr/static/dailypharm/Wigobi.png)
![[유한양행] 마그비 시리즈](https://cdn.platpharm.co.kr/2024/03/2403261023280000193.jpg)
![[CHD제약] 50년 전통의 천혜당 식염포도당](https://i.baropharm.com/products/202604/1775095858899.png)
![[켄뷰] 오리지널 폼타입, 로게인5%폼에어로졸60g](https://i.baropharm.com/products/dc84d96e-d0b4-46bc-bcc8-d62016406fe4.png)
![[아워팜] CJ웰케어, 바이오코어 1000억 유산균](https://i.baropharm.com/products/202604/1776750298620.png)
![[알엑스미] 알엑스미 리쥬영 울트라 PDRN 10000 딥리페어 크림](https://i.baropharm.com/partner/products/70c72dd0-cfd3-4d80-87e4-dc4f8de6658b.png?label=바뷰페로고)
![[리쥬올] 닥터 리쥬올 어드밴스드 PDRN 리쥬비네이팅 크림 30ml](https://i.baropharm.com/partner/products/a201d2b4-f21e-4b13-957c-846d286b3d21.jpg?label=바뷰페로고)
![[아워팜] 우리아이 맞춤설계, 바로타민 kids 엘더베리맛](https://i.baropharm.com/partner/products/3f39593e-6318-4dd9-a778-c008c868b5c8.png)
![[휴온스 ] 비듬을 한번에, 니조랄 2%액](https://i.baropharm.com/products/478a284d-4361-4b4a-8a00-8bab80f34319.png?label=PLAN_01)
![[레비온] PDRN+EGF, 레비온RX PDRN EGF 크림](https://i.baropharm.com/products/202512/1765949426601.png)
![[경동제약] 인태반 자양강장제, 파워콤프](https://i.baropharm.com/partner/products/0a2cbb4c-96c5-40a5-aec2-8beeae11682c.png)
![[한독] 붙이는 통증 전문가, 케토톱 액티브 플라스타(쿨) 40매](https://i.baropharm.com/products/202503/1741829602305.png)
![[켄뷰] 다양한 통증에, 타이레놀정 500mg 10정](https://i.baropharm.com/products/6c6ea4f4-7ab2-44f2-a165-f062d80f525b.png)
![[쥬베룩] 진짜 쥬베룩을 담은 약국전용 PDLLA 크림](https://i.baropharm.com/products/202604/1775343960671.png?label=바뷰페로고)




