- LOGIN
- MemberShip
- 2026-04-26 20:32:38
- Can rare disease access reforms resolve the blind spots?
- by Eo, Yun-Ho | translator Alice Kang | 2026-04-26 13:45:06
Attention is focused on whether the government’s policy to strengthen access to rare disease drugs can be properly implemented in Korea.
As many new drugs still remain unattended, in the “blind spots,” some are also expressing doubts about the effectiveness of the policy.
Last March, the Ministry of Health and Welfare approved measures to improve the drug pricing system, and formalized its direction to increase patient access to treatments for severe and rare diseases and to appropriately evaluate the value of innovative new drugs.
While the pharmaceutical industry views this as a meaningful first step toward lowering the reimbursement barrier for rare disease treatments in Korea’s health insurance system, it notes that innovative rare disease drugs subject to cost-effectiveness evaluations remain in a blind spot.
The pharmacoeconomic evaluation is a stage that takes the longest in South Korea’s health insurance reimbursement evaluation process. New drugs that do not meet the criteria for exemption from pharmacoceconomic evaluation or for which the weighted average price of alternative drugs cannot be accepted must follow the existing procedure.
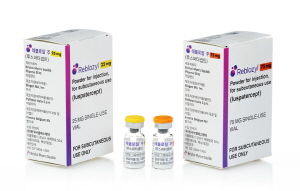
One example is ‘Reblozyl (luspatercept),’ a treatment for anemia in myelodysplastic syndromes (MDS) and beta-thalassemia. Reblozyl, which was approved in Korea in 2022, has remained a non-reimbursed drug to date after failing to pass the Health Insurance Review and Assessment Service (HIRA) Drug Reimbursement Evaluation Committee in August 2023.
This drug is the first erythropoiesis-inhibiting agent introduced in the MDS and anemia treatment landscape in decades. Based on the Phase III COMMANDS study, it is evaluated to have fundamentally reduced transfusion dependency by achieving a 1.7 times higher transfusion independence compared to existing treatment. A follow-up analysis published last year also suggested the potential for long-term survival benefits, including extended overall survival (OS).
Reblozyl is facing structural limitations in the reimbursement entry process. This is because the current health technology assessment framework, which requires setting the low cost of blood transfusions as the comparator, makes it difficult to reflect the drug’s true value.
Professor Joonshik Hong, Secretary of the Acute Myeloid Leukemia and Myelodysplastic Syndrome Research Group at The Korean Society of Hematology (Professor, Department of Hematology, Seoul National University Hospital) said, “Reblozyl not only practically changes the treatment paradigm by reducing prolonged hospital stays and the high burden of complications in patients who required repeated transfusions, but also has significant clinical meaning in that it is the first in the hematologic malignancy field to demonstrate long-term transfusion independence, thereby alleviating the burden on healthcare resources.”
He added, “Although it is effectively the optimal alternative and the only hope for patients with MDS-related anemia at moderate risk or lower who require blood transfusions, delays in its inclusion in the national health insurance reimbursement list mean that patients are forced to bear the full burden of transfusions and complications.”
In addition, in clinical practice, the need for a flexible evaluation system that reflects disease-specific characteristics is being raised for patients with de facto rare diseases who have difficulty making their voices heard within institutional blind spots.
In the case of MDS, there are only about 1,700 new cases annually in Korea, and only a very small fraction of those require treatment for transfusion-dependent anemia. Last March, a petition urging reimbursement coverage for Reblozyl was posted on the National Assembly’s public petition platform, but due to such limitations, the agreement rate remained at around 2% until just before its closure.
Professor Hong added, “The fact that MDS was excluded from the special calculation for rare diseases is merely because a separate review was not conducted due to it being applied a special designation for severe cancers. But it is, in fact, a rare disease. Just as paroxysmal nocturnal hemoglobinuria, which has a similar pathophysiology and requires chronic blood transfusions, is recognized as a rare disease, MDS also urgently requires flexible evaluation that takes into account its disease-specific characteristics.”
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.





