- LOGIN
- MemberShip
- 2026-04-26 21:54:14
- Biosimilars to Prolia compete for the market worth KRW 170B
- by Whang, byung-woo | translator Hong, Ji Yeon | 2025-04-10 05:57:18
As biosimilars have been introduced following the patent expiration of the osteoporosis treatment, 'Prolia (denosumab),' competition in the market is expected to heat up.
As biosimilars from Celltrion and Samsung Bioepis, distributed by Daewoong and Hanmi, respectively, become distributed, the original drug producer, Chong Kun Dang, and the biosimilar companies are expected to engage in active marketing activities.

Last year, Prolia's reimbursement criteria were expanded.
Reimbursement has been expanded allowing even borderline patients who reached the treatment target defined by the T‑score for osteoporosis, thereby extending its influence.
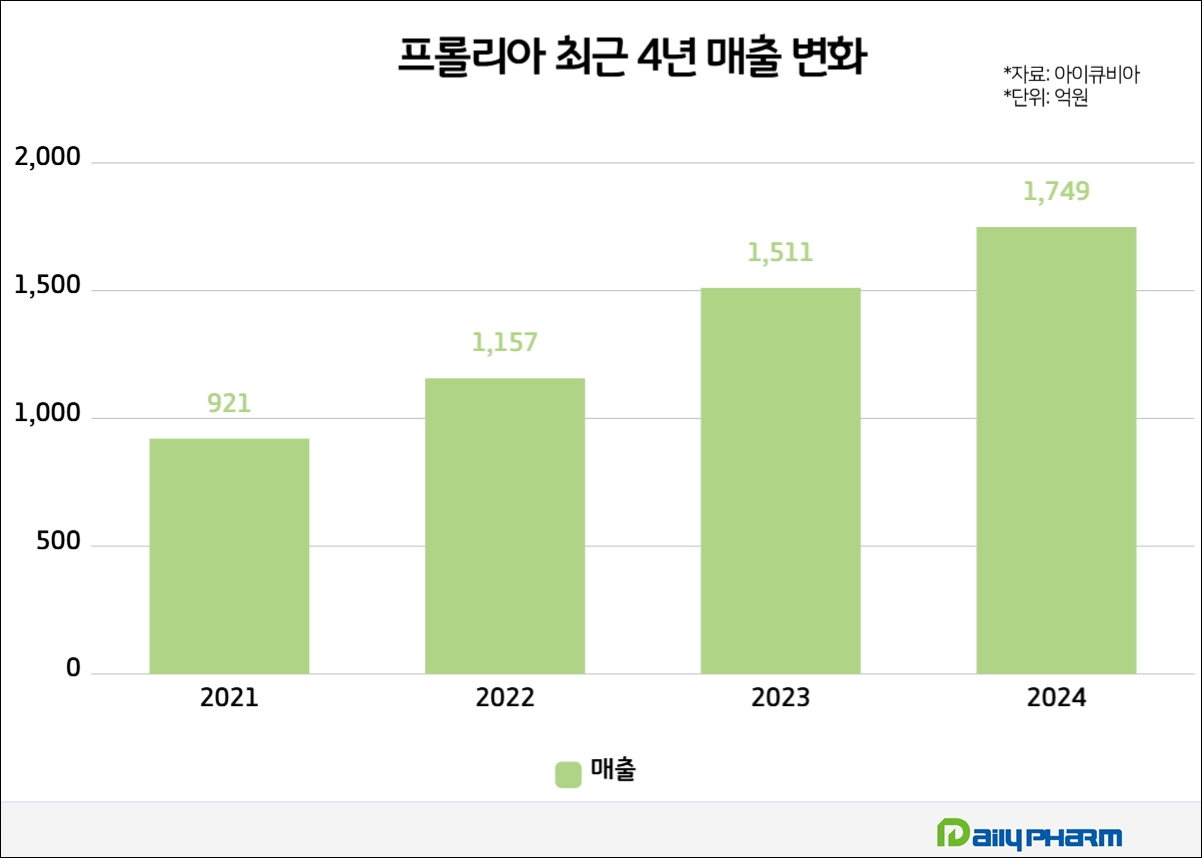
After surpassing KRW 100 billion in sales with KRW 115.7 billion in 2022, Prolia's sales continued to grow, reaching KRW 151.1 billion in 2023 and KRW 174.9 billion in 2024.
However, following the expiration of domestic patents last March, biosimilars have been introduced, inevitably impacting Prolia's sales.
The first to enter the market was Celltrion's Stoboclo, which captured the 'first mover' position by receiving marketing approval from the MFDS in November last year—the first biosimilar to denosumab to be approved.
The syringe is designed so that the needle is automatically concealed after injection, allowing for single-handed handling, and minimizing needle-related injury risks.
Subsequently, on the 4th, Samsung Bioepis' Prolia biosimilar, Obodence, received domestic marketing approval.
Although the reimbursement price for Obodence has not yet been set, it is expected to be launched on the market by the end of this year after completing the reimbursement listing process with the Ministry of Health and Welfare (MOHW).
Stoboclo, already available in the market, is expected to capture market share based on the price competitiveness of biosimilars.
As of April 1, Prolia's reimbursement price was adjusted from KRW 154,700 to KRW 123,760.
In contrast, Stoboclo's reimbursement price is KRW 111,384, approximately KRW 10,000 lower than the original product's price.
Although Samsung Bioepis' pricing strategy is difficult to predict, several opinions suggest it will be set at the same level as Stoboclo.
However, unlike overseas markets, where biosimilars have strong price competitiveness, the domestic market relies more on sales capabilities, which is likely to drive market competition.
We must wait and see, but according to the Health Insurance Review and Assessment Service (HIRA) announcement, by March 18, 2026, the price difference between the original drug, Prolia, and its biosimilar, Stoboclo, will be eliminated.
In other words, this implies that the price competitiveness of biosimilars will be lost.
Currently, the market is dominated by major domestic pharmaceutical companies with strong sales capabilities, such as Amgen-Chong Kun Dang, Celltrion-Daewoong, Samsung Bioepis-Hanmi Pharmaceuticals.
It is anticipated that competition among biosimilars will be influenced by whether they pass the Drug Committee (DC) reviews at hospitals.
Based on other biosimilar cases, hospitals tend not to secure two biosimilars, so the extent of a company's network of prescribing hospitals could determine its success.
From this perspective, it appears that Stoboclo, which was the first to enter the market, may initially have a competitive edge; however, given that osteoporosis treatments are prescribed not only in university hospitals but also in primary clinics, it remains to be seen what strategies each company will deploy.
In Amgen's case, its original product, containing the active ingredient denosumab, is expected to solidify its market position by emphasizing its authenticity and strengthening its partnership with Chong Kun Dang.
According to pharmaceutical industry sources, Amgen is actively working to expand its partnership with Chong Kun Dang, especially in university hospitals, to further reinforce its sales capabilities.
Prolia's long-term efficacy and safety data, accumulated over many years, may also serve as a strong competitive advantage.
Prolia's long-term benefits were demonstrated in two studies, FREEDOM (from August 1, 2004, to June 17, 2008) and FREEDOM Extension (from August 7, 2007, to July 19, 2015).
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.





