- LOGIN
- MemberShip
- 2026-05-02 19:40:14
- Market withdrawal and indication transfer
- by Kim, Jin-Gu | translator Kang, Shin-Kook | 2024-04-30 05:49:54

inno.N’s 'Dapa N.' Due to this clever co-promotion strategy between AstraZeneca Korea and HK inno.N, the prescription market worth KRW 50 billion annually is expected to significantly shift.
In particular, HK inno.N’s Dapa N, assuming the indication that no other generics have, is expected to become a dark horse in the SGLT-2 inhibitor market.
HK inno.N ‘Dapa N’ assumes the original indication…anticipated to expand its presence in the diabetes market According to pharmaceutical industry sources on the 30th, AstraZeneca Korea recently voluntarily canceled domestic approval for Forxiga tab.
At the same time, the company transferred chronic heart failure and chronic kidney disease indications to HK inno.N’s Dapa N.
The company granted the clinical documents to HK inno.N.
Dapa N will have the same reimbursement criteria as Forxiga.
In terms of indications, Dapa N essentially acquired the original product’s market position.
The analysis suggests that this transaction benefits both AstraZeneca Korea and HK inno.N.
HK inno.N’s expansion in the market for SGLT-2 inhibitor class diabetes treatment is expected.
This market has shifted significantly following the changes made by Forxiga, which ranked as the No.1 product.
Since Forxiga’s patent expired in April, generics have been launched.
In December, AstraZeneca decided to withdraw Forxiga from the Korean market.
Consequently, Forxiga’s prescription performance significantly dropped.
According to the medical market research firm UBIST, Forxiga’s prescription sales in Q1 were KRW 11.3 billion, down 22% compared to Q1 of last year.
AstraZeneca plans to stop distributing additional products once current stocks are depleted.
A significant drop in prescription sales is inevitable after Q2.
On the other hand, Forxiga generics have competed fiercely, showing rapid growth over the past year.
Forxiga generics, officially launched in Q2 last year, generated a prescription performance of net KRW 10.2 billion in Q1.
The market share for diabetes treatments containing dapagliflozin has expanded to 48%.
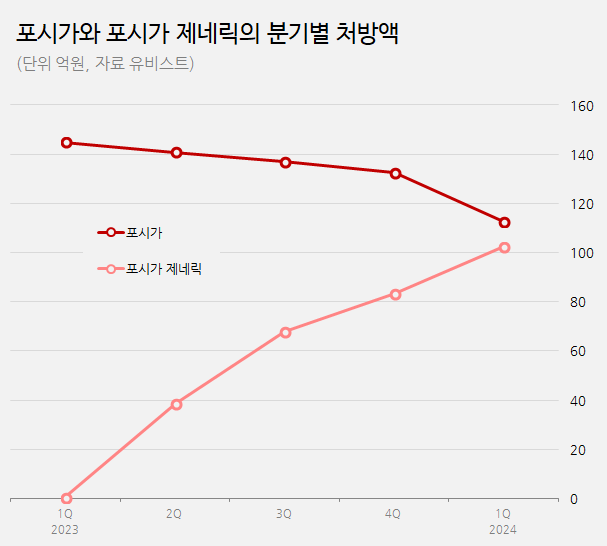
(unit: KRW 100 million, source: UBIST) However, HK inno.N’s Dapa N did not generate satisfactory performance compared to other generic products.
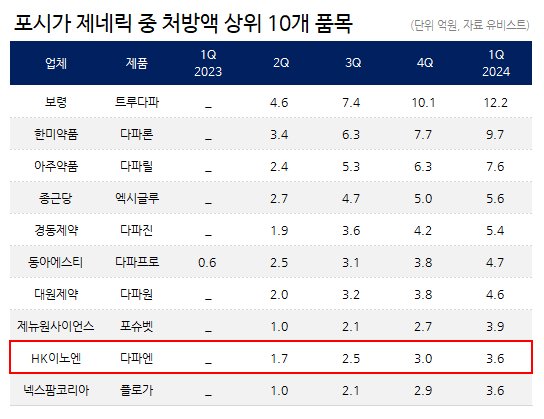
Dapa N’s prescription performance in Q1 was KRW 359 million.
Dapa N is ranked 9th among those products that generated less than KRW 1 billion, such as Boryung’s ‘Dapapro’ and Hanmi Pharmaceutical’s ‘Dapalon.’ In these circumstances, the analysis suggests that Dapa N has established an opportunity to expand its prescription performance by assuming the original product indication.
At the same time, Dapa N is expected to expand its presence in the market for diabetes treatment, including SGLT-2 inhibitors.
Forxiga generics are currently approved for diabetes treatment indications.
They cannot be used for treating chronic heart failure·chronic kidney disease, which AstraZeneca gained approval for these indications through additional clinical studies.
Separate usage patents protect indications of chronic heart failure and chronic kidney disease.
AZ Korea minimizes an annual KRW 50 billion gap…the key would be switching Forxiga→Dapa N in the prescription field The analysis suggests that this transfer is a favorable decision for AstraZeneca Korea.
It is expected to minimize the KRW 50 billion annual sales gap, especially after headquarters decided to withdraw Forxiga from the Korean market.
At the end of last year, AstraZeneca Korea signed a co-promotion agreement with HK inno.N for Xigduo·Sidapvia, a combination therapy containing dapagliflozin.
Accordingly, HK inno.N signed a contract to assume the role of domestic distribution of Forxiga until its withdrawal from South Korea.
This previous transaction resulted in both companies deciding to transfer the Forxiga indication to Dapa N.
Through this comprehensive collaboration for the diabetes treatment portfolio, AstraZeneca Korea can maintain its market presence.
Since this is the first case of a generic product inheriting the original product indication, it is a matter of great interest to the pharmaceutical industry.
The analysis indicates that indication transfer via granting clinical documents was the first, as it is unusual for a blockbuster original product to withdraw from the market in South Korea.
The key would be the preference for Dapa N in the prescription field.
In the endocrine field, general hospitals tend to prefer the original product.
Although Dapa N assumed the original product’s indication, it is uncertain whether the prescription field would regard it as the original product.
It is estimated to generate quarterly prescription performance of KRW 5 billion to 6 billion when it successfully substitutes Forxiga after the second quarter.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo
- "Vabysmo PFS shifts the retinal disease treatment persistence·efficiency"
- Reporter's view | Son, Hyung Min







