- LOGIN
- MemberShip
- 2026-05-02 10:19:09
- Commercialization of global RSV vaccines in progress in KOR
- by Son, Hyung-Min | translator Kang, Shin-Kook | 2024-07-31 05:52:10
A global respiratory syncytial virus (RSV) vaccine has entered late-stage clinical trials for the first time in Korea, testing its potential for commercialization.
Pfizer recently received approval to initiate a Phase III clinical trial in Korea to evaluate the immunogenicity of its RSV vaccine.
Moderna is applying for Japanese approval of its RSV vaccine, which was approved in the U.S.
in May, and making its way into Asian countries.
Among domestic biotech companies, EuBiologics has entered Phase I clinical trials in Korea.
RSV is a virus that causes pneumonia and bronchitis.
The virus can affect a person of any age, but the infection rate is particularly high in infants and young children.
It is the leading cause of hospitalization in infants and young children, and 90% of infants worldwide are infected with RSV before the age of 2.
When infected, RSV causes symptoms similar to the common cold, but some infants and children may experience a more severe course, leading to lower respiratory tract illnesses such as pneumonia and bronchiolitis.

The trial will be conducted at 16 institutions, including Samsung Medical Center, Severance Hospital, and Seoul St.
Mary's Hospital, from October this year to December next year.
In the trial, Pfizer will evaluate the safety, tolerability, and immunogenicity of the RSV vaccine in 360 older adults.
The primary endpoints will be local reactions (redness, swelling, and pain at the injection site) and systemic events (fever, fatigue, headache, vomiting, nausea, diarrhea, muscle pain, and joint pain), based on which the company will evaluate the adverse events and tolerability of PF-06928316.
Participants will be randomized in a 2:1 ratio to PF-06928316 or placebo.
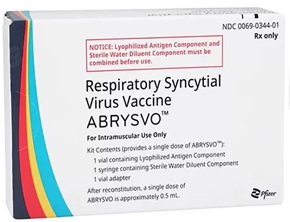
last year and launched under the brand name Abrysvo.
Abrysvo is indicated for adults 60 years of age and older, infants 6 months of age and younger, and pregnant women at less than 37 weeks gestation.
Recently, Pfizer confirmed the immunogenicity of Abrysvo in adults aged 18 to 59 years, raising the possibility of its indication expansion.
Abrysvo demonstrated non-inferior neutralization responses in 681 adults aged 18 to 59 years with certain chronic diseases and 200 immunocompromised adults compared to that identified in the original clinical trial that evaluated the vaccine in older adults.
Participants also achieved at least a four-fold increase in serum neutralizing titers following receipt of Abrysvo compared to pre-vaccination.
These results support the potential for Abrysvo’s expanded indication.
It also opened the door for Pfizer to enter clinical trials in Korea to evaluate the immunogenicity of the RSV vaccine in all ages.
Moderna receives approval in the U.S.
and seeks to enter the Asian market…EuBiologics starts clinical trial in Korea
Among the companies, Moderna has applied for mRNA-1345’s approval in Japan and is seeking to enter the Asian market.
Moderna submitted an application for mRNA-1345 to Japan's Ministry of Health, Labour and Welfare in May.
mRNA-1345 was approved in the U.S.
in May and was developed to prevent RSV in adults aged 60 and older.
The application is based on the interim analysis results of the Phase III ConquerRSV that demonstrated immunogenicity and tolerability of mRNA-1345.
The trial was conducted in 22 countries, including Japan.
The ConquerRSV trial was a randomized, double-blind, placebo-controlled study that enrolled approximately 37,000 adults aged 60 years and older in 22 countries, including the United States.
The interim analysis was based on two definitions of RSV lower respiratory tract disease (RSV-LRTD), defined as two or more symptoms or three or more disease symptoms.
Results showed that in RSV-LRTD defined as two or more symptoms, mRNA-1345 met all primary endpoints, including demonstrating 83.7% vaccine efficacy.
Adverse events with mRNA-1345 were mild to moderate, with the most commonly reported adverse events in the mRNA-1345 arm being injection site pain, fatigue, headache, myalgia, and arthralgia.
In addition to the U.S.
and Japan, Moderna plans to file for approval of mRNA-1345 in the European Union (EU) and other countries.
In Korea, EuBiologics has entered clinical trials.
The euRSV vaccine being developed by EuBiologics has recently been administered to 3 RSV patients at Korea University Guro Hospital.
Patients were randomized to placebo, low-dose EuRSV, and high-dose EuRSV to evaluate the vaccine’s tolerability and safety.
EuRSV is a recombinant protein subunit vaccine that combines the virus’s F-protein antigen with an immune booster.
In 2017, Eubiologics in-licensed the immune booster EuIMT from the Korea Institute of Science and Technology.
EuBiologics aims to enter global Phase 2/3 trials through its U.S.
subsidiary, Eupop Life Sciences, which holds the marketing rights for EuRSV in the North American and European markets.
In addition, SK Bioscience is also developing an mRNA-based RSV vaccine candidate like that being developed by Moderna.
SK Bioscience began RSV vaccine development in 2018 with the aim to commercialize it by 2029 but is still in the basic research stage.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo
- "Vabysmo PFS shifts the retinal disease treatment persistence·efficiency"
- Reporter's view | Son, Hyung Min







