- LOGIN
- MemberShip
- 2026-05-01 00:51:25
- Imfinzi passes first step to reimb in KOR… key is the price
- by Whang, byung-woo | translator Alice Kang | 2024-11-19 06:13:23
With the reimbursement standard set for the immuno-oncology drug Imfinzi (durvalumab), which is under review for reimbursement extensions, how the discussions will develop thereafter is gaining attention.
Although the first step has been taken, attention is being paid to the future process as the matter was mentioned during the National Assembly’s Health Insurance Review and Assessment Service National Audit.
The drug price is the key issue.
Consensus on the cost is expected to be crucial amid the rising health insurance expenses being spent on anticancer drugs.

As a result, Imfinzi was set reimbursement standards in combination with gemcitabine and cisplatin for the first-line treatment of patients with locally advanced or metastatic biliary tract cancer. In addition, AstraZeneca's Imjudo (tremelimumab) has also been set reimbursement standards in combination with Imfinzi in liver cancer, raising expectations for further coverage of the drug. In a response to a written inquiry during the NA Audit, HIRA had said, “As a result of the CDDC review that was held in November last year, the committee decided Imfinzi’s cost should fully be borne by patients due to its high price and high financial spending compared to clinical benefits.” However, the CDDC changed its decision and recognized Imfinzi’s clinical benefits this time around.
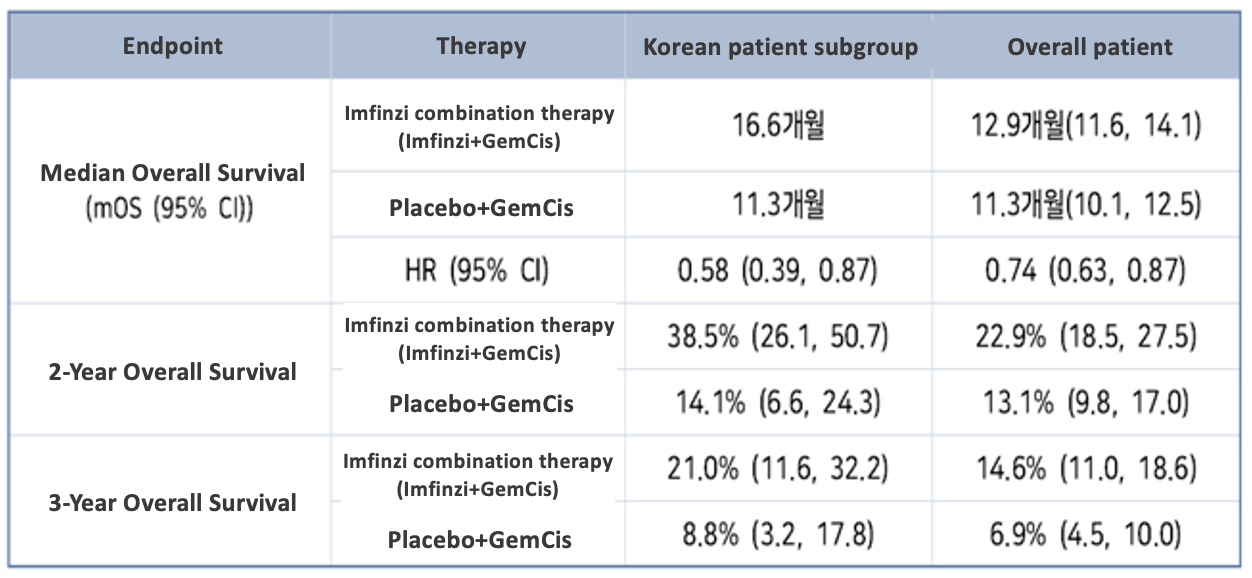
In fact, a Korean subgroup analysis of TOPAZ-1, Imfinzi’s Phase 3 trial in biliary tract cancer, which was presented at the Korean Society of Medical Oncology (KSMO) International Conference in September, showed improved median overall survival (mOS) and 3-year OS rate in Korean patients.
Korean patients treated with the Imfinzi combination showed an mOS of 16.6 months, compared to the 11.3 months found in Korean patients treated with conventional therapy, which is a 5.3-month extension in overall survival.
The OS rate at 3 years also improved over twofold, being 21.0% in the Imfinzi combination arm and 8.8% in the conventional therapy arm.
The key question is whether it will pass the next stage, the Drug Reimbursement Evaluation Committee review.
Although the company has succeeded in expanding the reimbursement standard for Imfinzi and setting the reimbursement standards for Imjudo in biliary tract cancer and liver cancer, respectively, there is also the burden of increased use for Imfinzi that would affect the drug’s price.
Currently, Imfinzi costs around KRW3.34 million per bottle, and the cost of administering the drug is even higher for liver cancer patients who receive the drug in combination with Imjudo.
In the end, it will be important to find a compromise between the fact that Imfinzi has become the global standard of care for biliary tract cancer in 12 years and its increasing burden on health insurance finances.
In the U.S., U.K., and Japan, Imfinzi was reimbursed within a year of its approval.
The industry believes the U.K.’s case would provide clues for Korea’s implementation.
During reimbursement discussions, the U.K.
used a quality-adjusted life years (QALYs) weight of 1.2 and a flexible ICER in recognition of the fact that Imfinzi was the first immuno-oncology drug approved for the first-line treatment of biliary tract cancer.
However, as Imfinzi’s ICER does not meet the criteria for the Korean government's 'preferential treatment for innovative new drugs', it remains to be seen how the discussions will unfold.
The industry analyzes that it will come down to what the pharmaceutical companies will propose in terms of financial sharing and whether the government will accept the proposal.
“AstraZeneca Korea is committed to providing innovative treatment options for biliary tract cancer patients in Korea.
We will continue to do our best in the coming process,” said an AstraZeneca official.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo
- "Vabysmo PFS shifts the retinal disease treatment persistence·efficiency"
- Reporter's view | Son, Hyung Min







